Вариабельность и уровень экспрессии микроРНК в ткани опухолей головы и шеи
Автор: Никитина Екатерина Геннадьевна, Уразова Людмила Николаевна, Черемисина Ольга Владимировна, Кульбакин Денис Евгеньевич, Стегний В.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 3 (63), 2014 года.
Бесплатный доступ
Малые некодирующие РНК (микроРНК) являются не только важнейшими регуляторами экспрессии генов, участвуя практически во всех базовых процессах в клетке, но и являются специфичными молекулами и могут быть использованы для многих целей в клинической диагностике. В данном исследовании проведена оценка уровня экспрессии микроРНК в опухолевой ткани пациентов с новообразованиями в разных анатомических сайтах головы и шеи. По результатам данного проекта получены новые данные относительно паттерна экспрессии восьми микроРНК в опухолевой ткани пациентов с раком гортани (РГ), языка (РЯ) и папиллярной карциномы щитовидной железы (РЩЖ), а именно микроРНК-18а, -21, -155, -200а, -200с, -205, -221 и -494. Определен спектр микроРНК, специфичных для анализируемых локализаций, что позволяет предположить наличие различий в механизмах участия одних и тех же микроРНК при онкогенезе опухолей разных эпитопов головы и шеи. Показано, что панель из микроРНК-200а, -200с, -21 и -205 является специфичной для определения двух локализаций (РГ и РЩЖ) и, вероятно, может быть использована для уточнения сайта вторичной опухоли и/или метастаза неясного генеза.
Опухоли головы и шеи, микрорнк
Короткий адрес: https://sciup.org/14056429
IDR: 14056429 | УДК: 617.51/.617.57-006.04:577.218
Variability and microRNA expression level in tissues of head and neck tumors
Small non-coding RNAs (miRNAs) are not only an important regulator of gene expression by participating in almost all basic processes in the cell, but are specific molecules and can be used for many applications in clinical diagnostics. In our study, we assessed the level of miRNA expression in tumor tissue of patients with head and neck tumors of various sites. New data regarding the expression pattern of eight miRNAs in tumor tissue from patients with cancer of the larynx, tongue and papillary thyroid carcinoma, namely: miR-18a, -21, -155, -200a, -200c, -205, -221 and -494 were obtained. The spectrum of miRNA-specific localizations was analyzed, suggesting the existence of differences in the mechanisms of participation of the same miRNA in carcinogenesis of tumors of different epitopes of the head and neck. The panel of miR-200a, -200c, -21 and -205 was shown to be specific for determining the two locations (laryngeal and thyroid cancers) and probably can be used to define the site of a secondary tumor and / or metastasis of unknown origin.
Текст научной статьи Вариабельность и уровень экспрессии микроРНК в ткани опухолей головы и шеи
В структуре онкологической заболеваемости опухоли головы и шеи (ОГШ) занимают 5-е место в мире по частоте встречаемости и 6-е место – по летальности. В России ежегодно регистрируются более 80 тыс. больных с этой патологией. Наблюдается тенденция к увеличению уровня заболеваемости и смертности при ОГШ, на фоне стабилизации этих показателей для других локализаций [1]. В настоящее время достигнуты значительные успехи в терапии зло качественных опухолей головы и шеи, которые связаны с совершенствованием методов лечения, однако показатели 5-летней выживаемости, к сожалению, не превышают 50 % [14]. Предпосылкой успешного лечения является своевременная и точная диагностика, что позволяет повысить эффективность лечения, увеличить сроки без-рецидивной выживаемости, а также улучшить качество жизни пациентов, снизив долю и тяжесть побочных эффектов [5].
Для ОГШ в качестве молекулярных биомаркеров для определения риска возникновения рака и неблагоприятного прогноза течения заболевания применяются мутации генов EGFR , k-Ras , b-Raf , p53 , а также инфицирование онкогенными вирусами, в частности вирусом папилломы человека, Эпштейна – Барр и другими [14]. Открытие принципиально нового класса малых молекул РНК (микроРНК), которые регулируют экспрессию генов, стало весьма значительным событием в биологии конца XX века [13]. В ходе биогенеза микроРНК претерпевают ряд изменений – от молекулы при микроРНК длиной 1000 нуклеотидов к конечной форме зрелой микроРНК (около 25 нуклеотидов). Делеции в генах микроРНК, а также сбой механизма их созревания могут являться важным звеном процесса трансформации клетки [12]. МикроРНК не только регулируют многие ключевые процессы в жизнедеятельности клетки и поддержании ее гомеостаза, но и участвуют в патогенезе многих заболеваний, в том числе и онкологических [8, 16].
Показано, что отдельные микроРНК (-21, -18а, -200а, -200с, -205) играют ключевую роль в регуляции процессов апоптоза, роста, инвазии, пролиферации клеток [4, 10, 11], клеточного цикла (-18а, -21, -200а, -200с, -221, -494) [17]. Кроме того, отмечено их непосредственное участие в формировании иммунного ответа (микроРНК-155) [19]. Учитывая роль этих молекул в столь значимых фи- зиологических процессах, логично предположить взаимосвязь экспрессии определенных микроРНК с патоморфологическими характеристиками опухоли и течением заболевания (развитие рецидивов, лимфогенных метастазов). Также существует возможность использования экспрессии определенного профиля микроРНК для идентификации происхождения ткани метастаза. Высказывается предположение о более высокой, чем у применяемых молекулярных маркеров, специфичности и чувствительности данного метода [7].
Крайняя противоречивость литературных данных не дает возможности составить четкие представления об участии тех или иных микроРНК-маркеров, которые бы обладали клинической значимостью в этиопатогенезе опухолей, локализованных, в частности, в области головы и шеи [2, 15]. Следовательно, представляется достаточно актуальным изучение микроРНК для оценки возможности применения в качестве потенциальных онкомаркеров, уровень экспрессии которых может быть специфичен для опухолей разных локализаций.
Целью исследования явилась оценка уровня и вариабельности экспрессии микроРНК в опухолевой ткани больных ОГШ.
Материал и методы
В исследование включены данные о 56 пациентах (таблица), получивших лечение в ФГБУ
Таблица
«НИИ онкологии» СО РАМН. Работа проведена с соблюдением принципов добровольности и конфиденциальности в соответствии с «Основами законодательства РФ об охране здоровья граждан» (Указ президента РФ, от 24.12.93 № 2288). На исследование получено разрешение этического комитета ФГБУ «НИИ онкологии» СО РАМН.
В работе был использован парный операцион-ный/биопсийный материал (опухолевая и прилежащая условно-нормальная ткань) от пациентов с первичным диагнозом плоскоклеточного рака гортани (n=34), языка (n=13) и папиллярной карциномы щитовидной железы (n=6). Диагноз пациентов морфологически верифицирован. Транспортировку и хранение (при –80°С) биоматериала осуществляли в пробирках типа Ep-pendorf в консервирующем растворе RNAlater (Sigma, USA). Тотальная фракция РНК из ткани была выделена набором реагентов mirVana™ (Ambion, USA). Количество РНК оценивали на спектрофотометре NanoDrop 2000 (ThermoSci-entific, USA) (выход продукта варьировал от 30 до 800 нг/мкл, А260/280=1,99). Целостность РНК оценивали на капиллярном электрофорезе на приборе TapeStation 2200 (Agilent Technologies, USA). Среднее значение RIN (RNA Integrity Number) составило 8,77 (от 8,3 до 9,0), что свидетельствует о высоком качестве образцов и пригодности их к анализу методом количественной ПЦР в режиме реального времени.
Мультиплексная обратная транскрипция была проведена с использованием специфичных к определенным микроРНК (hsa-miR-18a-5p, hsa-miR-21-5p, hsa-miR-155-5p, hsa-miR-200a-3p, hsa-miR-200c-3p, hsa-miR-205-5p, hsa-miR-221-3p, hsa-miR-494-3p) праймерам особой шпилевидной конструкции (IyevlevaA., et al 2012). Все реакции ПЦР в режиме реального времени проведены в триплете согласно протоколу [9]. В качестве гена-рефери выбрана микроРНК-103 [9], калибровка выполнена относительно нормальной ткани, уровень экспрессии микроРНК рассчитан согласно методу Pfaffl [18]. В качестве результата использовано логарифмически трансформированное по основанию е нормализованное значение уровня экспрессии (ln(fold+0,02)). Дискриминантный и корреляционный анализ, а также обработка данных с применением U-критерия Манна – Уитни проводились в программе Statistica 8.0.
Результаты исследования
Проведенный анализ экспрессии микроРНК в опухоли относительно прилежащей условнонормальной ткани для 8 микроРНК (-18а, -21, -155, 200а, -200с, -205, -221 и -494) на примере 3 локализаций выявил аберрантную экспрессию некоторых микроРНК в обследованных группах (рис. 1).
В своих исследованиях мы установили, что другие изученные микроРНК демонстрируют разнонаправленное изменение уровня экспрессии в обследуемых группах пациентов (рис. 1Б-Г). Следует отметить, что в опухолевой ткани больных раком языка выявлена значительная гиперэкспрессия не только микроРНК-21, -155, но и микроРНК-200с (72 % случаев, отмечены ln>0), а также гипоэкспрессия микроРНК-494 (100 % случаев – ln<0). Во всех исследованных образцах опухолевой ткани пациентов с диагнозом папиллярной карциномы щитовидной железы показана гиперэкспрессия микроРНК-155, -200а и гипоэкспрессия микроРНК205, в то время как для микроРНК-21 и -221 при повышенной их экспрессии в большинстве случа-
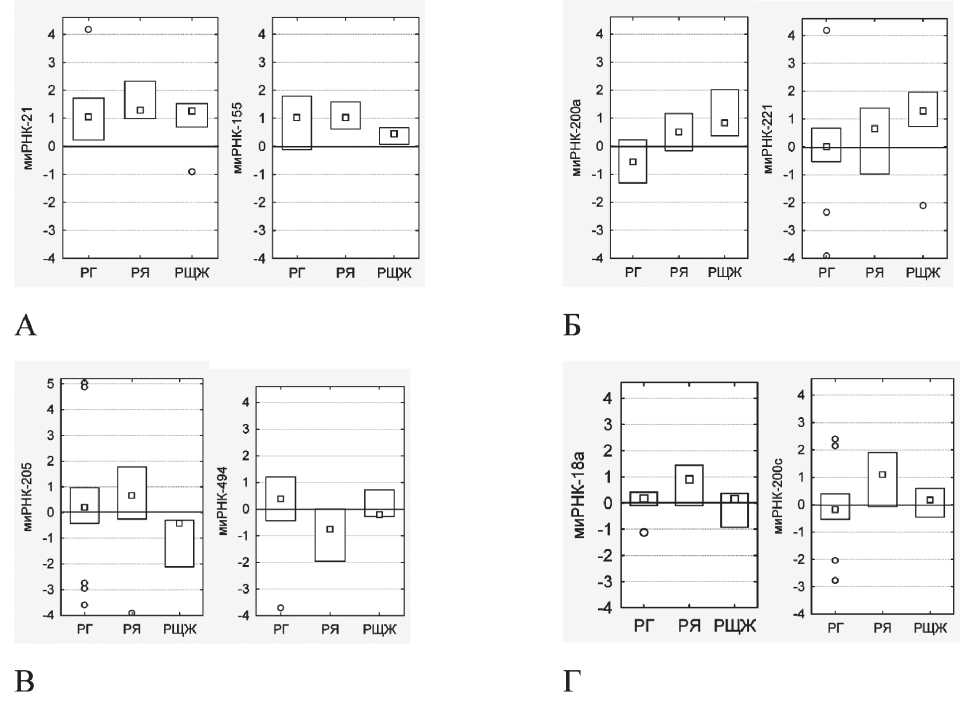
Рис. 1. Уровень экспрессии микроРНК в патологически измененной опухолевой ткани относительно условно-нормальной (значение нормы экспрессии – 0). Примечание: РГ – рак гортани; РЯ – рак языка; РЩЖ – рак щитовидной железы
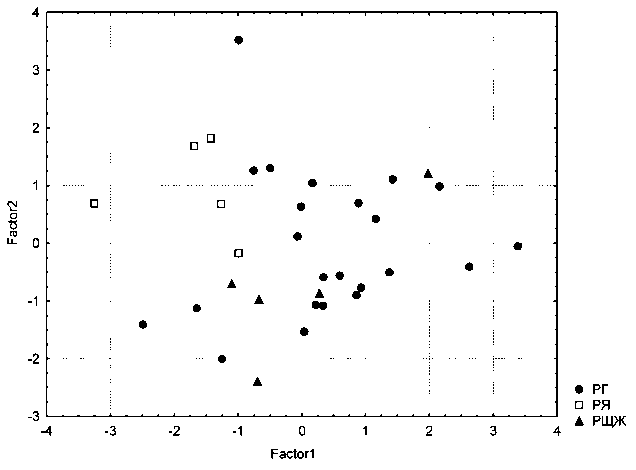
Рис. 2. Расположение объектов в пространстве на плоскости дискриминантных осей. Примечание: Factor 1 и 2 – условное значение, объединяющее данные по экспрессии анализируемых микроРНК. Точками, квадратами и ромбами отмечены пациенты с диагнозом РГ, РЯ и РЩЖ соответственно ев наблюдаются и единичные выбросы значений изученных показателей. Вероятно, эти микроРНК могут играть определенную роль в канцерогенезе изученных локализаций (рис. 1), что, однако, требует уточнения на более репрезентативных группах, унифицированных по анамнестическим и клиникоморфологическим показателям.
Сравнительный анализ уровня экспрессии каждой из анализируемых микроРНК между локализациями значимых различий в изученных показателях не выявил. Однако дискриминантный анализ показал, что есть значимое различие в значениях уровня экспрессии между 3 сравниваемыми группами (F(4.58)=4.094, p<0,0054), что позволяет судить о наличии специфичности экспрессии некоторых микроРНК в группах (рис. 2). Несмотря на разброс значений, что, вероятно, связано с гетерогенностью выборок по таким показателям, как пол, возраст и TNM (таблица), наблюдается тенденция к группированию случаев согласно диагнозу (рис. 2).
Обсуждение
Проведенный анализ позволил выделить микроРНК (-200а, -200с, -21 и -205), которые формируют специфичную картину экспрессии в группе и позволяют отнести анализируемые образцы к определенной локализации. Панель вышеперечисленных микроРНК специфична и с вероятностью 93,5 % или 66,6 % позволяет отнести анализируемые образцы к плоскоклеточной карциноме гортани или к папиллярной карциноме щитовидной железы соответственно. Кроме того, корреляционный анализ также выявил наличие связи между этими микроРНК. Наблюдалась положительная корреляция между микроРНК-200с и микроРНК-200а, -205 (r=0,44 и r=0,53 соответственно), а также между микроРНК-21 и -155 (r=0,51). Следует отметить, что все эти микроРНК объединяет участие в регуляции апоптоза, клеточного роста, инвазии и пролиферации [4, 10, 11, 21]. При этом микроРНК-200а, -200с, -205 играют определенную роль и в регуляции клеточного цикла [11, 20, 21]. В литературе широко представлены данные о значительной роли представителей семейства микроРНК-200, а также микроРНК-205 в онкогенезе, в частности, в эпителиально-мезенхимальном переходе и процессе приобретения клеткой эмбрионального фенотипа. Многочисленные исследования показали онкосупрессорную роль микроРНК-200
в канцерогенезе опухолей мочевого пузыря, молочной железы, рото- и носоглотки и др. [6]. Для микроРНК-205 свойственна двойственная роль в онкогенезе в зависимости от локализации опухоли и мишеней этой молекулы. Так, при раке молочной железы показана ее гипоэкспрессия, в то время как при опухолях легкого, мочевого пузыря, яичника, головы и шеи выявлена гиперэкспрессия этой микроРНК [21].
Полученные нами результаты позволили представить специфичную картину экспрессии изученных микроРНК в опухолевой ткани относительно прилежащей условно нормальной при трех локализациях опухолей в области головы и шеи – плоскоклеточном раке гортани и языка, а также папиллярной карциноме щитовидной железы, что может внести определенный вклад в имеющиеся литературные данные относительно роли микроРНК в процессах канцерогенеза. При этом различия в спектре их экспрессии в обследованных группах больных позволяют предположить отличия в механизмах их участия в процессе канцерогенеза опухолей отдельных локализаций.
Несмотря на отсутствие значимых различий по отдельным микроРНК между группами, статистический анализ позволил выявить микроРНК, формирующих специфичную картину экспрессии и позволяющих идентифицировать локализацию опухоли, что может быть использовано для уточнения сайта первичной или вторичной злокачественной опухоли и/или метастаза неясного генеза. Представляется целесообразным продолжить исследования с привлечением более многочисленных и унифицированных по анамнестическим и клиникоморфологическим показателям групп пациентов, что даст возможность получить новые данные относительно механизмов участия микроРНК в канцерогенезе опухолей различных локализаций, а также возможных аспектах использования в качестве диагностических и прогностических молекулярных маркеров в клинической онкологии.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект №12-04-31505) и гранта НШ-1279.2014.4.


