Варианты хирургического лечения омфалоцеле
Автор: Морозов Д.А., Филиппов Ю.В., Никитина А.С., Антонов М.А., Михайленко Е.А., Тихонова И.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Хирургия новорожденных
Статья в выпуске: 2 т.3, 2007 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/14916633
IDR: 14916633
Текст статьи Варианты хирургического лечения омфалоцеле
Саратовс^ий ^ос^дарственный медицинс^ий ^ниверситет
В статье представлены варианты хир^р^ичес^о^о лечения различных форм омфалоцеле ^ новорожденных, проводимые в ^лини^е хир^р^ии детс^о^о возраста Саратовс^о^о ^ос^дарственно^о медицинс^о^о ^ниверситета в период с 2000 по 2006 ^од.
The variants of surgical treatment of different forms of omphalocelis in newborns were analyzed and made in the pediatric surgery department of Saratov state medical university in period 2000–2006.
Патологию грыжи пупочного канатика (омфало-целе) определяют врожденная мальформация передней брюшной стенки в виде умбиликального дефекта, несостоятельность барьерной функции, быстрое инфицирование и дестр^^ция эмбриональных оболочек грыжевого мешка с развитием перитонита. Основной проблемой хирургии омфалоцеле является малый объем брюшной полости, не соответствующий объему грыжевого содержимого и не позволяющий выполнить первично-радикальные операции при больших грыжах (синдром висцеро-абдо-минальной диспропорции). В дополнение к этому значительные коррективы в лечение больных омфалоцеле вносят сочетанные пороки развития органов брюшной полости, сердца, мочеполовой системы, ануса и прямой кишки. Современные методы интенсивной терапии в неонатоло^ии позволяют принципиально изменить схем^ лечения данно^о порока, заменить консервативные методы и этапную методику R. Gross [1] (перевод эмбриональной грыжи в вентральную с последующей операцией в 9-12 месяцев) радикальной пластикой в период новорож -денности [2, 3].
В основу работы положен анализ лечения 18 новорожденных с омфалоцеле, находившихся в клинике детской хирургии в период 2000-2006 гг. Из 282 новорожденных с большими врожденными по-ро^ами развития пациенты с омфалоцеле составили 6,4%. Диагноз был поставлен при антенатальном ультразвуковом исследовании плода у 6 детей, у остальных - в раннем постнатальном периоде. Анализ проводили в двух группах больных с малым (10) и большим (8) омфалоцеле, тактика лечения которых была различной.
Малое омфалоцеле (дефект не более 6,0 см в диаметре) зарегистрировано у 10 новорожденных, содержимым ^рыжево^о меш^а во всех сл^чаях были петли тонкой кишки (фото 1). Следует отметить, что у трех детей оболочки грыжевого мешка были повреждены при отсечении пуповинного остатка в родильном доме, что повлекло эвентрацию тонкой кишки и инфицирование брюшной полости, а у одного новорожденно^о вдобаво^ произошло ятро^енное травматическое повреждение тонкой кишки. У од-но^о из пациентов имелась полная персистенция желточного протока.
Омфалоцеле не входит в состав ^лассичес^ой VACTERL-ассоциации, но достаточно часто сочетается с иными нарушениями других органов и систем. В исследуемой группе 5 пациентов (условно 50%) имели сочетанные пороки развития: анорек-тальн^ю а^енезию с ре^товестиб^лярным свищом (1), дивертикул Меккеля и дивертикулит (1), атрезию подвздошной кишки (1), двустороннюю врожденную катаракту (1), врожденный порок сердца (2), гипоспадию (1) и гидроцефалию (1), что потребовало соответств^ющих хир^р^ичес^их и лечебных мер, не оказавших влияния на выбор метода коррекции омфалоцеле. В то же время у одного больного серьезный порок сердца в последующем привел к летальному исходу, у другого - омфалоцеле было ассоциировано с асимметричной эмбриофе-тобластопатией и некорригируемыми сердечно-сосудистыми нарушениями. Всем пациентам после подготовки выполнена радикальная послойная пластика, у двух новорожденных (с персистенцией d. оmphaloentericus и дивертикулитом) оперативный прием был расширен до резе^ции подвздошной кишки (фото 2) и энтероэнтероанастомоза (Resorba 6.0).
У детей этой группы значимых нарушений гемодинамики и витальных функций не отмечали, послеоперационную терапию в отделении реанимации проводили по стандартному протоколу. Послеоперационных осложнений не было, кишечные анастомозы состоятельны. В этой подгруппе погибли двое пациентов с завершенной пласти^ой передней брюшной стенки. Причины смерти - атрезия трехстворчатого клапана сердца у новорожденного с множественными пороками развития и аплазия левых отделов сердца у новорожденного с асимметричной эмбриофе-тобластопатией (фото 3).
Большое омфалоцеле (диаметр дефекта 7,012,0 см) было установлено у 8 новорожденных (фото 4). У всех детей этой группы компонентом содержимого грыжевого мешка являлась печень, у 5 -шаровидная. В последнем случае вся печень развивается в грыжевом мешке, принимая форму шара. При этом она не имеет нормальной фиксации, ее перемещение на патоло^ичес^и длинных сос^дах («сосудистой ножке») приводит к выраженным гемодинамическим и сосудисто-рефлекторным нарушениям. Клинические признаки повреждения и инфицирования ^рыжевых оболоче^ имелись толь^о у одного ребенка.
Операцию выполняли в э^стренном поряд^е по истечении первых суток жизни, после предоперационной подготовки, направленной на стабилизацию основных витальных функций и согревание новорожденного. ИВЛ в предоперационном периоде не была показана ни у одного пациента. Оперативное вмешательство ос^ществляли под эндотрахеальным комбинированным наркозом с мониторингом гемодинамики и давления на вдохе. В ходе операции последовательно производили удаление амниотической оболочки и вартонова студня, лигирование пупочной вены и артерий, мобилизацию урахуса, ревизию брюшной полости на наличие сочетанных пороков развития. Затем для увеличения объема брюшной полости производили пальцевое растяжение передней брюшной стенки, вызывая паралич и частичный надрыв мышц. В трех наблюдениях это позволило выполнить одномоментное по^р^жение содержимо^о ^рыжево^о меш^а в брюшн^ю полость и полнослойн^ю ради^альн^ю пласти^^ передней брюшной стенки. Пятерым детям по причине выраженного синдрома висцеро-абдоминальной диспропорции применили аллотрансплантацию передней брюшной стенки, используя перчаточную резину в два слоя. Принципиальным считали подшивание аллотрансплантата к мышечно-апоневротическому краю дефекта.
Всем 8 новорожденным в послеоперационном периоде потребовались длительная ИВЛ в триггерном режиме, мониторинг гемодинамики и инотропная поддержка. В первые двое суток после операции проводилась нейролептаналгезия, затем седата-ция (фентанил, дроперидол, реланиум).
При планировании индивидуальной схемы лечения важную информацию, по нашему мнению, дает динамический контроль внутрибрюшного давления (ВБД). В первые сутки после первичной ра-ди^альной пласти^и ВБД повышается в среднем до 30 см водн. ст. (N-2-3 см), после пластики с предварительным аллопротезом - до 15 см водн. ст. На 5-7-е сутки после аллопластики, при полном погружении грыжевого содержимого в брюшную полость, ВБД снижается до 3-5 см, что подтверждает возможность проведения окончательной пластики. Восстановление функции кишечника обычно коррелирует со снижением ВБД. Энтеральное питание возможно при ^ровне давления ниже 5 см водн. ст.
Радикальную пластику передней брюшной стенки детям с первичной аллотрансплантацией выполняли на 4-8-е сутки после первой операции, когда отмечали ^величение объема брюшной полости с частичным или почти полным погружением содержимого омфалоцеле. Следует отметить, что лимитирующим фактором во всех случаях являлась патологически измененная печень, форсированное погружение ^оторой приводило ^ острым нар^шениям печеночной и общей гемодинамики.
ИВЛ после ради^альной операции проводили еще 3-5 суток. Стандартная терапия дополнялась комбинированным питанием (парэнтеральным, зондовым) с использованием полуэлементных смесей.
У одного ребенка диагностирован верхний срединный синдром в составе ^лассичес^ой пентады Cantrel: мышечно-апоневротического дефекта значительных размеров (12,0 х 6,0 см) от пуповинного кольца до мечевидного отростка грудины, дефекта переднего отдела диафрагмы (перикард и правый плевральный мешок плавно переходили в париетальную брюшину), расщепления грудины, врожденного порока сердца. Были выполнены первичная радикальная пласти^а передней брюшной стен^и и пласти^а диафрагмы.
В этой группе погиб один новорожденный на 5-е сутки после аллопластики передней брюшной стенки. Причиной смерти была тяжелая перинатальная травма головного мозга на фоне недоношенности.
В целом из всех 18 оперированных новорожденных с омфалоцеле погибли трое детей (диаграмма), летальность составила 16%.
Таким образом, сегодня пластика передней брюшной стенки при малых омфалоцеле не представляет значительных трудностей, и актуальность проблемы в данной группе детей определяется ят-ро^енными повреждениями ^ишечни^а и брюшной полости при невнимательном отсечении широ^о^о пуповинного остатка. При устранении дефекта передней брюшной стенки у пациентов с большим омфалоцеле важно не допустить нарушений дыхания, гемодинамики, а при погружении печени - нарушения кровотока по печеночным сосудам. Одним из этих пациентов может быть выполнена первичная ради-^альная пласти^а передней брюшной стен^и после ее пальцевого растяжения, другим - отсроченная радикальная пластика после аллотрансплантации перчаточной резиной.
Метод является относительно простым, эффективным, безопасным и недорогостоящим. Все дети требуют многокомпонентного реанимационного пособия и длительной ИВЛ, комбинированного парентерального и зондового энтерального питания. Тем не менее ^рамотное лечение в специализированных хирургических центрах в настоящее время позволяет достичь выздоровления и полной реабилитации новорожденных с омфалоцеле любых размеров, избавляя детей от этапных операций.
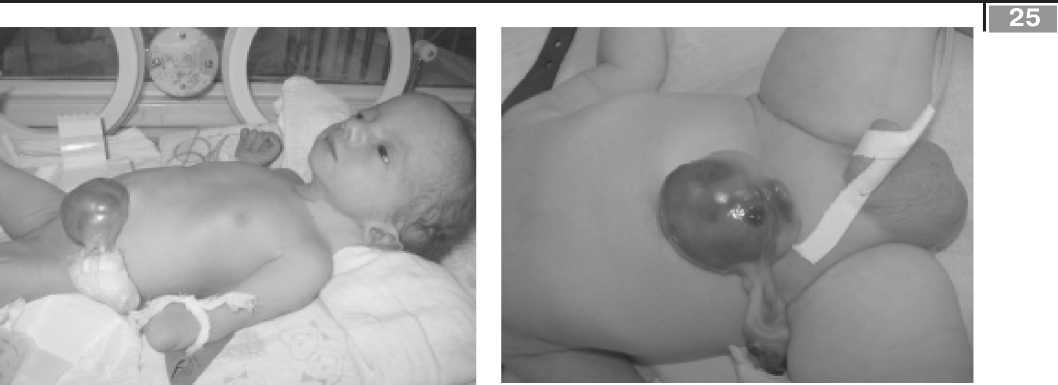
Фото 1. Малое омфалоцеле ^ новорожденно^о со множественными поро^ами развития (1 с^т.)
Фото 2. Омфалоцеле ^ новорожденно^о, ассоциированное с атрезией подвздошной ^иш^и, перфорацией ^иш^и в оболоч^е омфалоцеле, ^ипоспадией (1 с^т.)
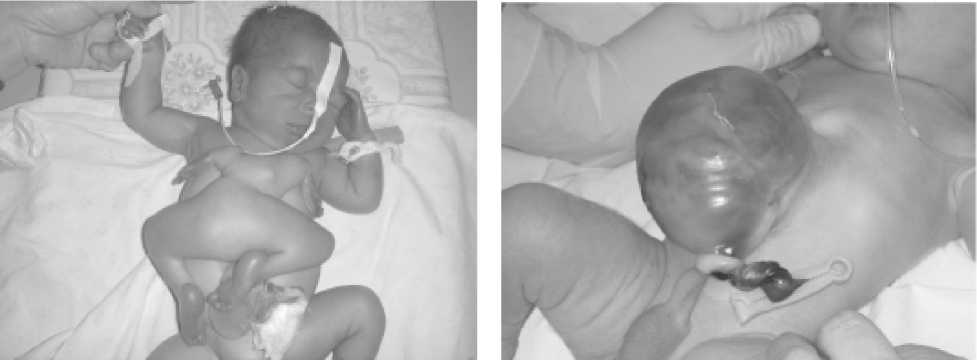
Фото 3. Малое омфалоцеле ^ новорожденно^о, имеюще^о асимметричн^ю эмбриофетобластопатию
Фото 4. Большое омфалоцеле ^ новорожденно^о.
В состав ^рыжево^о меш^а входит «шаровидная печень, выражен синдром висцеро-абдоминальной диспропорции
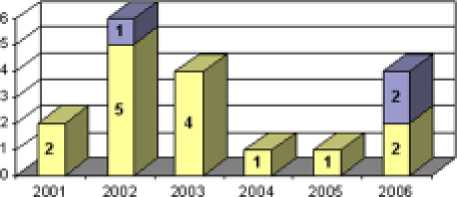
ОбЫжипи D Умерли
Диа^рамма. Динами^а пост^пления и рез^льтатов лечения новорожденных с омфалоцеле в период 2000–2006 ^^.
Список литературы Варианты хирургического лечения омфалоцеле
- Gross R. A new method for surgical treatment of large omphaloceles//Surgery. -1948. -Vol. 24. -P. 277-292
- Mauriozio P., Kiely M., Curry J. et all. Staged repair of giant omphaloceles in the neonatal period.//Journal of Pediatric Surgery. -2005. -№ 5.
- A. Wakhlu, A.K. Wakhlu. The management of exomphalos//Journal of Pediatric Surgery. -2000. -№ 1.


