Верификация радиационных рисков смертности российских участников ликвидации последствий аварии на Чернобыльской АЭС на основе дозового критерия
Автор: Чекин С.Ю., Ловачв С.С., Кащеева П.В., Туманов К.А., Максютов М.А., Власов О.К., Щукина Н.В.
Рубрика: Научные статьи
Статья в выпуске: 3 т.29, 2020 года.
Бесплатный доступ
По мере накопления данных в радиационной эпидемиологии изучается всё больше групп болезней. Оценки радиационных рисков для одних и тех же болезней у разных исследователей могут существенно отличаться. В этих условиях становится актуальным разработка простых критериев, которые определили бы достаточные условия наличия радиационного риска, который может быть оценён по имеющимся данным наблюдений. Цель настоящего исследования состоит в разработке критерия достаточности существования радиационного риска, определяемого по данным когортных наблюдений в рамках линейной (по дозе облучения) мультипликативной модели риска. На основе его расчёта, по данным о когорте российских участников ликвидации последствий аварии на Чернобыльской АЭС (ликвидаторов), наблюдаемых в Национальном радиационно-эпидемиологическом регистре (НРЭР) с 1986 по 2019 гг., определён перечень болезней, смертность от которых является статистически ассоциированной с дозой облучения. Разработанный критерий превышения средних доз для случаев смерти над усреднёнными с весами времён наблюдения дозами по всей когорте является достаточным условием существования радиационного риска в рамках линейной мультипликативной модели. Использование разработанного порогового критерия позволило сформулировать две новые гипотезы о моделях радиационных рисков смертности человека. 1) Для радиационного риска смертности от солидных злокачественных новообразований впервые показано существование двух временных фаз реализации этого стохастического эффекта (до 9 лет и свыше 24 лет после облучения). Необходима дальнейшая проверка статистической значимости наблюдаемой зависимости риска от времени. 2) Впервые показано существование радиационного риска смертности от болезней органов пищеварения и наличие латентного периода для этого риска порядка 9 лет. Количественная оценка радиационного риска и заключение о его статистической значимости должны быть получены в дальнейших исследованиях. Таким образом, разработанный пороговый критерий достаточности существования радиационного риска, определяемого в рамках линейной мультипликативной модели по данным когортных наблюдений, показал свою полезность при исследовании когорты ликвидаторов НРЭР. Дополнительные исследования вероятностного распределения дозовой невязки между случаями смерти и всей когортой требуются для разработки соответствующей статистики при проверке нулевой гипотезы об отсутствии радиационных рисков.
Радиационный риск, функция правдоподобия, нормальные уравнения, пороговый критерий, достаточные условия, смертность, инфекционные болезни, солидные злокачественные новообразования, болезни системы кровообращения, болезни органов дыхания, болезни органов пищеварения, травмы и отравления
Короткий адрес: https://sciup.org/170171539
IDR: 170171539 | УДК: 616-036.8:614.876(470.3):519.24 | DOI: 10.21870/0131-3878-2020-29-3-27-41
Dose-criterion based verification of radiation risks of death in the cohort of Russian participants of clean-up operations following the Chernobyl accident
As more data on health effects of radiation are accumulated, the more groups of diseases are investigated with the use of radiation epidemiology approaches and quantitative indicators. Radiation associated risk of the same disease estimated by different investigators may vary considerably. For this reason it has become necessary to develop simple criteria that could allow identification of sufficient conditions for radiation risk existence and its assessment with the use of available follow-up data. The purpose of the study was to develop the sufficiency criterion to identify radiation associated risk existence with data of the cohort study within frames of the linear (on radiation dose) multiplicative risk model. With the use of radiation risk estimates, personal dosimetry and health history data of the Chernobyl liquidators included in the cohort study and followed up at the National Radiation Epidemiological Registry (NRER) for the period from 1986 over 2019, we identified the diseases that caused death statistically associated with radiation dose. The developed criterion of exceedance of average doses related to death cases over averaged by the cohort doses with the follow-up time weights is the sufficient condition of radiation risk of death existence within the linear multiplicative risk model. The use of developed threshold criterion allowed formulating two new hypotheses on models for radiation risks of death. Hypothesis 1: For radiation risk of death from solid cancers. It is the first demonstration of the existence of two time-dependent phases of stochastic effect manifestation: 24 years after exposure to radiation. Further testing of the significance of dependence of risk from time is necessary. Hypothesis 2: It is the first time demonstrated the existence of radiation risk of death from the diseases of the digestive system, as well as the existence of the latency period for the risk manifestation, the length of the period is about 9 years. Quantitative estimate of radiation risk and conclusion on its statistical significance will be obtained in further studies. As a result, the developed threshold criterion of sufficiency for existence of radiation risk estimated within the linear multiplicative model with the use of the cohort study data has demonstrated its usefulness in the study of cohort of the NRER Chernobyl liquidators. Additional researches of probabilistic distribution of dose difference between cases of death and whole cohort are required for development of the corresponding statistics when checking a zero hypothesis of lack of radiation risks.
Текст научной статьи Верификация радиационных рисков смертности российских участников ликвидации последствий аварии на Чернобыльской АЭС на основе дозового критерия
Основным предметом изучения радиационной эпидемиологии долгое время являлись радиационно-индуцированные злокачественные новообразования (ЗНО). Зависимости доза-эффект для ЗНО были в основном установлены к 1990 г. на когорте лиц, переживших атомные бомбардировки 1945 г. городов Хиросимы и Нагасаки в Японии (когорта LSS – Life Span Study). Когорта LSS наблюдалась с 1950 г. и продолжает изучаться в настоящее время. В 1987 г. Preston et al. опубликовали результаты исследования смертности по причине рака в когорте
Чекин С.Ю.* – зав. лаб.; Ловачёв С.С. – мл. научн. сотр.; Кащеева П.В . – ст. научн. сотр., к.б.н.; Туманов К.А. – зав. лаб., к.б.н.; Максютов М.А. – зав. отд., к.т.н.; Власов О.Л. – зав. лаб., д.т.н.; Щукина Н.В. – ст. научн. сотр. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Данные LSS за 1986-1990 гг. [2] свидетельствуют, что вариации по времени и возрасту при облучении для радиационного риска смертности от рака могут находиться в диапазоне до 3-х крат (от минимальных до максимальных значений).
В 1992 г. Shimizu et al. [3] опубликовали первое большое систематическое исследование радиационных рисков нераковой смертности в когорте LSS за период наблюдений 1950-1985 гг. Для смертности от всех причин, за исключением рака, была найдена пороговая зависимость от дозы, с порогом от 0,6 до 2,8 Гр. Статистическая достоверность риска показана через 20 лет после облучения (с 1965 г.). Для болезней системы кровообращения и органов пищеварения радиационные риски смертности обнаруживали при дозах свыше 2 Гр. В 2000 г. было показано, что множественные травмы в долгосрочном плане связаны с облучением в возрасте до 10 лет или после 50 лет [4]. В целом исследования когорты LSS показали, что избыточный радиационный риск смертности от нераковых заболеваний сопоставим с радиационным риском смертности от рака [5-8], однако проявляется при дозах выше 0,5 Гр.
В диапазоне, специально ограниченном малыми дозами – менее 0,3 Гр, результаты радиационно-эпидемиологического анализа смертности, включая нераковые причины смерти, впервые были опубликованы в 2001 г. [9]. Когорта из 65 тыс. российских участников ликвидации аварии на Чернобыльской АЭС была сформирована по данным Национального радиационноэпидемиологического регистра (НРЭР) за период наблюдения 1991-1998 гг. (через 5 лет после аварии). Статистически значимые радиационные риски были получены для смертности от сердечно-сосудистых заболеваний (с оценкой избыточного относительного риска ERR/Гр=0,79 – примерно такого же порядка как для радиационных рисков рака в когортах LSS и НРЭР). В когортах НРЭР к настоящему времени показана существенная гетерогенность радиационных рисков нераковых заболеваний, связанная с наличием сопутствующих заболеваний [10-12].
На основании широкого обзора сведений о различных радиационных рисках человека в 2009 г. Little [13] пришёл к заключению, что радиационные риски нераковых заболеваний, оценённые в разных исследованиях, варьируют, по крайней мере, на два порядка величины.
По мере накопления данных в радиационной эпидемиологии изучается всё больше групп болезней. В этих условиях становится актуальным разработка простых критериев, которые определили бы достаточные условия наличия радиационного риска, который может быть оценён по имеющимся данным наблюдений.
Цель настоящего исследования состоит в разработке критерия достаточности существования радиационного риска, определяемого по данным когортных наблюдений в рамках линейной (по дозе облучения) мультипликативной модели риска.
На основе его расчёта, по данным о когорте российских участников ликвидации последствий аварии на Чернобыльской АЭС (ликвидаторов), наблюдаемых в НРЭР с 1986 по 2019 гг., будет определён перечень болезней, смертность от которых является статистически ассоциированной с дозой облучения.
Материалы и методы
В настоящее время НРЭР [14] является уникальным источником данных, позволяющим проводить исследования радиационных рисков по всему спектру диагнозов, включённых в международную классификацию болезней МКБ-10 [15].
Для исследования смертности ликвидаторов по данным НРЭР была сформирована ретроспективная когорта за период наблюдения 1986-2019 гг. В когорту были включены ликвидаторы мужского пола, зарегистрированные в НРЭР до 1 января 1992 г., въехавшие в зону чернобыльских работ в течение первого года после аварии (с 26.04.1986 по 31.12.1987 гг.) в возрасте 18-70 лет, с официально зарегистрированными индивидуальными дозами внешнего гамма-облучения всего тела, накопленными за весь период работ ликвидатора.
Общая списочная численность когорты составила 71107 человек (мужчин) со средним возрастом на дату въезда в зону аварии 34 года и средней накопленной за время работ дозой 0,133 Гр. Ликвидаторы женского пола не исследовались из-за их малочисленности при данных условиях выбора когорты (259 чел.).
Наиболее подробное исследование зависимостей доза-эффект в радиационной эпидемиологии основывается на когортных наблюдениях. В когортном методе исследования для модели относительного риска (RR) в качестве статистической модели смертности используется пуассоновский процесс с параметром интенсивности X = Хо ■ RR , где Хо - фоновая интенсивность случаев смерти в отсутствие дозового фактора; RR - относительный риск, зависящий от дозы, которая накапливается с течением времени. Величину относительного риска RR по наблюдаемым данным будем определять методом максимального правдоподобия. Для RR будем использовать параметрическое представление, линейное по параметрам: RR=1+ERR-D(t) , где D(t) - наблюдаемое значение дозы внешнего облучения, накопленной к моменту t ; ERR - избыточный относительный риск на единицу дозы (параметр модели).
Пусть вероятность для индивидуума прожить интервал времени [0, t ) задаётся выражением:
S(t) = exp( - J Ц( т )d т ) , (1)
а плотность вероятности умереть в момент t :
f(t) = M(t) ■ exp( - J p ( т )d т ) , (2)
где p(t) - смертность, зависящая от времени в силу внешних причин, таких как, например, накопленная организмом доза облучения.
В рамках линейной беспороговой (ЛБП) модели смертность линейно зависит от накопленной дозы D(t) :
^(t) = Xo ■ (1 + ERR ■ D(t)) ,(3)
где ERR - избыточный относительный риск на единицу дозы; Хо - фоновая смертность в определённой группе индивидуумов.
Тогда логарифмическая функция правдоподобия запишется в следующем виде:
l = m ■ ln(Xo ) + £ ln( 1 + ERR ■ D(tj)) - X 0 ■£ t, - X 0 ■ ERR £ J D ( т )d т ,(4)
j=1 i=1 i=1
где m - число случаев смерти; N - общее число человек под наблюдением; t i - время наблюдения (так называемое «время под риском») для i -го субъекта.
Обозначим через T полное число человеко-лет под наблюдением в когорте:
N
L t i = T , (5)
i = 1
а через < D > - среднюю по всей когорте дозу, рассчитанную из средних индивидуальных доз с весами ( O i ) индивидуальных времён наблюдения:
N
Oi = L Oi = 1,(6)
L t i i= 1 i = 1
-
< D > = - L f D,( t )d t = L (Oi- - j"D,( T )d T ) = L Oi-< Di > t .(7)
T i = 1 о i = 1 ti о
Если накопление индивидуальных доз по времени рассчитывается с точностью до года,
N ti интегралы в выражении для суммы по всем N субъектам наблюдения L f °, (t )d T можно i = 10
оценивать приближённо суммой погодовых доз от начала облучения ( t =0) до окончания облучения ( t = t i ) i -го субъекта.
Система нормальных уравнений метода максимального правдоподобия для определения параметров Х0 и ERR будет выглядеть следующим образом:
А о
m 1
T 1 + ERR •< D > ,
1 m D,
-
- l---- j ---=---------
- m ,.1+ ERR •D 1+ ERR•< D >
j =1
Если облучение было однократным в течение короткого, по сравнению со временем наблюдения, периода, логарифмическая функция правдоподобия имеет следующий вид:
N
m
i = l ао(1 + err • D,)t, + L in xо(1 + ERR • Dj) -i = 1
где N - общее число человек под наблюдением; m - число случаев смерти по изучаемой причине; t - индивидуальные времена наблюдения «под риском»; ERR - коэффициент избыточного относительного риска.
В этом случае для максимизации правдоподобия и оценки избыточного относительного риска нужно найти ERR из уравнения:
mD D
L ------- j------- m •------------- = о ,
jA 1+ ERR • D 1+ ERR • D
N где Dj - дозы для случаев смерти; D = L O, • D, - взвешенная средняя доза для всей когорты i = 1
с весом индивидуальных времен наблюдения.
Если принять, что фоновая интенсивность Л0 меняется в K подгруппах, то уравнение (10) для определения параметра ERR перепишется следующим образом:
K ( mk D „ z|z —-— k=1 i~i1 + ERR ■ Dik
1 + ERR ■ Dk
: 0 .
Как следует из уравнения (11), в рамках принятой мультипликативной ЛБП модели радиационного риска (3), когда выполняется условие:
K ( m k
C :Ц I dm - mk ■ Dk l> 0 , k : 1 V j : 1
точечная оценка коэффициента избыточного относительного риска ERR >0 (11), и относительный радиационный риск RR =1+ ERR ■ D >1.
Условие (12) можно переписать в эквивалентном виде:
K ( 1 mk^
C : Z mk "I --- ’I j - D k l> 0 .
k : 1 V mk j : 1
Как показывает представление (13), смысл критерия C >0 наличия радиационного риска (в рамках ЛБП модели (3)) заключается в следующем: среднеарифметическая доза для случаев смерти превышает, в некотором смысле, взвешенную с весом индивидуальных времен наблюдения среднюю дозу в когорте. Превышение достигается либо в каждой из K подгрупп, внутри которых фоновая интенсивность Л0 предполагается постоянной, либо при суммировании разностей (невязок) этих средних доз по K подгруппам, с множителями числа случаев смерти в подгруппах. Величину C в дальнейшем будем называть дозовой невязкой (между случаями смерти и всей когортой). C имеет размерность дозы, в данном исследовании - Гр.
Результаты и обсуждение
Для численной проверки правильности критерия (12) способом цифровой имитации были сгенерированы времена под риском для когорты численностью 100000 человек, с показателем интенсивности пуассоновского процесса Л =3’10 ‘3 ’(1+1 D ) для каждого / -го члена когорты. Период наблюдения за когортой принимался равным 30 годам, при однократном облучении в год, предшествовавший периоду наблюдения. Дозовое распределение принималось равномерным на интервале (0-0,5 Гр). Имитационное моделирование проводилось с помощью статистического программного обеспечения R версии 4.0.2 [16]. Сгенерировано 5411 терминальных случаев. Вычисление дозовой невязки по формуле (12) дало значение C =101,6 Гр. Для трёхлетних периодов наблюдения внутри всего 30-летнего периода среднее значение C =11,3 Гр со стандартным отклонением 3,8 Гр.
Полученные в имитационной когорте значения C можно рассматривать как ожидаемые верхние пределы для исследуемой когорты ликвидаторов, так как имитационная когорта имела среднюю дозу в 2 раза больше (0,250 Гр), чем когорта ликвидаторов (0,133 Гр), времена до наступления событий моделировались с коэффициентом ERR=1/Гр, который по порядку величины совпадает с различными оценками радиационных рисков в когорте ликвидаторов [9-12], а гетерогенность имитационной когорты по фоновому показателю интенсивности событий отсутствовала.
Для когорты ликвидаторов НРЭР конечными точками наблюдения в данном исследовании являлись случаи смерти по причинам, приведённым в табл. 1 (первая и вторая колонки).
Для последующего анализа когортные данные были сгруппированы в следующие 2880 подгрупп: по 5-летним интервалам возраста на момент начала работ в зоне аварии (до 69 лет – 12 интервалов), по 5-летним интервалам достигнутого возраста (до 99 лет – 20 интервалов) и по 3-летним интервалам времени от начала работ в зоне аварии (до 35 лет – 12 интервалов). Вклад в величину невязки C , как видно из формулы (12), дают только подгруппы с ненулевым числом случаев смерти.
При подсчёте взвешенных средних доз с весом индивидуальных времен наблюдения продолжительность периода наблюдения (время под риском) для каждого ликвидатора определялась от даты его въезда в зону аварии до минимальной из следующих дат: даты смерти по выбранной причине, даты выхода из-под наблюдения по иным причинам (включая смерть по иной причине) или даты окончания исследования – до 2019 г.
Результаты расчёта критерия (12) наличия радиационного риска по различным причинам смерти приведены в табл. 1 (последний столбец). Положительность C является достаточным условием существования радиационного риска в рамках мультипликативной ЛБП модели (3).
Таблица 1
Основные характеристики исследованной когорты по причинам смерти и соответствующие значения дозовой невязки C между случаями смерти и всей когортой
|
Причины смерти (основные) |
Рубрики МКБ-10 |
Число случаев |
Средний возраст, лет |
Средняя доза для случаев, Гр |
Дозовая невязка случаев C , Гр |
|
Инфекционные и паразитарные болезни |
A-B |
518 |
34,26 |
0,1308 |
-0,70 |
|
Солидные ЗНО |
C00-80 |
4874 |
36,88 |
0,1353 |
10,18 |
|
Болезни системы кровообращения |
I |
11846 |
36,34 |
0,1341 |
9,54 |
|
Болезни органов дыхания |
J |
1495 |
35,83 |
0,1306 |
-3,32 |
|
Болезни органов пищеварения |
K |
2054 |
34,68 |
0,1359 |
5,73 |
|
Травмы, отравления |
S-T |
5567 |
34,14 |
0,1306 |
-12,05 |
|
Все причины |
A-Z |
28831 |
35,75 |
0,1335 |
9,92 |
Для смертности от инфекционных и паразитарных болезней (рубрики МКБ-10: A-B), болезней органов дыхания (J), а также от травм, отравлений и других внешних воздействий (S-T) достаточные условия наблюдения радиационного риска в рамках ЛБП модели (3) отсутствуют, так как величина дозовой невязки C <0.
Для смертности от солидных ЗНО (рубрики МКБ-10: C00-C80), болезней системы кровообращения (I) и болезней органов пищеварения (K) достаточные условия наблюдения радиационного риска в рамках ЛБП модели (3) выполняются, так как величина C >0.
Для остальных исследованных конкретных причин смерти, не вошедших в табл. 1, число зарегистрированных случаев смерти составляло от 13 до 450 на одну группу болезней или иных причин смерти, и соответствующие радиационные риски смертности обнаружены не были ( C <0).
Для смертности от всех причин (последняя строка табл. 1) радиационный риск также наблюдался, так как 65% всех случаев смерти составили смерти от солидных ЗНО, болезней системы кровообращения и органов пищеварения. В среднем за весь период наблюдения величина C =9,92.
Важной характеристикой радиационного риска является не только форма его зависимости от дозы облучения, которая в данной работе принята в виде ЛБП модели (3), но и его зави- симость от времени после облучения, возраста при облучении и достигнутого возраста. Исследование зависимости радиационного риска от времени после облучения может включать, в частности, и определение латентного периода для этого риска (периода времени после облучения, в течение которого доза облучения не влияет на наблюдаемый показатель смертности).
Рассмотрим, с точки зрения достаточного критерия (12) для существования радиационного риска, зависимость риска от времени после облучения, отсчитывая последнее от начала работы ликвидатора в зоне аварии. Для этого суммирование по формуле (12) надо провести по всем стратам, кроме интервалов времени от начала работ, т.е. по 12-ти интервалам возраста на момент начала работ и по 20-ти интервалам достигнутого возраста. В результате величину дозовой невязки C можно представить графиком её зависимости от времени после облучения.
Для смертности от инфекционных и паразитарных болезней (A-B) и от болезней органов дыхания (J) значения дозовой невязки C случайным образом меняются от положительных к отрицательным значениям, не проявляя какой-либо временной закономерности, и в среднем имея небольшое отрицательное значение (табл. 1). Можно считать, что для смертности от инфекционных и паразитарных болезней и от болезней органов дыхания радиационный риск отсутствует.
Для смертности от солидных ЗНО (рубрики МКБ-10: C00-C80), болезней системы кровообращения (I) и болезней органов пищеварения (K) графики зависимости дозовой невязки C от времени после облучения приведены на рис. 1-6, где пунктирными линиями дополнительно показаны соответствующие сглаженные регрессионные зависимости. Значения C приведены для 3-летних интервалов наблюдения и накопленным итогом по времени наблюдения. Точки привязки графиков по оси времени определены, соответственно, по началу 3-летних интервалов наблюдения (0-2 года, 3-5 лет, 6-8 лет и т.д.) и по окончанию интервалов наблюдения (0-3 года, 0-6 лет, 0-9 лет и т.д.). Интервал времени 33-35 лет не всегда содержал случаи смерти, а их число было в сотни раз меньше, чем в других интервалах времени после облучения, поэтому этот интервал времени не показан на графиках и не включался в расчёт критерия радиационного риска (12). Порядок расположения рисунков соответствует порядку строк в табл. 1 для удобства соотнесения результатов анализа.
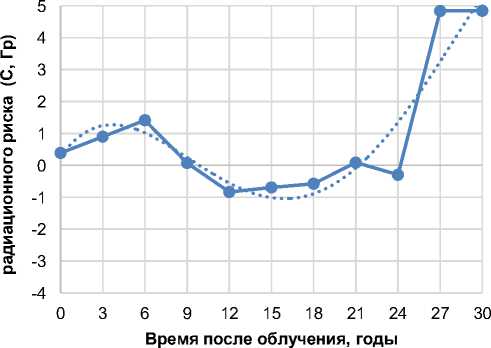
Рис. 1. Критерий радиационного риска для смертности от солидных ЗНО
(рубрика диагнозов МКБ-10: С00-С80.9) для 3-летних интервалов наблюдения.
Рис. 1 и 2 демонстрируют двухфазную кривую для радиационного риска смертности от солидных ЗНО (группа диагнозов МКБ-10: С00-С80.9): в первые 9 лет после облучения, а затем – только после 24 лет после облучения. Такая временная зависимость радиационного риска солидных ЗНО получена впервые в радиационной эпидемиологии, так как японская когорта LSS, по объективным причинам, начала исследоваться спустя 5 лет после облучения [1], и оценка радиационных рисков рака в когорте НРЭР также традиционно проводилась с этим 5-летним лагом [17, 18]. Двухфазность радиационного риска смертности от солидных раков требует дальнейшего исследования в более полном объёме, с использованием оценок максимального правдоподобия, поскольку введённый в данной работе пороговый критерий (12) является достаточным условием того, что точечная оценка ERR >0, но статистическую значимость оценки ERR критерий C в виде (12) не определяет. Кроме того, в связи с возможным наличием радиационного риска смертности от рака в первые 9 лет после облучения, требуется сравнительное исследование локализаций рака, относящихся к этому периоду, и локализаций, относящихся к времени 24 года после облучения и позже.
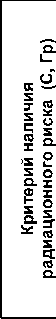
0 3 6 9 12 15 18 21 24 27 30 33
Время после облучения, годы
Рис. 2. Критерий радиационного риска для смертности от солидных ЗНО (рубрика диагнозов МКБ-10: С00-С80.9) накопленным итогом по времени после облучения.
Рис. 3 и 4 демонстрируют, что радиационный риск смертности от болезней системы кровообращения (группа диагнозов МКБ-10: I) устойчиво может наблюдаться уже через 2-3 года после облучения и сохраняется на протяжении, как минимум, 30-ти лет.
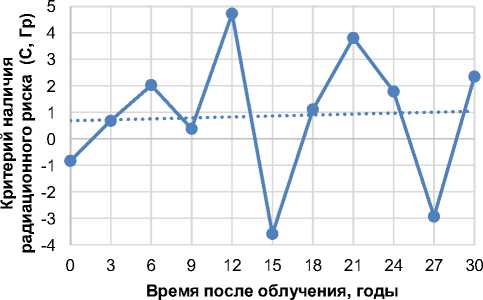
Рис. 3. Критерий радиационного риска для смертности от болезней системы кровообращения (рубрика диагнозов МКБ-10: I) для 3-летних интервалов наблюдения.
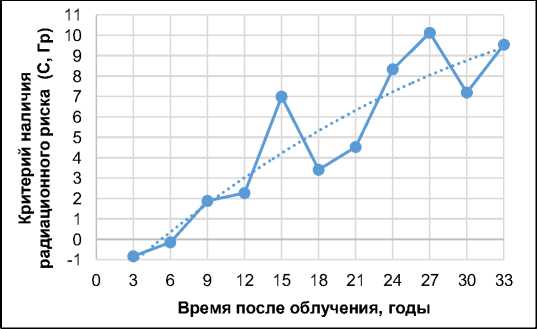
Рис. 4. Критерий радиационного риска для смертности от болезней системы кровообращения (рубрика диагнозов МКБ-10: I) накопленным итогом по времени после облучения.
Достаточный критерий наблюдения радиационного риска смертности от болезней органов пищеварения (группа диагнозов МКБ-10: K) выполняется в среднем за весь период наблюдения
(табл. 1), но рис. 5 и 6 показывают, что первые 8 лет после облучения могут быть отнесены к латентному периоду радиационно-обусловленной смертности от болезней органов пищеварения.
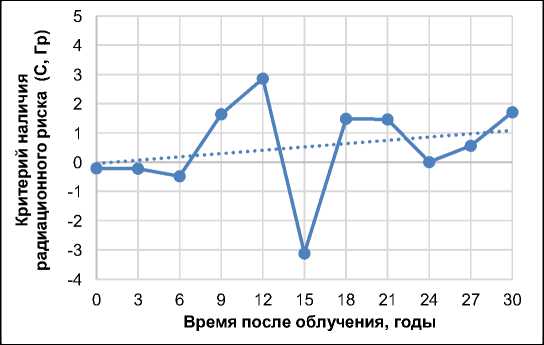
Рис. 5. Критерий радиационного риска для смертности от болезней органов пищеварения (рубрика диагнозов МКБ-10: K) для 3-летних интервалов наблюдения.
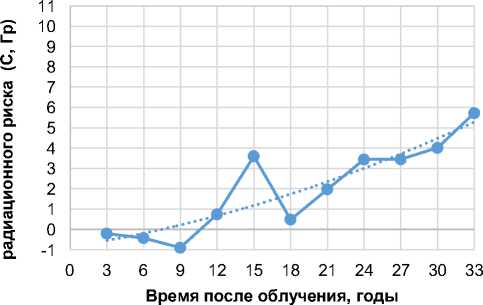
Рис. 6. Критерий радиационного риска для смертности от болезней органов пищеварения (рубрика диагнозов МКБ-10: K) накопленным итогом по времени после облучения.
Для смертности от травм, отравлений и других внешних воздействий (группа диагнозов МКБ-10: S-T) наблюдалось устойчивое нахождение величины C в области отрицательных значений. Это означает, что при одинаковых возрастах при облучении и одинаковых достигнутых возрастах ликвидаторы, получившие большие дозы облучения, впоследствии имели меньшую смертность от травм и отравлений. Вероятно, такой эффект является опосредованным и требует дальнейшего изучения.
Положительное значение итоговой дозовой невязки C для смертности от всех причин (табл. 1) определяется, в основном, вкладами от болезней системы кровообращения и от солидных ЗНО.
Следует отметить, что значения дозовой невязки C в табл. 1 менялись несущественно (в пределах 10% от исходной табличной величины) при значительном (в несколько раз) изменении ширины интервалов разбиения данных для осуществления суммирования в формуле (12), и не меняли знак. В этом смысле критерий (12) является достаточно робастным (устойчивым) по отношению к разбиению данных на подгруппы.
Критерий (12) определяет достаточное условие, при котором точечная оценка коэффициента ERR в модели риска (3) больше нуля для конкретного набора когортных данных. Если обобщать критерий (12) в статистическом смысле, то дозовую не в язку C надо считать случайной величиной. Исследование статистического распределения величины дозовой невязки C необходимо для использования её в качестве статистики и для выработки статистического критерия отрицания нулевой гипотезы (гипотезы об отсутствии радиационного риска). Хотя единственной случайной величиной, входящей в формулу C , является время до наступления события, статистическое распределение величины C , по-видимому, можно получить только методами имитационного моделирования для конкретной когорты наблюдения с конкретным набором индивидуальных доз облучения.
Заключение
Радиационные риски смертности от солидных ЗНО и болезней системы кровообращения в когорте ликвидаторов, зарегистрированных в НРЭР, уже оценивались более подробно [9-12, 17, 18]. Соответствующие большие значения дозовой невязки C =10,18 Гр и C =9,54 Гр (табл. 1) можно рассматривать как дополнительную верификацию существования этих радиационных рисков.
Использование разработанного порогового критерия (12) позволило сформулировать две новые гипотезы о моделях радиационных рисков смертности человека.
-
1) Для радиационного риска смертности от солидных ЗНО впервые показано существование двух временных фаз реализации этого стохастического эффекта (до 9 лет и свыше 24 лет после облучения), отображаемых на рис. 2 графиком зависимости величины C от времени после облучения. Необходима дальнейшая проверка статистической значимости наблюдаемой зависимости риска от времени.
-
2) Впервые показано существование радиационного риска смертности от болезней органов пищеварения. Величина дозовой невязки C =5,73 Гр (табл. 1) указывает на существование
радиационного риска смертности от этих болезней, а рис. 5 – на наличие латентного периода риска порядка 9 лет. Количественная оценка радиационного риска и заключение о его статистической значимости должны быть получены в дальнейших исследованиях.
Таким образом, разработанный пороговый критерий (12) достаточности существования радиационного риска, определяемого в рамках линейной мультипликативной модели (3) по данным когортных наблюдений, показал свою полезность при исследовании когорты ликвидаторов НРЭР.
Дополнительные исследования вероятностного распределения дозовой невязки C требуются для её использования в качестве статистики при проверке нулевой гипотезы об отсутствии радиационных рисков.
Список литературы Верификация радиационных рисков смертности российских участников ликвидации последствий аварии на Чернобыльской АЭС на основе дозового критерия
- Preston D.L., Kato H., Kopecky K.J., Fujita S. Studies of the mortality of A-bomb survivors: 8. Cancer mortality, 1950-1982 //Radiat. Res. 1987. V. 111, N 1. P. 151-178.
- Pierce D.A., Shimizu Y., Preston D.L., Vaeth M., Mabuchi K. Studies of the mortality of atomic bomb survivors. Report 12, Part I. Cancer: 1950-1990 //Radiat. Res. 1996. V. 146, N 1. P. 1-27.
- Shimizu Y., Kato H., Schull W.J., Hoel D.G. Studies of the mortality of A-bomb survivors. 9. Mortality, 1950-1985: Part 3. Noncancer mortality based on the revised doses (DS86) //Radiat. Res. 1992. V. 130, N 2. P. 249-266.
- Stewart A.M., Kneale G.W. A-bomb survivors: factors that may lead to a re-assessment of the radiation hazard //Int. J. Epidemiol. 2000. V. 29, N 4. P. 708-714.
- Preston D.L, Shimizu Y., Pierce D.A., Suyama A., Mabuchi K. Studies of mortality of atomic bomb survivors. Report 13: solid cancer and noncancer disease mortality: 1950-1997 //Radiat. Res. 2012. V. 178, N 2. P. 146-172.
- Shimizu Y., Kodama K., Nishi N., Kasagi F., Suyama A., Soda M., Grant E.J., Sugiyama H., Sakata R., Moriwaki H., Hayashi M., Konda M., Shore R.E. Radiation exposure and circulatory disease risk: Hiroshima and Nagasaki atomic bomb survivor data, 1950-2003 //BMJ. 2010. V. 340. P. b5349.
- Ozasa K., Shimizu Y., Suyama A., Kasagi F., Soda M., Grant E.J., Sakata R., Sugiyama H., Kodama K. Studies of the mortality of atomic bomb survivors, Report 14, 1950-2003: an overview of cancer and noncancer diseases //Radiat. Res. 2012. V. 177, N 3. P. 229-243.
- Takahashi I., Abbott R.D., Ohshita T., Takahashi T., Ozasa K., Akahoshi M., Fujiwara S., Kodama K., Matsumoto M. A prospective follow-up study of the association of radiation exposure with fatal and non-fatal stroke among atomic bomb survivors in Hiroshima and Nagasaki (1980-2003) //BMJ Open. 2012. V. 2, N 1. P. e000654.
- Ivanov V.K., Gorsky A.I., Maksioutov M.A, Tsyb A.F., Souchkevitch G.N. Mortality among the Chernobyl emergency workers: estimation of radiation risks (preliminary analysis) //Health Phys. 2001. V. 81, N 5. P. 514-521.
- Kashcheev V.V., Chekin S.Y., Maksioutov M.A, Tumanov K.A., Menyaylo A.N., Kochergina E.V., Kashcheeva P.V., Gorsky A.I., Shchukina N.V, Karpenko S.V., Ivanov V.K. Radiation-epidemiological study of cerebrovascular diseases in the cohort of Russian recovery operation workers of the Chernobyl accident //Health Phys. 2016. V. 111, N 2. P. 192-197.
- Kashcheev V.V., Chekin S.Y., Karpenko S.V., Maksioutov M.A, Menyaylo A.N., Tumanov K.A., Kochergina E.V., Kashcheeva P.V., Gorsky A.I., Shchukina N.V, Lovachev S.S., Vlasov O.K., Ivanov V.K. Radiation risk of cardiovascular diseases in the cohort of Russian emergency workers of the Chernobyl accident //Health Phys. 2017. V. 113, N 1. P. 23-29.
- Иванов В.К., Чекин С.Ю., Максютов М.А., Кащеев В.В., Карпенко С.В., Туманов К.А., Корело А.М., Кочергина Е.В., Власов О.К., Щукина Н.В. Радиационный риск заболеваемости гипертензиями сре-ди российских участников ликвидации аварии на Чернобыльской АЭС //Медицинская радиология и радиационная безопасность. 2017. Т. 62, № 1. С. 32-37.
- Little M.P. Cancer and non-cancer effects in Japanese atomic bomb survivors //J. Radiol. Prot. 2009. V. 29, N 2A. P. A43-A59.
- Медицинские радиологические последствия Чернобыля: прогноз и фактические данные спустя 30 лет /Под общей ред. чл.-корр. РАН В.К. Иванова, чл.-корр. РАН А.Д. Каприна. М.: ГЕОС, 2015. 450 с.
- International Statistical Classification of Diseases and Related Health Problems 10th Revision. ICD-10 Version 2019. [Электронный ресурс]. URL: https://icd.who.int/browse10/2019/en (дата обращения 10.08.2020).
- The R Project for Statistical Computing. [Электронный ресурс]. URL: https://www.r-project.org/ (дата обращения 10.08.2020).
- Иванов В.К., Карпенко С.В., Кащеев В.В., Чекин С.Ю., Максютов М.А., Туманов К.А., Щукина Н.В., Кочергина Е.В., Зеленская Н.С., Лашкова О.Е. Радиационные риски российских участников ликвидации последствий аварии на Чернобыльской АЭС за период 1992-2017 гг. Часть I: заболеваемость солидными раками //Радиация и риск. 2019. Т. 28, № 4. C. 16-30.
- Иванов В.К., Карпенко С.В., Кащеев В.В., Чекин С.Ю., Максютов М.А., Туманов К.А., Щукина Н.В., Кочергина Е.В., Зеленская Н.С., Лашкова О.Е., Иванов С.А., Каприн А.Д. Радиационные риски российских участников ликвидации последствий аварии на Чернобыльской АЭС за период 1992-2017 гг. Часть II: смертность от солидных раков //Радиация и риск. 2020. Т. 29, № 1. С. 18-31.


