Верификация стромального клеточного фактора SDF-1 в гравидарном эндометрии при неразвивающейся беременности после применения технологий экстракорпорального оплодотворения
Автор: Траль Татьяна Георгиевна, Толибова Гулрухсор Хайбуллоевна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.30, 2022 года.
Бесплатный доступ
Иммунологический фактор в генезе репродуктивных потерь, в том числе при использовании технологий экстракорпорального оплодотворения, остается не до конца ясным в связи с множественными патогенетическими механизмами иммунологических взаимодействий в системе мать-плацента-плод. Цель настоящего исследования заключается в изучении особенности экспрессии стромального клеточного фактора SDF-1 (stromal cell-derived factor) в гравидарном эндометрии при неразвивающейся беременности при использовании технологий экстракорпорального оплодотворения. Исследовали абортивный материал 5-8 недель при использовании технологий экстракорпорального оплодотворения с разными вариантами гравидарной трансформации. Всего исследовано 92 образца, из них 77 - абортивный материал неразвивающейся беременности после использования технологий экстракорпорального оплодотворения и 15 - образцы абортивного материала при беременности, прерванной по желанию женщины хирургическим путем. Выполнено гистологическое исследование окраской гематоксилином и эозином с описанием вариантов гравидарной трансформации стромы и желез эндометрия и иммуногистохимическое исследование фактора SDF-1 в гравидарном эндометрии обследованных групп. Исходя из гистологической картины, в зависимости от морфологического варианта гравидарной трансформации эндометрия было сформировано 5 групп случаев: полноценная гравидарная трансформация стромы и желез эндометрия и стромы с железами секреторного типа; неполноценная гравидарная трансформация стромы с железами секреторного типа, пролиферативного типа, с обоими типами и контрольная группа наблюдений. Методом морфометрии определяли площадь экспрессии маркера в гравидарном эндометрии (железах и строме). Результаты исследования показали достоверное снижение экспрессии SDF-1 в железах компактного слоя гравидарного эндометрия независимо от вариантов его трансформации после использования технологий экстракорпорального оплодотворения, что вероятно связано с нарушением синтеза хемокина SDF-1 гландулоцитами еще на этапе циклической трансформации эндометрия. Достоверное повышение экспрессии SDF-1 в строме гравидарного эндометрия обусловлено исходным нарушением морфофункционального состояния эндометрия у пациенток с бесплодием. Верификация стромального клеточного фактора в эндометрии на этапе прегравидарной подготовки позволит скорректировать подготовительный этап применения технологий экстракорпорального оплодотворения для пациенток с эндометриальной дисфункцией.
Эндометрий, стромальный клеточный фактор, sdf-1, неразвивающаяся беременность, экстракорпоральное оплодотворение
Короткий адрес: https://sciup.org/143178623
IDR: 143178623
Verification of the stromal cell factor SDF-1 in the gravidar endometrium in missed miscarriage after the use of in vitro fertilization technologies
The immunological factor in the genesis of reproductive losses, including the use of in vitro fertilization technologies, remains not completely clear due to the multiple pathogenetic mechanisms of immunological interactions in the mother-placenta-fetus system. The purpose of this study is to study the expression of the factor SDF-1 (stromal cell-derived factor) in the endometrium during missed miscarriage using in vitro fertilization technologies. Abortive material 5-8 weeks' old was studied using in vitro fertilization technologies with different variants of gravidar transformation of the endometrium. A total of 92 samples were studied, of which 77 were abortive material from a missed miscarriage after the use of in vitro fertilization technologies and 15 were samples of abortive material from a pregnancy terminated surgically. A histological study was performed by staining with hematoxylin and eosin with a description of the variants of gravidar transformation of the stroma and endometrial glands and an immunohistochemical study of the SDF-1 factor in the endometrium of the examined groups. Based on the histological picture, depending on the morphological variant of the transformation of the endometrium, 5 groups of cases were formed: complete transformation of the stroma and glands of the endometrium and stroma with glands of the secretory type; incomplete transformation of the stroma with glands of the secretory type, proliferative type, with both types and the control group of observations. The expression area of the marker in the endometrium (glands and stroma) was determined by morphometry. The results of the study showed a significant decrease in the expression of SDF-1 in the glands of the compact layer of the endometrium, regardless of the options for its transformation after the use of in vitro fertilization technologies, which is probably associated with a violation of the synthesis of the SDF-1 chemokine by glandulocytes at the stage of cyclic transformation of the endometrium. A significant increase in the expression of SDF-1 in the stroma of the endometrium is due to the initial violation of the its morphological and functional state in patients with infertility. Verification of stromal cell factor in the endometrium at the stage of pregravidar preparation will allow to correct this stage of the application of in vitro fertilization technologies for patients with endometrial dysfunction.
Текст научной статьи Верификация стромального клеточного фактора SDF-1 в гравидарном эндометрии при неразвивающейся беременности после применения технологий экстракорпорального оплодотворения
Введение . Репродуктивные потери первого триместра остаются актуальной проблемой современного общества. К сожалению, следует признать, что, несмотря на определенные успехи и внедрение новых технологий в репродуктивную медицину, частота репродуктивных потерь достигает 20% с преобладанием неразвивающейся беременности, как при естественно наступившей беременности, так и при беременности после экстракорпорального оплодотворения (далее – ЭКО), не имея тенденции к снижению [1-4]. Полиэтиологичность ранних самопроизвольных выкидышей не вызывает сомнений [5-6] и большая часть их этиологических аспектов хорошо изучена, однако влияние иммунологического фактора в генезе репродуктивных потерь остается не до конца ясным в связи с множественными патогенетическими механизмами иммунологических взаимодействий в системе мать-плацента-плод [7-11].
Последние годы особую роль в патогенезе репродуктивных потерь отводят хе-мокинам. В эксперименте как in vitro, так и in vivo показано, что хемокины участвуют в гра-видарной трансформации эндометрия и успешной инвазии трофобласта в комплексе с другими медиаторами [12-13]. Показано, что процесс инвазии трофобласта, обусловленный полноценным взаимодействием бластоцисты и эндометрия, является приоритетным моментом последующего развития беременности и особая роль отводится молекулам фактора CXCL12 (SDF-1 - Stromal cell-derived factor-1), синтезируемому клетками трофобласта и эндометрия, как фактору, потенцирующему восприимчивость эндометрия к наступлению и развитию беременности [1417]. В эксперименте на модели животных также продемонстрирована значимость CXCL12, как фактора, принимающего непосредственное участие в прегравидарной подготовке эндометрия и процессов нидации эмбриона [18].
Цель исследования: изучить особенности экспрессии стромального клеточного фактора SDF-1 в гравидарном эндометрии при неразвивающейся беременности после применения технологий экстракорпорального оплодотворения.
Материалы и методы исследования. Гистологическое и иммуногистохимическое исследование проведено на отобранных к исследованию 92 образцах абортивного материала, поступившего в патологоанатомическое отделение Научно-исследовательского института акушерства, гинекологии и репро-дуктологии имени Д.О. Отта, 77 образцах абортивного материала после неразвиваю-щейся беременности наступившей после применения ЭКО (5-8 недель) и 15 образцах абортивного материала развивающейся беременности, прерванной хирургическим путем (5-8 недель). Операционный материал фиксировали в 10% нейтральном формалине, далее обезвоживали в гистологическом процессоре в спиртах нарастающей концентрации, заливали в парафин и изготавливали срезы толщиной 3-4 мкм. После депарафинирования окрашивали препараты гематоксилином и эозином. При световой микроскопии (увеличениях ×100, ×200, ×400) оценивали полноценность изменений стромы и желез эндометрия (компактного и спонгиоз-ного слоев), состояние клубков спиральных артерий, степени трофобластической инвазии в зоне плацентарного ложа. Иммуногистохимическое исследование проводили на парафиновых срезах. В качестве системы визуализации использовали Abcam Mouse and Rabbit Specific HRP Plus (ABC) Detection IHC Kit (RTU)[ab93697], (Abcam, Великобритания). Для проведения иммуногистохимической реакции использовали одноэтапный протокол с демаскировкой антигена. Оценку экспрессии клеточного стромального фактора проводили с использованием первичных поликлональных кроличьих антител к Anti-SDF1 [клон ab 9797] в стандартном разведении (1:100) производства Abcam (Великобри- тания). Визуализацию экспрессии SDF 1 проводили на микроскопе Olympus BX46 и программного обеспечения «CellSens 47 Entry». Экспрессию изучаемого маркера рассчитывали с помощью программы ВидеоТест-Морфология 5.2 (Россия) на 5 микрофотографиях с каждого микропрепарата. Параметры распределения в выборках оценивали с помощью критерия Колмогорова– Смирнова. Данные представлены в виде среднего и 95% доверительного интервала -М (95% ДИ). Для определения статистически значимых различий между количественными параметрами нормально распределенных данных исследуемых групп использовали однофакторный дисперсионный анализ (ANOVA) с расчетом 95% доверительного интервала. Различия считали значимыми при p<0,05.
Результаты исследования и обсуждение. Результаты гистологического исследования показали, что гравидарная трансформация эндометрия неразвивающейся беременности после применения ЭКО характеризуется полиморфными вариантами. Исходя из гистологической картины, в зависимости от морфологического варианта гравидарной трансформации эндометрия было сформировано 5 групп: I группа - полноценная гра-видарная трансформация стромы и желез эндометрия (n=20); II группа - полноценная гравидарная трансформация стромы с железами секреторного типа (n=15); III группа -неполноценная гравидарная трансформация стромы с железами секреторного типа (n=15); IV группа - неполноценная гравидарная трансформация стромы с железами пролиферативного типа (n=15); V группа - неполноценная секреторная трансформация с железами секреторного и пролиферативного типа (n =12) и контрольная группа (n =15).
Полноценная гравидарная трансформация эндометрия контрольной группы и I группы имела сходные и черты и была представлена зрелыми децидуоцитами, формирующими эпителиальный пласт и щелевидными железами с низким кубическим эпителием. Клубки спиральных артерий крупные, толстостенные, инвазия трофобласта в зоне плацентарного ложа была умеренной.
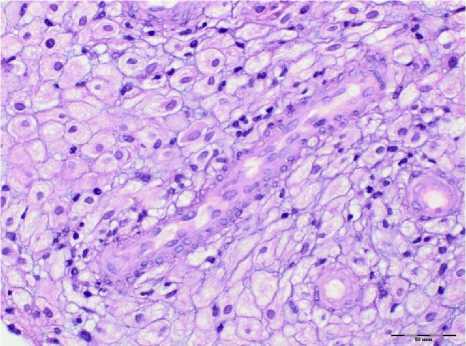
Рис. 1. Полноценная трансформация желез и стромы эндометрия при неразвива-ющейся беременности. Окр.: гематокси-лином-эозином. Ув.: х400.
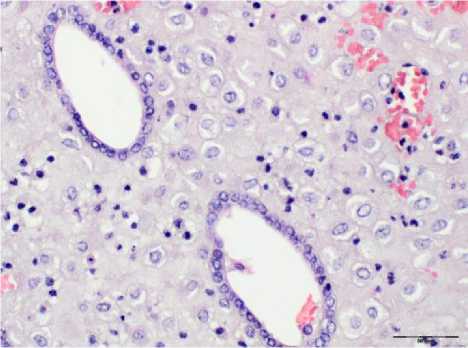
Рис. 2. Полноценная трансформация желез и стромы эндометрия при неразвива-ющейся беременности после ЭКО. Окр.: гематоксилином-эозином. Ув.: х400.
Гравидарный эндометрий II группы также характеризовался полноценной трансформацией, однако железы соответствовали секреторной фазе цикла с пузырьковидными ядрами, высоким призматическим эпителием и апокриновой секрецией. Изменений со стороны клубков спиральных артерий и инвазии трофобласта не выявлено. Неполноценная гравидарная трансформация эндометрия III группы была представлена незрелыми деци-дуоцитами звездчатой формы, расположенными разрозненно в отечной строме с наличием плазмоцитарно-моноцитарной инфильтрации разной степени выраженности. Железы эндометрия имели черты секреторной фазы цикла. Клубки спиральных артерий были развиты слабо, наблюдалась умеренная или слабая инвазия трофобласта в зоне плацентарного ложа.
В IV группе исследования строма состояла из предецидуальных клеток и незрелых децидуоцитов с отеком и инфильтрацией клетки мононуклеарной ряда. Железы эндометрия были тубулярного или слабо извитого строения с пикнотическим ядром, слабо раз- витой цитоплазмой с ровным апикальным краем, клубки спиральных артерий недоразвиты, инвазия трофобласта слабая. В V группе в отечной неполноценной гравидарно измененной строме определялись железы, соответствующие секреторной и пролиферативной фазе цикла с тонкостенными мелкими клубками спиральных артерий и слабой инвазией трофобласта в зоне плацентарного ложа.
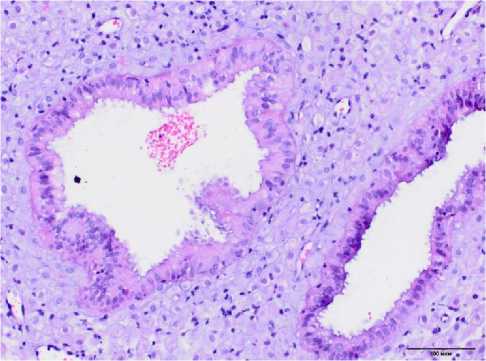
Рис. 3. Полноценная трансформация стромы эндометрия с железами секреторного типа при неразвивающейся беременности после ЭКО. Окр.: гематоксилином-эозином. Ув.: х400.
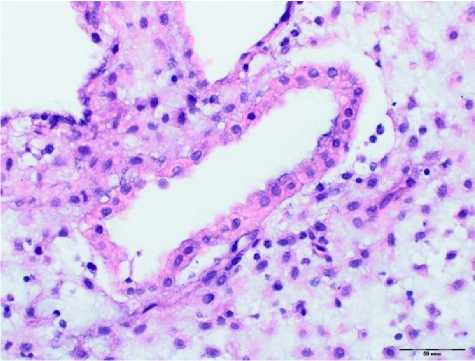
Рис. 4. Неполноценная трансформация стромы эндометрия с железами секреторного типа при неразвивающейся беременности после ЭКО. Окр.: гематоксилином-эозином. Ув.: х400.
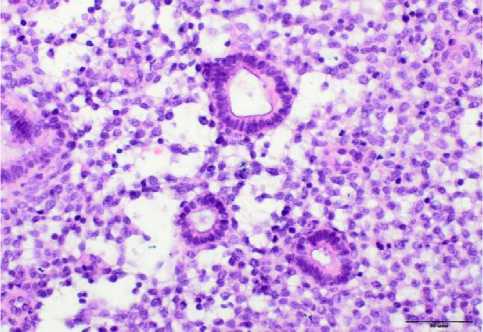
Рис. 5. Неполноценная трансформация стромы эндометрия с железами пролиферативного типа при неразвивающейся беременности после ЭКО. Окр.: гематоксили-ном-эозином. Ув.: х400.
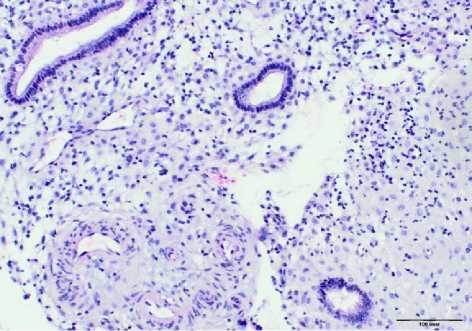
Рис. 6. Неполноценная трансформация стромы эндометрия с железами секреторного и пролиферативного типа при нераз-вивающейся беременности после ЭКО. Окр.: гематоксилином-эозином. Ув.: х400.
Результаты иммуногистохимического исследования показали снижение экспрессии SDF-1 в железах гравидарного эндометрия при неразвивающейся беременно- сти после ЭКО по сравнению с контрольной группой (табл. 1).
Достоверное снижение экспрессии SDF-1 в железах гравидарного эндометрия при неразвивающейся беременности после ЭКО по сравнению с контрольной группой верифицировано во II группе при полноценной гравидарной трансформации стромы с железами секреторного типа (p<0,001), IV группе при неполноценной гравидарной трансформации стромы с железами пролиферативного типа (p<0,001) и V группе с неполноценной гравидарной трансформации с железами секреторного и пролиферативного типа (p<0,001).
Сравнение внутри групп показало, что в эндометрии IV группы (неполноценная гравидарная трансформация стромы и
Таблица 1
Экспрессия стромального клеточного фактора в железах гравидарного эндометрия M(95% ДИ)/M(95% CI)
|
Группы/Groups |
Среднее значение/ Average meaning |
95% доверительный интервал для среднего значения/95% confidence interval for mean |
F-statistics ANOVA |
|
|
Нижняя граница/ Lower bound |
Верхняя граница / Upper bound |
|||
|
Контрольная (n=15) |
22,43 |
20,99 |
23,87 |
14,455 |
|
I группа (n=20) |
20,32 |
16,97 |
23,66 |
|
|
II группа (n=15) |
15,17 |
13,64 |
16,70 |
|
|
III группа (n=15) |
18,57 |
16,06 |
21,07 |
|
|
IV группа (n=15) |
10,43 |
9,35 |
11,52 |
|
|
V группа (n=12) |
16,11 |
14,71 |
17,52 |
|
Примечание: k - контрольная группа; pk-1=1,000; pk-2<0,001; pk-3=0,381; pk-4<0,001; pk-5<0,001; p1- 2 =0,034; p 1-3 =1,000; p1 ~ 4 ~ <0,001; p 1- 5=0,143; p2 ~ 3=1,000; p2 — 4=0,028; p2 — 5=1,000; p3 — 4<0,001; p3 — 5=1,000; p4 - 5=0,020.
При оценке экспрессии маркера в стромальном компоненте гравидарного эндометрия верифицировано достоверное повышение в I группе при полноценной гравидарной трансформации желез и стромы эндометрия (p<0,001), а также достоверное снижение экспрессии во II группе при наличии желез секреторного типа (p<0,055) по сравнению с контрольной группой (табл. 2).
Экспрессия SDF-1 в полноценном гравидарном эндометрии была достоверно выше в I группе по сравнению с II, III и V группами (p<0,001). Во II группе с полноценной гравидарной трансформацией стромы и железами секреторного типа экспрессия данного маркера была достоверно железы пролиферативного типа) отмечается достоверное снижение экспрессии маркера (p<0,001) по сравнению с I группой (полноценная гравидарная трансформация стромы и желез). Аналогичные данные получены при сопоставлении III и IV групп. Снижение экспрессии SDF-1 в железах гравидарного эндометрия после ЭКО, вероятно, связано с нарушением его синтеза гранулоцитами еще на этапе циклической трансформации эндометрия, что согласуется с данными Tsutsumi et al [19].
ниже по сравнению с III и IV группой (р<0,001).
Полученные результаты сравнения внутри групп позволяют сделать вывод о том, что достоверное повышение экспрессии SDF-1 в абортивном материале после ЭКО связано с неполноценной гравидар-ной трансформацией желез и стромы, а также слабым развитием клубков спиральных артерий и нарушением процессов инвазии трофобласта в зоне плацентарного ложа. Несмотря на полноценность грави-дарных изменений в I группе, также выявлено достоверно повышение экспрессии при сравнении с контрольной группой, что свидетельствует о нарушениях рецепторного профиля в эндометрии [20].
Таблица 2
Экспрессия стромального клеточного фактора в строме гравидарного эндометрия M(95% ДИ)/M(95% CI)
|
Группы/Groups |
Среднее значение/ Average meaning |
95% доверительный интервал для среднего значения/95% confidence interval for mean |
F-statistics ANOVA |
|
|
Нижняя граница/ Lower bound |
Верхняя граница / Upper bound |
|||
|
Контрольная (n=15) |
26,19 |
24,13 |
28,25 |
14,455 |
|
I группа (n=20) |
40,05 |
35,79 |
44,31 |
|
|
II группа (n=15) |
21,30 |
18,91 |
22,77 |
|
|
III группа (n=15) |
29,39 |
26,61 |
32,17 |
|
|
IV группа (n=15) |
33,18 |
30,72 |
35,64 |
|
|
V группа (n=12) |
28,27 |
26,61 |
30,89 |
|
Примечание: k - контрольная группа; pk - 1<0,001; pk-2<0,055; pk-3=1,000; pk-4=0,025; pk-5=1,000; p1-2<0,001; p 1- 3<0,001; p 1- 4=0,031; p 1- 5<0,001; p2 -3 <0,001; p2 - 4<0,001; p2 - 5=0,003; p 3- 4=1,000; p 3- 5=1,000; p4 -5 =0,619.
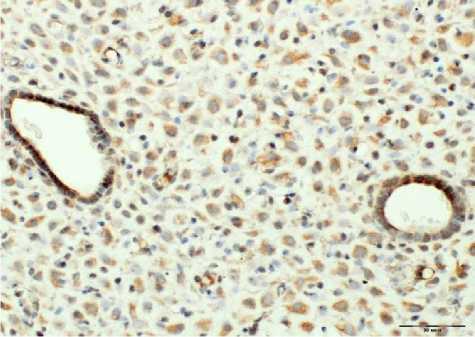
Рис. 11. Экспрессия SDF-1 в неполноценной трансформированной строме с железами пролиферативного типа при нераз-вивающейся беременности после ЭКО. Ув.: х400.
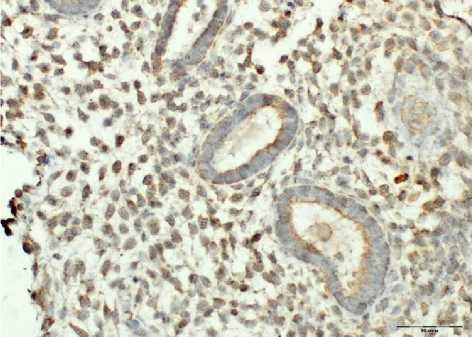
Рис. 12. Экспрессия SDF-1 в не полноценной трансформированной строме с железами секреторного и пролиферативного типа при неразвивающейся беременности после ЭКО. Ув.: х400.
Гинекологический статус пациенток, планирующих протокол ЭКО, указывает на высокую частоту воспалительных заболеваний полости матки с развитием гипоксии эндометрия, активацией патологического неоангиогенеза и последующим формированием эндометриальной дисфункции [21-24].
Стромальный клеточный фактор кроме непосредственно контроля инвазии трофобласта сопровождает и моделирует процессы ангиогенеза в эндометрии. Повышенная секреция SDF-1 связана с повреждением тканей, в том числе, обусловленном гипоксией с последующим замедлением роста и дифференцировки клеток [25]. Полученные нами результаты подтверждают данные исследования и позволяют рассматривать SDF-1 не только как фактор, связанный с нарушением гравидарной трансформации, сосудистой патологией и
Список литературы Верификация стромального клеточного фактора SDF-1 в гравидарном эндометрии при неразвивающейся беременности после применения технологий экстракорпорального оплодотворения
- Adamyan LV, Artymuk AV, Belokrinitskaya TE i dr. Vykidysh v rannie sroki beremennosti: diagnostika i taktika vedeniya. Klinicheskie reko-mendatsii (protokol lecheniya). M., 2016.- 34pp. URL: http://www.consultant.ru/document/cons_doc_LAW_319533/240913a69b434b476239176ef4c4f02fbc6ebcac/ In Russian
- Early Pregnancy Loss. ACOG. Practice Bulletin Number 150, Obstetrics end Gynecology. 2015;125(5):1258-1267. DOI: 10.1097/01.AOG.0000465191.27155.25.
- Molchanova OK, Ordiyants IM, Lutsenko IV, Podstavkina VA. Sovremennye predstavleniya o mole-kulyarnykh mekhanizmakh regulyatsii implantatsii. Akusherstvo i ginekologiya: Novosti. Mneniya. Obuchenie. 2020;8(3-29):106-111. In Russian
- Radzinsky VE, Solovyova AV, Dimitrova VI i dr. Nerazvivayushchayasya beremennost’. 3-e izd. Pod red. V.E. Radzinskogo. M.: GEOTAR-Media, 2019.- 184pp. In Russian
- Klinicheskie rekomendatsii. Akusherstvo i ginekologiya. Izd. 4, pererab. i dop. Pod red. V.N. Serova, G.T. Sukhikh. M.: GEOTAR-Media, 2014.- 1024pp. In Russian
- Carr BR, Blackwell RE. Textbook of Reproductive Medicine. 2nd ed., translated to Russian under the general editorship of I.V. Kuznetsova. M.: Praktika; 2015.- 832pp. In Russian
- Gilbert-Barness E and Debich-Spicer D. Embryo and Fetal Pathology: Color Atlas with Ultrasound Cor-relation. Cambridge, United Kingdom: Cambridge University Press, 2004. 711pp
- Feldt-Rasmussen U, Mathiesen ER. Endocrine disorders in pregnancy: Physiological and hormonal as-pects of pregnancy. Best Pract Res Clin Endocrinol Metab 2011;25:875-84. DOI: 10.1016/j.beem.2011.07.004
- Wang, NF, Kolte AM, Larsen EC et al. Immunologic Abnormalities, Treatments, and Recurrent Preg-nancy Loss: What Is Real and What Is Not? Clin. Obstet Gynecol. 2016;59:509-523. DOI: 10.1097/GRF.0000000000000215
- Kaur R, Gupta K. Endocrine dysfunction and recurrent spontaneous abortion: An overview. Int J Appl Basic Med Res. 2016;6(2):79-83. DOI: 10.4103/2229-516X.179024
- Park SY, Yun S, Ryu BJ, et al. Trophoblasts regulate natural killer cells via control of interleukin-15 receptor signaling. Am J Reprod Immunol. 2017;78(2). DOI: 10.1111/aji.12628
- Mathew DJ, Lucy MC, Geisert D. Interleukins, interferons, and establishment of pregnancy in pigs. Re-production. 2016;151(6):111-122. DOI: 10.1530/REP-16-0047
- Salamonsen LA, Hannan NJ, Dimitriadis E. Cytokines and chemokines during human embryo implan-tation: roles in implantation and early placentation. Semin Reprod Med. 2007;25:437–444. DOI: 10.1055/s-2007-991041
- Milovanov AP. Tsitotrofoblasticheskaya invaziya — vazhneyshiy mekhanizm platsentatsii i progressii beremennosti. Archiv Patologii. 2019;81(4):5-10. DOI:10.17116/patol2019810415. In Russian
- Milovanov AP, Ozhiganova IN. Embriokhorial'naya nedostatochnost': anatomofiziologicheskie predpo-sylki, obosnovanie, definitsii i patogeneticheskie mekhanizmy. Arkhiv patologii. 2014;76(3):4-8. In Rus-sian
- Jaleel MA, Tsai AC, Sarkar S, et al. Stromal cell-derived factor-1 (SDF-1) signalling regulates human placental trophoblast cell survival. Mol Hum Reprod. 2004;10(12):901-909. DOI: 10.1093/molehr/gah118
- Zheng J, Wang H, Zhou W. Modulatory effects of trophoblast-secreted CXCL12 on the migration and invasion of human first-trimester decidual epithelial cells are mediated by CXCR4 rather than CXCR7. Reprod Biol Endocrinol. 2018;16(1):17. DOI: 10.1186/s12958-018-0333-2
- Złotkowska A, Andronowska A. Chemokines as the modulators of endometrial epithelial cells remodel-ing. Sci Rep. 2019;9:12968. DOI: 10.1038/s 41598-019-49502-5
- Tsutsumi A, Okada H, Nakamoto T, et al. Еstrogen induces stromal cell-derived factor 1 (SDF-1/CXCL12) production in human endometrial stromal cells: a possible role of endometrial epithelial cell growth. Fertil Steril. 2011;95(1):444-447. DOI: 10.1016/j.fertnstert.2010.08.037
- Tolibova GH, Tral’ TG, Aylamazyan EK, Kogan IY. Molecularnye mechanismy tsiklicheskoy transfor-matsii endometriya. Zhurnal akusherstva i zhenskikh bolezney. 2019;68(1):5-12. DOI: 10.17816/ JOWD6815-12. In Russian
- Bazina MI, Egorova AT, Khodorovich NA i dr. Khronicheskij endometrit: skrytaya ugroza reproduktsii. Doktor.Ru. Ginekologiya Endokrinologiya. 2015;14:20-27. In Russian
- Sukhikh, GT, Shurshalina AV. Khronicheskij endometrit: rukovodstvo. M.: GEOTAR-Media, 2013.- 64pp. In Russian
- Shurshalina AV. Khronicheskij endometrit kak prichina narushenij reproductivnoj funktsii. Gynecologi-ya. 2014;4:4-6. In Russian
- Tolibova GH, Tral TG, Kleshchev MA. Endometrial’naya disfuktsiya: algoritm klinicheskikh i morfolo-gicheskikh issledovanij: rukovodstvo dlya vrachey. S-Pb., 2016.- 44pp. In Russian
- Zheng N, Chen J, Liu W, et al. Mifepristone Inhibits Ovarian Cancer Metastasis by Intervening in SDF-1/CXCR4 Chemokine Axis. Oncotarget. 2017;8(35):59123-59135. DOI: 10.18632/oncotarget.19289


