ВИЧ-ассоциированная плазмобластная лимфома у беременной: клиническое наблюдение
Автор: Гаркуша Т.А., Алябьев Ф.В., Аршавская М.П., Хорошкина Н.И., Баринов Е.Х.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Морфология. Патология
Статья в выпуске: 5 т.15, 2025 года.
Бесплатный доступ
Плазмобластная лимфома (ПБЛ) – редкая агрессивная В-клеточная лимфома, ассоциированная с состояниями иммунодефицита, в первую очередь с ВИЧ-инфекцией и вирусом Эпштейна – Барр (EBV). Сочетание ПБЛ и беременности представляет казуистическую редкость. В статье представлено клиническое наблюдение пациентки 31 года с ВИЧ-инфекцией IV стадии (клиническая стадия по ВОЗ) без приёма антиретровирусной терапии (АРВТ). На 25–26 неделе беременности у пациентки диагностирована генерализованная форма ПБЛ с поражением кожи, лимфатических узлов, молочных желёз, лёгких, печени и головного мозга. Заболевание сопровождалось диссеминированным туберкулёзом лёгких, цитомегаловирусной инфекцией и завершилось неблагоприятным акушерским исходом – материнской смертью после родоразрешения путём кесарева сечения. Данный случай демонстрирует агрессивность течения ПБЛ на фоне беременности и тяжёлого иммунодефицита, подчеркивая необходимость раннего выявления ВИЧ-инфекции, назначения АРВТ женщинам репродуктивного возраста и важность междисциплинарного подхода при ведении подобных пациенток.
Лимфома плазмобластная [D054405], ВИЧ-инфекции [D015658], осложнения беременности инфекционные [D011251], вирус Эпштейна-Барр [D004854], иммунодефицит [D007153], антиретровирусная терапия [D023241], материнская смертность [D008428], туберкулез [D014376], междисциплинарные исследования [D058025], кесарево сечение [D002585]
Короткий адрес: https://sciup.org/143185338
IDR: 143185338 | УДК: 618.3-06:616.155.392-006.448-022.6:578.828 | DOI: 10.20340/vmi-rvz.2025.5.MORPH.1
HIV-Associated plasmablastic lymphoma in pregnancy: a case report
Plasmablastic lymphoma (PBL) is a rare and aggressive B-cell lymphoma associated with immunodeficiency states, primarily with HIV infection, and Epstein–Barr virus (EBV). The coexistence of PBL and pregnancy represents an exceptional rarity. This article presents a clinical case of a 31-year-old patient with stage IV HIV infection (WHO clinical stage) without antiretroviral therapy (ART). At 25–26 weeks of gestation, the patient was diagnosed with generalized PBL involving the skin, lymph nodes, mammary glands, lungs, liver, and brain. The disease was complicated by disseminated pulmonary tuberculosis and cytomegalovirus infection, and ended with an unfavorable obstetric outcome – maternal death following cesarean section. This case illustrates the aggressiveness of PBL during pregnancy in the setting of profound immunodeficiency, emphasizing the importance of early HIV detection, initiation of ART in women of reproductive age, and a multidisciplinary approach to the management of such patients.
Текст научной статьи ВИЧ-ассоциированная плазмобластная лимфома у беременной: клиническое наблюдение
Плазмобластная лимфома (ПБЛ) — высокоагрессивная В-клеточная лимфома, согласно классификации ВОЗ опухолей кроветворной и лимфоидной тканей (5-е издание, 2022), характеризующаяся плазмобластной/иммунобластной морфологией и фенотипом терминально дифференцированных В-клеток с утратой пан-В-клеточных маркеров [1]. Заболевание тесно ассоциировано с иммунодефицитными состояниями, такими как ВИЧ-инфекция (составляя до 2% всех лимфом у ВИЧ-позитивных пациентов), ятрогенная иммуносупрессия после трансплантации органов, а также с инфицированием вирусом Эпштейна – Барр (EBV), который выявляется в 31–62% случаев [1, 2].
Типичной для ПБЛ является экстранодальная локализация, прежде всего в полости рта. Однако описаны случаи с поражением желудочнокишечного тракта, костей, мягких тканей, кожи и других органов [3, 4]. Морфологически PBL характеризуется деструктивным инфильтратом из крупных плазмобластных и иммунобластных клеток, нередко с рисунком «звёздного неба», выраженной митотической активностью и очагами некроза. Иногда встречаются промежуточные лимфоплаз-мацитоидные клетки и плазмоциты. Клиническое течение отличается быстрым прогрессированием и неблагоприятным прогнозом: медиана общей выживаемости даже на фоне полихимиотерапии составляет от 6 до 32 месяцев [1, 5].
Характерными признаками являются экспрессия антигенов, ассоциированных с плазматическими клетками (CD138, CD38, MUM1/IRF4, BLIMP1, XBP1), и отсутствие экспрессии CD20, PAX5 и ALK. Приблизительно в 60% случаев выявляется EBV (EBER)-позитивность. Индекс пролиферации Ki-67, как правило, превышает 90%.
Отягощающими факторами являются высокий международный прогностический индекс, распространённая стадия заболевания и перестройки гена MYC.
Возникновение ПБЛ во время беременности описано в единичных случаях [6]. Ведение таких пациенток представляет чрезвычайную сложность, обусловленную необходимостью баланса между агрессивным лечением лимфомы, потенциальной тератогенностью химиотерапевтических препаратов и сохранением жизни и здоровья матери и плода.
Целью настоящей публикации является представление редкого клинического случая ВИЧ-ассоциированной генерализованной плазмобластной лимфомы у беременной, обсуждение диагностических и терапевтических сложностей, а также акцентирование важности прегравидарной подготовки и раннего назначения АРВТ ВИЧ-инфицированным женщинам.
Клиническое наблюдение
Пациентка М., 31 год, была экстренно госпитализирована в отделение анестезиологии-реанимации 11.02.2025 в тяжёлом состоянии. При поступлении предъявляла жалобы на резкую общую слабость, потерю массы тела (на 15 кг за 2 месяца), фебрильную лихорадку (до 39 °C), продуктивный кашель, одышку в покое, а также на множественные болезненные узловые образования на коже туловища и конечностей и быстрое, болезненное увеличение обеих молочных желёз.
Из анамнеза известно, что ВИЧ-инфекция была диагностирована за 3 года до госпитализации, однако пациентка за медицинской помощью не обращалась и АРВТ не получала. На момент поступления срок беременности составлял 25–26 недель, отмечалось начало регулярной родовой деятельности. При осмотре: состояние тяжёлое. Кожные покровы бледные, с множественными плотными, болезненными при пальпации инфильтратами багрово-синюшного цвета диаметром от 2 до 5 см на груди, спине, животе и бёдрах. Двустороннее массивное увеличение молочных желёз (до 15–20 см в диаметре) каменистой плотности. Периферические лимфатические узлы (шейные, подмышечные, паховые) увеличены до 2–3 см, плотные, малоподвижные. Аускультативно в лёгких – обильные разнокалиберные хрипы. Печень выступала из-под края рёберной дуги на 6 см.
Результаты обследования
Лабораторные данные. Общий анализ крови: Hb – 68 г/л, лейкоциты – 3,1×10⁹/л, тромбоциты – 80×10⁹/л. Биохимический анализ крови: креатинин – 180 мкмоль/л, ЛДГ – 1250 Ед/л. Иммунный статус: CD4+ лимфоциты – 26 кл/мкл. Вирусная нагрузка ВИЧ – 550 000 копий/мл.
Инструментальные данные
КТ органов грудной клетки: множественные очаги деструкции в верхней челюсти; двусторонние инфильтраты в лёгких с полостями распада; массивное увеличение внутригрудных лимфатических узлов (до 5 см).
КТ головного мозга: множественные очаговые образования (до 1,5 см) в больших полушариях.
УЗИ органов брюшной полости: гепатомегалия (размер печени по среднеключичной линии – 18 см), множественные гипоэхогенные очаги в печени; увеличение забрюшинных и мезентериальных лимфоузлов.
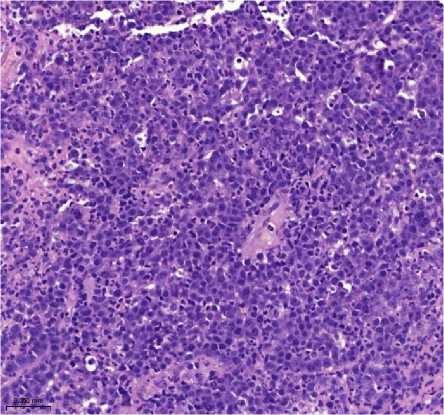
Морфологическая верификация: проведена биопсия кожного инфильтрата и увеличенного шейного лимфатического узла (рис. 1 и 2).
А
Б
В
Г
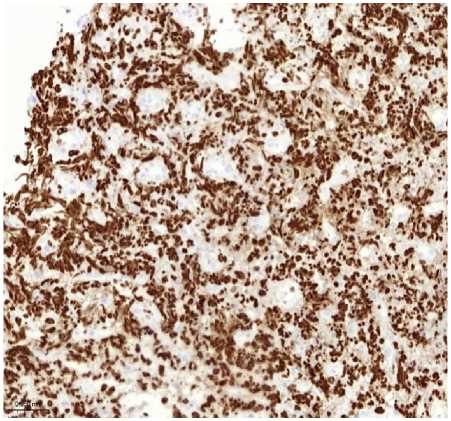
Д
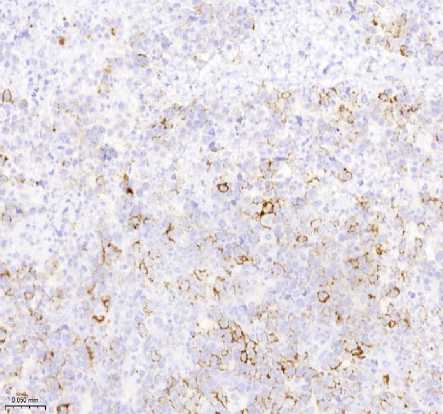
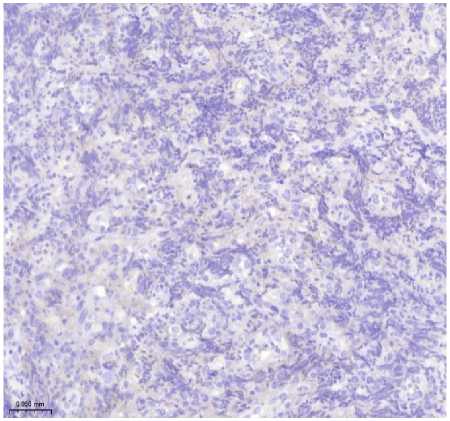
Рисунок 1. Плазмобластная лимфома. Биопсия кожи. Визуализируются клетки среднего размера с крупным ядром и заметными ядрышками. А. Окраска гематоксилином и эозином, увеличение ×200. Б. Иммуногистохимическое исследование с антителом CD138, увеличение ×200. В. Иммуногистохимическое исследование с антителом CD20, увеличение ×200. Г. SISH исследование к EBV, увеличение ×200. Д. Иммуногистохимическое исследование с антителом Ki67, увеличение ×200
Figure 1. Plasmoblastic lymphoma. Skin biopsy. Medium-sized cells with a large nucleus and prominent nucleoli are visualized. A. Hematoxylin and eosin staining, magnification ×200. Б. Immunohistochemical study with CD138 antibody, magnification ×200. В. Immunohistochemical study with CD20 antibody, magnification ×200. Г. SISH study for EBV, magnification ×200. Д. Immunohistochemical study with Ki67 antibody, magnification ×200
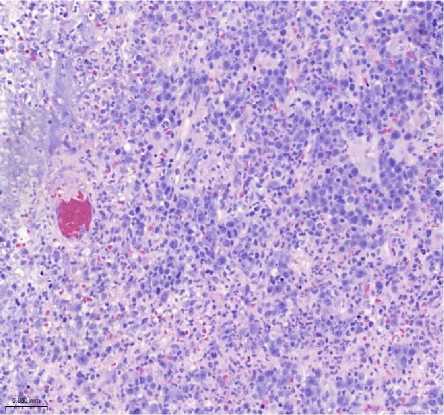
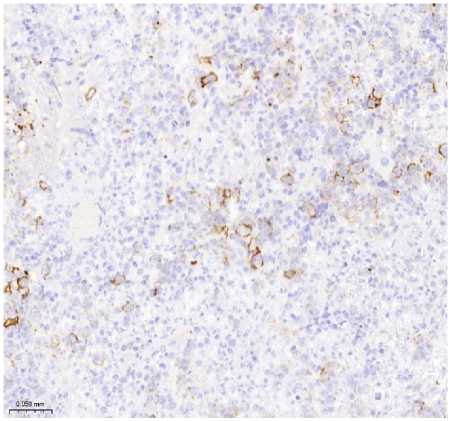
Б
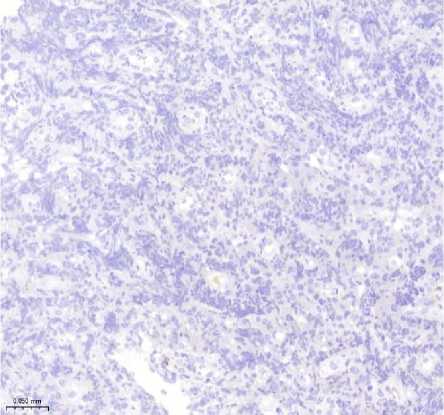
В
Г
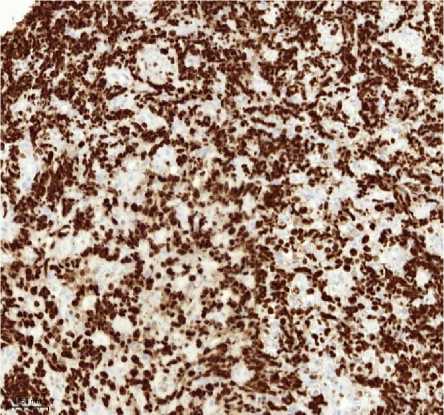
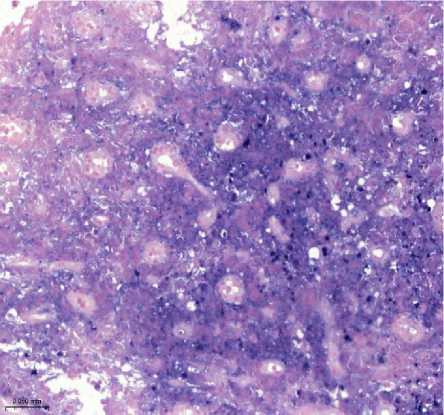
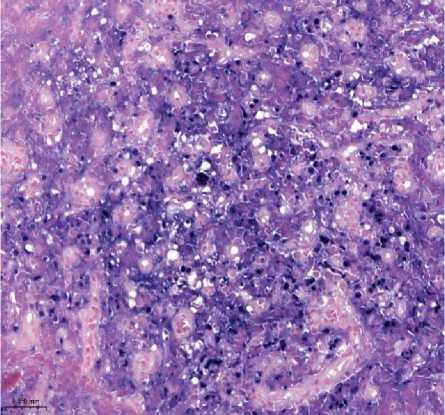
Рисунок 2. Плазмобластная лимфома. Биопсия лимфатического узла. Визуализируются клетки среднего размера с крупным ядром и заметными ядрышками. А. Окраска гематоксилином и эозином, увеличение ×200. Б. Иммуногистохимическое исследование с антителом CD138, увеличение ×200. В. Иммуногистохимическое исследование с антителом CD20, увеличение ×200. Г. SISH исследование к EBV, увеличение ×200. Д. Иммуногистохимическое исследование с антителом Ki67, увеличение ×200
Figure 2. Plasmoblastic lymphoma. Lymph node biopsy. Mediumsized cells with a large nucleus and prominent nucleoli are visualized. A. Hematoxylin and eosin staining, magnification ×200. Б. Immunohistochemical study with CD138 antibody, magnification ×200. В. Immunohistochemical study with CD20 antibody, magnification ×200. Г. SISH study for EBV, magnification ×200. Д. Immunohistochemical study with Ki67 antibody, magnification ×200
Гистологическое исследование: выявлен диффузный инфильтрат из крупных атипичных клеток с плазмобластным и иммунобластным фенотипом, ядрами неправильной формы, выраженным ядрышком и обильной базофильной цитоплазмой. Отмечались многочисленные фигуры митоза и обширные участки некроза.
Иммуногистохимическое исследование (ИГХ): Опухолевые клетки экспрессировали CD138, CD38, MUM1/IRF4; EBER (ISH) - положительно. Отмечалась негативная экспрессия CD20, PAX5, CD3. Индекс пролиферации Ki-67 >90%.
На основании данных морфологии и ИГХ был установлен диагноз: плазмобластная лимфома.
Сопутствующие заболевания: диссеминированный туберкулёз лёгких с бактериовыделением (подтверждён микроскопией мокроты); цитомегаловирусная инфекция (ДНК ЦМВ в крови - 105 ко-пий/мл); хронический пиелонефрит, обострение; анемия тяжёлой степени.
Динамика состояния и лечения пациентки
На фоне проводимой интенсивной терапии (коррекция анемии, респираторная поддержка, начало противотуберкулёзной терапии) состояние пациентки оставалось крайне тяжёлым. В связи с прогрессированием дыхательной недостаточности и нестабильностью гемодинамики 14.02.2025 было выполнено экстренное кесарево сечение. Родилась живая недоношенная девочка массой 600 г, которая была переведена в отделение выхаживания глубоконедоношенных. Проведение специфической полихимиотерапии по поводу ПБЛ было невозможно ввиду критического состояния пациентки и послеродового периода. Несмотря на продолжающуюся интенсивную терапию, через 13 дней после операции констатирована смерть пациентки.
Патологоанатомическое исследование подтвердило диагноз генерализованной плазмобластной лимфомы с поражением кожи, лимфатических узлов, молочных желёз, лёгких, печени, костного мозга и головного мозга.
Обсуждение
Представленное клиническое наблюдение демонстрирует молниеносное течение ВИЧ-ассоциированной ПБЛ на фоне беременности. Данный случай является иллюстрацией классических характеристик ПБЛ по классификации ВОЗ 5-го издания [1]: плазмобластная морфология, иммунофенотип (CD138+/CD38+/MUM1+, CD20-), ассоциация с EBV и развитие на фоне глубокого иммунодефицита (CD4+ < 50 кл/мкл).
Особенностью данного случая является генерализованный характер поражения с вовлечением кожи и молочных желёз, что, хотя и описано в литературе [3, 4], встречается реже, чем классическая оральная локализация. Крайне быстрая динамика заболевания и фатальный исход соответствуют агрессивному течению ПБЛ, особенно при наличии таких неблагоприятных прогностических факторов, как висцеральное поражение, высокий уровень ЛДГ и очень низкое количество CD4+ лимфоцитов [5, 7].
Ключевой проблемой в ведении данной пациентки стала невозможность проведения своевременной АРВТ и специфической химиотерапии. Беременность на большом сроке и критическое состояние пациентки сделали применение стандартных режимов (таких как DA-EPOCH, CHOP или бор-тезомиб-содержащие схемы) [8] невозможным. Присоединение диссеминированного туберкулёза и ЦМВ-инфекции усугубило состояние пациентки и предопределило неблагоприятный исход.
Данное наблюдение наглядно подчёркивает несколько важных аспектов:
-
1. Необходимость активного выявления ВИЧ-инфекции и раннего назначения АРВТ женщинам репродуктивного возраста, что является ключевым методом профилактики развития СПИД-ассоциированных лимфом.
-
2. Важность междисциплинарного взаимодействия между акушерами-гинекологами, онкогематологами, инфекционистами и реаниматологами при ведении беременных с онкогематологически-ми заболеваниями.
-
3. Необходимость диагностической настороженности в отношении лимфопролиферативных заболеваний при появлении у ВИЧ-инфицированных пациентов любых опухолевых образований, особенно с быстрым ростом.
Заключение
Описанный случай ВИЧ-ассоциированной плазмобластной лимфомы у беременной пациентки является редким и трагическим примером столкновения агрессивной онкопатологии, тяжёлого иммунодефицита и гестационного процесса. Катастрофическое течение заболевания и фатальный исход свидетельствуют о необходимости прегра-видарного консультирования и раннего начала АРВТ у всех ВИЧ-позитивных женщин, до начала беременности, а также разработки чётких междисциплинарных алгоритмов для ведения подобных сложных случаев.


