Видеолапароскопическая трансхиатальная экстирпация пищевода при местно-распространенном раке пищевода и кардио-эзофагеального перехода
Автор: Хоробрых Т.В., Агаджанов В.Г., Салихов Р.Е., Мищенко Н.П., Спартак А.А., Андриянов А.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 1 (79), 2022 года.
Бесплатный доступ
Введение. Рак пищевода является одним из наиболее неблагоприятных заболеваний пищеварительного тракта, с высоким уровнем летальности.Цель исследования. Целью проведения данной работы является повышение эффективности хирургического лечения больных с местно-распространенными формами рака пищевода, осложненными опухолевым стенозом и кровотечением за счет рационального использования малоинвазивных технологий на этапе хирургического лечения.Материалы и методы исследования. В рамках комбинированного лечения были прооперированы 2 больных с местно-распространенными формами рака пищевода и кардиоэзофагеального перехода.Результаты. Описан опыт применения лапароскопически ассистированной трансхиатальной экстирпации пищевода при местно-распространенном раке пищевода и кардиоэзофагеального перехода у двух пациентов с тяжелыми сопутствующими заболеваниями. Демонстрируется возможность проведения операций у пациентов с местно-распространенным раком пищевода и кардио-эзофагеального перехода с субкомпенсированными сопутствующими заболеваниями, в том числе за счет рациональной комбинации возможностей лапароскопических технологий и минилапаротомного доступа.Заключение. Эндовидеохирургически ассистированные операции безопасны и выполнимы у пациентов с местно-распространенными формами рака пищевода и кардиоэзофагеального перехода, в том числе за счет рационального использования возможностей минидоступа. Эндовидеохирургически ассистированное пособие позволяет расширить показания к оперативному лечению у коморбидных пациентов.
Рак пищевода, рак кардио-эзофагеального перехода, лапароскопическая трансхиатальная экстирпация пищевода
Короткий адрес: https://sciup.org/142234237
IDR: 142234237 | УДК: 616.329-089
Videolaparoscopic transchiatal extirpation of the esophagus in locally advanced cancer of the esophagus and cardio-esophageal junction
Introduction. Esophageal cancer is one of the most unfavorable diseases of the digestive tract, with a high mortality rate.Te purpose of the study. Te purpose of this work is to increase the e ectiveness of surgical treatment of patients with locally advanced forms of esophageal cancer complicated by tumor stenosis and bleeding due to the rational use of minimally invasive technologies at the stage of surgical treatment.Materials and methods of research. As part of the combined treatment, 2 patients with locally advanced forms of esophageal cancer and cardioesophageal junction were operated on.Treatment results. Te experience of using laparoscopically assisted transchiatal extirpation of the esophagus in locally advanced esophageal cancer and cardioesophageal transition in two patients with severe concomitant diseases is described. Te possibility of performing operations in patients with locally advanced esophageal cancer and cardio-esophageal transition with subcompensated concomitant diseases is demonstrated, including through a rational combination of laparoscopic technologies and minilaparotomic access.Conclusion. Endovideosurgically assisted operations are safe and feasible in patients with locally advanced forms of esophageal cancer and cardioesophageal junction, including through the rational use of the possibilities of mini-access. Te endovideosurgically assisted manual makes it possible to expand the indications for surgical treatment in comorbid patients
Текст научной статьи Видеолапароскопическая трансхиатальная экстирпация пищевода при местно-распространенном раке пищевода и кардио-эзофагеального перехода
Совершенствование хирургической техники и прогресс анестезиологии и реаниматологии, позволили снизить послеоперационную летальность при раке пищевода до 5–10%. При этом уровень послеоперационных осложнений по-прежнему остается высоким, достигая 35–50 % (. Sugarbaker D. J., Bueno R., Krasna M. J. Adult chest surgery. NY: The McGraw-Hill Companies, 2009. P. 865.).
Тенденция к снижению хирургической агрессии вообще, в том числе и в торакоабдоминальной хирургии очевидна. [1–3].
Еще в 1995 г. A. De Paula и соавт. представили первый опыт применения эндовидеолапароскопического доступа при трансхиатальной экстирпации пищевода [4].
Тем не менее, в мире, наиболее часто применяемым доступом при раке пищевода, является трансторакальный доступ (гибридная хирургия, тораколапароскопически ассистриро-ванный доступ) [5]. Целый ряд исследований демонстрирует преимущества трансхиатального доступа, как более безопасного, и менее травматичного, особенно у пациентов с тяжелым коморбидным статусом [6–7].
К моменту написания данной статьи нами выполнено 8 виде-олапароскопических трансхиатальных экстирпаций пищевода. Представляем свой опыт применения видеолапароскопической трансхиатальной экстирпации пищевода при местно-распространенном раке пищевода и кардио-эзофагеального перехода у двух пациентов с тяжелыми сопутствующими заболеваниями.
Материалы и методы
Два пациента с местно-распространенным осложненным раком пищевода и кардио-эзофагеального перехода. Предоперационное обследование включало сбор анамнеза, анализы крови и клиническое обследование, включавшее ЭГДС, МСКТ, УЗИ брюшной полости и лимфатических узлов шеи, рентгеноскопию пищевода, эндосонографию и бронхоскопию.
Решением предоперационного мультидисциплинарного консилиума, пациентам было отказано в проведении однолегочной вентиляции легких из-за высоких рисков интрапе-рационных осложнений.
Результаты (2 клинических случая)
Клинический случай № 1.
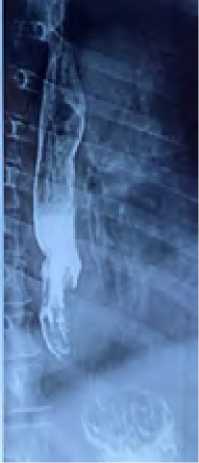
Рис. 1. Рентгенограмма с контрастным веществом больного Е.
Fig. 1. Radiograph with contrast agent of the patient E.
Больной Е., 68 лет, поступил в клинику с жалобами дискомфорт, тяжесть в эпигастрии после приема пищи, отрыжку воздухом, изжогу, периодические приступы боли за грудиной, снижение массы тела на 12 кг за последние 5 месяцев. По данным комплексного обследования у больного диагностирован: рак нижнегрудного отдела пищевода T3N1M0 (рис. 1–2), гистологически –плоскоклеточный ороговевающий рак (рис. 3), дисфагия 2–3 ст. ГПОД.
Сопутствующие заболевания: ХОБЛ GOLD 4 (кислород, зависимый пациент с сатурацией на атмосферном воздухе 90–92%), гипертоническая болезнь III ст., 2 ст., риск ССО3, недостаточность аортального клапана 2–3 ст., нарушение ритма сердца: постоянная форма фибрилляции предсердий, сахарный диабет 2 типа, мочекаменная болезнь, кисты левой почки. ТУР от 2015 года, ожирение (ИМТ >30 кг/м2).
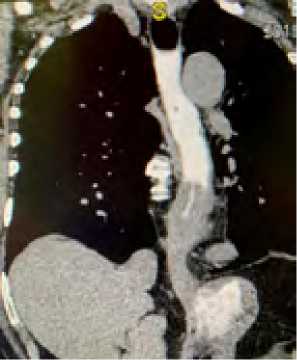
Рис. 2. МСКТ больного Е.
Fig. 2. MSCT of the patient E.
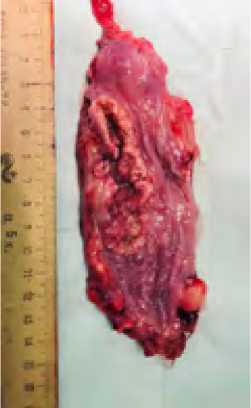
Рис 3. Макропрепарат – резецированный пищевод.
Fig. 3. Macropreparation – resected esophagus.
Клинический случай № 2.
Больной Ф., 78 лет, поступал в клинику с жалобами на затруднение прохождения пищи твёрдой пищи по пищеводу, снижение массы тела на 7 кг за последние 3 месяца, головокружение, слабость. По данным комплексного обследования у больного диагностирован: рак кардио-эзофагеального перехода (КЭР) T3N2M0, тип II по классификации Зиверта, осложненный декомпенсированным опухолевым стенозом, дисфагией 2–3 ст. (рис. 4–5), гистологически – умеренно дифференцированная аденокарцинома, (рис. 6). Из сопутствующих заболеваний у пациента имели место рак предстательной железы, лучевая терапия от 2010 г. ГПОД, гипертоническая болезнь III ст., 3 ст., риск ССО 4, облитерирующий атеросклероз артерий нижних конечностей, дисциркуляторная энцефалопатия 3 ст., умеренный вестибуло-атаксический синдром, когнитивные нарушения, последствия ОНМК по ишемическому типу в бассейне правой СМА от 2004 г., стенозирующий атеросклероз брахиоцефальных артерий: окклюзия ВСА слева, гемодинамически значимый стеноз ВСА справа в проксимальной трети 75 %, стентирование правой ВСА от 27.08.19, стенозирующий атеросклероз НПА до 85 % процентов, синдром Лериша тип С.
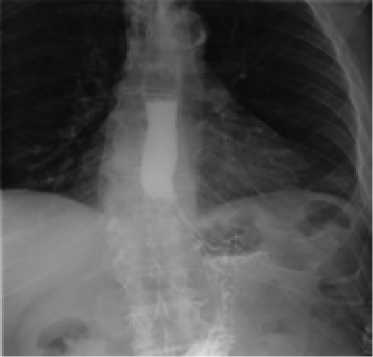
Рис. 4. Рентгенограмма с контрастным веществом больного Ф.
Fig. 4. Radiograph with contrast agent of the patient F.
Перед операцией мультидисциплинарным онкоконсилиумом проведена оценка таких показателей как, степень распространенности онкологического процесса, коморбидный статус пациента (в том числе переносимость однолегочной вентиляции), наличие отдаленных метастазов, результаты проведенного химиотерапевтического/химиолучевого лечения.
В ходе предоперационного обследования у данных пациентов диагностировали сердечно-легочную недостаточность, не позволявшую выполнение оперативного вмешательства с проведением однолегочной вентиляции.
Учитывая комборбидный статус пациентов, невозможность выполнения однолегочной вентиляции, операцией выбора стала лапароскопически ассистированная трансхиатальная экстирпация пищевода с формированием узкого желудочного трансплантата из минилапаротомного доступа и эзофагога-стростомией на шее.
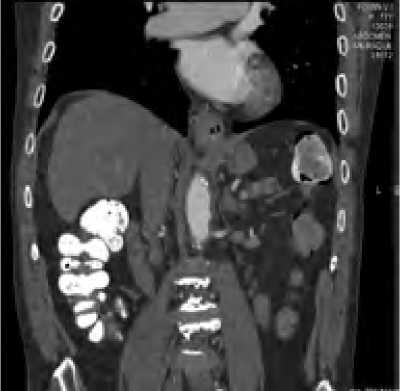
Рис. 5. МСКТ больного Ф.
Fig. 5. MSCT of the patient F.
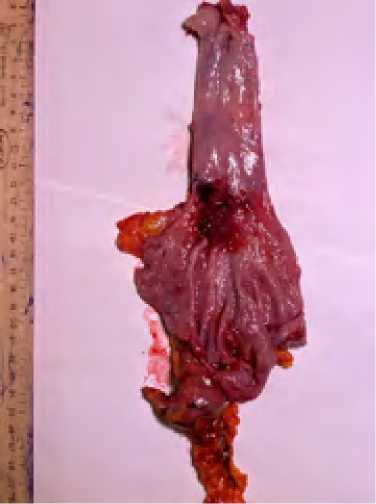
Рис 6 . Макропрепара т – резецированный пищевод вместе с кардиальным отделом желудка Fig. 6. Macropreparation – is a resected esophagus together with the cardiac part of the stomach
Техника выполнения операции
Операцию выполняли под комбинированным эндотрахе-альным наркозом. Операционная бригада состояла из 3 человек
– хирург располагался между ног пациента, ассистенты – по обеим сторонам. Пациент находился в положении Фовлера. Первый оптический троакар устанавливался открыто, по методу Хассона над пупком. После ревизии органов брюшной полости, установка троакаров выполнялась веерообразно (V-shaped) в правом мезогастрии и правом подреберье 12 мм и 10 мм соответственно, в левом мезогастрии и левом подреберье 10 и 5 мм соответственно. Первым этапом выполнялась парциальная сагитальная диафрагмотомия без пересечния нижнедиафрагмальных сосудов, далее производилась мобилизация пищевода трансхиатально до верхнее-грудной апертуры в одном блоке с мягкими тканями и регионарными лимфоузлами. Последним абдоминальным этапом производилась мобилизация желудка по большой кривизне с сохранением правой желудочно-сальниковой артерии. Лимфаденэктомия в объеме 2S (при локализации онкопроцесса в нижнегрудном отеделе пищевода), которая включала удаление параэзофагеальных, парааортальных, бифуркационных, правых и левых корневых лимфатических узлов, абдоминальных лимфоузлов
Вторым этапом выполнялась коллотомия слева параллельно кивательной мышце, мобилизован шейный отдел пищевода, расширенный до 3 см, с гипертрофированной стенкой, пересечен на 1 см ниже глоточно-пищеводного перехода.
Третьим этапом выполнялась минилапаротомия до 5 см по срединной линии, тотчас от мечевидного отростка грудины. Из большой кривизны желудка при помощи линейных степлеров – выкраивался трансплантат с кровоснабжением из правой желудочно-сальниковой артерии. Линия механических швов перитонизировалась серо-серозным непрерывным викриловым швом 3/0 на атравматичной игле.
Интраоперационных осложнений не было. Объём интраоперационной кровопотери составил (±200 мл). Послеоперационный период протекал гладко, без осложнений. Пациенты находились в РАО 3±1 день. На 4–5 сутки при контрольной рентгенографии с контрастным веществом, затеков в области анастомоза не обнаружено. Питание начинали на 5 сутки. Пациенты были выписаны на 8 сутки после оперативного вмешательства.
Патоморфологическое заключение 1 клинический случай: умеренно дифференцированная плоскоклеточная карцинома пищевода с ороговеванием G2, pT3N0M0 с перифокальным воспалением.
Из грудной полости удалено 26 лимфатических узла, по результатам гистологического исследования операционного материала в 2 из них обнаружили раковые клетки. Из брюшной полости удалили 29 лимфоузлов, при этом в 1 из них были обнаружены опухолевые клетки.
Патоморфологическое заключение 2 клинический случай: умеренно дифференцированная аденокарцинома G2, pT3N2M0
Из грудной полости удалено 24 лимфатических узлов, в 3 из них обнаружили раковые клетки. Из брюшной полости удалили 34 лимфоузла, при этом в 4 из них были обнаружены опухолевые клетки.
Опухолевый рост в краях резекции не выявлен.
Обсуждение
Возможности современных эндовидеохирургических технологий позволяют существенно снизить уровень хирургической агрессии, что очень актуально при хирургическом лечении местно-распостраненного рака пищевода и желудка [8].
Снижение травматизации при помощи тораколапаро-скопической операции безусловно дает преимущество в уменьшении травматичности самой операции, однако не всегда удается провести однолегочную вентиляцию легких при таких сопутствующих заболеваниях, как у описанных пациентов.
Преимуществом эндовидеохирургического трансхиатального доступа является уменьшение травматизации, даже в сравнении с тораколапароскопической экстирпацией пищевода [9, 10], что сделало возможным выполнение оперативного вмешательства, избежав однолегочной вентиляции и помогло удерживать сатурацию на уровне не менее 94 %, и позволило избежать таких осложнений, как несостоятельность анастомозов.
Важными показателями эффективности эндовидеохирургического пособия при минимально инвазивной эзофагэктомии является сокращение сроков пребывания пациентов в реанимационном отделение, ранняя активизация выписка из стационара.
Очень важным показателем эффективности применения минимально инвазивной эзофагэктомии стала возможность начала адьювантной терапии уже через 3 недели после операции.
Выполнение лапароскопически ассистированной трансхиатальной экстирпации пищевода у представленных пациентов с декомпенсированными сопутствующими заболеваниями, позволило уменьшить хирургическую агрессию, минимизировать риски послеоперационных осложнений и ускорить послеоперационную реабилитацию.
Заключение
Лапароскопически ассистированная трансхиатальная экстирпация пищевода выполнима у пациентов с местно-распространенным раком пищевода и кардио-эзофагеального перехода с субкомпенсированными сопутствующими заболеваниями, в том числе за счет рациональной комбинации возможностей лапароскопических технологий и минилапа-ротомного доступа.
Список литературы Видеолапароскопическая трансхиатальная экстирпация пищевода при местно-распространенном раке пищевода и кардио-эзофагеального перехода
- Zhou C., Zhang L., Wang H., Ma X., Shi B., Chen W. Superiority of minimally invasive oesophagectomy in reducing in-hospital mortality of patients with resectable oesophageal cancer: a metaanalysis. PLoS ONE, 2015, № 10(7),e0132889.
- DOI: 10.1371/journal.pone.0132889
- Lee Y, Min SH, Park KB, Park YS, Ahn SH, Park DJ, Kim HH. Longterm Outcomes of Laparoscopic Versus Open Transhiatal Approach for the Treatment of Esophagogastric Junction Cancer. J Gastric Cancer, 2019, Mar; № 19(1), рр. 62-71.
- Subramanyeshwar Rao Tammineedi, Sujit Chyau Patnaik1, Syed Nusrath. Minimal Invasive Esophagectomy - a New Dawn of Esophageal Surgery Indian Journal of Surgical Oncology.
- DOI: 10.1007/s13193-020-01191-7
- De Paula A.L., Hashiba K., Ferreira E. A., De Paula R. A., Grecco E. Laparoscopic transhiatal esophagectomy with esophagogastro-plasty. Surg Laparosc Endosc., 1995, № 5, рр. 1-5.
- Dunst C.M., Swanström L.L. Minimally invasive esophagectomy. J Gastrointest Surg, 2010, № 14(SUPPL.1), рр. 108-114.
- Orringer Mark B. MD*, Marshall Becky, Chang Andrew C. MD*, Lee Julia M.S., Pickens Allan M.D.*, Lau Christine L. MD. Two Tousand Transhiatal Esophagectomies. Ann Surg., 2007, № 246(3), рр. 363-374.
- Orringer M.B., Marshall B., Iannettoni M.D. Transhiatal Esophagectomy: Clinical Experience and Refnements. Ann Surg., 1999, № 230(3), рр. 392-403.
- William H Allum 1, Luigi Bonavina, Stephen D Cassivi, Miguel A Cuesta, Zhao Ming Dong, Valter Nilton Felix, Edgar Figueredo, Piers A C Gatenby, Leonie Haverkamp, Maksat A Ibraev, Mark J Krasna, René Lambert, Rupert Langer, Michael P N Lewis, Katie S Nason, Kevin Parry, Shaun R Preston, Jelle P Ruurda, Lara W Schaheen, Roger P Tatum, Igor N Turkin, Sylvia van der Horst, Donald L van der Peet, Peter C van der Sluis, Richard van Hillegersberg, Justin C R Wormald, Peter C Wu, Barbara M Zonderhuis. Surgical treatments for esophageal cancers. Ann N Y Acad Sci., 2014, Sep; № 1325, рр. 242-268. https://.
- DOI: 10.1111/nyas.12533 EDN: UGMTOD
- Kelly R. Haisley, Walaa F. Abdelmoaty, Christy M. Dunst. Journal of Gastrointestinal Surgery Laparoscopic Transhiatal Esophagectomy for Invasive Esophageal Adenocarcinoma.
- DOI: 10.1007/s11605-019-04506-4
- Namm J.P., Posner M.C. Transhiatal Esophagectomy for Esophageal Cancer. J Laparoendosc Adv Surg Tech., 2016, № 26(10), рр. 752-757.


