Влияние антибактериальных факторов на смешанную культуру Escherichia coli и Staphylococcus epidermidis в условиях повышенного осмотического давления
Автор: Елтышева Ирина Валерьевна, Затворницкий Лев Евгеньевич, Масленникова Ирина Леонидовна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Комменсальные штаммы кишечника человека Escherichia coli K12 и кожи Staphylococcus epidermidis нередко встречаются в одних и тех же атипичных биотопах, где они могут выступать инфекционными агентами. Цель работы - изучение эффективности действия хлорамфеникола, це-фтриаксона, пиобактериофага поливалентного и хлоргексидина на моновидовые и смешанные культуры условно-патогенных микроорганизмов E. coli К12 и S. epidermidis на фоне 2%-ного NaCl. Показано, что эффект цефтриаксона и хлорамфеникола, с антибактериальными свойствами только в отношении E. coli, нивелировался в условиях повышенного осмотического давления в концентрациях 12-200 мг/л в смешанной культуре. Для E. coli К12 отмечено снижение эффективности действия бактериофага при высоком осмотическом давлении, что является противоположным по отношению к S. epidermidis. Что касается хлоргексидина, то в условиях 2%-ного NaCl его действие на E. coli K12 и S. epidermidis усиливалось в моновидовых и смешанных культурах. В целом, повышение осмотического давления среды выступало синергистом ингибирования роста бактерий антибиотиками и бактериостатиком.
Смешанные культуры, антибиотики, бактериофаг, хлоргексидин
Короткий адрес: https://sciup.org/147229631
IDR: 147229631 | УДК: 579.264: | DOI: 10.17072/1994-9952-2020-1-19-25
Influence of antibacterial factors on the mixed culture of Escherischia coli and Staphylococcus epidermidis under conditions of increased osmotic pressure
Commensal strains of the human intestine Escherichia coli K12 and of the human skin Staphylococcus epidermidis are often found in the same atypical biotopes, where they can act as infectious agents. The metabolism of bacteria changes in polymicrobial associations and in the presence of increased osmotic pressure in biotopes, associated with a number of pathological conditions that may affect their sensitivity to antibacterial factors of various nature. In this regard, the aim of the work was to study the effectiveness of chloramphenicol, ceftriaxone, polyvalent pyobacteriophage and chlorhexidine on single and mixed cultures of opportunistic microorganisms E. coli K12 and S. epidermidis at a background of 2% NaCl. It was shown that the effect of ceftriaxone, a broad-spectrum antibiotic, and chloramphenicol, with antibacterial properties only against E. coli, were leveled under conditions of increased osmotic pressure at concentrations of 12-200 mg/l in a mixed culture. For E. coli K12, a decrease in the effectiveness of the bacteriophage at high osmotic pressure was noted, which is the opposite in effect towards S. epidermidis. As for chlorhexidine, its effect on E. coli K12 and S. epidermidis was enhanced in single and mixed cultures under conditions of 2% NaCl. In general, in most cases, an increase in the osmotic pressure of the medium acted as a synergist for inhibiting bacterial growth with antibiotics and bacteriostatic.
Текст научной статьи Влияние антибактериальных факторов на смешанную культуру Escherichia coli и Staphylococcus epidermidis в условиях повышенного осмотического давления
Staphylococcus epidermidis – комменсал кожи человека, нередко могут встречаться в одних и тех же атипичных биотопах, где они могут выступать инфекционными агентами: в мочеполовых путях ( E. coli группы A – 12; S. epidermidis – 11.6%), в трофических язвах ( E. coli – 6.4 – 14.3; S. epidermi-dis – 28.2%), в ожоговых ( E. coli – 6.3; S. epider-midis – 4.4%), хирургических ранах ( E. coli группы А – 20 изолятов; S. epidermidis – 2.2% ), на постоянных медицинских устройствах, таких как катетеры, импланты [Moet et al., 2007; Otto, 2009; DiMuzio et al., 2014; Chakraborty et al., 2015; Hinojosa et al., 2016; Козлова и др., 2017; Assadian, Humphreys, Ousey, 2018; Méric et al., 2018; Oliveira et al., 2018; Szweda, Gorczyca, Tylingo, 2018].
С этих позиций использование антибиотиков с широким спектром действия при полимикробных инфекциях вполне оправдано. Однако примерно 50% всех госпитальных инфекций в настоящее время вызываются резистентными к антибиотикам микроорганизмами [Фадеева и др., 2006], причем среди комменсальной группы E. coli и S. epidermidis все чаще выявляются случаи множественной устойчивости [Chakraborty et al., 2015; Козлова и др., 2017]. Поэтому использование наряду с антибиотиками поливалентных бактериофагов или универсальных бактериостатиков, таких как хлоргексидин, для санации поверхностных, глубоких гнойных ран, труднозаживающих трофических язв до сих пор не потеряло своей значимости [Schmidt et al., 2018].
В некоторых ситуациях, таких как ряд патологических состояний (сахарный диабет, ожирение, гипертензия, заболевания щитовидной железы и др. [Akbaş, Kilinç, 2018], физические нагрузки, жаркие климатические условия, инфекционные процессы могут протекать на фоне интенсивного потоотделения, в ходе которого концентрация Na+ и Cl- варьирует в пределах 10 – 90 мМ [Baker, 2019] и в близлежащих биотопах может достигать 12 – 21 мМ [Hendricks et al., 2018]. Учитывая бактерицидный характер действия высоких концентраций NaCl, а также разную устойчивость видов E. coli и S. epidermidis к высокому осмотическому давлению можно предположить разницу в составе по-лимикробного сообщества в этих условиях и, возможно, в устойчивости к антимикробным препаратам с разным механизмом действия.
В связи с этим, целью данной работы было изучение эффективности действия хлорамфеникола, цефтриаксона, пиобактериофага поливалентного и хлоргексидина на моновидовые и смешанные культуры условно-патогенных микроорганизмов E. coli К12 и S. еpidermidis на фоне 2%-ного NaCl .
Материалы и методы исследования
В качестве объекта исследования использовали референтный штамм S. еpidermidis (ATCC 29887) и генно-инженерный штамм E. coli К12 TG1 (pXen7) c полным lux-опероном светящейся бактерии Photorhabdus luminescens [Данилов и др., 2002].
Культивирование бактерий проводили на жидкой богатой питательной среде Luria-Bertani (LB) (Sigma, США). В ряде вариантов конечная концентрация NaCl в среде была 2%.
Ночные культуры S. еpidermidis и E. coli К12, выращенные на LB, разводили свежей питательной средой до концентрации бактерий 106 кл/мл. Планктонные моновидовые и смешанные культуры S. еpidermidis и E. coli К12 (соотношение 1:1) вносили по 200 мкл в лунки плоскодонных полистироловых планшетов (Медполимер, Россия) и выращивали в термостате при 37ºС в течение суток.
Для оценки влияния антибактериальных препаратов на моновидовые и смешанные культуры S. еpidermidis и E. coli К12 использовали хлорамфеникол (1 – 200 мг/л) (Northeast pharmaceutical group Co., Китай), цефтриаксон (1 – 200 мг/л) (Синтез, Россия), пиобактериофаг поливалентный очищенный (разведение в 10 – 800 раз) (Микроген, Россия), 0.05%-ный водный раствор хлоргексидина биглюконата (разведение в 10 – 1500 раз) (Сама-рамедпром, Россия).
Интенсивность роста моновидовых культур оценивали через 24 ч. по оптической плотности при длине волны 600 нм (ОП 600) на микроплан-шетном ридере Synergy H1 (BioTek, США). Влияние антибактериальных препаратов на E. coli в смешанной культуре оценивали согласно уровню ингибирования биолюминесценции через 4 ч. культивирования по сравнению с соответствующим контролем. Соотношение видов в культурах оценивали через 24 ч. путем высевов на селективные среды: для E. coli K12 – LB агар c 100 мг/л ампициллина (учитывались светящиеся колонии, КОЕ/мл); для S. еpidermidis – LB c 3% NaCl (конечная концентрация).
Повторность экспериментов трехкратная. Статистическая обработка проводилась с использованием программы Excel: рассчитывали среднее арифметическое, стандартное отклонение, t -критерий Стьюдента.
Результаты и их обсуждение
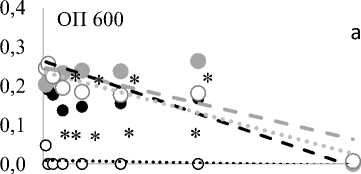
В результате проведенных исследований было показано, что в условиях повышенного осмотического давления рост E. coli K12 ингибировался (p < 0.05), а S. epidermidis – нет (p = 0.26). Однако при действии 10–100 мг/л цефтриаксона на моно-видовые культуры развитие обоих видов бактерий на фоне 2%-ного NaCl замедлялось (рис. 1, а). Подобное ингибирующее действие отмечено у хлорамфеникола (1–100 мг/л) только для E. coli K12, поскольку S. epidermidis обладал устойчивостью к данному антибиотику (рис. 1, б). Таким образом, действие осмотического фактора усиливало антибактериальное действие антибиотика на моновидо-вые культуры.
0 50 100 150 200
Концентрация, мг/л
0,4
0,3
0,2
0,1
0,0
-0,1
0,3
0,2
0,1
0,0
ОП 600
б
** * * *• Ч.О
* **
0,0 20,0 40,0 60,0 80,0100,0
Концентрация, мг/л
ОП 600
*



в

Разведение, раз
.^. —.^.^.ж.тт..-:
0 100 200 300 400 500 600 700
0 2 ОП 600
.28 8 о________- аз L ^л^"
’ Разведение. раз
оо q——-
0 200 400 600
• E.cdi, 0.9*4 NaCl о Е. cdi, 2% NaCl
S. epic etmicis. 0.9* о NaCl О S. epidamidis: 2*4 NaCl ---Линейная (E coli, 09*4 NaCl) .........Линейная (E coli, 296 NaCl)
~ Линейная (S. epidemucis. 0.9*4 NaQ)
Линейная (S. epidetmidis. 2*4 NaCl)
Рис. 1 . Влияние цефтриаксона (а), хлорамфеникола (б), бактериофага (в), хлоргексидина (г) на рост E. coli K12 и S. epidermidis в моновидовой культуре на фоне 2%-ного NaCl
При действии поливалентного бактериофага отмечена его высокая активность в отношении E. coli К12, но на фоне 2%-ного NaCl эффективность действия данного препарата на оба вида снижалась при разведении в 10 раз (рис. 1, в). Что касается хлоргексидина, то в условиях повышенного осмотического давления его действие на E. coli K12 и S. epidermidis усиливалось (рис. 1, г). Это связано с тем, что действие бактериостатика обусловлено его связыванием c фосфолипидами плазматической мембраны, что приводит к нарушению осмотического равновесия [Hidalgo, Dominguez, 2001], поэтому присутствие 2%-ного NaCl вносило дополнительный вклад в нарушение целостности клеток, вызывая гибель бактерий обоих видов.
В составе смешанных культур действие вышеуказанных антибактериальных веществ на клетки E. coli K12 оценивалось по биолюминесценции, поскольку энергетическое обеспечение свечения бактерий тесно взаимосвязано с основными метаболическими путями [Пшеничнов, Масленникова, Никитина, 2003]. Присутствие S. epidermidis ингибировало обмен веществ E. coli , причем сильнее в среде с 2%-ным NaCl (63.2±16.0 против 33.8±12.9; р = 0.001) Однако степень ингибирования свечения E. coli К12 в составе смешанной культуре было меньше (79.3±6.6), чем в моновидовой (86.6±5.5) (р = 0.035) при действии 2% NaCl, что может свидетельствовать о том, что в полимикробной ассоциации с S. epidermidis вероятность выживания E. coli К12 увеличивается при повышении осмотического давления окружающей среды. Вероятно, наличие в составе мембран стафилококков 8 видов протонных помп и 6 видов транспортных систем осмопротекторов [Rogers, Fey, Rupp, 2009] позволяет обеспечивать защиту от NaCl не только собственных клеток, но и бактерий-ассоциантов.
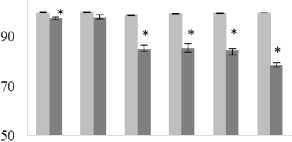
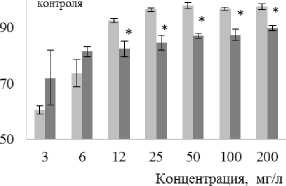
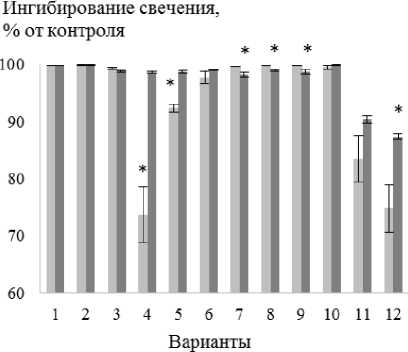
На рисунке 2 представлены данные действия антибактериальных препаратов на E. coli К12 в составе смешанной культуры. Показано, что эффект обоих антибиотиков (цефтриаксона с широким спектром действия, хлорамфеникола с антибактериальными свойствами только в отношении E. coli ) нивелировался в условиях повышенного осмотического давления в концентрациях 12 – 200 мг/л. Подобного рода снижение восприимчивости к антибиотикам ранее отмечалось у моновидовых культур S. aureus , E. coli на фоне высокого содержания NaCl в среде, связанное с индукцией защитных белков стресса и снижением активности сайтов связывания клеточной стенки [McMahon et al., 2007]. Вероятно, что данный механизм, также обеспечивает увеличение резистенстности E. coli K12 к актибиотикам и в условиях смешанного сообщества.
Инбирование свечения, % от контроля
6 12 25 50 100 200
Концентрация, мг/л
Ингибирование б свечения, % от
Ингибиро ванне свечения, % от В
6 12 24 48 96 192 384
Разведение, раз
Ингибирование свечения, % от
12 24 48 96 192 384 768
0,9%NaCl ■ 2%NaCl Разведение, раз
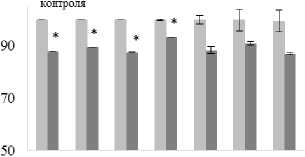
Рис. 2 . Влияние цефтриаксона (а), хлорамфеникола (б), бактериофага (в), хлоргексидина (г) на E. coli в составе смешанной культуры с S. epidermidis
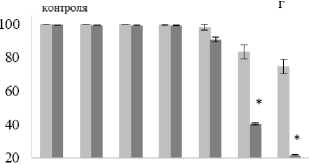
Бактерицидное действие хлоргексидина на клетки E. coli К12 не зависело от осмотического фона, за исключением вариантов с сильным разведением препарата (больше 350 раз) (рис. 2, г). Если оценивать суммарное воздействие антибактериального препарата и 2%-ного NaCl, то дополнительный бактерицидный эффект последнего явно проявлялся только при низких концентрациях хло-рамфекола и хлоргексидина (частично данные эксперимента представлены на рис. 3).
Что касается состава смешанной культуры, то при действии осмотического фактора выживаемость обоих видов снижалась (рис. 4). При действии 200 мг/л цефтриаксона роста бактерий не было, при низкой (6 мг/л) – действие соли не оказывало влияния на КОЕ/мл S. epidermidis. В отношении действия хлорамфеникола показано, что в условиях смешанной культуры клетки E. coli выживали при 200 мг/л, в то время, как в моновидовой культуре антибиотик в концентрации 100 мг/л полностью ингибировал рост данного вида. Подобный эффект появления устойчивости к антибиотикам в смешанных культурах описан ранее для видов S. aureus и E. coli [Shahidi et al., 1969]. По всей видимости, комменсал кожи S. epidermidis в составе смешанной культуры также может способствовать появлению устойчивости к антибиотикам у видов-ассоциантов. Механизмы подобной устойчивости могут быть связаны с инактивацией бактериями-ассоциантами антибиотиков, с изменениями в экспрессии генов, вызванные метаболитами и сигналами кворума, ингибированием цепи переноса электронов и c изменениями свойств клеточных мембран [Orazi, O’Toole, 2019]. Однако, присутствие осмотического фактора нивелировало появившуюся устойчивость E. coli к хлорамфениколу и оказывало бактерицидное действие, свидетельствуя об изменении механизмов устойчивости бактериальных ассоциаций в данных условиях.
■ АБ препарат "АБ препарат + 2%NaCl
Рис. 3. Суммарное влияние 2%-ного NaCl и антибактериального (АБ) препарата на E. coli
K12 в составе смешанной культуры с
S. epidermidis :
1, 2, 3 – цефтриаксон (6, 12, 50 мг/л); 4, 5, 6 – хлорамфеникол (6, 12, 50 мг/л); 7, 8, 9 – бактериофаг (разведение в 6, 50, 200 раз); 10, 11, 12 – хлоргексидин (разведение в 100, 400, 700 раз)
В отношении бактериофага выявлено, что его литическое действие вне зависимости от исходного количества проявлялость только на E. coli К12 в смешанной культуре со S. epidermidis. Данный эффект выборочного лизиса бактериофагом видов бактерий в смешанной культуре связан с ранее описанным феноменом «Kill the winner», согласно которому более успешно пролиферирующие виды в сообществе, в условиях нашего эксперимента E. coli K12, в большей степени подвергаются давлению фаговой инфекции [Weinbauer, 2004].
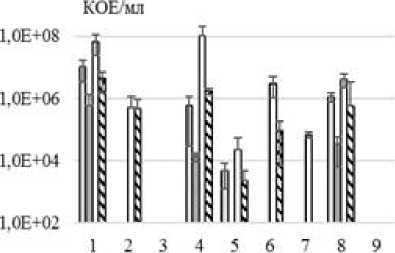
Варианты
-
□Е. coli, 0,9%NaCl
ОЕ coli,2%NaCl
OS. epidennidis, O.9°oNaCl
3S. epidennidis, 2% NaCl
Рис. 4 . Жизнеспособность E. coli К12 и
-
S. epidermidis в смешанной культуре при действии антибактериальных факторов:
-
1 – контроль; 2, 3 – цефтриаксон (6, 200 мг/л); 4,
-
5 – хлорамфеникол (6, 200 мг/л); 6, 7 – бактериофаг (разведение в 200 и 10 раз); 8, 9 – хлоргексидин (разведение в 400 и 10 раз)
Кроме этого, если ранее для E. coli К12 отмечено снижение эффективности действия бактериофага при высоком осмотическом давлении, согласно данным высевов, у S. epidermidis данный эффект не обнаружен. Вероятно, тип взаимодействия бактериофагов с грамположительными бактериями (не исключающий формирование пор в клеточной стенке) [Moller, Lindsay, Read, 2019], частично объясняет усиление гибели S. epidermidis при повышенном осмотическом давлении среды.
Что касается хлоргексидина, то его действие в составе смешанной культуры было аналогично моновидовым культурам (рис. 4). При сильном разведении бактериостатика 2%-ный NaCl сильнее ингибировал выживаемость обоих видов бактерий.
Заключение
Существование бактериальных видов в составе сообщества неизменно сопровождается изменениями в экспрессии генов и соотвественно в регуляции метаболизма, необходимые для антагонистических или мутуалистических форм взаимодействия членов ассоциации. В связи с этим механизмы действия антибактериальных факторов различной природы могут модифицироваться и не проявляться в такой же степени, как в моновидовой культуре. Дополнительно к выше указанному, различные стрессорные факторы внешней среды, та- кие как анормальные температуры, осмоляльность или кислотность среды, могут вносить коррективы реагирования бактериальных видов, а именно появление устойчивости к антибактериальным агентам, обусловленные разными механизмами. В целом, в большинстве случаев повышение осмотического давления среды выступало синергистом ингибирования роста бактерий антибиотиками и бак-териостатиком.
Исследование выполнено в рамках государ-ственнного задания номер госрегистрации темы: 01201353249.
Список литературы Влияние антибактериальных факторов на смешанную культуру Escherichia coli и Staphylococcus epidermidis в условиях повышенного осмотического давления
- Данилов В.С. и др. Сенсорные биолюминесцентные системы на основе lux-оперонов разных видов люминесцентных бактерий // Вестник МГУ. Cер. 16: Биология. 2002. № 3. С. 20-23.
- Козлова Ю. и др. Генетическая и биохимическая характеризация стафилококков, встречающихся в Новосибирске // Вавиловский журнал генетики и селекции. 2017. Т. 21, № 8. С. 952-958.
- Пшеничное Р.А., Масленникова И.Л., Никитина Н.М. Влияние антибактериальных факторов и биостимуляторов клеточного метаболизма на бактериальную люминесценцию // Прикладная биохимия и микробиология. 2003. Т. 39, № 3. С. 307-312.
- Фадеева Т.В. и др. Актуальные проблемы госпитальной инфекции: реинфицирование, суперинфицирование и резистентность возбудителей к антимикробным препаратам // Бюллетень Восточно-Сибирского научного центра СО РАМН. 2006. № 5. С. 298-301.
- Akba§ A., Kiling F. Investigation on aetiological factors in patients with hyperhidrosis // Cutaneous and Ocular Toxicology. 2018. Vol. 37, № 4. P. 344-349.
- Assadian O., Humphreys P.N., Ousey K.J. Disinfection of artificially contaminated gloved hands reduces transmission of Staphylococcus epidermidis to catheter valves // Journal of Hospital Infection. 2018. Vol. 100, № 3. P. e57-e59.
- Baker L.B. Physiology of sweat gland function: The roles of sweating and sweat composition in human health // Temperature (Austin). 2019. Vol. 6, № 3. P. 211-259.
- Chakraborty A. et al. Characterization of Escherichia coli phylogenetic groups associated with extraintestinal infections in South Indian population // Annals of Medical and Health Sciences Research. 2015. Vol. 5, № 4. P. 241-246.
- DiMuzio E.E. et al.Trends in bacterial wound isolates and antimicrobial susceptibility in a pediatric burn hospital // Journal of burn care and research. 2014. Vol. 35, № 5. P. e304-11.
- Hendricks A.J. et al. Sweat mechanisms and dysfunctions in atopic dermatitis // Journal of Dermato-logical Science. 2018. Vol. 89, № 2. P. 105-111.
- Hidalgo E., Dominguez C. Mechanisms underlying chlorhexidine-induced cytotoxicity // Toxicology in vitro. 2001. Vol. 15, № 4-5. P. 271-276.
- Hinojosa C.A. et al. Impact of the bacteriology of diabetic foot ulcers in limb loss // Wound Repair and Regeneration. 2016. Vol. 24, № 5. P. 923-927.
- Jonczyk E. et al. The influence of external factors on bacteriophages - review // Folia Microbiologica (Praha). 2011 Vol. 56, № 3. P. 191-200.
- McMahon M.A. et al. Environmental stress and antibiotic resistance in food-related pathogens // Applied and Environmental Microbiology. 2007. Vol. 73, № 1. P. 211-217.
- Meric G. et al. Disease-associated genotypes of the commensal skin bacterium Staphylococcus epi-dermidis // Nature communications. 2018. Vol. 9, № 1. P. 5034.
- Moet G.J. et al. Contemporary causes of skin and soft tissue infections in North America, Latin America, and Europe: report from the SENTRY Antimicrobial Surveillance Program (1998-2004) // Diagnostic microbiology and infectious disease. 2007. Vol. 57, № 1. P. 7-13.
- Moller A.G., Lindsay J.A., Read T.D. Determinants of phage host range in Staphylococcus species // Applied and environmental microbiology. 2019. Vol. 85, № 11. P: e00209-19.
- Oliveira W.F. et al. Staphylococcus aureus and Staphylococcus epidermidis infections on implants // The Journal of hospital infection. 2018. Vol. 98, № 2. P. 111-117.
- Orazi G., O'Toole G.A. «It takes a village»: mechanisms underlying antimicrobial recalcitrance of polymicrobial biofilms // The Journal of bacteriology. 2019. Vol. 202, № 1. P. e00530-19.
- Otto M. Staphylococcus epidermidis - the «accidental» pathogen // Nature reviews. Microbiology. 2009. Vol. 7, № 8. P. 555-567.
- Rogers K.L., Fey P.D., Rupp M.E. Coagulase-negative staphylococcal infections // Infectious disease clinics of North America. 2009. Vol. 23, № 1. P. 73-98.
- Schmidt K. et al. Chlorhexidine antiseptic irrigation eradicates Staphylococcus epidermidis from biofilm: an in vitro study // Clinical orthopedics and related research. 2018. Vol. 476, № 3. P. 648653.
- Shahidi A., Ellner P.D. Effect of mixed cultures on antibiotic susceptibility testing // Applied microbiology. 1969. Vol. 18, № 5. P. 766-770.
- Szweda P., Gorczyca G., Tylingo R. Comparison of antimicrobial activity of selected, commercially available wound dressing materials // Journal of wound care. 2018. Vol. 27, № 5. P. 320-326.
- Weinbauer M.G. Ecology of prokaryotic viruses // FEMS microbiology reviews. 2004. Vol. 28, № 2. P. 127-181.


