Влияние биоугля на развитие яровой пшеницы (Triticum aestivum L.) и кислотность дерново-подзолистой почвы в Западной Сибири
Автор: Пономарев К. О., Первушина А. Н., Коротаева К. С., Юртаев А. А., Петухов А. С., Табакаев Р. Б., Шаненков И. И.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Рубрика: Статьи
Статья в выпуске: 113, 2022 года.
Бесплатный доступ
Цель исследования состояла в установлении влияния внесения в почву биоуглей, полученных из разных, характерных для Западной Сибири органических отходов сельского хозяйства (коровий навоз, солома), деревообрабатывающей (сосновые опилки) и пищевой промышленности (скорлупа кедрового ореха) на морфометрические характеристики растений (на примере яровой пшеницы (Triticum aestivum L.)) и свойства дерново-подзолистой почвы. Оценка влияния осуществлялась в ходе проведения вегетационных экспериментов с использованием климатических камер. В результате вегетационных исследований установлено, что внесение всех отмеченных видов биоуглей в слой почвы приводит к достоверному (p
Органические отходы, биоугольный мелиорант, вегетационный опыт, морфометрические показатели пшеницы, почвенные свойства
Короткий адрес: https://sciup.org/143179661
IDR: 143179661 | УДК: 631.4 | DOI: 10.19047/0136-1694-2022-113-110-137
Biochar influence on the development of spring wheat (Triticum aestivum L.) and acidity of soddy-podzolic soil in Western Siberia
The paper purpose was to establish the effect of applying biochar obtained from various organic wastes of agriculture (cow manure, straw), woodworking (pine sawdust) and food industry (pine nut shell), which are typical of Western Siberia, on the morphometric characteristics of plants (using spring wheat (Triticum aestivum L.) as the example) and the soddy-podzolic soil properties. The assessment of biochar influence was performed by a series of vegetation experiments using climatic chambers. As a result, it was found that the introduction of all the noted biochar types into the soil layer leads to a significant (p
Текст научной статьи Влияние биоугля на развитие яровой пшеницы (Triticum aestivum L.) и кислотность дерново-подзолистой почвы в Западной Сибири
Большая часть органических отходов, которая образуется в процессе деятельности пищевой, аграрной и деревообрабатывающей промышленности, чаще всего не используется и утилизируется путем сжигания (Wang et al., 2014; Mohan et al., 2018; Sarauer et al., 2019) . При таком неэффективном способе утилизации окружающая среда загрязняется летучей золой и парниковыми газами, доля которых в атмосфере растет (Kumar et al., 2022) . Одним из решений проблемы утилизации биоотходов предприятий без вреда для окружающей среды является их депонирование в почве, способствующее секвестрации углерода. Однако важно понимать, что процесс разложения в почве органического вещества в исходном виде занимает 5–10 лет, при этом в атмосферу продолжают выделяться CO 2 и другие газы (Mohan et al., 2018; Adeodun et al., 2022) . Поэтому в настоящее время с целью решения ряда вопросов, таких как утилизация отходов, снижение эмиссии парниковых газов, долгосрочное связывание углерода в почве, а также повышение плодородия почвы и урожайности культур, органическое сырье подвергают термохимической обработке с получением биоугля (Zhang et al., 2016; Amin, 2020) .
Биоуголь представляет собой нелетучий углеродистый остаток, получаемый в процессе пиролиза биомассы (т. е. в условиях высоких температур и ограниченного доступа кислорода) (Zhang et al., 2016; Gabhane et al., 2020) . Внесение биоугля в почву положительно влияет на поглощение элементов питания растениями. Это доказывает многолетний опыт фермеров из Европы, Америки,
Китая, Австралии и Индии (Zhang et al., 2016) . Исследователями неоднократно установлено, что использование биоугля улучшает физико-химические свойства почвы (Igaz et al., 2018; Juriga, Šimanský, 2019) и ее водно-воздушный режим (Baiamonte et al., 2015; Juriga et al., 2021) , повышает урожайность сельскохозяйственных культур (Graber et al., 2010; Cornelissen et al., 2018) и за счет секвестрации углерода приводит к сокращению выбросов парниковых газов (Amin, 2020; Sun et al., 2022) . Однако известны и противоположные результаты (Wardle et al., 2008; Griffin et al., 2017; Juriga, Šimanský, 2019; Meschewski et al., 2019) , когда авторы показывали, что использование биоугля в качестве мелиоранта приводит к ухудшению микробиологической активности почвы, снижению морфометрических характеристик растений и увеличению эмиссии парниковых газов. Негативное влияние объясняется постепенным истощением щелочных соединений из углеродистого мелиоранта (Cornelissen et al., 2018) и снижением сорбционной способности (Ren et al., 2018) , которое может возникнуть из-за закрытия пор почвенными агрегатами (Beusch, 2021) . Слабо выраженный положительный эффект или его отсутствие от внесения биоуглей в почву можно наблюдать при их неверном подборе для конкретного региона.
Вид сырья, из которого получают биоуголь, и способ его переработки необходимо подбирать с учетом особенностей рассматриваемого региона – вида характерных отходов и свойств почвы. Различия в почвенных свойствах приводят к разному эффекту от внесения биоугля (Zhao et al., 2013; Beusch, 2021). Среди почв Западной Сибири часто встречаются легкие по гранулометрическому составу (Гвоздецкий, 1973; Kapitonova et al., 2019). Влагоудерживающая способность таких почв низкая (Kapitonova et al., 2019). При инфильтрации атмосферных осадков полезные вещества просачиваются через такую почву, становясь недоступными для растений. Благодаря высокой пористости и удельной площади гидрофильной поверхности биоугля внесение его в почву с легким гранулометрическим составом позволит повысить запасы продуктивной влаги (Белашов, Рижия, 2020). Но с экономической точки зрения поиск сырья и его переработка или закупка и транспортировка коммерческого биоугля могут быть нецелесообразны, по сравне- нию с получаемым эффектом от применения биоугольного мелиоранта в сельском хозяйстве (Jones et al., 2012). Использование органических отходов предприятий рассматриваемого региона с переработкой их в биоуголь является важным аспектом.
Все виды биомассы (растительные, древесные и сельскохозяйственные органические отходы), характерные для Западной Сибири, отличаются элементным составом (органической и минеральной частями) и свойствами. Поэтому использование биоугля, полученного из разных видов биомассы, в качестве мелиоранта, очевидно, окажет разное влияние на удержание элементов и сохранение питательных веществ в почвах (Yao et al., 2012; Zhao et al., 2013) . Биоуголь из отходов жизнедеятельности крупного рогатого скота имеет высокую концентрацию питательных веществ, а количество золы и ее состав в сырье обеспечивают биоуглю щелочные свойства (Cantrell et al., 2012; Zhao et al., 2013) . Биоуголь из рисовой соломы ускоряет нитрификацию, снижает выщелачивание азота из почвы и ее объемную плотность, улучшает поглощение азота, фосфора и калия растениями и повышает урожайность пшеницы и проса (Zhao et al., 2014; He et al., 2016) . Известно (Igalavithana et al., 2020) , что биоуголь, полученный из сосновых опилок, отличается более высоким потенциалом поглощения СО 2 , чем, например, биоуголь из шлама бумажной фабрики. Также стоит добавить, что хорошо изучено влияние биоуглей из опилок березы и осины на свойства дерново-подзолистой супесчаной почвы (Rizhiya et al., 2015) , которая является типичной для Западной Сибири, и мало изучено влияние биоуглей из древесины сосны, которая также характерна для данного природного региона. О влиянии на свойства почвы биоугля, полученного из такого растительного материала как скорлупа орехов, известно мало. Изучение скорлупы в качестве одного из перспективных видов биомассы для получения биоугля требует дальнейших исследований как минимум из-за щелочного pH (Ahmadou et al., 2019) .
Таким образом, внесение в почву биоугля из органических отходов сельского хозяйства, деревообрабатывающей и пищевой промышленности играет важную роль в экологическом менеджменте за счет управления местными отходами, повышения плодородия почвы и смягчения последствий изменения климата (Amin,
2020; Joseph et al., 2021) . Поскольку выбор сырья зависит от конкретного региона, то из определенных и типичных для Западной Сибири органических отходов – соломы, навоза, опилок, скорлупы кедровых орехов – важно выбрать те, которые будут обладать наибольшими агрономическими преимуществами. Поэтому цель исследования состояла в установлении влияния внесения в почву биоугля, полученного из разных, характерных для Западной Сибири органических отходов, на морфометрические характеристики растений и почвенные свойства.
ОБЪЕКТЫ И МЕТОДЫ
Почву для экспериментов отбирали из пахотного горизонта (0–20 см) с территории Биостанции ТюмГУ, расположенной в Нижнетавдинском районе Тюменской области. Территория биостанции характеризуется дерново-подзолистой почвой с лесами (сосновыми, осиновыми, березовыми) и болотными комплексами (Гвоздецкий, 1973) . Почву перед экспериментами высушивали до воздушно-сухого состояния в вентилируемом помещении, просеивали через сито с диаметром отверстий 10 мм, чтобы удалить посторонние включения (камни, корни и пр.), и анализировали согласно аттестованным методикам: кислотность по водной вытяжке – ГОСТ 26423-85, кислотность по солевой вытяжке – ГОСТ 2648385, гигроскопическая влажность – ГОСТ 28268-89. Плотность сложения почвы определили с использованием алюминиевого бюкса. Гранулометрический состав исследован с использованием анализатора размеров частиц Pario.
В экспериментах использовали исходную почву (контроль) и почвы, в которые внесли биоугли. Биоугли получили из характерной для Западной Сибири биомассы: сосновые опилки, скорлупа кедровых орехов, отходы жизнедеятельности крупного рогатого скота (навоз), пшеничная солома. Для этого биомассу помещали в реактор, после чего осуществляли ее нагрев до 600 ℃ со скоростью 10 ℃ в минуту (Tabakaev et al., 2019). В процессе нагрева происходило термическое разложение биомассы с выделением летучих продуктов в виде паров смолы и газа, которые удалялись из реактора через трубку, соединенную с колбой. В колбе пары смолы конденсировались, газ собирался в пробоотборной емкости для дальнейшего анализа. При достижении требуемого значения температуры внутри реактора производили выдержку (15 минут) до полного визуального окончания процесса, после чего нагрев прекращали, реактор охлаждался естественным способом. При остывании реактора до комнатной температуры биоуголь извлекался из реактора для дальнейшего использования и изучения его характеристик. В таблице 1 приведен элементный состав и зольность биоуглей.
Таблица 1. Элементный состав и зольность биоуглей
Table 1. Elemental composition and ash content of biochars
|
Биоуголь |
С d |
H d |
N d |
S d |
O d |
A d |
|
% |
||||||
|
Сосновые опилки |
88.87 |
2.45 |
0.13 |
0.02 |
4.06 |
4.47 |
|
Скорлупа кедровых орехов |
88.89 |
2.21 |
0.41 |
0.01 |
6.66 |
1.82 |
|
Отходы жизнедеятельности крупного рогатого скота (навоз) |
52.62 |
1.53 |
1.74 |
0.14 |
8.79 |
35.18 |
|
Пшеничная солома |
78.61 |
1.99 |
1.01 |
0.03 |
4.87 |
13.49 |
Примечание. Данные в таблице приведена на сухую массу: С d – углерод; H d – водород; N d – азот; S d – сера; O d – кислород; A d – зольность.
В таблице 2 приведены содержащиеся в биоуглях активные микроэлементы. Фосфор представлен в сравнительной форме по отношению к доле фосфора в опилках из-за отсутствия калибровочного элемента в атомно-эмиссионном спектрофотометре .
Полученные в результате пиролиза биоугли массой 21.38 г смешали с 2 кг почвы и внесли в вегетационные сосуды, что соответствовало дозе биоугля 30 т/га.
Таблица 2. Содержание микроэлементов в вытяжке из рассматриваемых биоуглей
Table 2. Сontent of trace elements in extracts from the considered biochars
|
© s a . S ^ |
5 я ea a о 4 и s о о и |
се и В 3 и 5 ® § 5 ® и и |
wo£®_ д д © д * 5 ® „ “ д о м
О д и а |
д * я ч в |
|
K |
1 565 |
2 993 |
36 500 |
15 560 |
|
Ca |
2 773 |
242 |
28 175 |
9 258 |
|
Mg |
284 |
78 |
7 448 |
2 437 |
|
Na |
132 |
47 |
6 643 |
1 196 |
|
Fe |
216 |
14.4 |
5 320 |
2 335 |
|
Al |
185 |
7.1 |
1 187 |
2 012 |
|
Si |
164 |
25 |
994 |
848 |
|
Р i / P опилки |
1.0 |
2.0 |
241.0 |
89.5 |
Примечание. K – калий; Ca – кальций; Mg – магний; Na – натрий; Fe – железо; Al – алюминий; Si – кремний; P – фосфор.
Доза внесения в почву биоугля выбрана согласно рекомендациям исследователей (Lehmann et al., 2011; Литвинович и др., 2016; Agbede, Oyewumi, 2022). Установлено, что использование биоугля в количестве 30 т/га привело к достижению наиболее высокого (по сравнению с дозами внесения 0, 10 и 20 т/га) урожая (Agbede, Oyewumi, 2022), достоверной прибавке сухой биомассы (Литвинович и др., 2016), увеличению микробной биомассы (Lehmann et al., 2011). В каждый сосуд добавили 20 семян яровой пшеницы (Triticum aestivum L.) сорта “Ирень”. Сосуды с посаженной культурой помещались в климатическую камеру роста Jeio Tech GC-1000TLH (Jeio Tech (Lab Companion), Южная Корея) в рандомизированном порядке. Климатическая камера позволяла регулировать освещенность, температуру и влажность. Освещенность в камере поддерживалась на уровне 20 кЛк на верхней полке и 8 кЛк на нижней в течение 16 часов в сутки (режим “день”), 0 кЛк в течение 8 часов (режим “ночь”). Температуры в режимах “день” и “ночь” выбирались в фенологических фазах прорастания, кущения и выхода в трубку: 15/12 °С, 18/15 °С, 23/16 °С соответственно. Влажность почвы поддерживали на уровне 60% от полной влагоемкости. Вегетационные сосуды располагались в шахматном порядке случайным образом. Каждые два дня пинцетом удаляли сорняки, поливали растения дистиллированной водой и меняли местами сосуды, расположенные на верхней и нижней полках, с целью идентичности условий эксперимента. Через 10 дней после посева определили всхожесть семян и проредили растения до 15 культур в емкости. В конце эксперимента были определены морфометрические характеристики растений: высота растения, количество листьев, длина корней и масса его отдельных органов (листья, стебель, корень). Масса почвы, биоугля, растений измерялась с использованием весов ViBRA LN-3202RCE (ViBRA (Shinko Denshi), Япония) с погрешностью 0.01 г. Повторность опыта – четырехкратная. Статистическая обработка данных проводилась с помощью дисперсионного анализа. В зависимости от закона распределения (нормальная, логнормальная или другие модели) использовались параметрические критерии Стьюдента, Родионова или Колмогорова–Смирнова, U – критерий Манна– Уитни. Достоверные статистические различия между средними значениями приняты при уровне надежности p < 0.05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Характерные для Западной Сибири дерново-подзолистые почвы обладают низким содержанием питательных веществ (Rizhiya et al., 2015) . Наличие питательных веществ, влаги и воздуха в почве является важным фактором урожайности и развития растений. В таблице 3 приведены свойства почвы-контроля и ее химико-физические характеристики.
Результаты анализа свойств почвы (табл. 3) показали, что почва является нейтральной, что характерно для пахотного горизонта дерново-подзолистых почв (Rizhiya et al., 2015) .
Таблица 3. Свойства почвы-контроля и ее химико-физические характеристики
Table 3. Control soil properties and its chemical and physical characteristics
|
ρ , г/см3 |
W , % |
ПВ , % |
p Hh2o |
p Hkc l |
С , % |
H , % |
N , % |
S , % |
|
1.4 |
1.3 |
30.16 |
7.22 |
6.52 |
0.90 |
0.00 |
0.07 |
0.01 |
Примечание. ρ – плотность сложения почвы; W – гигроскопическая влажность почвы; ПВ – полная влагоемкость на 100 г абсолютно сухой почвы; pH H2O – кислотность по водной вытяжке; pH KCl – кислотность по солевой вытяжке; C – углерод; H – водород; N – азот; S – сера.
По гранулометрическому составу (песок – 87%, пыль – 4%, глина – 9%), установленному методом Ферре, почва относится к супесям. Такие почвы пропускают значительную долю влаги и содержат малое количество органических веществ (Капитонова, Аксарина, 2019) . Формирование нарушенных почвенных массивов в Сибири вызвано факторами антропогенного и природного характера. Известно (Новохатин, 2015) , что при формировании урожая пшеницы особое влияние в вегетационный период оказывает обеспеченность зерновой культуры влагой и теплом. Так как 80% Западной Сибири составляет Западно-Сибирская равнина, то открытость местности к северу приводит к беспрепятственному проникновению арктических воздушных масс. Последнее оказывает влияние на промерзание почвы (глубина промерзания может достигать 2 м, а оттаивание начинается только с апреля (Новохатин, 2015) ). Таким образом, характерные для Западной Сибири почвы требуют мелиорации и погашения кислотности.
Внесение биоугля в исходную почву привело к увеличению лабораторной всхожести семян на 5–15% (табл. 4).
Рост всхожести семян при добавлении биоугля в почву отмечалось и другими исследователями (Jabborova et al., 2021). Данные (табл. 4) свидетельствует о том, что добавление в почву биоугля из разных видов биомассы будет оказывать различное, но в то же время положительное влияние на экологические функции почвы и морфофизиологическое состояние растений. Морфометрические характеристики растений в исследуемых почвах опреде- лены после вегетационного опыта, который длился 39 дней (рис. 1).
Таблица 4. Лабораторная всхожесть семян в исследуемых почвах
Table 4. Laboratory germination of seeds in studied soils
|
Вариант почвенной смеси |
А |
Б1 |
Б2 |
Б3 |
Б4 |
|
ВС , % |
82.5 |
93.8 |
97.5 |
90 |
87.5 |
Примечание. ВС – лабораторная всхожесть семян; А – почва-контроль; Б1 – почва с биоуглем из сосновых опилок; Б2 – почва с биоуглем из скорлупы кедровых орехов; Б3 – почва с биоуглем из отходов жизнедеятельности крупного рогатого скота (навоза); Б4 – почва с биоуглем из пшеничной соломы.
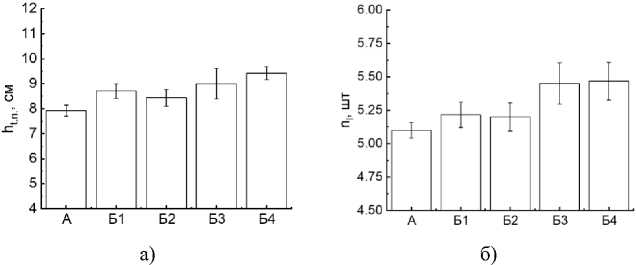
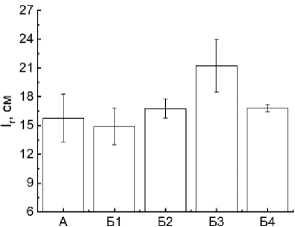
Достоверное ( p < 0.05) увеличение высоты пшеницы ( h tn ) установлено при внесении в почву биоугля из сосновых опилок, отходов жизнедеятельности крупного рогатого скота и пшеничной соломы (рис. 1). Наибольшая высота стебля наблюдалась у растений в почвах с навозом и пшеничной соломой, что, по-видимому, связано с высоким содержанием в них K и Si (табл. 2). При этом высокая концентрация и других неорганических компонентов ( Ca , Mg , Na , Fe , Al , Р ) в биоуглях привела к достоверному ( p < 0.05) росту количества листьев ( n l ) у растений. Рост надземной массы яровой пшеницы свидетельствует о достаточном уровне влажности почвы и лучшем потреблении азота растениями. В таких условиях процессы фотосинтеза и дыхания будут протекать интенсивнее.
Длина корня пшеницы ( l r ) достоверно ( p < 0.005) выше в почве с биоуглем из отходов жизнедеятельности крупного рогатого скота. Внесение этого биоугля в почву привело к значительному увеличению в ней азота и фосфора, что обычно достигается внесением в почву соответствующих удобрений. Наличие этих элементов в почве ведет к интенсивному развитию корневой системы, что обеспечивает охват растением необходимой площади питания и в дальнейшем получение более высокого урожая пшеницы. Результаты согласуются с выводами других авторов
(Jabborova et al., 2021), показавших, что даже внесение 1% биоугля в почву влияет на развитие растений и рост их морфометрических характеристик.
в)
Рис. 1. Зависимости а ) высоты пшеницы до верхнего узла, из которого выходит флаговый лист, б ) количества листьев и в ) длины корня растения от варианта почвенной смеси, в которой она выращена: А – почва-контроль; Б1 – почва с биоуглем из сосновых опилок; Б2 – почва с биоуглем из скорлупы кедровых орехов; Б3 – почва с биоуглем из отходов жизнедеятельности крупного рогатого скота (навоза); Б4 – почва с биоуглем из пшеничной соломы.
Fig. 1. Dependences of a ) the wheat height to the top node from which the flag leaf emerges, б ) the number of leaves and в ) the root length on the soil mixture variant: А – soil-control; Б1 – soil with biochar from pine sawdust; Б2 – soil with biochar from pine nut shells; Б3 – soil with biochar from cattle waste (manure); Б4 – soil with biochar from wheat straw.
Результаты исследований показали, что внесение биоугля в почву не вызвало достоверного прироста по массе растения. Однако можно заметить (рис. 2), что добавление в почву биоугля из соломы привело к увеличению массы растения на 22.5%.
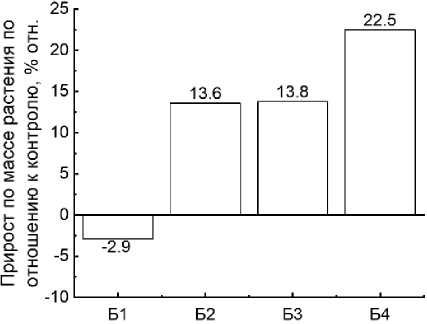
Рис. 2. Прирост по массе культуры по отношению к контролю: А – почва-контроль; Б1 – почва с биоуглем из сосновых опилок; Б2 – почва с биоуглем из скорлупы кедровых орехов; Б3 – почва с биоуглем из отходов жизнедеятельности крупного рогатого скота (навоза); Б4 – почва с биоуглем из пшеничной соломы.
Fig. 2. Growth in culture weight relative to control: А – soil-control; Б1 – soil with biochar from pine sawdust; Б2 – soil with biochar from pine nut shells; Б3 – soil with biochar from cattle waste (manure); Б4 – soil with biochar from wheat straw.
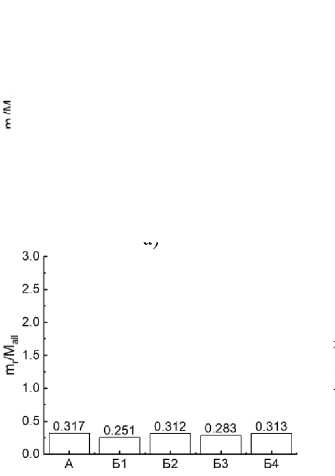
Эти данные свидетельствуют о том, что при необходимости увеличения массы культуры, например, для контролируемого выпаса скота, необходимо фокусироваться на выборе сырья, из которого будет изготовлен биоуголь, вносимый в почву. Установлено, что отношения масс отдельных частей растения к его общей массе и к массе корня достоверно не отличались. Исключением являлось отношение массы стебля пшеницы к общей массе растения в почве с биоуглем из навоза, которое достоверно ( p < 0.05) увеличилось по сравнению с контролем (рис. 3).
в)
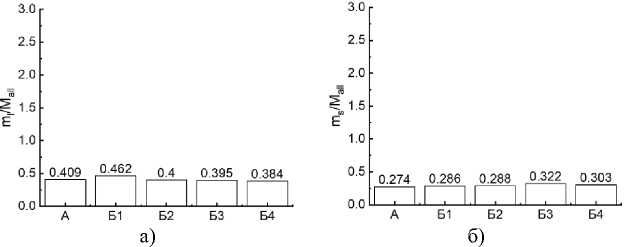
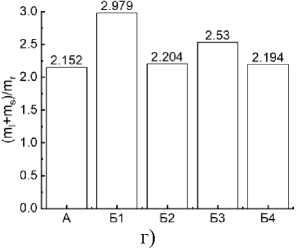
Рис. 3. Зависимости отношения масс а ) листьев, б ) стеблей, в ) корней к общей массе растения, и г ) отношения массы надземной части пшеницы к массе ее подземной (корневой) части: А – почва-контроль; Б1 – почва с биоуглем из сосновых опилок; Б2 – почва с биоуглем из скорлупы кедровых орехов; Б3 – почва с биоуглем из отходов жизнедеятельности крупного рогатого скота (навоза); Б4 – почва с биоуглем из пшеничной
соломы.
Fig. 3. Ratio of the masses of а ) leaves, б ) stems в ) roots to the total plant mass and г ) ratio of the wheat aerial part mass to its underground (root) part mass: А – soil-control; Б1 – soil with biochar from pine sawdust; Б2 – soil with biochar from pine nut shells; Б3 – soil with biochar from cattle waste (manure); Б4 – soil with biochar from wheat straw.
Крепкие стебли и длинные корни пшеницы в почве с биоуглем из отходов жизнедеятельности крупного рогатого скота могут быть объяснены малой величиной отношения углерода к азоту (C : N) в этом биоугле. В биоуглях из навоза, соломы, скорлупы орехов и опилок отношение C : N составляло 30, 78, 215 и 687 соответственно. Отсюда следует, что в почве Б3 наблюдается накоп- ление минеральных форм азота, которые легко усваиваются растениями (Novak et al., 2010; Tangmankongworakoon, 2019; Dubrovina, 2021). Результаты согласуются с данными других ученых (Geng et al., 2022). Отношение кислорода к углероду (O : C) у биоугля из навоза в 2–4 раза выше, чем у других биоуглей, что характеризует биоуголь как гидрофильный, адсорбционный материал, но ниже 0.4, что указывает на его высокую стабильность и большой период полураспада (Leng et al., 2019). Эти свойства биоугля обеспечивают долгосрочное удержание влаги в почве (снижаются риски пересыхания и переувлажнения). Таким образом, применение биоугля, полученного из отходов крупного рогатого скота, позволяет улучшить водно-воздушный баланс в почве и обеспечить растение полезным питанием. Это является важным результатом, так как корневая система яровой пшеницы менее развита по сравнению с другими злаковыми культурами (Алферов, 2020), а использование биоугля приводит к развитию подземных органов растения, что благоприятно влияет на достижение и поглощение корнями питательных элементов и влаги.
Внесение биоугля в почву влияет на ее свойства (Dubrovina, 2021) . Изменение кислотности почвы является важным фактором, потому что от pH почвы зависит микробная активность и доступность питательных веществ для растений. Показано (рис. 4), что кислотность исследуемой почвы после экспериментов составляла 7.1 и 6.3 по водной и солевой вытяжкам, соответственно.
Кислотность контроля после экспериментов составляла 7.1 по водной и 6.3 по солевой вытяжкам (рис. 4). После уборки растений показатель pH почвы с опилками и скорлупой кедровых орехов немного уменьшился (кислотность увеличилась) до 7.0 (6.2 по солевой) и 7.1 (6.2 по солевой) соответственно. Кислотность почв с навозом и соломой уменьшилась, т. к. pH увеличился до 7.8 (7 по солевой) и 7.4 (6.6 по солевой) соответственно. Сдвиг pH почвы на 0.2–0.4 единицы считается значительным влиянием биоугля на кислотность почвы (Wang et al., 2014) . Улучшение pH почвы некоторыми биоуглями связано с тем, что при пиролизе сырья кислотные функциональные группы и катионы в нем образуют щелочные вещества (карбонаты и оксиды), которые нейтрализуют ионы водорода в почве, снижая ее кислотность.
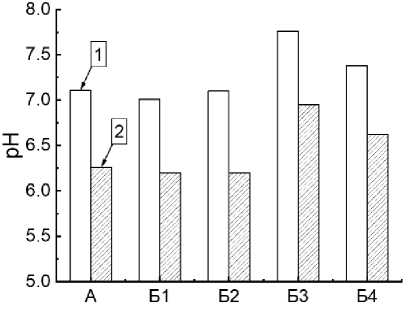
Рис. 4. Кислотность почвы по водной ( 1 ) и солевой ( 2 ) вытяжкам: А – почва-контроль; Б1 – почва с биоуглем из сосновых опилок; Б2 – почва с биоуглем из скорлупы кедровых орехов; Б3 – почва с биоуглем из отходов жизнедеятельности крупного рогатого скота (навоза); Б4 – почва с биоуглем из пшеничной соломы.
Fig. 4. Soil acidity according to water ( 1 ) and salt ( 2 ) extracts. А – soilcontrol; Б1 – soil with biochar from pine sawdust; Б2 – soil with biochar from pine nut shells; Б3 – soil with biochar from cattle waste (manure); Б4 – soil with biochar from wheat straw.
В биоугле из соломы и навоза щелочных веществ было больше, что видно по высокому содержанию золы (табл. 2). Таким образом, сдвиг реакции (pH) почвы в сторону щелочности с CMB и WSB может быть связан как с добавлением основных катионов в почву (например, таких как K, Ca, Mg, Na), так и декарбоксилированием органических анионов и аммонификацией лабильного органического азота в биоуглях (Raza et al., 2021) . В таких условиях буферность почвы при внесении в нее биоугля повышается, что согласуется с результатами других исследователей (Geng et al., 2022) . Поэтому на почвах с внесенным биоуглем из соломы и навоза урожайность будет выше (Cornelissen et al., 2018) . Однако определение урожайности и оценка продолжительности влияния биоугля на кислотность почвы требует проведения дополнительных специальных экспериментов, в том числе с добавлением традиционных (азотных, фосфорных, калийных) удобрений (Jones et al., 2012) .
ЗАКЛЮЧЕНИЕ
По результатам экспериментальных исследований установлено, что при внесении в дерново-подзолистый слой почвы биоугля, полученного из характерных для Западной Сибири органических отходов, наблюдается достоверный ( p < 0.05) рост морфометрических характеристик яровой пшеницы. При использовании биоуглей из соломы и навоза в качестве мелиорантов достигается снижение кислотности почвы. Агрономические преимущества у биоуглей из пшеничной соломы и отходов жизнедеятельности крупного рогатого скота проявляются лучше, чем у биоуглей из сосновых опилок и скорлупы кедровых орехов, что связано с более высокой концентрацией питательных элементов и щелочных веществ в них. Полученные результаты полезны с точки зрения оценки экологических рисков использования биоугольных мелиорантов в почвах, типичных для бореального биоклиматического пояса. Последующие эксперименты, включающие в себя опыты совместного внесения биоугля и удобрений в почву, позволят разработать рекомендации по использованию технологии термической конверсии региональных органических отходов в мелиоранты, улучшающие качество почв и повышающие их плодородие.
Список литературы Влияние биоугля на развитие яровой пшеницы (Triticum aestivum L.) и кислотность дерново-подзолистой почвы в Западной Сибири
- Алферов А.А. Ассоциативный азот, урожай и устойчивость агроэкосистемы. М.: РАН, 2020. 184 с. https://doi.org/10.25680/VNIIA.2019.21.92.152.
- Балашов Е.В., Рижия Е.Я. Влияние биоугля на плотность сложения и водоудерживающую способность супесчаной дерново-подзолистой почвы разной степени окультуренности // Агрофизика. 2020. № 2. С. 1-9. https://doi.org/10.25695/AGRPH.2020.02.01.
- Гвоздецкий Н.А. Физико-географическое районирование Тюменской области. М.: Изд-во Московского университета, 1973. 246 с.
- Капитонова О.А., Аксарина К.Ю. О некоторых физико-химических свойствах почв песчаных обнажений северных районов Западной Сибири // Динамика окружающей среды и глобальные изменения климата. 2019. Т. 10. № 1. С. 28-38. https://doi.org/10.17816/edgcc10533.
- Литвинович А.В., Хаммам А.А.М., Лаврищев А.В., Павлова О.Ю. Мелиоративные свойства и удобрительная ценность различных по размеру фракций биоугля (по данным лабораторных экспериментов) // Агрохимия. 2016. № 9. C. 46-53.
- Новохатин В.В. Биоклиматические ресурсы Северного Зауралья // Аграрный вестник Урала. 2015. № 8 (138). С. 22-28
- Adeodun S.A., Sangodoyin A.Y., Ogundiran M.B. Optimisation of biochar yield from sorted wood wastes as sustainable alternatives to burning to ash // Ecological Chemistry and Engineering S. 2022. Vol. 29. No. 1. P. 15-26. https://doi.org/10.2478/eces-2022-0003.
- Agbede T.M., Oyewumi A. Benefits of biochar, poultry manure and biochar-poultry manure for improvement of soil properties and sweet potato productivity in degraded tropical agricultural soils // Resources, Environment and Sustainability. 2022. Vol. 7. P. 100051. https://doi.org/10.1016/j.resenv.2022.100051.
- Ahmadou A., Napoli A., Durand N., Montet D. High physical properties of cashew nut shell biochars in the adsorbtion of mycotoxins // International Journal of Food Research. 2019. Vol. 6. P. 18-28. https://doi.org/10.2478/eces-2022-0003.
- Amin A.E.E.A.Z. Bagasse pith-vinasse biochar effects on carbon emission and nutrient release in calcareous sandy soil // Journal of Soil Science and Plant Nutrition. 2020. Vol. 20. No. 1. P. 220-231. https://doi.org/10.1007/s42729-019-00125-9.
- Baiamonte G., De Pasquale C., Marsala V., Cimò G., Alonzo G., Crescimanno G., Conte P. Structure alteration of a sandy-clay soil by biochar amendments // Journal of Soils and Sediments. 2015. Vol. 15. No. 4. P. 816-824. https://doi.org/10.1007/s11368-014-0960-y.
- Beusch C. Biochar as a soil ameliorant: how biochar properties benefit soil fertility - a review // Journal of Geoscience and Environment Protection. 2021. Vol. 09. No. 10. P. 28-46. https://doi.org/10.4236/gep.2021.910003.
- Cantrell K.B., Hunt P.G., Uchimiya M., Novak J.M., Ro K.S. Impact of pyrolysis temperature and manure source on physicochemical characteristics of biochar // Bioresource Technology. 2012. Vol. 107. P. 419-428. https://doi.org/10.1016/j.biortech.2011.11.084.
- Cornelissen G., Jubaedah, Nurida N.L., Hale S.E., Martinsen V., Silvani L., Mulder J. Fading positive effect of biochar on crop yield and soil acidity during five growth seasons in an Indonesian Ultisol // Science of the Total Environment. 2018. Vol. 634. No. 0806. P. 561-568. https://doi.org/10.1016/j.scitotenv.2018.03.380.
- Dubrovina I.A. Effects of biochar on the agrochemical indicators and enzyme activity of soils in the middle taiga of Karelia // Eurasian Soil Science. 2021. Vol. 54. No. 12. P. 1957-1966. https://doi.org/10.1134/S106422932112005X.
- Gabhane J.W., Bhange V.P., Patil P.D., Bankar S.T., Kumar S. Recent trends in biochar production methods and its application as a soil health conditioner: a review // SN Applied Sciences. 2020. Vol. 2. No. 7. P. 1-21. https://doi.org/10.1007/s42452-020-3121-5.
- Geng N., Kang X., Yan X., Yin N., Wang H., Pan H., Yang Q., Lou Y., Zhuge Y. Biochar mitigation of soil acidification and carbon sequestration is influenced by materials and temperature // Ecotoxicology and Environmental Safety. 2022. Vol. 232. P. 113241. https://doi.org/10.1016/j.ecoenv.2022.113241.
- Graber E.R., Harel Y.M., Kolton M., Cytryn E., Silber A., David D.R., Tsechansky L., Borenshtein M., Elad Y. Biochar impact on development and productivity of pepper and tomato grown in fertigated soilless media // Plant and Soil. 2010. Vol. 337. No. 1. P. 481-496. https://doi.org/10.1007/s11104-010-0544-6.
- Griffin D.E., Wang D., Parikh S.J., Scow K.M. Short-lived effects of walnut shell biochar on soils and crop yields in a long-term field experiment // Agriculture, Ecosystems and Environment. 2017. Vol. 236. P. 21-29. https://doi.org/10.1016/j.agee.2016.11.002.
- He L., Liu Y., Zhao J., Bi Y., Zhao X., Wang S., Xing G. Comparison of straw-biochar-mediated changes in nitrification and ammonia oxidizers in agricultural oxisols and cambosols // Biology and Fertility of Soils. 2016. Vol. 52. No. 2. P. 137-149. https://doi.org/10.1007/s00374-015-1059-3.
- Igalavithana A.D., Choi S.W., Shang J., Hanif A., Dissanayake P.D., Tsang D.C.W., Kwon J.H., Lee K.B., Ok Y.S. Carbon dioxide capture in biochar produced from pine sawdust and paper mill sludge: Effect of porous structure and surface chemistry // Science of the Total Environment. 2020. Vol. 739. P. 139845. https://doi.org/10.1016/j.scitotenv.2020.139845.
- Igaz D., Šimanský V., Horák J., Kondrlová E., Domanová J., Rodný M., Buchkina N.P. Can a single dose of biochar affect selected soil physical and chemical characteristics? // Journal of Hydrology and Hydromechanics. 2018. Vol. 66. No. 4. P. 421-428. https://doi.org/10.2478/johh-2018-0034.
- Jabborova D., Ma H., Bellingrath-Kimura S.D., Wirth S. Impacts of biochar on basil (Ocimum basilicum) growth, root morphological traits, plant biochemical and physiological properties and soil enzymatic activities // Scientia Horticulturae. 2021. Vol. 290. P. 110518. https://doi.org/10.1016/j.scienta.2021.110518.
- Jones D.L., Rousk J., Edwards-Jones G., DeLuca T.H., Murphy D.V. Biochar-mediated changes in soil quality and plant growth in a three-year field trial // Soil Biology and Biochemistry. 2012. Vol. 45. P. 113-124. https://doi.org/10.1016/j.soilbio.2011.10.012.
- Joseph S., Cowie A.L., Van Zwieten L., Bolan N., Budai A., Buss W., Cayuela M.L., Graber E.R., Ippolito J.A., Kuzyakov Y., Luo Y., Ok Y.S., Palansooriya K.N., Shepherd J., Stephens S., Weng Z., Lehmann J. How biochar works, and when it doesn’t: A review of mechanisms controlling soil and plant responses to biochar // GCB Bioenergy. 2021. Vol. 13. No. 11. P. 1731-1764. https://doi.org/10.1111/gcbb.12885.
- Juriga M., Aydln E., Horák J., Chlpík J., Rizhiya E.Y., Buchkina N.P., Balashov E.V., Šimanský V. The importance of initial application and reapplication of biochar in the context of soil structure improvement // Journal of Hydrology and Hydromechanics. 2021. Vol. 69. No. 1. P. 87-97. https://doi.org/10.2478/johh-2020-0044.
- Juriga M., Šimanský V. Effects of biochar and its reapplication on soil pH and sorption properties of silt loam haplic Luvisol // Acta Horticulturae et Regiotecturae. 2019. Vol. 22. No. 2. P. 65-70. https://doi.org/10.2478/ahr-2019-0012.
- Kapitonova O.A., Aksarina K.Y., Yu A.K. On some physical and chemical properties of soils of sandy outcrops of the West Siberian northern regions // Environmental dynamics and global climate change. 2019. Vol. 10. No. 1. P. 28-37. https://doi.org/10.17816/edgcc10533.
- Kumar A., Bhattacharya T., Mukherjee S., Sarkar B. A perspective on biochar for repairing damages in the soil-plant system caused by climate change-driven extreme weather events // Biochar. 2022. Vol. 4. No. 1. P. 1-23. https://doi.org/10.1007/s42773-022-00148-z.
- Lehmann J., Rillig M.C., Thies J., Masiello C.A., Hockaday W.C., Crowley D. Biochar effects on soil biota - A review // Soil biology and biochemistry. 2011. Vol. 43. No. 9. P. 1812-1836. https://doi.org/10.1016/j.soilbio.2011.04.022.
- Leng L., Huang H., Li H., Li J., Zhou W. Biochar stability assessment methods: A review // Science of the Total Environment. 2019. Vol. 647. P. 210-222. https://doi.org/10.1016/j.scitotenv.2018.07.402.
- Meschewski E., Holm N., Sharma B.K., Spokas K., Minalt N., Kelly J.J. Pyrolysis biochar has negligible effects on soil greenhouse gas production, microbial communities, plant germination, and initial seedling growth // Chemosphere. 2019. Vol. 228. P. 565-576. https://doi.org/10.1016/j.chemosphere.2019.04.031.
- Mohan D., Abhishek K., Sarswat A., Patel M., Singh P., Pittman C.U. Biochar production and applications in soil fertility and carbon sequestration - a sustainable solution to crop-residue burning in India // RSC Advances. 2018. Vol. 8. No. 1. P. 508-520. https://doi.org/10.1039/c7ra10353k.
- Novak J.M., Busscher W.J., Watts D.W., Laird D.A., Ahmedna M.A., Niandou M.A.S. Short-term CO2 mineralization after additions of biochar and switchgrass to a Typic Kandiudult // Geoderma. 2010. Vol. 154. No. 3-4. P. 281-288. https://doi.org/10.1016/j.geoderma.2009.10.014.
- Raza S., Zamanian K., Ullah S., Kuzyakov Y., Virto I., Zhou J. Inorganic carbon losses by soil acidification jeopardize global efforts on carbon sequestration and climate change mitigation // Journal of Cleaner Production. 2021. Vol. 315. P. 128036. https://doi.org/10.1016/j.jclepro.2021.128036.
- Ren X., Yuan X., Sun H. Dynamic changes in atrazine and phenanthrene sorption behaviors during the aging of biochar in soils // Environmental Science and Pollution Research. 2018. Vol. 25. No. 1. P. 81-90. https://doi.org/10.1007/s11356-016-8101-3.
- Rizhiya E.Y., Buchkina N.P., Mukhina I.M., Belinets A.S., Balashov E.V. Effect of biochar on the properties of loamy sand Spodosol soil samples with different fertility levels: A laboratory experiment // Eurasian Soil Science. 2015. Vol. 48. No. 2. P. 192-200. https://doi.org/10.1134/S1064229314120084.
- Sarauer J.L., Page-Dumroese D.S., Coleman M.D. Soil greenhouse gas, carbon content, and tree growth response to biochar amendment in western United States forests // GCB Bioenergy. 2019. Vol. 11. No. 5. P. 660-671. https://doi.org/10.1111/gcbb.12595.
- Sun Y., Lyu H., Cheng Z., Wang Y., Tang J. Insight into the mechanisms of ball-milled biochar addition on soil tetracycline degradation enhancement: Physicochemical properties and microbial community structure // Chemosphere. 2022. Vol. 291. P. 132691. https://doi.org/10.1016/j.chemosphere.2021.132691.
- Tabakaev R., Ibraeva K., Astafev A., Dubinin Y., Yazykov N., Zavorin A., Yakovlev V. Thermal enrichment of different types of biomass by low-temperature pyrolysis // Fuel. 2019. Vol. 245. P. 29-38. https://doi.org/10.1016/j.fuel.2019.02.049.
- Tangmankongworakoon N. An approach to produce biochar from coffee residue for fuel and soil amendment purpose // International Journal of Recycling of Organic Waste in Agriculture. 2019. Vol. 8. No. 1. P. 37-44. https://doi.org/10.1007/s40093-019-0267-5.
- Wang Y., Yin R., Liu R. Characterization of biochar from fast pyrolysis and its effect on chemical properties of the tea garden soil // Journal of Analytical and Applied Pyrolysis. 2014. Vol. 110. No. 1. P. 375-381. https://doi.org/10.1016/j.jaap.2014.10.006.
- Wardle D.A., Nilsson M.C., Zackrisson O. Fire-derived charcoal causes loss of forest humus // Science. 2008. Vol. 320. No. 5876. P. 629. https://doi.org/10.1126/science.1154960.
- Yao Y., Gao B., Zhang M., Inyang M., Zimmerman A.R. Effect of biochar amendment on sorption and leaching of nitrate, ammonium, and phosphate in a sandy soil // Chemosphere. 2012. Vol. 89. No. 11. P. 1467-1471. https://doi.org/10.1016/j.chemosphere.2012.06.002.
- Zhang D., Yan M., Niu Y., Liu X., van Zwieten L., Chen D., Bian R., Cheng K., Li L., Joseph S., Zheng J., Zhang X., Zheng J., Crowley D., Filley T.R., Pan G. Is current biochar research addressing global soil constraints for sustainable agriculture? // Agriculture, Ecosystems and Environment. 2016. Vol. 226. P. 25-32. https://doi.org/10.1016/j.agee.2016.04.010.
- Zhao L., Cao X., Mašek O., Zimmerman A. Heterogeneity of biochar properties as a function of feedstock sources and production temperatures // Journal of Hazardous Materials. 2013. Vol. 256-257. P. 1-9. https://doi.org/10.1016/j.jhazmat.2013.04.015.
- Zhao X., Wang S., Xing G. Nitrification, acidification, and nitrogen leaching from subtropical cropland soils as affected by rice straw-based biochar: Laboratory incubation and column leaching studies // Journal of Soils and Sediments. 2014. Vol. 14. No. 3. P. 471-482. https://doi.org/10.1007/s11368-013-0803-2.


