Влияние церия и алюминия на растворимость кислорода в жидкой стали
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 2 т.13, 2013 года.
Бесплатный доступ
Построены поверхности растворимости компонентов в металлических расплавах для системы Fe-Ce-Al-O. Показано, что в области достижимых концентраций кислорода, церия и алюминия возможно блокирование поверхности химически активных неметаллических включений. Выполнен анализ сравнительной раскислительной способности церия и алюминия путем построения диаграмм расходов активных металлов на рафинирование стали. Установлена большая раскислительная способность церия по отношению к алюминию.
Алюмоцерий, диаграммы, неметаллические включения
Короткий адрес: https://sciup.org/147156829
IDR: 147156829 | УДК: 669.18.046.552
Influence of cerium and aluminum on solubility of oxygen in liquid steel
Surfaces of solubility of components in metal melts are drawn for the Fe-Ce-Al-O system. It is shown that in the achievable range of oxygen, cerium and aluminum concentrations blocking of the surface of chemically active nonmetallic inclusions is possible. The analysis of comparative deoxidizing ability of cerium and aluminum is carried out by drawing diagrams of consumption of active metals for steel refinement. It is established that cerium has higher deoxidizing ability than aluminum.
Текст научной статьи Влияние церия и алюминия на растворимость кислорода в жидкой стали
Лигатуры с церием обычно вводятся в предварительно глубоко раскисленный алюминием металл. В этом случае возможна реализация процессов комплексного раскисления стали алюминием и церием. Эта ситуация в теоретическом плане в литературе не рассматривалась. Поэтому при последовательном рассмотрении процессов, протекающих при введении церия в металл, необходимо определить координаты поверхности растворимости компонентов в жидком металле (ПРКМ) для системы Fe–Ce–Al–O и Fe–Ce–Al–С–O.
При термодинамическом анализе фазовых равновесий для условий взаимодействия алюминия и церия с кислородом в жидком железе была установлена возможность существования области составов металла, равновесного с оксидным расплавом (FeO, Al2O3, CeO2, Ce2O3) переменного состава, твердыми оксидами алюминия и церия (трех- и четырехвалентного), герцинитом, и алюминатами церия (Ce2O3·Al2O3, Ce2O3·11Al2O3). В присутствии углерода возможно образование газовой фазы (CO, CO2). Температурные зависимости констант равновесия приведены в табл. 1.
Активности составляющих оксидного расплава (FeO, Al 2 O 3 , Ce 2 O 3 ) рассчитывали по теории субрегулярных растворов [1]. Найденные энергетические параметры приведены в табл. 2. В приближении теории совершенных растворов была ранее рассчитана диаграмма состояния системы FeO–Ce2O3. Активность CeO2 в оксидном расплаве приравнивали к ионной доле катионов церия четырехвалентного. Активности компонентов металлического расплава рассчитывали по теории Вагнера с использованием параметров взаимодей-
Таблица 1
Зависимость констант равновесия от температуры
|
Реакция |
lg K = – A / T + B |
|
|
A |
B |
|
|
(FeO) = [Fe] + [O] |
6320 |
4,734 |
|
(Al 2 O 3 ) = 2[Al] + 3[O] |
58 320 |
18,02 |
|
(CeO 2 ) = [Ce] + 2[O] |
39 540 |
11,99 |
|
(Ce 2 O 3 ) = 2[Ce] + 3[O] |
64 128 |
17,37 |
|
|Al 2 O 3 | = 2[Al] + 3[O] |
64 000 |
20,48 |
|
|CeO 2 | = [Ce] + 2[O] |
43 694 |
13,55 |
|
|Ce 2 O 3 | = 2[Ce] + 3[O] |
68 500 |
19,60 |
|
|FeO·Al 2 O 3 | = [Fe] + 2[Al] + 4[O] |
74 580 |
26,37 |
|
|Ce 2 O 3 ·Al 2 O 3 | = 2[Ce] + 2[Al] + 6[O] |
161 590 |
53,54 |
|
|Ce 2 O 3 ·11Al 2 O 3 | = 2[Ce] + 22[Al] + 36[O] |
742 720 |
223,44 |
|
{CO} = [C] + [O] |
1168 |
–2,07 |
|
{CO 2 } = [C] + 2[O] |
9616 |
2,51 |
Таблица 2
Параметры теории субрегулярных ионных растворов FeO–Al 2 O 3 –Ce 2 O 3
|
Система |
Энергетические параметры, кал/моль |
||
|
FeO–Al 2 O 3 |
Q 1112 = 661 |
Q 1122 = –16 329 |
Q 1222 = –4917 |
|
Al 2 O 3 –Ce 2 O 3 |
Q 2224 = –2800 |
Q 2244 = –24 314 |
Q 2444 = –14 966 |
Параметры взаимодействия ei j , T = 1600 °С, растворитель – жидкое железо [2]
На рис. 1 представлены результаты расчета координат ПРКМ в виде проекций на плоскость составов при 1600 °С. В областях, ограниченных контрастными линиями, нанесены составы металла, равновесного с указанными оксидными фазами. Тонкими линиями показаны изокислородные сечения (в логарифмической шкале). Следует отметить на рис. 1 наличие двух зон составов металла, равновесного с оксидными расплавами. В области I оксидный расплав обогащен FeO, в области VII – содержится значительное количество Ce 2 O 3 . Из рис. 1 видно, что при содержании алюминия больше 0,0001 мас. % образование фазы CeO2 уже вряд ли возможно. Для образования включений CeO2 необходимо иметь в металле бóльшую концентрацию кислорода, порядка сотых долей процента, и низкую концентрацию церия.
Добавление в систему углерода (рис. 2) приводит к тому, что в равновесии с металлом при концентрации церия порядка сотых долей процента и алюминия около тысячных долей процен- та устойчивой оксидной фазой может быть только Ce2O3 или Ce2O3 с равновесным с ним оксидным расплавом. Область IX характеризует постоянное содержание кислорода (lg[O] = –2,17 или [O] ≈ 0,0067 мас. %), которое определяется концентрацией углерода ([С] = 0,4 мас. %) и общим давлением ( Pобщ = 1 атм).
Для дальнейшего анализа процессов взаимодействия церия и алюминия с кислородом, альтернативной оценки их участия в процессе раскисления необходимо установить связь между добавками алюминия и церия в сталь, глубиной раскисления и фазовым составом образующихся неметаллических включений, т. е. построить так называемые диаграммы расхода рафинирующих компонентов.
Связь между составом металла, составами равновесных с ним неметаллических фаз и составом сплава для раскисления может быть установлена при решении балансовых уравнений. Расчет проводился на 1 т исходного металла (до раскисления). Допустим, что раскисление алюмоцерием следует провести таким образом, чтобы в равновесии
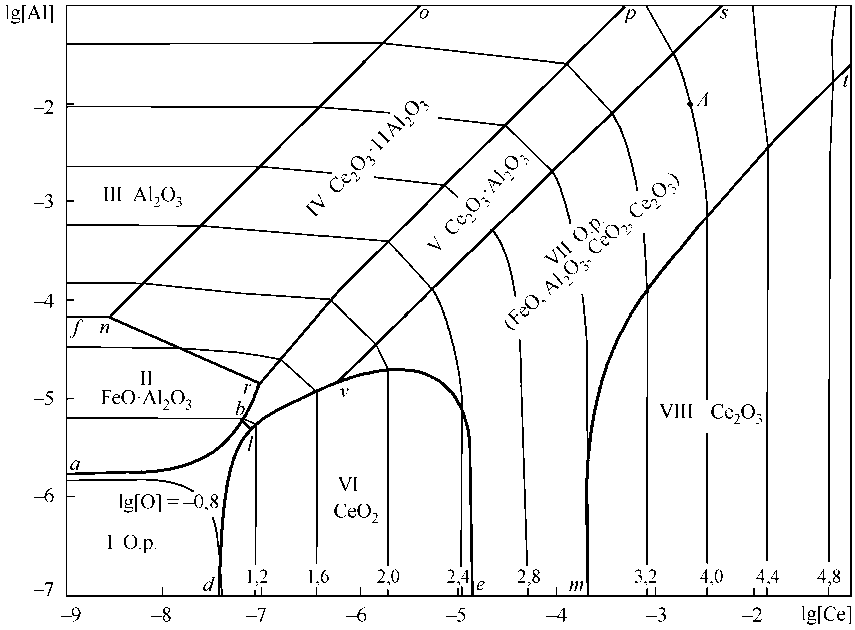
Рис. 1. ПРКМ системы Fe–Ce–Al–O, Т = 1600 °C
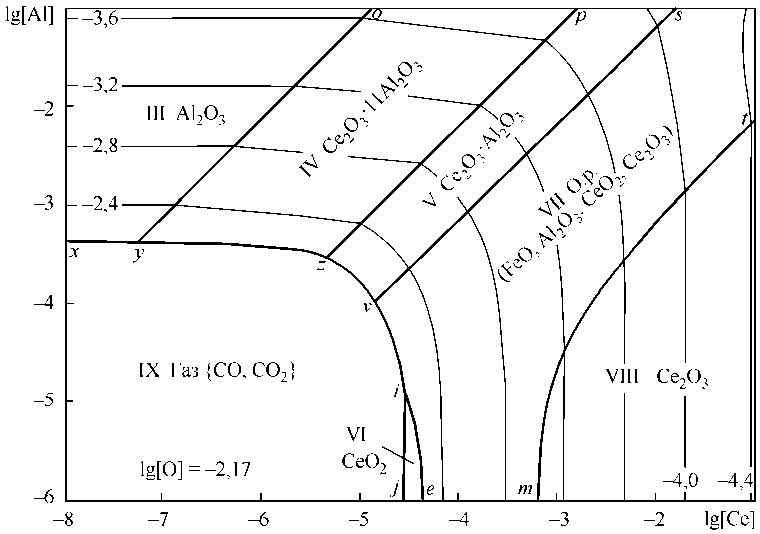
Рис. 2. ПРКМ системы Fe–Ce–Al–С–O, Т = 1600 °C, P общ = 1 атм, [С] = 0,4 мас. %
с металлом находились жидкие неметаллические включения (FeO, Al2O3, CeO2, Ce2O3). Для составления балансовых уравнений, кроме этого, необходимо знать химический состав металла перед раскислением, состав металла после раскисления и состав неметаллических включений. Для каждого из элементов рассматриваемой системы Fe–Al–Ce–O можно записать следующие балансовые уравнения
для получения при раскислении оксидного расплава:
1000 [ FeL _ [ Fe ] v . ( FeO,% ) M Fe v ; (1)
100 100 y 1 100 M FeO y 2 ;
1000 [ 0 ] исх [ О ] v +( ( FeO,% ) + 3 ( Al 2 O 3 ,% ) +
У + + +
100 100^ 1 ( M FeO M A1 2 O 3
M – молярные массы соединений и элементов.
В балансовом уравнении (3) для алюминия учтена возможность предварительного раскисления металла алюминием, церий вводится в предварительно раскисленный металл.
Состав жидкого металла и оксидной фазы после раскисления определен по результатам расчета равновесия (см. рис. 1), состав исходного металла задан ( I А1 ] исх = 0, [ О ] исх = 0,01-0,001 мас. %). Уравнения (1)–(4) позволяют найти величины z Al , z Ce , y 1 и y 2 . Зная эти величины, можно опреде-
лить, какое количество введенного в металл алю-
+
2 ( CeO2,% ) 3 ( Ce2O3,% ) ) Moy2 _^_------^ .-------- "-_ ;
миния расходуется непосредственно на связывание кислорода (раскисление)
M CeO2 M Ce2O3v г +1000[AlL |A'I . Al 100 100 y1
2 ( А12Оз,% ) Mai +
100M Al2O3
_ [ Ce ] z Ce 100 y 1
;
z
p
Al —
2 ( AI 2 O 3 ) M ai 100 M Al 2 O 3
y 2 ,
какое – на легирование стали
z Al — z Al -
2 ( AI 2 O 3 ) M ai 100 M Al2O3 y 2 .
(
+ ■
( CeO2,% ) + 2 ( Ce2O3,% ) ) M
V где [K]исх
M CeO2
M Ce 2 O 3 J
Ce y ;
100 2
и [ K ] - концентрации компонентов в
исходном и раскисленном металле, мас. %; (K) – концентрации компонентов в оксидном расплаве, мас. %; z Al , z Ce – расход церия и алюминия на раскисление и легирование 1000 кг исходного
жидкого металла, кг; y 1 и y 2 – количество металлической и оксидной фаз после раскисления, кг;
Результаты балансовых расчетов приведены в табл. 4 для условий равновесия, заданных точкой А (см. рис. 1), с указанием состава металла и равновесной оксидной фазы.
Баланс приведен для различных степеней исходной окисленности металла. С уменьшением степени окисленности исходной стали величина z Al z Ce увеличивается, что свидетельствует о бóльшей раскислительной способности церия.
В табл. 4, к сожалению, можно привести лишь результаты точечных расчетов. Более полную информацию о связи количества введенных модификаторов и раскислителей можно получить при построении диаграмм расхода добавок. На рис. 3–5
построены так называемые диаграммы расхода
Расход компонентов для раскисления стали алюмоцерием
|
[ 0 ] исх ,% |
Лигатура |
Баланс по раскислителям, кг/т |
|||||
|
z Al z Ce |
z Al , кг/т |
z Ce , кг/т |
Алюминий |
Церий |
|||
|
z Aрl, кг/т |
z Aрl , % |
z Cрe, кг/т |
z C р e , % |
||||
|
0,010 |
0,264 |
0,1246 |
0,4719 |
0,0246 |
19,74 |
0,4493 |
9,552 |
|
0,005 |
0,458 |
0,1122 |
0,2449 |
0,0122 |
10,87 |
0,2224 |
9,079 |
|
0,001 |
1,612 |
0,1022 |
0,0634 |
0,0022 |
2,526 |
0,0408 |
6,441 |
Примечание. Состав металла ([O] = 0,0001, [Al] = 0,01, [Ce] = 0,002 мас. %); состав оксидного распла- ва (О.р.) x = 0,0001; x = 0,2215; x = 0,0045; x = 0,7739 определяется координатами
( Fe2 + ) ( Al3 +) ( Ce4 + ) ( Ce3 +)
т. А (см. рис. 1)
раскисляющих и модифицирующих компонентов. По оси абсцисс отложен полный расход церия (на раскисление и легирование), по оси ординат – полный расход алюминия в кг/т.
На рис. 3–5 показано, при каких расходах в кг/т церия и алюминия реализуется соответственное фазовое равновесие. Тонкими линиями нанесены изокислородные сечения диаграммы расходов, контрастными выделены области фазовых равновесий. Обозначения областей на рис. 3 согласованы с обозначениями областей фазовых равновесий на рис. 1 (области I – VIII). Рис. 4 – укрупненная часть рис. 3. На рис. 4 видно, что при ничтожных расходах церия область равновесий с корундом практически не проявляется. При добавках церия 40–50 г/т в равновесии с металлом обра- зуется фаза Ce2O3·11Al2O3. В области V заданы составы металла, равновесного с Ce2O3·Al2O3. Такое соединение можно получить в качестве неметаллических включений при одновременном расходе алюминия 500 г/т и церия ~300 г/т. При бóльших расходах церия можно получить либо шлакокристаллические включения (оксидный расплав + Ce2O3·Al2O3), либо жидкоподвижные включения в составе (FeO, Al2O3, Ce2O3) со следами CeO2. Фаза Ce2O3 может быть получена в качестве неметаллических включений при расходах церия больше 500 г/т металла и малом содержании алюминия в металле. На рис. 5 приведена диаграмма расхода алюминия и церия при исходном содержании кислорода в металле 0,001 мас. %. Видно, что для этих условий при обычных расходах церия
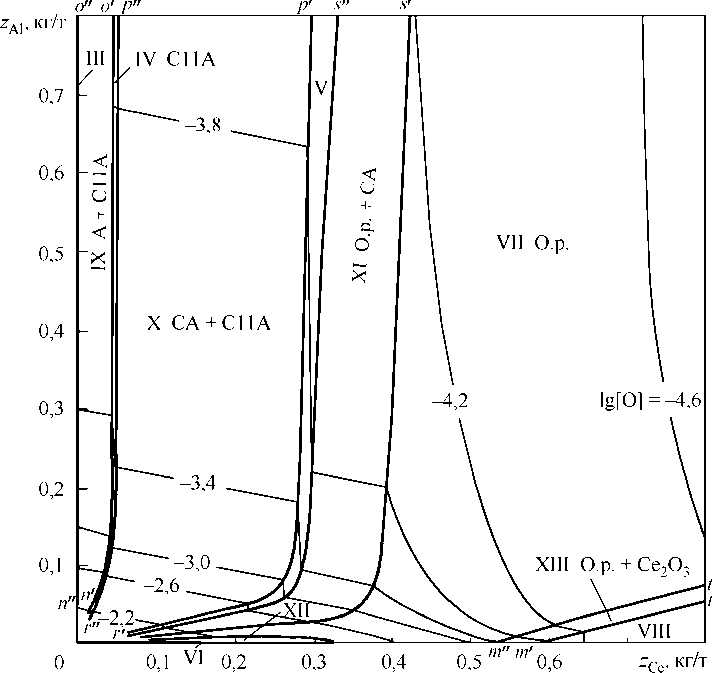
Рис. 3. Диаграмма расхода алюминия и церия, [O] исх = 0,01 мас. % СА – Ce 2 O 3 ·Al 2 O 3 , С11А – Ce 2 O 3 ·11Al 2 O 3
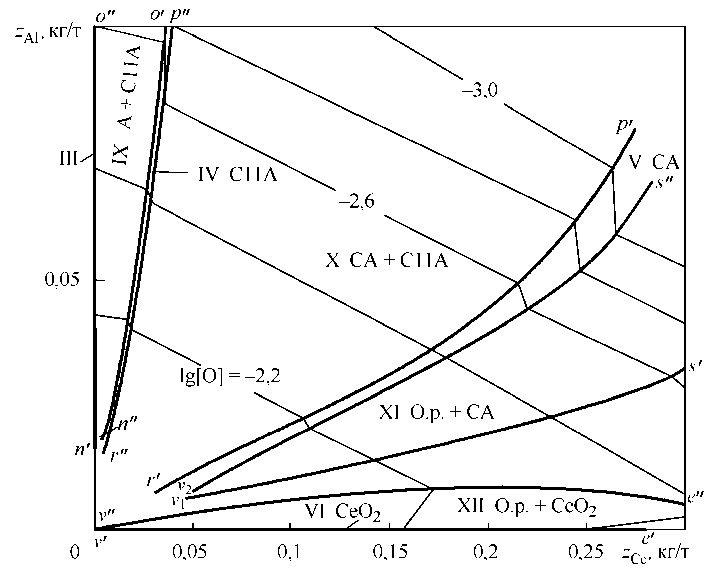
Рис. 4. Диаграмма расхода алюминия и церия, [O] исх = 0,01 мас. %. Дополнение к рис. 3
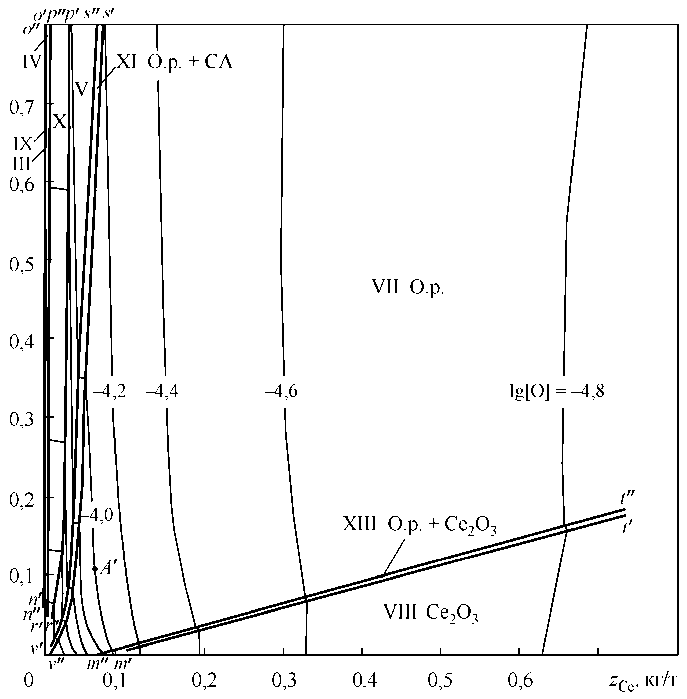
Рис. 5. Диаграмма расхода алюминия и церия, [O] исх = 0,001 мас. %
на раскисление и модифицирование и при малых расходах алюминия (до 100 г/т) возможно образование Ce2O3. При расходах алюминия порядка 300–500 г/т и расходах церия 200–300 г/т равновесной с металлом фазой будет оксидный расплав (FeO, Al 2 O 3 , Ce 2 O 3 ).
Выводы. Построены поверхности растворимости компонентов в металлических расплавах для системы Fe–Ce–Al–O. Показано, что в области достижимых концентраций кислорода, церия и алюминия возможно блокирование поверхности химически активных неметаллических включений. Выпол- нен анализ сравнительной раскислительной способности церия и алюминия путем построения диаграмм расходов активных металлов на рафинирование стали. Установлена большая раскислительная способность церия по отношению к алюминию.
Работа выполнена в рамках Государственного задания Министерства образования и науки РФ и частично поддержана грантом РФФИ № 13-08-12167.
Список литературы Влияние церия и алюминия на растворимость кислорода в жидкой стали
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСИС. -2009. -519 с.
- Bůžek Z. Základní termodynamické údaje o metalurgických reakcích a o interakdch prvků v sous-tavách významných pro hutnickou teorii a praxi/Z. Buzek//Hutnicke listy. -1979. -Т. 20, № 1-2. -S. 3-111.


