Влияние цинксодержащего кальций-фосфатного покрытия на остеоинтеграцию чрескожных имплантатов для протезирования конечностей
Автор: Стогов М.В., Еманов А.А., Кузнецов В.П., Комарова Е.Г., Горбач Е.Н., Киреева Е.А., Толкачева Т.В., Шаркеев Ю.П.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 5 т.30, 2024 года.
Бесплатный доступ
Введение. Повышение интеграции чрескожных имплантатов является важной задачей для их применения в клинической практике.Цель работы - оценка остеоинтеграции титановых чрескожных имплантатов с кальций-фосфатным покрытием, содержащим ионы цинка.Материалы и методы. Исследования выполнены на 12 кроликах-самцах, которым имплантировали оригинальный имплантат в культю большеберцовой кости. После имплантации на кость устанавливали компрессионное устройство, поддерживавшее нагрузку 3,5Н в течение 5 нед. Длительность наблюдения - 26 недель. Животные разбиты на две группы: группа контроля (n = 6) - имплантировано изделие без покрытия; опытная группа (n = 6) - имплантировано изделие с цинк-замещенным кальций-фосфатным покрытием.Результаты. Выпадение имплантата отмечали в одном случае у животных группы контроля, в опытной группе случаев выпадения имплантатов не отмечено. Выявлено, что весовая концентрация Са и Р во всех зонах костно-имплантационного блока животных опытной группы достоверно превышала аналогичные показатели контрольной группы. В контрольной группе отмечали длительное сохранение высоких значений уровня С-реактивного белка, чего не наблюдали в основной группе.Обсуждение. Комплекс исследований показал, что имплантат с цинксодержащим кальций-фосфатным покрытием имеет признаки улучшенной интеграции в отличие от изделия без покрытия. Отсутствие серьезных нежелательных реакций на тестируемые изделия свидетельствует о приемлемой переносимости и безопасности применения.Заключение. При использовании имплантатов с цинк-модифицированным кальций-фосфатным покрытием обнаружены признаки более эффективной остеоинтеграции по сравнению с изделием без дополнительного покрытия.
Протезирование, чрескожный имплантат, остеоинтеграция, кальций-фосфатное покрытие
Короткий адрес: https://sciup.org/142243286
IDR: 142243286 | УДК: 616.718.5-77:615.461]-092.9 | DOI: 10.18019/1028-4427-2024-30-5-677-686
The effect of zinc-containing calcium phosphate coating on the osseointegration of transcutaneous implants for limb prosthetics
Introduction Increasing the integration of transcutaneous implants is an important goal for their application in clinical practice.The purpose of the work was to evaluate the osseointegration of transcutaneous titanium implants with calcium-phosphate coating containing zinc ions.Materials and methods The studies were performed on 12 male rabbits, who underwent implantation of an original implant into the tibial stump. After implantation, a compression device was installed on the bone, maintaining a load of 3.5 N for 5 weeks. Duration of observation was 26 weeks. The animals were divided into two groups: a control group (n = 6) with an implant without coating and an experimental group (n = 6) with a zinc-substituted calcium-phosphate coated implant.Results The implant fell out in one case in animals from the control group; no cases of implant loss were noted in the experimental group. It was revealed that the weight concentration of Ca and P in all zones of the bone-implant block of the animals in the experimental group significantly exceeded similar indicators in the control group. In the control group, long-term persistence of high levels of C-reactive protein was noted, which was not observed in the experimental group.Discussion This series of studies has shown that an implant with a zinc-modified calcium-phosphate coating exhibited a more effective integration, in contrast to an uncoated product. The absence of serious adverse reactions to the tested products indicates acceptable tolerability and safety of its use.Conclusion The implants with a zinc-modified calcium-phosphate coating showed signs of more effective osseointegration compared to the product without additional coating.
Текст научной статьи Влияние цинксодержащего кальций-фосфатного покрытия на остеоинтеграцию чрескожных имплантатов для протезирования конечностей
Чрескожное остеоинтеграционное протезирование является развивающимся методом лечения пациентов с потерей конечностей [1, 2]. К настоящему времени параллельно с двухэтапной технологией протезирования развивается одноэтапная процедура [3, 4], требующая новых решений для улучшения остеоинтеграции имплантируемой части, т.к. проблема стабильности имплантата в условиях одноэтапного процесса является ключевой [5]. Ранее нами показано, что эффективная остеоинтеграция чрескожных имплантатов при одноэтапной процедуре может достигаться за счёт применения дополнительных фиксирующих имплантат устройств в совокупности с возможностью этих устройств обеспечивать механическую компрессию имплантата [6]. Другой вариант для реализации одностадийного ускоренного протокола остеоинтеграции — использование имплантатов типа Press-Fit [7].
Однако такие подходы являются недостаточными для оптимальной остеоинтеграции имплантатов в условиях одноэтапности процесса. Поэтому возникла необходимость разработки дополнительных технологий, стимулирующих процесс интеграции чрескожных имплантатов, в том числе за счет модификации поверхности имплантируемой части [8, 9]. Так, одним из способов повышения остеоинтеграции имплантатов является нанесение на его поверхность биоинертного оксидного или биоактивного кальций-фосфатного покрытия [10]. Среди методов нанесения покрытий на имплантаты на основе титана следует выделить метод микродугового оксидирования, который позволяет импрегнировать в состав покрытия дополнительные эссенциальные микроэлементы, обеспечивающие положительные для остеогенеза эффекты. В ряде работ продемонстрировано положительное влияние на остеоинтеграционные процессы внедрения в состав кальций-фосфатного покрытия ионов цинка, стронция и кремния [11–13].
Цель работы — оценка остеоинтеграции титановых чрескожных имплантатов с кальций-фосфатным покрытием, содержащим ионы цинка.
МАТЕРИАЛЫ И МЕТОДЫ
Изделия . В работе использованы имплантаты из сплава Ti6Al4V для протезирования культей трубчатых костей [14] (рис. 1, а). На рабочую поверхность имплантата наносили цинксодержащее кальцийфосфатное (КФ) покрытие (Zn-КФ) с помощью метода дугового оксидирования (рис. 1, б). Имплантаты изготавливали из порошка Ti6Al4V со средним размером частиц 23,5 мкм производства фирмы Advanced Powders&Coatings Inc. (Канада) методом селективного лазерного сплавления на 3D-принтере EOS EOSINT M 280 (Германия). Нанесение покрытий на имплантаты проводили на полупромышленной установке Micro-Arc 3.0.

Рис. 1. Внешний вид имплантатов: а — без нанесенного покрытия (контроль); б — с Zn-КФ покрытием (опыт)
Для нанесения покрытий имплантаты погружали в ванну с электролитом. Осаждение покрытий проводили в электролите-суспензии состава (мас. %): H 3 PO 4 — 27; CaCO 3 — 7; синтетический цинк-замещенный гидроксиапатит (Zn-ГА) (Ca 10 Zn 9 (PO 4 ) 6 (OH) 2 ) — 5; остальное — дистиллированная вода. Zn-ГА в нанокристаллическом состоянии со средним размером зерен 30–50 мкм синтезирован меха-нохимическим методом в Институте химии твердого тела и механохимии СО РАН [15]. Параметры нанесения покрытий: анодное напряжение — 200 В, длительность импульсов — 100 мкс, частота импульсов — 50 Гц, длительность обработки — 5 минут. Толщину покрытий определяли с помощью цифрового микрометра Зубр (точность измерений 1 мкм). Массу покрытий измеряли на аналитических весах CAS CAUX-220 (точность измерений 1 мг). Шероховатость поверхности определяли с помощью контактного «Профилометра-296» по параметру Ra, как среднеквадратичное отклонение профиля в пределах базовой длины. Масса сформированных на имплантатах покрытий составила (29,3 ± 2,1) мг, толщина — (33,5 ± 2,8) мкм, шероховатость Ra — (2,3 ± 0,5) мкм (рис. 1, б). Морфология, структура, состав и свойства сформированных покрытий описаны ранее [11, 13].
Все изделия для имплантации поступали в индивидуальных упаковках не стерильными. Перед применением имплантаты проходили стерилизационную обработку в сухожаровом шкафу при температуре 180 ºС в течение 1 ч. Максимальный срок хранения изделий перед применением составил 6 мес.
Дизайн исследований in vivo . Эксперимент проводили на 12 кроликах-самцах породы шиншилла в возрасте от 8 до 9 мес., средний вес кроликов — (3,4 ± 0,2) кг. Всем кроликам осуществляли удаление большеберцовой кости на границе верхней и средней трети. После чего обрабатывали сверлом костномозговой канал, вкручивали имплантат в культю большеберцовой кости. Мягкие ткани послойно ушивали внутренними швами, формировали лоскут из кожи, в котором выполняли отверстие для выхода части имплантата наружу. Далее на кость устанавливали удерживающее компрессионное устройство [16] с протезом из фторопласта. Кость подвергали компрессионной нагрузке 3,5Н в течение 5 нед. Длительность наблюдения — 26 недель. Животные разбиты на две группы: группа 1 ( n = 6) — животным имплантировали изделие без покрытия (контроль); группа 2 ( n = 6) —животным имплантировали изделие с цинк-замещенным кальций-фосфатным покрытием (основная группа). Клинический контроль осуществляли во время всего послеоперационного периода. Обращали внимание на состояние животных, термометрию, пульс, дыхание, локальный статус конечности, состояние мягких тканей, а также послеоперационных ран.
Регулирующие стандарты . Исследование выполнено в соответствии со стандартами ISO 10993-1-2021. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования в процессе менеджмента риска; ISO 10993-6-2021. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации.
Этические принципы . Исследование проведено при соблюдении принципов гуманного обращения с лабораторными животными в соответствии с требованиями Европейской конвенции по защите позвоночных животных, используемых для экспериментов и других научных целей, и Директивой 2010/63/EU Европейского парламента и Совета Европейского союза от 22 сентября 2010 г. по охране животных, используемых в научных целях. До начала исследования получено одобрение локального этического комитета (протокол № 1 (71) от 28.04.2022).
Эвтаназия . Плановую эвтаназию животных производили после миорелаксации раствором димедрола 1 % (0,02 мг/кг) и рометара 2 % (5 мг/кг), далее вводили летальную дозу барбитуратов.
Для определения эффективности остеоинтеграции осуществляли рентгенологические, гистологические и биохимические исследования.
Рентгенологическое исследование . Для рентгенографии использовали рентгеновский аппарат Compact (Италия). Рентгенологическое исследование оперированной конечности животного выполняли в кра-ниокаудальной и латеромедиальной проекциях. Рентгенографию проводили до и после оперативного вмешательства, на 5, 12, 26 нед. после имплантации.
Гистологическое исследование . У эвтаназированных животных осуществляли послойную препарацию от мягких тканей культи большеберцовой кости с интрамедуллярно интегрированным имплантатом. Фиксацию материала проводили в 10 % растворе нейтрального формалина не менее 10 сут. Затем костно-имплантационный блок продольно распиливали, оставляя имплантат в одной из половин.
Фрагмент кости без имплантируемого изделия деминерализовывали в смеси растворов муравьиной и соляной кислот, дегидратировали в этиловом спирте. После этапов пропитки в нескольких порциях «жидкого» 5 % целлоидина заливали в густой 40 % целлоидин и уплотняли блоки в хлороформе.
Срезы готовили при помощи санного микротома Reichard (Германия) и окрашивали их гематоксилином и эозином, пикрофуксином и по методу Массона по технологии плавающих срезов. Гистологические препараты изучали с использованием стереомикроскопа AxioScope.A1, цифровые изображения получали с помощью цифровой камеры AxioCam ICc 5.
Другую часть костно-имплантационного блока культи большеберцовой кости дегидратировали, заливали в камфен и высушивали на воздухе до полной его возгонки. Высушенные препараты напыляли Pt в специальном напылителе IB-6 (EICO, Japan).
Количественное определение содержания Са и Р (W, в весовых %) в различных участках костно-имплантационных блоков выполняли методом энергодисперсионного рентгеновского микроанализа с использованием спектрометра BRUKER QUANTAX 200 – XFlash 6/10 (Bruker Nano GmbH, Германия), в комплекте со сканирующим микроскопом (СЭМ) Zeiss EVO MA18 (Carl Zeiss Group, Германия). Анализ количественных показателей осуществлялся в программе ESPRIT (Bruker Nano GmbH, Германия).
Биохимическое исследование включало определение в сыворотке крови животных концентрации общего белка, мочевины, креатинина, глюкозы, лактата, общего кальция, неорганического фосфата, калия, натрия, хлоридов, С-реактивного белка (СРБ), а также активности щелочной фосфатазы (ЩФ) и тар-тратрезистентного (костного) изофермента кислой фосфатазы (ТрКФ), креатинкиназы, трансаминаз. Исследования выполнены на автоматическом биохимическом анализаторе Hitachi/BM 902 (Италия) с использованием наборов реагентов Витал Диагностикс, Вектор-Бест (Россия).
Статистические методы исследования . Результаты в таблицах представлены в зависимости от характеристик сравниваемых выборок (нормальность оценивали по критерию Шапиро – Уилка) либо в виде среднего арифметического и стандартного отклонения (Xi ± SD), либо в виде медианы, 1–3 квартиля (Me, Q1–Q3). Процедуру статистической оценки значимости отличий показателей на сроках эксперимента с дооперационными значениями проводили с использованием W-критерия Вилкоксона. Достоверность различий между группами на сроках наблюдения оценивали с помощью непараметрического Т-критерия Манна – Уитни. Минимальный уровень значимости (р) принимали равным 0,05.
РЕЗУЛЬТАТЫ
Клинический контроль животных в послеоперационном периоде показал, что состояние у кроликов всех групп было удовлетворительным, внеплановой гибели не выявлено. В первые трое суток во всех наблюдениях определяли отеки в области культи, отмечали снижение аппетита. Динамическая функция конечности у всех животных восстанавливалась на 4–5 сутки после операции. Воспаления мягких тканей не отмечено. В течение первой недели после демонтажа специального устройства
(6 нед. после имплантации) отмечено выпадение имплантата в одном случае у животного группы 1, в опытной группе таких случаев не выявлено.
Рентгенологическое исследование показало, что у животных первой группы через 5 нед. после имплантации имелись участки резорбции на стыке кость / имплантат, у животных группы 2 эти признаки не определялись (рис. 2).
После 12 недель имплантации в обеих группах отмечены признаки остеоинтеграции, резорбцию не визуализировали, определяли незначительные периостальные наслоения в стадии компактиза-ции (рис. 3). К 26 чнед. после имплантации отмечена полная органотипическая перестройка кости в периимплантной зоне (рис. 4). Однако у животных группы 2 костные напластования были в стадии компактизации, располагались за ограничительным кольцом, что свидетельствовало об актив-
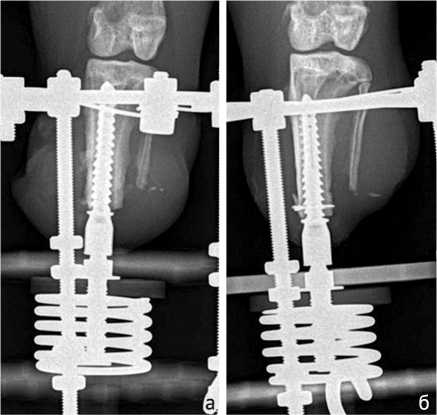
Рис. 2. Рентгенограммы через 5 недель после имплантации: а — группа 1; б — группа 2
ном костном интегративном процессе на границе кость–имплантат (рис. 4, б).
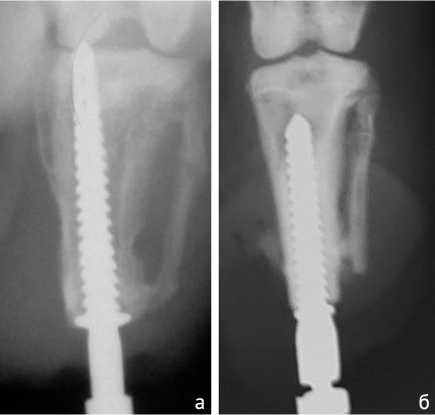
Рис. 3. Рентгенограммы через 12 недель после имплантации: а — группа 1; б — группа 2
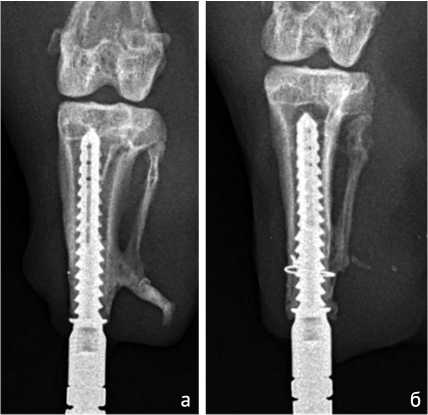
Рис. 4. Рентгенограммы через 26 недель после имплантации: а — группа 1; б — группа 2
Таким образом, у животных группы 2 рентгенологическая картина на всех этапах эксперимента определялась наличием стабильности и отсутствием резорбции, что оценивается как положительные признаки остеоинтеграционных свойств изделия.
Гистологические исследования . В группе 1 через 26 недель эксперимента между поверхностью имплантата и костной тканью наблюдали плотный контакт, был сформирован единый костно-имплантационный блок. На всем протяжении культи кости сохранялась непрерывная компактная пластинка. Выраженных периостальных напластований не обнаруживали. В дистальной и средней частях культи большеберцовой кости отмечали врастание костной ткани в резьбовые межреберные углубления имплантата (рис. 5).
Гистоструктурная характеристика культи большеберцовой кости при интеграции имплантатов в опытной группе через 26 недель эксперимента обнаруживала в ложе культи большеберцовой кости сохранность метафизарно-эпифизарной части и непрерывную компактную пластинку, которая объединялась с поверхностью имплантата в метаэпифизарной области и в проксимальных участках диафиза с эндо-стально образованной костной тканью среднеячеистого трабекулярного строения. В дистальной части компактная пластинка плотно прилегала к имплантату. Наличие костной ткани обнаруживалось в резьбовых углублениях имплантата (рис. 6).
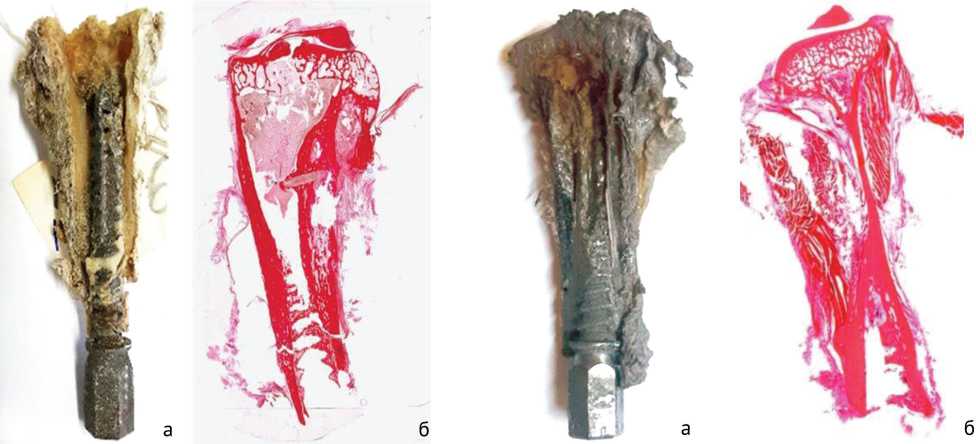
Рис. 5. Костно-имплантационный блок, формирующийся у животных контрольной группы к 26 неделе наблюдений: а — большеберцовая кость кролика с интрамедуллярно интегрированным имплантатом (продольный распил); б — продольный гистотопографический срез большеберцовой кости кролика после извлечения имплантата. Окраска пикрофуксином. Ув. ×1,5
Рис. 6. Костно-имплантационный блок, формирующийся у животных опытной группы к 26 неделе наблюдений: а — большеберцовая кость кролика с интрамедуллярно интегрированным имплантатом (продольный распил); б — продольный гистотопографический срез большеберцовой кости кролика после извлечения имплантата. Окраска пикрофуксином. Ув. ×1,5
Анализ количественных данных содержания остеотропных элементов показал, что через 26 недель наблюдения в субстрате формирующегося на поверхности имплантата у кроликов группы 2 элементов кальция и фосфора было достоверно больше во всех областях имплантата относительно животных группы контроля (табл. 1).
Таблица 1
Массовая доля W (Са) и W (Р) в различных участках культи большеберцовой кости (Xi ± SD)
|
Область исследования |
Кальций, вес % |
Фосфор, вес % |
||
|
Группа 1 |
Группа 2 |
Группа 1 |
Группа 2 |
|
|
Проксимальная |
7,3 ± 0,4 |
15,1 ± 0,7* |
3,6 ± 0,1 |
5,2 ± 0,3* |
|
Срединная |
9,1 ± 0,3 |
15,3 ± 0,7* |
4,6 ± 0,2 |
5,8 ± 0,2* |
|
Дистальная |
10,3 ± 0,3 |
13,2 ± 0,7* |
4,5 ± 0,3 |
5,8 ± 0,4* |
|
Интактные животные |
19,30 |
± 0,91 |
8,12 ± 0,39 |
|
Примечание : * — достоверные отличия относительно группы 1 (контроль) при р < 0,05.
Таким образом, проведенное гистологическое исследование показало, что изделие с кальций-фосфатным покрытием обладало более выраженными остеоинтегративными характеристиками в изученных группах. В дистальной части культи отмечено наползание плотной соединительной ткани на ограничивающую кольцевую конструкцию и структуры имплантата, предшествующие ей, что способствовало формированию наружного барьера и предотвращению развития внутрикостной инфекции. Отрицательным моментом является имбибиция частиц имплантата в пограничные с ним ткани.
Лабораторные исследования . Изменения активности фосфатаз и концентрации кальция и фосфатов в сыворотке крови экспериментальных животных представлены в таблице 2.
Таблица 2
Активность фосфатаз, концентрация кальция и фосфата в сыворотке крови кроликов на сроках (недели) эксперимента, Ме (Q1–Q3)
|
Срок |
Группа |
ЩФ, Е/л |
ТрКФ, Е/л |
Кальций, ммоль/л |
Фосфат, ммоль/л |
|
0 |
1 |
53 (48–63) |
26 (22–26) |
2,67 (2,61–2,70) |
1,22 (1,14–1,34) |
|
2 |
54 (32–70) |
28 (21–33) |
2,69 (2,52–2,75) |
1,34 (1,21–1,44) |
|
|
3 |
1 |
42 (38–46)* |
41 (35–42)* |
2,78 (2,65–2,91) |
1,31 (1,20–1,57) |
|
2 |
55 (47–63)^ |
29 (24–40) |
2,75 (2,62–2,80) |
1,14 (1,10–1,20)* |
|
|
6 |
1 |
57 (49–69) |
34 (29–38)* |
2,65 (2,54–2,72) |
1,34 (1,23–1,42) |
|
2 |
60 (53–65) |
19 (17–21)*^ |
2,65 (2,60–2,71) |
1,09 (1,07–1,18)*^ |
|
|
12 |
1 |
58 (45–66) |
20 (16–28) |
2,65 (2,57–2,73) |
1,43 (1,42–1,45) |
|
2 |
46 (45–57) |
24 (23–26) |
2,51 (2,47–2,59) |
1,04 (1,02–1,19)*^ |
|
|
26 |
1 |
61 (56–66) |
20 (16–29) |
2,71 (2,62–2,78) |
1,39 (1,26–1,45) |
|
2 |
58 (42–63) |
23 (22–28) |
2,79 (2,55–2,83) |
1,03 (0,98–1,14)*^ |
Примечание : * — различия с дооперационными (срок 0) значениями, р < 0,05; ^ — различия показателей с контрольной группой при р < 0,05.
Обнаружено, что у животных группы 1 (контроль) активность ЩФ относительно дооперационного уровня снижалась на 3 неделе после имплантации. У кроликов группы 2 повышение активности ЩФ на сроках относительно значений до операции не отмечено, но ЩФ на 3 неделе была выше относительно группы контроля. Активность ТрКФ на 3 и 6 неделях повышалась у животных группы контроля относительно исходных значений. В группе 2 отмечено достоверное снижение активности ТрКФ на 6 неделе после имплантации как относительно дооперационного уровня, так и относительно группы контроля на данном сроке. Концентрация общего кальция в сыворотке крови всех экспериментальных групп статистически значимо не изменялась как относительно дооперационных значений, так и между группами. В группе 2 на всех сроках эксперимента отмечено снижение концентрации неорганического фосфата в сыворотке крови относительно исходных значений и относительно животных группы контроля.
Отмечены значительные отличия в динамике С-реактивного белка (СРБ) (табл. 3). Так, достоверно повышенные значения СРБ в контрольной группе (группа 1) наблюдали до 26 недели эксперимента, в группе 2 — до 5 недели. В группе 2 на 26 неделе эксперимента отмечали статистически значимое снижение концентрации лактата как относительно исходных, дооперационных значений, так и относительно значений группы контроля. Другие биохимические показатели не имели достоверных отличий в обеих группах.
Таблица 3
Концентрация СРБ и лактата в сыворотке крови кроликов на сроках эксперимента, Ме (Q1–Q3)
|
Показатель |
Группа |
Сроки (недели) эксперимента |
||||
|
0 |
3 |
5 |
12 |
26 |
||
|
СРБ, мг/мл |
1 |
0 (0–1) |
13* (6–22) |
10* (4–17) |
2 (0–3) |
4* (2–21) |
|
2 |
0 (0–1) |
6* (2–14) |
6* (5–10) |
3 (0–4) |
0 (0–2) |
|
|
Лактат, ммоль/л |
1 |
9,5 (7,4–10,1) |
10,4 (8,3–12,3) |
9,0 (7,4–9,9) |
8,8 (7,5–11,4) |
10,5 (8,9–11,4) |
|
2 |
9,1 (7,5–10,8) |
9,5 (7,8–10,2) |
9,5 (8,1–10,0) |
6,4 (4,9–7,8) |
4,8*^ (2,7–7,5) |
|
Примечание : * — различия с дооперационными (срок 0) значениями, р < 0,05; ^ — различия показателей с контрольной группой при р < 0,05.
ОБСУЖДЕНИЕ
Развитие технологии одноэтапной остеоинтеграции чрескожных имплантатов является перспективным методом для решения задач протезирования костей, при этом ряд работ указывает, что переход к такой процедуре способствует улучшению результатов лечения целевых пациентов [17, 18]. Развитие этого варианта технологии чрескожного остеоинтеграционного протезирования лежит в направлении повышения остеоинтеграции имплантата, обеспечивающей его стабильность, устойчивость к инфицированию и достаточную герметизацию мягких тканей вокруг внешней части имплантата [19, 20].
Учитывая имеющиеся данные, в рамках развития способов стимуляции остеоинтеграции нами оценён новый имплантат для протезирования культей трубчатых костей с модифицированной поверхностью. Обнаружено, что применение имплантата с Zn-содержащим КФ покрытием имеет признаки улучшенной интеграции в отличие от изделия без покрытия. Кроме того, имплантация изделий с кальций-фосфатным покрытием не вызывала у животных признаков отторжения, интоксикации (как локальной, так и системной), системной воспалительной реакции в течение всего срока наблюдения. Отсутствие серьезных нежелательных реакций на тестируемые изделия позволяет заключить, что все исследуемые имплантаты имели приемлемую переносимость и безопасность.
Литературные данные по оценке возможностей повышения интегративных свойств имплантатов с Zn-содержащим КФ покрытием достаточно скудны. Имеется работа, в которой также отмечается способность такого покрытия улучшать остеоинтеграцию металлических чрескожных имплантатов [21]. Тем не менее, перспективность применения такого покрытия очевидна, о чем свидетельствуют многочисленные данные по улучшенной остеоинтеграции дентальных имплантатов с КФ покрытием [22–24]. Дополнительным фактором в пользу применения изделий с КФ покрытием является то, что отдельные исследования указывают на способность таких покрытий снижать воспалительную реакцию и инфицирование зоны имплантации [25, 26].
Дальнейшее совершенствование остеоинтегративных характеристик разработанного изделия может быть связано с увеличением числа дополнительных микроэлементов в составе КФ покрытия [27, 28], применением имплантатов с быстро рассасывающимися гидрогелями, загруженными антибиотиками [29]. Интересным выглядит возможность нанесения на металлические имплантаты покрытий из биополимеров, особенно части поверхности имплантатов, интегрируемых с мягкими тканями [30], а также использование искусственных полимеров вместо титана [31, 32].
Очевидно, что полученные нами результаты имеют ограничения в части объемов выборок экспериментальных животных. Экстраполяция результатов исследования для клинической практики возможна, т.к. использованная экспериментальная модель приближена к модели клинического применения (одноэтапное протезирование), в том числе за счет достаточно длительного срока наблюдения после имплантации.
ЗАКЛЮЧЕНИЕ
Применение имплантатов с цинк-модифицированным кальций-фосфатным покрытием обнаруживало признаки более эффективной остеоинтеграции по сравнению с изделием без дополнительного покрытия. Такие имплантаты с модифицированной КФ поверхностью в разработанном дизайне на основе полученных данных по их эффективности и безопасности могут быть применимы для задач протезирования культей мелких костей в рамках одноэтапной технологии протезирования.
Список литературы Влияние цинксодержащего кальций-фосфатного покрытия на остеоинтеграцию чрескожных имплантатов для протезирования конечностей
- Overmann AL, Forsberg JA. The state of the art of osseointegration for limb prosthesis. BiomedEngLett. 2019;10(1):5-16. doi: 10.1007/s13534-019-00133-9
- Rehani M, Stafinski T, Round J, et al. Bone-anchored prostheses for transfemoral amputation: a systematic review of outcomes, complications, patient experiences, and cost-effectiveness. Front Rehabil Sci. 2024;5:1336042. doi: 10.3389/fresc.2024.1336042
- Aschoff HH, Örgel M, Sass M, et al. Transcutaneous Osseointegrated Prosthesis Systems (TOPS) for Rehabilitation After Lower Limb Loss: Surgical Pearls. JBJSEssent Surg Tech. 2024;14(1):e23.00010. doi: 10.2106/JBJS.ST.23.00010
- Zaid MB, O'Donnell RJ, Potter BK, Forsberg JA. Orthopaedic Osseointegration: State of the Art. J Am Acad Orthop Surg. 2019;27(22):e977-e985. doi: 10.5435/JAAOS-D-19-00016
- Rennie C, Rodriguez M, Futch KN, Krasney LC. Complications Following Osseointegrated Transfemoral and Transtibial Implants: A Systematic Review. Cureus. 2024;16(3):e57045. doi: 10.7759/cureus.57045
- Еманов А.А., Горбач Е.Н., Стогов М.В. и др. Выживаемость чрескожных имплантатов в условиях различной механической нагрузки на кость. Гений ортопедии. 2018;24(4):500-506. doi: 10.18019/1028-4427-2018-24-4-500-506.
- Haque R, Al-Jawazneh S, Hoellwarth J, et al. Osseointegrated reconstruction and rehabilitation of transtibial amputees: the Osseointegration Group of Australia surgical technique and protocol for a prospective cohort study. BMJ Open. 2020;10(10):e038346. doi: 10.1136/bmjopen-2020-038346
- Liu Y, Rath B, Tingart M, Eschweiler J. Role of implants surface modification in osseointegration: A systematic review. J Biomed Mater Res A. 2020;108(3):470-484. doi: 10.1002/jbm.a.36829
- Стогов М.В., Еманов А.А., Кузнецов В.П. и др. Сравнительная оценка остеоинтеграции новых чрескожных имплантатов из ультрамелкозернистого сплава Ti Grade 4. Гений ортопедии. 2023;29(5):526-534. doi: 10.18019/10284427-2023-29-5-526-534. EDN: ELJGET.
- Li TT, Ling L, Lin MC, et al. Recent advances in multifunctional hydroxyapatite coating by electrochemical deposition. J Mater Sci. 2020;55:6352-6374. doi: 10.1007/s10853-020-04467-z
- Komarova EG, Sharkeev YP, Sedelnikova MB, et al. Zn- or Cu-Containing CaP-Based Coatings Formed by Micro-arc Oxidation on Titanium and Ti-40Nb Alloy: Part I-Microstructure, Composition and Properties. Materials (Basel). 2020;13(18):4116. doi: 10.3390/ma13184116
- Sedelnikova MB, Komarova EG, Sharkeev YP, et al. Modification of titanium surface via Ag-, Sr- and Si-containing micro-arc calcium phosphate coating. BioactMater. 2019;4:224-235. doi: 10.1016/j.bioactmat.2019.07.001
- Sedelnikova MB, Komarova EG, Sharkeev YP, et al. Zn-, Cu- or Ag-incorporated micro-arc coatings on titanium alloys: Properties and behavior in synthetic biological media. Surf Coat Technol. 2019;369:52-68. doi: 10.1016/j. surfcoat.2019.04.021
- Кузнецов В.П., Губин А.В., Корюков А.А., Горгоц В.В. Имплант культи трубчатой кости. Патент РФ на полезную модель № 152558. 10.06.2015. Бюл. № 16. Доступно по: https://www.fips.ru/registers-doc-view/fips_servlet?DB=RU PM&DocNumber=152558&TypeFile=html. Ссылка активна на 23.07.2024.
- Bulina NV, Khvostov MV, Borodulina IA, et al. Substituted hydroxyapatite and ß-tricalcium phosphate as osteogenesis enhancers. Ceram Int. 2024. doi: 10.1016/j.ceramint.2024.06.136
- Кузнецов В.П., Губин А.В., Горгоц В.В., и др. Устройство для остеоинтеграции имплантата в кость культи нижней конечности. Патент РФ на полезную модель № 185647. 13.12.2018. Бюл. № 35. Доступно по: https://www.fips. ru/registers-doc-view/fips_servlet?DB=RUPM&DocNumber=185647&TypeFile=html. Ссылка активна на 23.07.2024.
- Al Muderis M, Lu W, Tetsworth K, et al. Single-stage osseointegrated reconstruction and rehabilitation of lower limb amputees: the Osseointegration Group of Australia Accelerated Protocol-2 (OGAAP-2) for a prospective cohort study. BMJ Open. 2017;7(3):e013508. doi: 10.1136/bmjopen-2016-013508
- Evans AR, Tetsworth K, Quinnan S, Wixted JJ. Transcutaneous osseointegration for amputees. OTA Int. 2024;7(2 Suppl):e326. doi: 10?1097/OI9.0000000000000326
- Hoellwarth JS, Tetsworth K, Rozbruch SR, et al. Osseointegration for Amputees: Current Implants, Techniques, and Future Directions. JBJSRev. 2020;8(3):e0043. doi: 10.2106/JBJS.RVW.19.00043
- Shrivas S, Samaur H, Yadav V, Boda SK. Soft and Hard Tissue Integration around Percutaneous Bone-Anchored Titanium Prostheses: Toward Achieving Holistic Biointegration. ACS Biomater Sci Eng. 2024;10(4):1966-1987. doi: 10.1021/ acsbiomaterials.3c01555
- Zastulka A, Clichici S, Tomoaia-Cotisel M, et al. Recent Trends in Hydroxyapatite Supplementation for Osteoregenerative Purposes. Materials (Basel). 2023;16(3):1303. doi: 10.3390/ma16031303
- Ghanem A, Kellesarian SV, Abduljabbar T, et al. Role of Osteogenic Coatings on Implant Surfaces in Promoting Bone-To-Implant Contact in Experimental Osteoporosis: A Systematic Review and Meta-Analysis. Implant Dent. 2017;26(5):770-777. doi: 10.1097/ID.0000000000000634
- Lu M, Chen H, Yuan B, et al. Electrochemical Deposition of Nanostructured Hydroxyapatite Coating on Titanium with Enhanced Early Stage Osteogenic Activity and Osseointegration. Int J Nanomedicine. 2020;15:6605-6618. doi: 10.2147/IJN.S268372
- Sotova C, Yanushevich O, Kriheli N, et al. Dental Implants: Modern Materials and Methods of Their Surface Modification. Materials (Basel). 2023;16(23):7383. doi: 10.3390/ma16237383
- Kaspiris A, Vasiliadis E, Pantazaka E, et al. Current Progress and Future Perspectives in Contact and Releasing-Type Antimicrobial Coatings of Orthopaedic Implants: A Systematic Review Analysis Emanated from In Vitro and In Vivo Models. InfectDisRep. 2024;16(2):298-316. doi: 10.3390/idr16020025
- Van den Borre CE, Zigterman BGR, Mommaerts MY, Braem A. How surface coatings on titanium implants affect keratinized tissue: A systematic review. J Biomed Mater Res B Appl Biomater. 2022;110(7):1713-1723. doi: 10.1002/ jbm.b.35025
- Li K, Xue Y, Yan T, et al. Si substituted hydroxyapatite nanorods on Ti for percutaneous implants. Bioact Mater. 2020;5(1):116-123. doi: 10.1016/j.bioactmat.2020.01.001
- Wang S, Zhao X, Hsu Y, et al. Surface modification of titanium implants with Mg-containing coatings to promote osseointegration. Acta Biomater. 2023;169:19-44. doi: 10.1016/j.actbio.2023.07.048
- Corona PS, Vargas Meouchi EA, García Hernández JM, et al. Single-stage transcutaneous osseointegrated prosthesis for above-knee amputations including an antibiotic-loaded hydrogel. Preliminary results of a new surgical protocol. Injury. 2024;55(4):111424. doi: 10.1016/j.injury.2024.111424
- Wang X, Lei X, Yu Y, et al. Biological sealing and integration of a fibrinogen-modified titanium alloy with soft and hard tissues in a rat model. Biomater Sci. 2021;9(15):5192-5208. doi: 10.1039/d1bm00762a
- Chen Z, Chen Y, Wang Y, et al. Polyetheretherketone implants with hierarchical porous structure for boosted osseointegration. Biomater Res. 2023;27(1):61. doi: 10.1186/s40824-023-00407-5
- Chen T, Jinno Y, Atsuta I, et al. Current surface modification strategies to improve the binding efficiency of emerging biomaterial polyetheretherketone (PEEK) with bone and soft tissue: A literature review. J Prosthodont Res. 2023;67(3):337-347. doi: 10.2186/jpr.JPR_D_22_00138


