Влияние доксорубицина и антибиотиков на динамику развития популяций Staphylococcus aureus и Escherichia coli
Автор: Шаповал Ольга Георгиевна
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Микробиология
Статья в выпуске: 1 т.6, 2010 года.
Бесплатный доступ
Инфекционные осложнения у онкологических больных часто возникают на фоне проводимой противоопухолевой терапии, что требует назначения антимикробных препаратов. Одними из основных возбудителей инфекций в онкологии являются стафилококки и кишечные палочки. целью данной работы явилось исследование влияния доксорубицина и цефтриаксона на динамику развития популяций штаммов Staphylococcs aureus, доксорубицина и амикацина — на динамику развития популяций штаммов Escherichia coli. Пять штаммов каждого вида (одного стандартного и четырех клинических) культивировали в мясо-пептонном бульоне, содержащем не-ингибирующие концентрации опытных препаратов. через разные промежутки времени после посева осуществляли измерение оптической плотности растущих культур. Установлено, что доксорубицин в неингибирующих концентрациях усиливает подавляющее действие указанных антибиотиков на динамику развития популяций опытных штаммов
Динамика развития популяции, доксорубицин
Короткий адрес: https://sciup.org/14917005
IDR: 14917005
Doxorubicine and antibiotics influence on dynamics of population development of Staphylococcus aureus and Escherichia coli
Infectious complications in oncologic patients often occur as a result of antitumor therapy that demands the prescription of antimicrobic preparations. one of the main infectious agents in oncology is Staphylococci and Escherichia coli. The aim of this work is to study doxorubicine and ceftriaxon influence on dynamics of population development of strains of Staphylococcus aureus, doxorubicine and amikacine - on dynamics of population development of strains of Escherichia coli. Five strains of each type (one-standard and four-clinical) cultivated in meatpeptone broth, which contains non-inhibitory concentrations of experimental preparations. in any period of time after the sowing the measurement of optical density of growing cultures has been carried out. it has been determined, that doxorubicine in non-inhibitory concentrations increases overwhelming effect of these antibiotics on dynamics of population development of experimental strains
Текст научной статьи Влияние доксорубицина и антибиотиков на динамику развития популяций Staphylococcus aureus и Escherichia coli
1Введение. В онкологической практике нередко возникают показания для назначения антибиотиков на фоне проводимой противоопухолевой терапии. Даже при отсутствии клинически документированных проявлений инфекции выраженные нарушения иммунного статуса пациентов требуют профилактического назначения противомикробных препаратов [1]. Поэтому проблема сочетанного действия противоопухолевых препаратов и антибиотиков на микроорганизмы — возбудители гнойно-воспалительных заболеваний, имеет теоретическое и практическое значение.
Методы. Нами было изучено влияние противоопухолевого препарата доксорубицина (из группы ан-трациклинов) и цефтриаксона в отношении 5 штаммов Staphylococcus aureus (стандартного – S.aureus АТСС 29213 и 4 клинических), доксорубицина и амикацина – в отношении 5 штаммов Escherichia coli (стандартного – E. coli АТСС 25922 и 4 клинических) на динамику развития популяций указанных бакте-
410012 Саратов, ул. Б. Казачья, д.112,
ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Росздрава, кафедра микробиологии, вирусологии и иммунологии, Тел.: (8452) 66-98-20.
рий. Клинические штаммы стафилококков были выделены из гнойного отделяемого ран. Кишечные палочки представляли собой уринокультуры. Оба вида микроорганизмов сохраняют свое значение среди основных возбудителей бактериальных инфекций у онкологических больных, в частности инфекций кровотока, мягких тканей и мочевыводящих путей [2].
Предварительно, методом двукратных серийных разведений в мясо-пептонном бульоне при микробной нагрузке 2×10 5 микробных тел/мл (по стандарту мутности ГИСК им. Л.А. Тарасевича), определяли минимальную ингибирующую концентрацию (МИК) цефтриаксона для штаммов S.aureus, амикацина – для штаммов E. coli [3]. Этот же метод использовали для определения МИК доксорубицина в отношении обоих видов.
С учетом полученных значений МИК изучали влияние доксорубицина и соответствующего антибиотика на динамику развития популяций штаммов. С этой целью суточные агаровые культуры штаммов S.aureus из расчета 2×10 5 м.т./мл засевали во флаконы с мясо-пептонным бульоном:
-
1- содержащим МИК цефтриаксона;
-
2- содержащим МИК доксорубицина;
-
3- содержащим цефтриаксон и доксорубицин в ½ МИК;
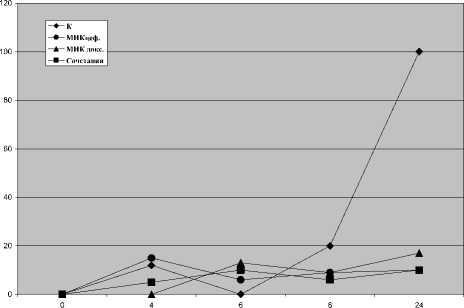
время культивировании. ч
Рис. 1. Динамика развития популяции штамма S.aureus АТСС 29213
-
4- не содержащим препаратов.
Суточные агаровые культуры штаммов E.coli из расчета 2×10 5 м.т./мл засевали во флаконы с мясопептонным бульоном:
-
1- содержащим МИК амикацина;
-
2- содержащим 100 мкг/мл доксорубицина;
-
3- содержащим ½ МИК амикацина и 100 мкг/мл доксорубицина;
-
4- не содержащем препаратов.
Концентрация доксорубицина 100 мкг/мл соответствует его сывороточной концентрации у человека в течение часа после внутривенного введения [4]. Ее использование было обосновано отсутствием чувствительности опытных штаммов E.coli к этому препарату (МИК 1000 мкг/мл).
Сразу после посева и по мере культивирования при t 37°С через 4, 6, 8 и 24 часа измеряли оптическую плотность (D) бульонных культур на спектрофотометре СФ-26 при длине волны 560 нм [5].
Результаты. При определении антимикробной активности цефтриаксона установлено, что 2 штамма S.aureus (S.aureus АТСС 29213 и S.aureus № 56) были чувствительны к этому антибиотику (МИК 1,5 мкг/мл), а 3 штамма – устойчивы (МИК для штаммов № 97 и № 108 составила 3,1, для штамма № 161 – 12,5 мкг/мл) [3].
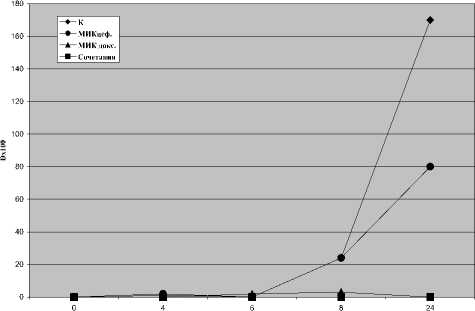
Рис. 2. Динамика развития популяции штамма S.aureus № 56
Опытные штаммы E.coli были чувствительны к амикацину: МИК для штаммов E. coli АТСС 25922, E. coli № 35, № 823 и № 879 – 1,5, № 22 – 3,1 мкг/мл [3].
Доксорубицин, как указывалось выше, в отношении опытных штаммов E.coli был не активен (МИК 1000 мкг/мл). В отношении опытных штаммов S.aureus его активность была умеренной: МИК для штамма S.aureus АТСС 29213 1,5 мкг/мл, № 56 – 6,2, № 97 и № 108 – 12,5, № 161 – 25 мкг/мл.
Согласно полученным данным зависимости оптической плотности (D) микробных культур от времени культивирования осуществляли построение графиков (в качестве примера приведены кривые, построенные для штаммов S.aureus АТСС 29213 – рисунок 1 и № 56 – рисунок 2).
Примечание: К — вариант штамма, культивируемый в среде без препаратов. МИКцеф. — вариант штамма, культивируемый в среде с МИК цефтриаксона. МИКдокс. — вариант штамма, культивируемый в среде с МИК доксорубицина. Сочетания — вариант, культивируемый в среде с 1/2 МИК цефтриаксона и 1/2 МИК доксорубицина.
Из полученных данных следовало, что сочетание неингибируюших концентраций цефтриаксона и доксорубицина задерживало развитие микробных популяций сопоставимо с МИК каждого из препаратов. Этот эффект был особенно выражен для 3 штаммов – S. aureus АТСС 29213, № 56 и № 161 (у всех отмечалась полная задержка или отсутствие вступления в логарифмическую фазу).
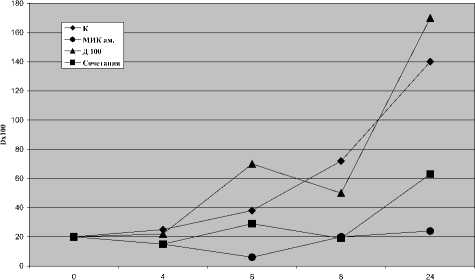
Рис. 3. Динамика развития популяции E.coli ATCC 25922
Графики, построенные для штаммов E.coli, демонстрировали, что сочетания сывороточной концентрации доксорубицина и ½ МИК амикацина задерживали наступление логарифмической фазы у 3 штаммов (E.coli АТСС 25922, № 22 и № 879). У штаммов № 35 и № 823 в этих условиях задержка логарифмической фазы сменялась проявлениями адаптации по мере культивирования. На рисунках 3 и 4 приведены кривые, построенные для штаммов E.coli АТСС 25922 и № 35.
Статистический анализ с помощью непараметрического критерия Манна-Уитни [6] совокупностей полученных значений D для штаммов S.aureus? в разных условиях культивирования показал, что культуры, развивающиеся в среде без препаратов, достоверно отличаются от культур, растущих в среде с МИК цефтриаксона и МИК доксорубицина. В условиях МИК цефтриаксона и сочетаний ½ МИК этого
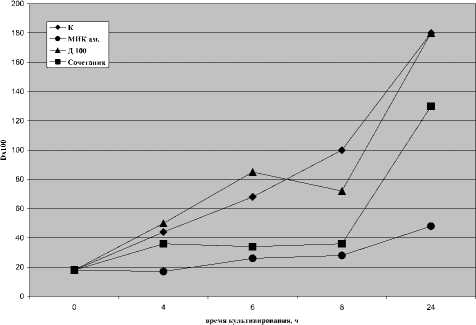
Рис. 4. Динамика развития популяции штамма E.coli № 35
Примечание: К — вариант штамма, культивируемый в среде без препаратов. МИКам. — вариант штамма, культивируемый в среде с МИК амикацина. Д100 — вариант штамма, культивируемый в среде со 100 мкг доксорубицина. Сочетания — вариант, культивируемый в среде с 1/2 МИК амикацина и 100 мкг доксорубицина.
антибиотика и доксорубицина – различия значений D незначимы.
Подобно штаммам S. aureus достоверные различия значений D были получены при сравнении развития популяций E.coli, культивируемых в бульоне без препаратов, и в мясо-пептонном бульоне с МИК амикацина. В условиях МИК амикацина и сочетания его ½ МИК со 100 мкг доксорубицина полученные значения D существенно не отличались. Стимулирующее действие сывороточной концентрации доксорубицина на развитие популяций E.coli при сравнении с культурами, которые культивировали в среде без препаратов, было существенно только через 6 часов культивирования, то есть к моменту окончания фазы адаптации.
Обсуждение. Поскольку доксорубицин в отношении опытных штаммов S. aureus проявил умеренную антимикробную активность, наличие его потенциру- ющего действия на антимикробную активность цефтриаксона было предполагаемо.
Стимулирующий эффект сывороточных концентраций доксорубицина на антимикробную активность амикацина обусловлен, очевидно, усилением поступления доксорубицина в клетки опытных штаммов E. coli в связи с характерной для действия аминогликозидов деструкцией цитоплазматических мембран бактериальных клеток [7].
Заключение. Представленные результаты позволяют считать, что неингибирующая и сывороточная концентрации доксорубицина потенцируют подавляющее действие цефтриаксона и амикацина на задержку развития микробных популяций указанных видов. Это имеет положительное значение при совместном использовании доксорубицина и указанных антибиотиков в лечении инфекционных осложнений у онкологических больных.
Список литературы Влияние доксорубицина и антибиотиков на динамику развития популяций Staphylococcus aureus и Escherichia coli
- Reduction of chemotherapy-induced febrile leucopenia by prophylactic use of ciprofloxacin and roxithromycin in small-cell lung cancer patients: an EORTC double-blind placebo-controlled phase III study/V.C. Tjan-Heijnen, RE. Postmus, A. Ardizzoni et al.//Annals of oncology. -2001. -V. 12. -№ 10. -P. 1359-1368.
- Нозокомиальные инфекции в онкологической клинике: современное состояние проблемы/А.А. Соколов, С.Д. Митрохин, В.И. Минаев, А.Н. Махсон//Российский онкологический журнал. -2007. -№ 1. -С. 29-37.
- Определение чувствительности микроорганизмов к антибактериальным препаратам: Методические указания. -МУК 4.2.1890-04. -91 с.
- Липосомы и другие наночастицы как средство доставки лекарственных веществ/А.П. Каплун, Ле Банг Шон, Ю.М. Краснопольский, В.И. Швец//Вопросы медицинской химии. -1999. -Т. 45. -№ 1. -С. 3-12.
- Райкова, С.В. Противостафилококковая активность (нитро) фурфурулиденсодержащих гексагидроиндазолов: Автореф. дисс... канд. мед. наук/С.В. Райкова. -Саратов: Саратовский государственный медицинский университет, 2005. -21 с.
- Гланц, С. Медико-биологическая статистика/С. Гланц. -М.: Практика, 1999. -459 с.
- Франклин, Т. Биохимия антимикробного действия/Т. Франклин, Дж. Сноу. -М.: Мир, 1984. -240 с.


