Влияние факторов воспаления на показатели свертывающей системы крови при почечной патологии
Автор: Сибирева Ольга Филипповна, Серебров Владимир Юрьевич, Канская Наталья Викторовна, Жаворонок Татьяна Васильевна, Позднякова Ирина Анатольевна, Степанова Екатерина Алексеевна
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.31, 2016 года.
Бесплатный доступ
Изучается роль генетически обусловленных и приобретенных форм патологии гемостаза при нефропатии и воспалении в почках с учетом выраженности альбуминурии и клиренса креатинина для оценки прогноза заболевания и осложнений его течения, а также для разработки новых подходов к лечению хронической почечной недостаточности (ХПН).
Хроническая почечная недостаточность, сосудисто-тромбоцитарный гемостаз, плазменные антикоагулянты, цитокины
Короткий адрес: https://sciup.org/14920081
IDR: 14920081 | УДК: 616.151.5-02:616.61-002
The effects of inflammatory factors on the indices of blood coagulation system in the presence of renal pathology
The role of genetically-associated and acquired forms of hemostasis pathology in the presence of nephropathy and kidney inflammation was studied taking into account severity of albuminuria and creatinine clearance to evaluate the prognosis and complications of the disease and to develop new approaches for the treatment of chronic renal disease.
Текст научной статьи Влияние факторов воспаления на показатели свертывающей системы крови при почечной патологии
В настоящее время установлена связь между клинической выраженностью нефропатии и интенсивностью воспаления в почках. На экспериментальных моделях показана взаимосвязь макрофагальной инфильтрации клубочков и канальцев с выраженностью почечного фиброза, альбуминурией и клиренсом креатинина. На фоне этого возросла диагностическая значимость различных маркеров воспаления, в частности, сопряженность уровня провоспалительных цитокинов при хронической почечной патологии и изменений показателей свертывающей системы крови [1–5, 8, 9].
Для оценки активности процессов иммунологически обусловленного воспаления, протекающих в почках, актуально определение уровня провоспалительных цитокинов. Интерлейкин-1β (IL-1β) опосредует эффект стимулирования миграции и пролиферации фибробластов, что очень важно в патогенезе склероза почек. Уровень интерлейкина-6 (IL-6) повышен в крови при многих па- тологических состояниях, включая мезангиопролифера-тивный гломерулонефрит. Данный интерлейкин регулирует пролиферацию мезангиальных эпителиоцитов, образование гранулем и формирование фиброза в почках. Фактор некроза опухолей альфа (TNF-α) выступает одним из медиаторов деструкции тканей, что имеет место при хроническом воспалении, этому цитокину также отводят существенную роль в развитии внутрисосудистого свертывания крови и полиорганной недостаточности. Современные представления о гемостазе как связующем звене между иммунитетом и воспалением подкрепляются данными, полученными при изучении механизмов индукции и прогрессирования гломерулонефрита. В процессе иммунного воспаления в клубочках почки локально активируется система гемостаза, связанная со стимулирующим влиянием продуцируемых клетками иммунной системы цитокинов на сосудисто-тромбоцитарный гемостаз, плазменное звено коагуляции и фибринолиз
[1, 6–8]. Провоспалительные цитокины (IL-1 β , IL-6, TNF- α ) также хорошо известны как индукторы высвобождения тканевого фактора моноцитами [1, 8].
Цель исследования: проанализировать взаимосвязь параметров гемокоагуляции с показателями факторов воспаления, прямо или опосредованно влияющих на систему свертывания крови, а также выяснить роль патологии системы гемостаза в патогенезе хронической болезни почек (ХБП).
Материал и методы
Обследован 481 больной ХБП, из них 213 пациентов с хроническим гломерулонефритом (ХГН), 176 – с сахарным диабетом 1 и 2-го типа (СД1, СД2), и 92 – с хроническим алкоголизмом (ХА). В обследование не вовлекались больные ХБП, не давшие информированного согласия на участие, пациенты в возрасте более 60 лет и с тяжелыми сопутствующими заболеваниями. В группу сравнения вошло 50 здоровых доноров.
В группу 1 вошло 142 пациента – 86 мужчин и 56 женщин, средний возраст – 38,50 (23,00; 51,00) лет с сохраненной функцией почек, т.е. без депрессии скорости клубочковой фильтрации (более 80 мл/мин/1,73 м2).
У 71 пациента была диагностирована азотемическая стадия болезни, из них 30 больных – 15 мужчин и 15 женщин, средний возраст 48,00 (40,00; 53,00) лет, длительность заболевания 7,50 (3,00; 18,00) лет – были с кон-сервативно-курабельной стадией ХПН – группа 2, и 41 больной – 15 женщин и 26 мужчин, средний возраст 47,00 (38,00; 56,00) лет, длительность заболевания 11,50 (6,00; 18,00) лет – с терминальной стадией ХПН – группа 3, получавшие терапию программным гемодиализом (би-карбонатный диализ) по 4 ч три раза в неделю на аппаратах “искусственная почка” “4008S” фирмы Fresenius (Германия) и “Multimat” фирмы Bellco (Италия).
Диабетическая нефропатия III–IV стадий верифицирована у 36 (55,39%) больных СД1 и 52 (46,85%) больных СД2 при наличии микроальбуминурии или протеинурии. Начинающуюся нефропатию (стадия микроальбуминурии) диагностировали при уровне альбуминурии от 30 до 300 мг в сутки, выраженную нефропатию (стадия протеинурии) – при более высоких значениях суточной потери белка с мочой. У всех больных с диабетической нефропатией азотовыделительная функция почек была сохранена.
У 43 (46,74%) больных ХА при тщательном обследовании патологии со стороны почек не выявлено (группа 1). У 49 (53,26%) пациентов имелись признаки алкогольного поражения почек – алкогольная нефропатия (группа 2), из них 12 (24,49%) были с микроальбуминурией и 37 (75,51%) – с наличием протеинурии.
Материалом являлась периферическая кровь, взятая утром натощак из локтевой вены в количестве 10 мл.
Методы исследования. Исследовали показатель протромбина по Квику, тромбиновое и каолиновое время, количество тромбоцитов, уровень эндотелина-1, агрегацию тромбоцитов с адреналином и ристомицином, скорость и время агрегации тромбоцитов, антитромбин ІІІ (АТ ІІІ), фактор Виллебранда (ФВ), уровень растворимых фибринмономерных комплексов, С-белка, активность факторов свертывания V, VІІ и VІІІ. Оценивали содержание цитокинов IL-1β, IL-6, TNF-α хемолюминесцентным иммуноферментным методом и уровень С-реактивного протеина (СРП) в сыворотке крови с помощью реактивов фирмы “Siemens Diagnostics” (Великобритания) производства компании Diagnostics Products Corporation. Статистический анализ полученных данных проводили при помощи пакетов статистических программ Statistica 6.0 и Биостатистика 4.03.
Результаты и обсуждение
Причиной активации свертывающей системы при ХГН является наличие системного воспалительного процесса. На это указывает установленная нами статистически значимая положительная корреляционная зависимость между показателями содержания в крови СРП и D-димера (rs=0,38; p<0,05), индексом активности нефрита и фактором VIIIа (rs=0,48; p<0,05), уровнем IL-6 и фактором VIIа (rs=0,42; p<0,05) и отрицательная – между уровнями IL-8, СРП и активностью АТ III (rs=–0,51, rs=–0,61; p<0,05 соответственно). При прогрессировании ХБП важна роль цитокинов как регуляторов гемостаза и иммунитета. Цитокины стимулируют сосудисто-тромбоцитарный гемостаз, процесс свертывания крови и приводят к торможению фибринолиза. Эта реакция проявляется за счет активации эндотелия и макрофагов (моноцитов), экспрессирующих ФВ, тканевой фактор, а также ингибиторы фибринолиза. Одновременно IL-1 β , ІL-6 и TNF- α стимулируют гепатоциты, способствуя увеличению синтеза белков острой фазы воспаления, в частности, фибриногена, α 2-макроглобулина, α 1-антитрипсина и α 2-антиплазмина, принимающих участие в свертывании крови и ингибирующих фибринолиз. Одним из основных белков острой фазы выступает СРП, имеющий непосредственное отношение к течению иммунологических реакций. В больших дозах он тормозит фагоцитоз, активирует систему комплемента, способствует продукции IL-1 β и TNF- α , играющих важную роль не только в развитии воспаления, но и регуляции синтеза белков острой фазы и иммунном ответе. Под влиянием IL-1 β клетки эндотелия усиленно синтезируют и секретируют тканевой фактор. В экспрессии тканевого фактора моноцитами также участвует СРП, тем самым индуцируя диссеминированное внутрисосудистое свертывание. Связываясь с фактором активации тромбоцитов, СРП способствует агрегации тромбоцитов, стимулируя в них образование тромбоксана-А2, вызывающего необратимую агрегацию кровяных пластинок. Возможно, СРП блокирует действие гепарина и тем самым ускоряет переход фибриногена в фибрин под действием тромбина. Также СРП способен образовывать комплексы с фибриногеном, активирующие систему комплемента [1–3, 7–9].
Кроме группы больных алкоголизмом во всех остальных сравниваемых группах уровень СРП превышал контрольные значения, однако в группах больных ХГН это увеличение было кратно больше, чем в группе больных СД. Гиперкоагуляция при СД обеспечивается за счет увеличенной продукции белка ингибитора активаторов плаз-
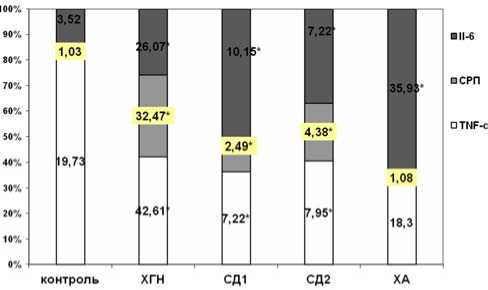
Рис. 1. Уровень IL-6, СРП и TNF- α в крови при ХГН, СД, ХА в группе контроля. Примечание: * – различия с группой контроля статистически значимы. Ось абсцисс – название обследуемых групп; ось ординат – уровень IL-6, СРП и TNF- α (%)
миногена-1 под действием СРП, особенно в условиях гипергликемии. 8.
Уровни ІL-6, ІL-8 также были повышены в разной сте- 9 пени во всех группах (рис. 1), в том числе и у больных . алкоголизмом. У больных ХГН гиперпродукция провос-палительных цитокинов и высокое содержание СРП ука-
Скопец И.С., Везикова Н.Н., Марусенко И.М. и др. Острый коронарный синдром: комплексный взгляд на проблему. Значение госпитального и амбулаторного этапов лечения пациентов // Архив внутр. медицины. – 2012. – № 3. – С. 58–64.
Шимохина Н.Ю., Петрова М.М., Савченко А.А. Агрегационная активность тромбоцитов в системе гемостаза у больных с осложненным течением гипертонической болезни в сочетании с ишемической болезнью сердца в различные периоды ишемического инсульта // Кардиология. – 2010. – № 8. – С. 21–24.
Шимохина Н.Ю., Савченко А.А., Чижикова И.К. и др. Особенности системы гемостаза и хемилюминисцентной активности нейтрофильных гранулоцитов у больных острым коронарным синдромом // Сиб. мед. обозрение. – 2012. – Т. 6(78). – С. 21–24.
Шимохина Н.Ю., Савченко А.А., Петрова М.М., Каскаева Д.С. Прогностическое значение определения метаболического статуса тромбоцитов у больных с цереброваскулярными осложнениями гипертонической болезни в сочетании с ишемической болезнью сердца // Кардиология. – 2012. – Т. 6(52). – С. 14–18.
Ярилин А.А. Иммунология. – М. : Гэотар-Медиа, 2010. – 752 с.
Levi M. The coagulant response in sepsis and inflammation // Hamostaseologie. – 2010. – Vol. 30. – P. 10–16.
Поступила 01.02.2016
зывают на наличие системного воспалительного процесса. Уровень TNF- α у больных ХА был сопоставимым с таковым в контроле, а у больных СД был ниже значений нормы, вероятно, потому что активация секреции TNF- α типична для генерализованных процессов преимущественно бактериальной этиологии.
Надо отметить, что у больных СД и ХА с нефропатией изменения показателей тромбоцитарного и коагуляционного гемостаза были более выраженными, чем у пациентов этих групп без нефропатии. Это, опять же, согласуется с итогами воспроизведения феномена Шварцмана и эндотоксинового шока, когда особенно интенсивно гиперкоагуляция развивалась при совместном введении ІІ-1 β и TNF- α , сопровождаясь инициацией и значительным увеличением синтеза и экспрессии тканевого фактора эндотелиальными клетками [8]. У больных СД, больных ХА с нефропатией и у пациентов с консервативно-курабельной стадией ХПН было замечено повышение уровня IL-1 β в крови. Повышение синтеза IL-1 β приводит к активации ряда генов в клетках эндотелия сосудов и в мезангиальных клетках почек и к увеличению продукции коллагена IV типа, составляющего здесь основу межклеточного матрикса. В этой связи увеличение уровня IL-1 β можно считать предиктором развития и прогрессирования нефропатии.
Список литературы Влияние факторов воспаления на показатели свертывающей системы крови при почечной патологии
- Козлов В.А., Борисов А.Г., Смирнова С.В. и др. Практические аспекты диагностики и лечения иммунных нарушений: руководство для врачей. -Новосибирск: Наука, 2009. -274 с.
- Кузник Б.И. Цитокины и система гемостаза. Сообщение 1. Цитокины и сосудисто-тромбоцитарный гемостаз//Тромбоз, гемостаз и реология. -2012. -№ 2. -С. 12-23.
- Национальные клинические рекомендации. -4-е изд. -М.: Силицея-Полиграф, 2011. -568 с.
- Скопец И.С., Везикова Н.Н., Марусенко И.М. и др. Острый коронарный синдром: комплексный взгляд на проблему. Значение госпитального и амбулаторного этапов лечения пациентов//Архив внутр. медицины. -2012. -№ 3. -С. 58-64.
- Шимохина Н.Ю., Петрова М.М., Савченко А.А. Агрегационная активность тромбоцитов в системе гемостаза у больных с осложненным течением гипертонической болезни в сочетании с ишемической болезнью сердца в различные периоды ишемического инсульта//Кардиология. -2010. -№ 8. -С. 21-24.
- Шимохина Н.Ю., Савченко А.А., Чижикова И.К. и др. Особенности системы гемостаза и хемилюминисцентной активности нейтрофильных гранулоцитов у больных острым коронарным синдромом//Сиб. мед. обозрение. -2012. -Т. 6(78). -С. 21-24.
- Шимохина Н.Ю., Савченко А.А., Петрова М.М., Каскаева Д.С. Прогностическое значение определения метаболического статуса тромбоцитов у больных с цереброваскулярными осложнениями гипертонической болезни в сочетании с ишемической болезнью сердца//Кардиология. -2012. -Т. 6(52). -С. 14-18.
- Ярилин А.А. Иммунология. -М.: Гэотар-Медиа, 2010. -752 с.
- Levi M. The coagulant response in sepsis and inflammation//Hamostaseologie. -2010. -Vol. 30. -P. 10-16.


