Влияние гипоксии на молекулярное состояние гемоглобина эритроцитов крыс при физических нагрузках
Автор: Федяшкина Анастасия Николаевна, Максимов Георгий Владимирович
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Краткие сообщения
Статья в выпуске: 3-4, 2013 года.
Бесплатный доступ
В статье рассматриваются изменения конформации гемопорфирина при развитии гипоксии, связанной с разной физической нагрузкой у крыс.
Гемопорфирин, гипоксия, физическая нагрузка, спектр комбинационного рассеяния
Короткий адрес: https://sciup.org/14720024
IDR: 14720024 | УДК: 599.323.4:
The influence of hypoxia on the molecular state of erythrocyte hemoglobin of rats during physical activity
This article discusses the conformation changes of hemoporphirine in the development of hypoxia that is associated with a different physical activity of rats.
Текст краткого сообщения Влияние гипоксии на молекулярное состояние гемоглобина эритроцитов крыс при физических нагрузках
Молекула гемоглобина может находиться в двух конформациях – напряженной и расслабленной. Расслабленная комформация связывает кислород в 70 раз быстрее, чем напряженная. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Одной из важных причин нарушения кислородтранспортной системы может быть изменение конформации гемопорфирина гемоглобина (Гб) и его сродства к кислороду (О2) [4]. Применение спектроскопии комбинационного рассеяния (КР) позволяет выявить изменения конформации гемопорфирина при развитии гипоксии, связанной с разной физической нагрузкой.
В эксперименте использовались беспородные крысы обоего пола с массой тела от 130 до 230 г, разделенные на 4 группы. Первую (контрольную) группу составляли интактные животные; во второй группе животные подвергались физическим нагрузкам малой интенсивности (4 ч в месяц, что со- ставляло 1 ч в неделю); в третьей группе животные подвергались средним физическим нагрузкам (10 ч. в месяц, или 2–3 раза в неделю по 1 ч); в четвертой группе животные подвергались сильным физическим нагрузкам (24 ч в месяц, или 6 раз в неделю по 1 ч). В ходе исследований у крыс проводили забор крови из хвостовой вены, кровь гепаринизировали, затем отмывали эритроциты и готовили мазок эритроцитарной массы на предметном стекле.
Исследование выполнялось с помощью рамановского спектрометра in via Basis, для получения спектров геморфирина гемоглобина использовался микроскоп с регистрацией комбинационного рассеяния света in via Basis фирмы Renishaw с короткофокусным высокосветосильным монохроматором (фокусное расстояние не более 250 мм), длина волны излучения используемого лазера составляла 532 нм, мощность излучения 100 мВт, объектив 50х. Регистратор данных — CCD детектор (1024 х 256 пикселей с пельтье-охлаждением до -70 °С) с решет
кой 1 800 штр/ мм. Оцифрованные спект- Производилась коррекция базовой линии, ры обрабатывались в программе WIRE 3.3. сглаживание спектров (рис. 1).
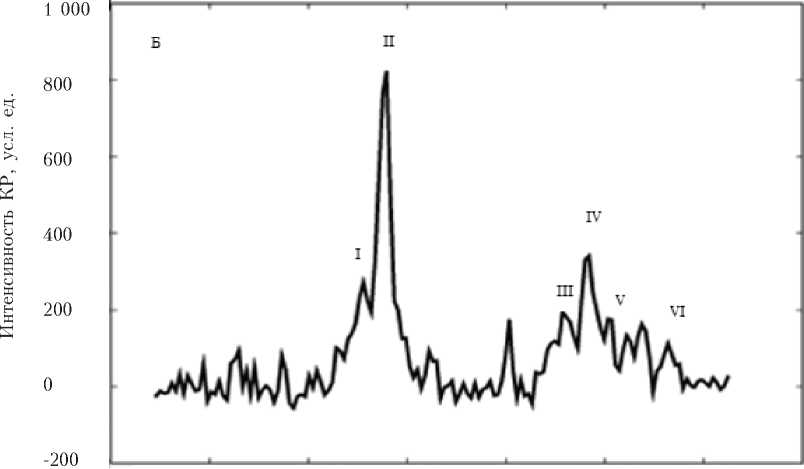
Частотный сдвиг, см-1
Р и с. 1 . Спектр гемопорферина гемоглобина
В работе для анализа конформации и О2-связывающих свойств Гб использовались определенные характерные полосы спектра КР, которые позволяли исследовать конформацию ГП в дезоксигемоглобине (д-Гб) и способность д-Гб связывать лиганд, а также конформацию ГП в оксигемоглобине (о-Гб) и способность о-Гб сбрасывать кислород: 1 355, 1 375, 1 548–1 552, 1 580– 1 588 см– 1. Полосы 1 355 и 1 375 см–1 связаны с симметричными колебаниями пиррольных колец (связи СаСb, СaN и СaNСa) в молекулах дезоксигемоглобина и гемоглобина, связанного с лигандами, соответственно [3]. Данное соотношение интенсивностей I1375/(I1355 + I1375) является характеристикой относительного количества о-Гб в суспензии эритроцитов. Полосы 1 548–1 552 см–1 и 1 580–1 588 см–1 связаны с колебанием метиновых мостиков между пирролами (связи CaCm, CaCmH) в молекулах Гб, в одних из которых гемопорфирин растянут и деформирован (1 548–1 552 см–1) а в других имеет более компактную недеформированную конформацию (1 580–1 588 см–1) [1]. Если сравниваемые пробы отличаются по содержанию относительному о-Гб, то необходимо учитывать зависимость интенсивностей полос 1 548–1 552 см–1 и 1 580–1 588 см–1 от количеств д-Гб и о-Гб. При такой нормировке отношение интенсивностей I1355/I1550 отражает относительную способность всего Гб в пробе связывать лиганды (в том числе О2), а соотношение I1375/I1580 – относительную способность Гб выделять лиганды [2].
Относительное количество о-Гб в суспензии эритроцитов снижалось при слабых и средних интенсивностях физических нагрузок (4 и 10 ч) на 3 и 12 % по отношению к контролю, которое восстанавливался при более длительном воздействии (24 ч) (рис. 2).
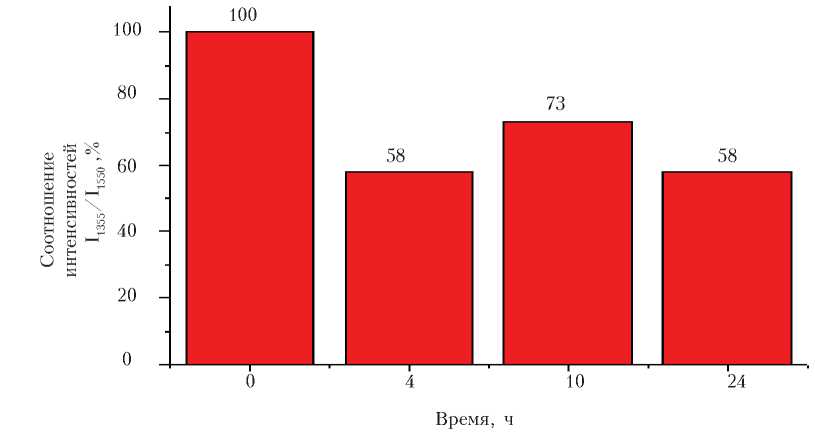
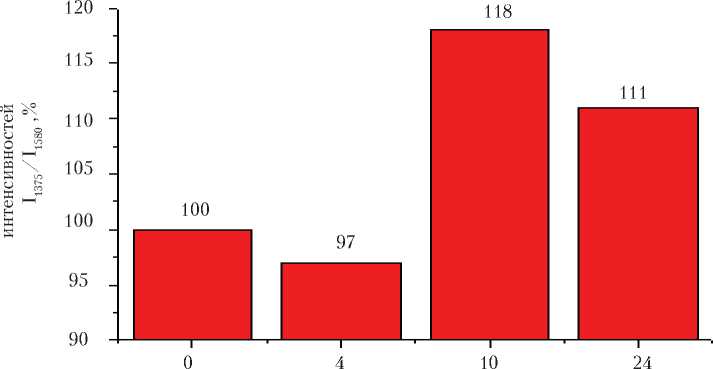
X х Рис. 2. Диаграмма относительного количества о-Гб в суспензии эритроцитов Способность Гб связывать лиганды контролем. При воздействии средней ин-в том числе О2) значительно снижалось тенсивности (10 ч) также происходило при слабых (4 ч) и высоких интенсив- снижение связывающей способности на ностях (24) на 42 % по сравнению с 27 % (рис. 3). Рис. 3. Диаграмма относительной способности Гб в пробе связывать лиганды Способность Гб выделять лиганды практически не изменялась при слабой интенсивности (3 %), но при более длительном воздействии способность выделять О2 увеличивалась на 11 и 18 % (рис. 4). Время, ч Рис. 4. Диаграмма относительной способности Гб в пробе выделять лиганды На основе полученных экспериментальных данных было установлено, что при физических нагрузках относительное содержание о-Гб и способность Гб связывать лиганды (в том числе О2) в суспензии эритроцитов ниже по сравнению с контролем, но способность Гб выделять лиганды увеличивается. Показано, что функциональное состояние крыс при слабой и высокой интенсивности физических нагрузок отражается в способности связывать и сбрасывать кислород.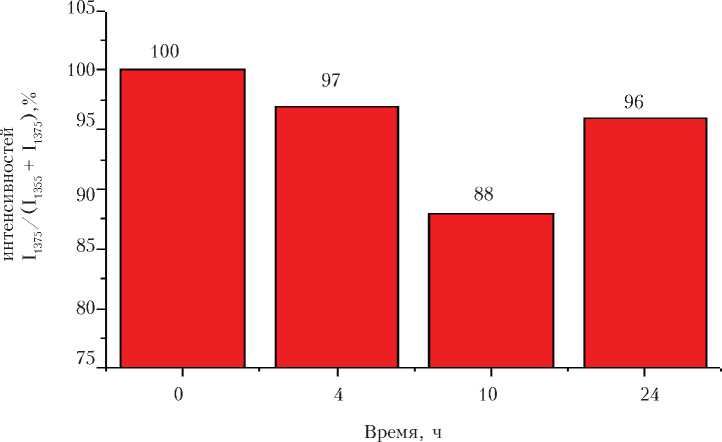
Список литературы Влияние гипоксии на молекулярное состояние гемоглобина эритроцитов крыс при физических нагрузках
- Кэри П. Применения спектроскопии КР и РКР в биохимии/П. Кэри. -М.: Мир, 1985. -272 с.
- Нанобиотехнологии: практикум/А. М. Абатурова [и др.]. -М.: БИНОМ. -Лаб. знаний, 2012. -384 с.
- Спектроскопия порфиринов: колебательные состояния/К. Н. Соловьев [и др.]. -Минск: Наука и техника, 1985. -415 с.
- Сродство гемоглобина к кислороду: Изменение сродства гемоглобина к кислороду: Эффект Бора. [Электронный ресурс]//МедУнивер -медицинский информационный портал для интересующихся медициной. -Режим доступа: http://meduniver.com/Medical/Physiology/432.html. -Дата обращения 09.07.2013.


