Влияние гуминовых препаратов на свойства деградированных почв техногенных пустошей
Автор: Трегубова П.Н., Копцик Г.Н., Степанов А.Л., Степанов А.А., Корнеечева М.Ю., Куприянова Ю.В.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Рубрика: Статьи
Статья в выпуске: 97, 2019 года.
Бесплатный доступ
Работа направлена на изучение возможности применения экзогенного органического вещества - гуминовых препаратов (ГП) - для ремедиации почв техногенных пустошей вблизи медно-никелевых комбинатов на Кольском полуострове. В краткосрочных лабораторных экспериментах исследовали возможность стабилизации подвижных форм тяжелых металлов гуминовыми препаратами различного происхождения (торфяной гумат “Флексом” и угольный гумат “Экстра”) в сравнении с ГП, инокулированными биологическими препаратами (микоризообразователями и азотфиксаторами) и минеральными добавками (NPK и CaCO3). Эксперименты проводили в течение 45 дней после 14 дней прединкубации в климатической камере Binder при контролируемом режиме освещенности, температуры и влажности, соответствующем условиям полярного дня в Кольской Субарктике. По окончании экспериментов оценивали изменение химических свойств почвы, состояние микробного сообщества и тест-культуры (щучки дернистой). Применение торфяного гумата не эффективно без дополнительных мер (сочетания с CaCO3), при этом эффекта от кооперации с биологическими добавками не отмечено...
Техногенные пустоши, ремедиация, гуматы, тяжелые металлы, органическое вещество, кислотность почв
Короткий адрес: https://sciup.org/143166809
IDR: 143166809 | УДК: 631.618:631.45 | DOI: 10.19047/0136-1694-2019-97-129-149
Influence of humic preparations on degraded soils properties of technogenic barrens
This research aim was testing the applicability of exogenic organic matter - extracted humic substances - for the remediation of technogenic barrens soils near Cu-Ni smelter (Kola Peninsula). In short-term laboratory experiments we studied the possibility of stabilization of heavy metals labile forms by commercial humic substances (HS) of different origin (peat humate “Flexom” and coal humate “Extra”) in comparison with HS, inoculated by microorganisms - nitrogen fixers and mycorrhizae-forming fungi and mineral fertilizers (NPK и CaCO3). Experiments were provided during 45 days after 14 days of pre-incubation under controlled conditions in climate chamber with light, temperature and humidity imitating the polar day conditions in Kola Subarctic. After experiments we evaluated changes in soil chemical properties, soil microbial community and test-culture (Deschampsia cespitosa). Peat humate application is ineffective without additional manipulations (e.g. combination with CaCO3), cooperation with biological applicants cannot be pointed out. Application of coal humate favours to metals stabilization, soil microorganism’s activation, test-culture growth. It may be effective to combine coal humate with biological applicants like mycorrhizae-forming fungi. So, coal-humates may be perspective growth-stimulator, ameliorant and detoxicant in remediation of degraded soils in conditions of polymetallic contamination.
Текст научной статьи Влияние гуминовых препаратов на свойства деградированных почв техногенных пустошей
Урбанизация, промышленная и сельскохозяйственная деятельность человека неизбежно сопровождаются издержками и сопутствующим им спектром экологических проблем (Добровольский, 1997; Антропогенные почвы…, 2003; Panagos et al., 2013) . Постоянное выраженное протекание процессов, не характерных для естественных условий формирования ландшафта, ухудшает способность почвы выполнять свои экосистемные функции, в отдельных случаях разрушая ее полностью (Adriano, 2001; Toth et al., 2016) . В настоящее время среди антропогенных факторов, сопровождающихся деградацией почв, наибольшее распространение получило загрязнение тяжелыми металлами (ТМ) (Panagos et al., 2013) . Актуальным на сегодняшний момент является изучение способов восстановления подвергшихся загрязнению почв – ремедиации, основной задачей которой является уменьшение биологической доступности токсиканта (Park et al., 2011) . Эффективность ремедиации зависит как от факторов, обеспечивающих почвообразование, так и от свойств самих ТМ (Копцик, 2014) .
Перспективным в ремедиации загрязненных ТМ почв является использования гуминовых препаратов (ГП) – производных природного органического вещества, преимущественно получаемых путем щелочной экстракции (Степанов, Якименко, 2016; Janoš et al., 2010; Pukalchik et al., 2017). Применение ГП в данном направлении обусловлено тем, что органическое вещество является важным компонентном почвенных экосистем, непосредственно участвующим в контроле поведения как элементов питания, так и токсикантов (Орлов, 1993; Соколова и др., 2009; McBride, 1990; Borûvka, Drábek, 2004; Perminova et al., 2005; Trevisan et al., 2010). Наличие широкого спектра функциональных групп обуславливает способность ГП вступать в ионные и донорно-акцепторные взаимодействия, образовывать водородные связи, активно участвовать в сорбционных процессах, проявлять полярные и амфифильные свойства. Таким образом, способность ГП связывать ионы металлов в комплексы при определенных условиях может приводить к снижению концентрации свободных ионов, что отвечает целям ремедиации. Отмечается также, что ГП улучшают физикохимические свойства почв, активизируют микрофлору, повышают коэффициент использования минеральных удобрений, усиливают защитные свойства растений к условиям среды (Орлов, 1993; Куликова, 2008; Perminova et al., 2005). Однако с упомянутой неоднородной функциональной организацией сопряжены и сложности: гуминовые вещества могут способствовать как стабилизации подвижных форм ТМ, так и усиливать их биологическую доступность (Halim et al., 2003).
Целью данного исследования была отработка метода ремедиации загрязненных почв техногенных пустошей Кольской Субарктики, основанного на внесении ГП в условиях, имитирующих природные условия региона.
ОБЪЕКТЫ И МЕТОДЫ
Объект исследования, приуроченный к г. Мончегорску Мурманской обл., находится в подзоне северной тайги, Кольско-Печорской подпровинции Североевропейской таежной провинции (Растительность…, 1980) . Для территории характерна замедленность биохимических процессов, короткий вегетационный период.
В рамках исследования была проведена серия лабораторных экспериментов на почвах техногенной пустоши, сформировавшейся в локальной зоне воздействия горно-металлургического комбината (ГМК) “Североникель” в результате многолетних выбросов веществ, сопутствующих технологическому процессу, – диоксида серы и ТМ, преимущественно Ni и Cu. Протяженность пустоши достигает 5–6 км по направлению преобладающих югоюго-западных ветров, ее характерными чертами являются практически полное отмирание растительности, редуцированный, либо полностью смытый вследствие развития водной и ветровой эрозии органогенный горизонт почв, кислая реакция среды, низкая емкость катионного обмена, высокое содержание главных загрязняющих металлов – Ni и Cu. Использованная в эксперименте почва – абразем альфегумусовый иллювиально-многогумусовый супесчаный на моренных отложениях – была отобрана с участка в 2 км от ГМК. Профиль представлен выходящим на поверхность иллювиальным горизонтом BF, переходным BC и почвообразующей породой С. Координаты участка 67°56.457′ с.ш., 32°50.074′ в.д.
В качестве тестовой была использована монокультура ‒ щучка дернистая, Deschampsia cespitosa , нативная для Кольского полуострова, собранная и предоставленная сотрудниками Полярно-альпийского ботанического сада-института им. Н.А. Аврорина Кольского научного центра РАН.
Эксперименты проводили в контролируемых условиях в климатической камере Binder с режимом освещения, имитирующим полярный день, при температуре и влажности, характерных для летнего сезона в Мончегорском районе согласно данным метеостанции г. Мончегорск с сайта “Расписание погоды” (табл. 1).
Таблица 1. Гидротермический режим в течение экспериментов Table 1. Hydrothermal regime during experiments
|
Время, часы |
Tемпература, °C |
Влажность, % |
|
00:00 ‒ 06:00 |
10.3 |
82.8 |
|
06:00 ‒ 12:00 |
11.9 |
75.4 |
|
12:00 ‒ 18:00 |
15.0 |
62.5 |
|
18:00 ‒ 24:00 |
13.4 |
70.4 |
В качестве добавок на образцах горизонта BF нами были протестированы коммерческие гуматы – Na/K соли гуминовых веществ различного происхождения: торфяной гумат “Флексом” (ГТ) и угольный гумат (ГУ) “Экстра”. В соответствии с проведенными ранее экспериментами, ГУ вносился в концентрации 0.5 % углерода к массе почвы, дозы ГТ подбирались из ряда от рекомендованных производителем до максимально возможных без нарушения водно-воздушного режима почвы.
Внесение органических добавок в подобранных дозах сравнивали с эффектом от внесения 1) минеральных добавок – CaCO3 и NPK; 2) ГП, инокулированных биологическими препаратами – микоризообразователями (Glomus intraradices, Glomus proliferum, Cenococcum geophilum) и азотфиксаторами (Azotobacter chroococcum, Rhodococcus erythropolis, Pseudomonas fluorescens) – в целях стабилизации подвижных форм ТМ и усиления биологической активности загрязненной почвы. В данной работе мы оцениваем содержание соединений ТМ, экстрагируемых водой. Оценка содержания фракций, извлекаемых ацетатно-аммонийным буфером, не входила в задачи исследования ввиду отмечающейся в литературе избыточной реакционной способности буфера, из чего следует, что не вполне корректно проводить им экстракцию для определения легкодоступных для растений форм (Водяницкий и др., 2012).
Подбор вариантов и доз внесения в краткосрочном лабораторном эксперименте первой серии.
Задачи эксперимента: сравнить эффект от внесения набора доз ГП различного происхождения (совместно с NPK) на свойства почв техногенной пустоши и состояние тест-культуры. В эксперименте были использованы следующие варианты: (i) азофоска (NPK) – в качестве контрольного; (ii) карбонат кальция совместно с азофоской (CaCO 3 + NPK); (iii) ГТ в концентрациях 3 (рекомендация производителя), 300 и 3000 л/га совместно с NPK; (iv) ГУ в концентрации 0.5 % углерода к массе почвы совместно с NPK.
Проверка сочетаемости препаратов, включая микробные, в краткосрочном лабораторном эксперименте второй серии.
Задачи эксперимента: сравнить влияние препаратов в подобранных концентрациях (ГТ – 3000 л/га и ГУ 0.5 %) самих по себе (по результатам первой серии) и совместно с микробными препаратами и CaCO3 на свойства почв и состояние тест-культуры. ГП были инокулированы микроорганизмами-микоризообразователя-ми (M) и азотфиксаторами (А). В эксперименте были использованы следующие варианты: (i) контроль (без внесения добавок); (ii) ГТ, инокулированный организмами-азотфиксаторами, совместно с азофоской (ГТA + NPK); (iii) ГТ, инокулированный организмами-азотфиксаторами, совместно с азофоской и CaCO3 (ГТA + NPK + CaCO3); (iv) ГТ, инокулированный организмами-микоризо-образователями, совместно с азофоской (ГТM + NPK); (v) ГУ, инокулированный организмами-азотфиксаторами, совместно с азофоской (ГУA + NPK); (vi) ГУ, инокулированный организмами- азотфиксаторами, совместно с азофоской и CaCO3 (ГУA + NPK + CaCO3); (vii) ГУ, инокулированный организмами-микоризо-образователями, совместно с азофоской (ГУM + NPK).
В обеих сериях период предварительной инкубации составил 14 дней, продолжительность инкубации – 45 дней.
По прошествии экспериментов в предварительно растертых до 0.25 мм почвенных образцах определено общее содержание углерода методом сухого сжигания на экспресс-анализаторе АН-7529. В водной вытяжке из почвы были измерены pH потенциометрически, содержание водорастворимых соединений углерода (DOC) и азота (DN) на Shimadzu TOC Analyzer, содержание водорастворимых форм ТМ с помощью масс-спектрометрии с индуктивно-связанной плазмой (ICP MS 7500a, Agilent). Содержание углерода микробной биомассы (C micr ) определяли в свежих образцах почв, лишенных корней, методом фумигации-экстракции (Vance et al., 1987) . В течение эксперимента оценивали эмиссию диоксида углерода почвами в динамике методом закрытых камер с помощью ИК СО 2 -газоанализатора AZ 7752. Также была оценена надземная и подземная фитомасса тест-культуры.
Таким образом, эксперименты проводили в двух сериях, для которых использовали отобранные с участка пустоши усредненные образцы почвы; варианты в разных сериях не повторялись; в первой серии контрольным можно считать вариант с внесением NPK, во второй – без внесения добавок. Для удобства представления экспериментальные результаты объединены. Полученные данные обработаны методами описательной статистики и корреляционного анализа в программах RStudio и Excel.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Свойства почвы. Почва пустоши в контрольном варианте и варианте внесения NPK в среднем характеризуется кислой реакцией среды – pH = 4.7–4.9, низким общим содержанием органического углерода – TC = 1.1–1.4 % (табл. 2). Внесение карбоната кальция сопровождается снижением кислотности; торфяной гумат в выбранных концентрациях сам по себе не способствует тому же эффекту, в то время как внесение угольного гумата значимо повышает pH до 5.4–6.2 в среднем по вариантам.
Таблица 2. Свойства почвы пустошей в конце экспериментов: pH – pH водной вытяжки, TC – общее содержание углерода (%), DOC – содержание водорастворимого углерода (мг/кг), DN – содержание водорастворимого азота (мг/кг). Min и Max – минимальное и максимальное значение показателя, Q1 и Q3 – первый и третий квартили, Med – медиана
Table 2. Properties of techogenic barren soil in the end of experiments: pH – pH of water extract, TC – total carbon content (%), DOC – dissolved organic carbon content (mg/kg), DN – dissolved nitrogen content (mg/kg). Min and Max – minimum and maximum of parameter, Q1 and Q3 – first and third quartiles, Med – median
|
Вариант эксперимента |
pH |
TC |
||||||||
|
Min |
Q1 |
Med |
Q3 |
Max |
Min |
Q1 |
Med |
Q3 |
Max |
|
|
K |
4.6 |
4.6 |
4.7 |
4.8 |
4.9 |
1.0 |
1.1 |
1.1 |
1.2 |
1.2 |
|
NPK |
4.7 |
4.8 |
4.8 |
4.9 |
5.2 |
1.2 |
1.3 |
1.4 |
1.5 |
1.6 |
|
CaCO 3 |
4.8 |
5.1 |
5.2 |
5.3 |
5.5 |
1.5 |
1.5 |
1.5 |
1.5 |
1.6 |
|
ГТ3 |
4.9 |
5.0 |
5.0 |
5.0 |
5.0 |
1.5 |
1.5 |
1.6 |
1.6 |
1.6 |
|
ГТ300 |
4.5 |
4.6 |
4.7 |
4.7 |
4.7 |
1.5 |
1.5 |
1.5 |
1.5 |
1.6 |
|
ГТ3000 |
4.9 |
4.9 |
5.0 |
5.0 |
5.1 |
1.6 |
1.6 |
1.7 |
1.7 |
1.7 |
|
ГТА3000+CaCO 3 |
6.2 |
6.2 |
6.2 |
6.3 |
6.3 |
1.1 |
1.1 |
1.1 |
1.1 |
1.2 |
|
ГТМ3000 |
4.8 |
4.8 |
4.8 |
4.8 |
4.9 |
1.1 |
1.1 |
1.1 |
1.2 |
1.2 |
|
ГТА3000 |
5.0 |
5.0 |
5.0 |
5.1 |
5.1 |
1.1 |
1.1 |
1.1 |
1.1 |
1.1 |
|
ГУ |
5.1 |
5.3 |
5.5 |
5.6 |
5.7 |
1.7 |
1.9 |
2.0 |
2.0 |
2.0 |
|
ГУА+CaCO 3 |
6.1 |
6.2 |
6.3 |
6.3 |
6.3 |
1.4 |
1.4 |
1.4 |
1.4 |
1.4 |
|
ГУМ |
6.0 |
6.0 |
6.0 |
6.1 |
6.2 |
1.4 |
1.4 |
1.4 |
1.4 |
1.4 |
|
ГУА |
6.0 |
6.0 |
6.0 |
6.0 |
6.1 |
1.5 |
1.5 |
1.5 |
1.5 |
1.5 |
|
Вариант эксперимента |
DOC |
DN |
||||||||
|
Min |
Q1 |
Med |
Q3 |
Max |
Min |
Q1 |
Med |
Q3 |
Max |
|
|
K |
241 |
266 |
280 |
285 |
288 |
13.9 |
14.7 |
15.7 |
17.4 |
20.2 |
|
NPK |
87.9 |
88.0 |
90.3 |
101 |
128 |
158 |
198 |
228 |
263 |
313 |
|
CaCO 3 |
123 |
126 |
143 |
165 |
186 |
127 |
160 |
189 |
223 |
272 |
|
ГТ3 |
99.4 |
107 |
110 |
111 |
115 |
207 |
209 |
223 |
247 |
277 |
|
ГТ300 |
98.8 |
103 |
106 |
107 |
109 |
324 |
327 |
334 |
341 |
344 |
|
ГТ3000 |
83.5 |
96.6 |
102 |
105 |
107 |
135 |
179 |
195 |
206 |
232 |
|
ГТА3000 + CaCO 3 |
195 |
196 |
252 |
316 |
340 |
112 |
123 |
132 |
149 |
184 |
|
ГТМ3000 |
240 |
272 |
297 |
324 |
363 |
144 |
172 |
183 |
186 |
186 |
|
ГТА3000 |
252 |
282 |
302 |
332 |
395.4 |
175 |
181 |
189 |
195 |
197 |
|
ГУ |
131 |
138 |
144 |
149 |
153 |
137 |
154 |
179 |
219 |
280 |
|
ГУА + CaCO 3 |
220 |
304 |
349 |
367 |
368 |
104 |
114 |
126 |
136 |
142 |
|
ГУМ |
259 |
279 |
286 |
302 |
344 |
126 |
134 |
143 |
157 |
178 |
|
ГУА |
260 |
280 |
299 |
320 |
345 |
124 |
130 |
132 |
142 |
173 |
То же относится и к общему содержанию углерода – внесению угольного гумата соответствует обогащение почвы пустоши углеродом на предполагаемые при постановке эксперимента 0.5 %. Кажущиеся различия в содержании водорастворимого углерода по всей видимости связаны с исходной неоднородностью, обуславливавшей разницу в pH и TC в вариантах K и NPK (разница в 0.2–0.3 единицы и процента соответственно). Относительно этих контрольных вариантов для двух экспериментальных серий значимых изменений с внесением карбоната кальция и органических добавок в содержании DOC отметить нельзя. Кроме того, к сожалению, в данной работе нельзя признать содержание водорастворимого углерода информативным показателем: корреляции с почвенными свойствами, в частности, с содержанием водорастворимых форм ТМ, не соответствуют ожидаемым зависимостям и не согласуются с литературными данными. Предполагается, что растворенное органическое вещество напрямую связано с подвижностью биологически доступных форм ТМ (Добровольский, 1997; Yin et al., 2002) , чего нам отметить не удалось. В то же время логичны различия в содержании растворимого азота в почвах после эксперимента: максимум и минимум содержания совпадает с высокими и низкими содержаниями Ni и Cu в аналогичных вариантах и, вероятно, свидетельствует о его низком потреблении.
Деградированные почвы пустоши характеризуются сильным загрязнением Ni и Cu (рис. 1). Поскольку достоверных различий между содержанием водорастворимых соединений металлов в контрольном варианте и варианте с NPK нет, для удобства восприятия на рисунках 1 и 2 они объединены в один вариант – К*. Аналогичным образом объединены варианты с инокуляцией – И – торфяного (ГТИ3000) и угольного (ГУИ) гуматов микроорганизмами.
Содержание водорастворимых соединений Ni и Cu в контрольном варианте достигает 4–5 мг/кг и 10–12 мг/кг, что превышает ПДК подвижных соединений металлов даже с учетом привязки норматива (ГН 2.1.7.2041-06) к более реакционноспособному ацетатно-аммонийному буферу. Внесение торфяного гумата не влечет за собой стабилизации водорастворимых соединений Ni и Cu либо наблюдается их относительная мобилизация. Выбранной концентрации угольного гумата достаточно для снижения концентраций ТМ в водной вытяжке в 4–10 раз. Можно было бы ожидать, что сочетание органических добавок с карбонатом кальция усилит их стабилизирующий эффект, однако, если это верно для торфяного гумата, для угольного гумата значимых различий в сравнении с чистым препаратом не наблюдается.
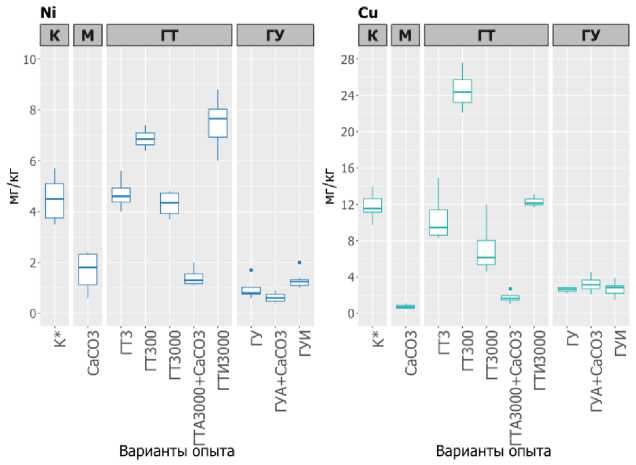
Рис. 1. Содержание водорастворимых соединений Ni и Cu в почве в конце экспериментов. Здесь и далее: К – контроль, М – с минеральными добавками, ГТ – с торфяным гуматом, ГУ – с угольным гуматом. На графиках “box-plot with whiskers” изображены общий, межквартильный размах (первый и третий квартиль) и медиана, число повторностей равно четырем.
Fig. 1. Content of water-soluble Ni and Cu in soils in the end of experiments. Hereinafter K – control, M – with mineral ameliorants, ГТ – with peat humate, ГУ – with coal humate. On graphs “box-plot with whiskers” – range, interquartile range (between 1st and 3rd quartiles), median with number of replicants is 4.
В то же время в литературе отмечается постепенное снижение эффекта стабилизации карбонатом кальция, равно как и известью, биологически доступных форм ТМ с течением времени
(Копцик и др., 2016) , поэтому дополнительное сочетание препаратов может быть целесообразным. Содержание водорастворимых форм железа слабо меняется в вариантах эксперимента, тогда как для алюминия наблюдается схожий с медью тренд увеличения подвижности в варианте с торфяным гуматом ГТ300.
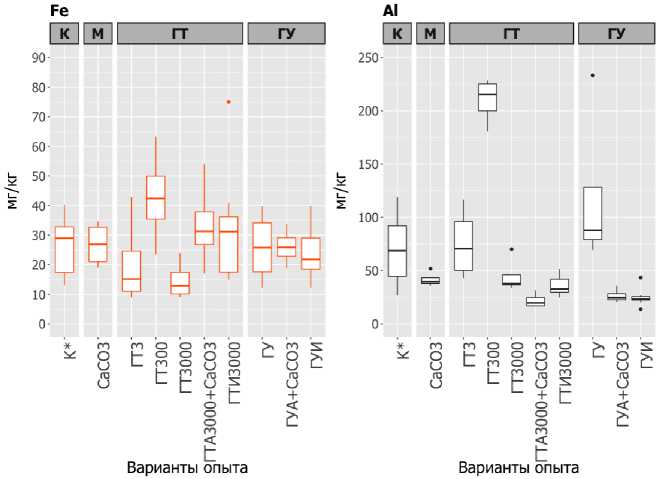
Рис. 2. Содержание водорастворимых соединений Fe и Al в почве в конце экспериментов.
Fig. 2. Content of water-soluble Fe and Al in soils in the end of experiments.
Биологический отклик. Микробная биомасса в контрольном варианте эксперимента составила порядка 150 мг/кг в среднем в пересчете на углерод (рис. 3). Ее увеличение наблюдается в вариантах с угольным гуматом, и тенденция к увеличению прослеживается всюду, куда вносился карбонат кальция. Это наблюдение согласуется с эмиссией диоксида углерода почвами в течение экспериментов (рис. 4).
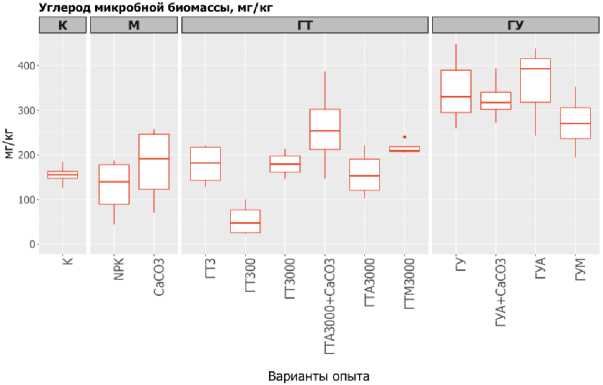
Рис. 3. Содержание углерода микробной биомассы в почве в конце экспериментов.
Fig. 3. Content of microbial biomass carbon in soils the end of experiments.
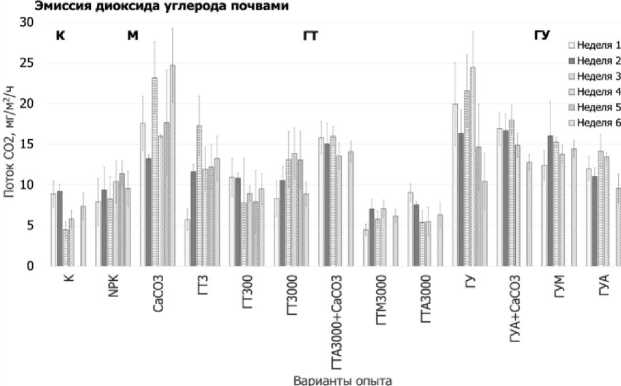
Рис. 4. Динамика почвенного дыхания в течение шести недель экспериментов.
Fig. 4. Soil respiration dynamics during 6 weeks of experiments.
Контрольные значения почвенного дыхания являются экстремально низкими, и, даже при его относительном увеличении в вариантах с внесением карбоната кальция и угольного гумата, уровень дыхания соответствует скорости эмиссии CO2 из загрязненных почв техногенных пустошей (Кадулин, Копцик, 2013).
Отклик микробного сообщества на торфяный гумат не отмечен в рамках экспериментов – содержание углерода микробной биомассы, равно как и скорость эмиссии CO 2 , значимо не отличаются от контрольных вариантов, за исключением заметного обеднения Cmicr в варианте ГТ300, обусловленного, вероятно, относительным увеличением подвижности ТМ.
В целом между содержанием углерода микробной биомассы и водорастворимых соединений Ni и Cu отмечается обратная связь (коэффициенты корреляции Спирмена – 0.67 и – 0.58).
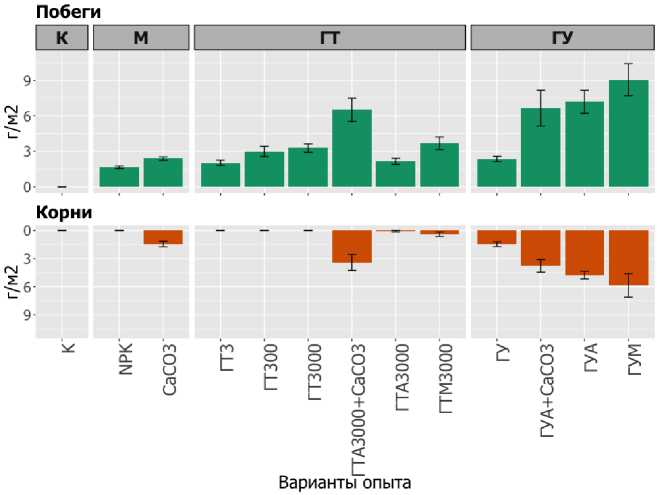
Рис. 5. Фитомасса тест-культуры, щучки дернистой, в конце экспериментов (средние и стандартные отклонения).
Fig. 5. Test-culture ( Deschampsia cespitosa ) phytomass in the end of experiments (means and standart errors).
Как видно на рисунке 5, для произрастания тест-культуры наиболее благоприятным является воздействие угольного гумата в концентрации 0.5 % и CaCO3 без внесения дополнительного органического вещества, так как в этих вариантах развивались и побеги, и корни.
При этом, по всей видимости, росту надземной массы тест-культуры торфяной гумат способствует так же, как и угольный. Обратная зависимость между интенсивностью прорастания и содержанием водорастворимых Ni и Cu в почве выше для корней (коэффициенты корреляции – 0.75 и – 0.71), чем для побегов щучки (коэффициенты корреляции – 0.45 и – 0.41) соответственно, что может косвенно указывать на отмечающиеся в литературе протекторные функции корней, с одной стороны, и гуминовых препаратов, с другой (Куликова, 2008; Farouk et al., 2011) . Отметим также разницу во влиянии азотфиксаторов и микоризообразователей на рост и развитие надземной и подземной фитомассы внутри вариантов с ГТ и ГУ. Для угольного гумата характерно наличие положительного эффекта от сочетания с микоризообразователями и азотфиксаторами, в то время как для торфяного гумата его не наблюдается.
ВЫВОДЫ
Внесение торфяных гуматов калия без дополнительных стабилизирующих агентов – в данном случае, карбоната кальция – не способствует снижению подвижности ТМ, активизации почвенной микробиоты и обогащению почвы водорастворимыми соединениями углерода. Эффект от инокуляции биопрепаратами не отмечен. Угольные гуматы уменьшают подвижность ТМ, способствуют активизации почвенной микробиоты и положительно влияют на рост тест-культуры. Наблюдается эффект от кооперации с микоризообразователями ‒ улучшение развития корневой системы тест-культуры. Применение угольных гуматов в описанных условиях не требует сочетания с дополнительными добавками.
Согласно нашим расчетам, стоимость гуминовых препаратов (в концентрации 0.5 % к массе почвы) и NPK для внесения в верхний (0–10 см), наиболее загрязненный слой маломощных подзолов / абраземов техногенных пустошей составляет 15–23 тыс. га. Это в среднем на порядок меньше затрат на промывание-экстракцию и в 5–20 раз меньше затрат на выемку и отсыпку за- грязненного слоя, приводимых в литературных источниках (Копцик, 2014). Таким образом, применение гуминовых препаратов может представлять экологически благоприятный и экономически приемлемый способ стабилизации загрязненных почв на ограниченных территориях техногенных пустошей.
В заключение отметим, что для понимания механизмов стабилизации биологически доступных форм ТМ необходимо проведение дополнительных экспериментальных исследований с последующим изучением структурно-функциональных характеристик вносимого органического вещества. Полученные в ходе таких экспериментов зависимости могут быть важным шагом к прогнозированию восстановления глубоко нарушенных экосистем.
БЛАГОДАРНОСТЬ
Исследования выполнены при финансовой поддержке РФФИ в рамках научного проекта № 18-04-01028.
Список литературы Влияние гуминовых препаратов на свойства деградированных почв техногенных пустошей
- Герасимова М.И., Строганова М.Н., Можарова Н.В., Прокофьева Т.В. Антропогенные почвы: генезис, география, рекультивация. Смоленск: Ойкумена, 2003. 268 с.
- Водяницкий Ю.Н., Ладонин Д.В., Савичев А.Т. Загрязнение почв тяжелыми металлами. М.: Изд-во Почвенного института им. В.В. Докучаева, 2012. 306 с.
- Гигиенические нормативы ГН 2.1.7.2041-06. Предельно допустимые концентрации (ПДК) химических веществ в почве.
- Орлов Д.С. Гуминовые вещества в биосфере. М.: Наука, 1993. 238 с.
- Добровольский В.В. Биосферные циклы тяжелых металлов и регуляторная роль почвы//Почвоведение. 1997. № 4. С. 431-441.
- Исаченко Т.И., Лавренко Е.М. Ботанико-географическое районирование//Растительность Европейской части СССР. Л.: Наука, 1980. 236 с.
- Кадулин М.С., Копцик Г.Н. Эмиссия CO2 почвами в зоне влияния ГМК Североникель в Кольской субарктике//Почвоведение. 2013. № 11. С. 1387-1396
- DOI: 10.1134/S1064229313110045
- Кашулина Г.М. Аэротехногенная трансформация почв Европейского Субарктического региона. Апатиты: КНЦ РАН, 2002. Ч. 1. 158 с.
- Копцик Г.Н. Современные подходы к ремедиации почв, загрязненных тяжелыми металлами (обзор литературы)//Почвоведение. 2014. № 7. С. 851-868
- DOI: 10.1134/S1064229314070072
- Копцик Г.Н., Копцик С.В., Смирнова И.Е. Альтернативные технологии ремедиации техногенных пустошей в Кольской Субарктике//Почвоведение. 2016. № 11. C. 1375-1391
- DOI: 10.7868/S0032180X16090082
- Куликова Н.А. Защитное действие гуминовых веществ по отношению к растениям в водной и почвенной средах в условиях абиотических стрессов. Дисс. … докт. биол. наук. М.: МГУ, 2008.
- Соколова Т.А., Трофимов С.Я. Сорбционные свойства почв. Адсорбция. Катионный обмен: учебное пособие по некоторым главам химии почв. Тула: Гриф и К, 2009. 172с.
- Степанов А.А., Якименко О.С. Ремедиация загрязненных городских почв с применением гуминовых препаратов//Научное электронное периодическое издание ЮФУ "Живые и биокосные системы". 2016. № 18. URL: http://www.jbks.ru/archive/issue-18/article-5/.
- Adriano D.C. Trace elements in the Terrestrial Environment. New York: Springer, 2001. 867 p.
- Borûvka L., Drábek O. Heavy metal distribution between fractions of humic substances in heavily polluted soils//Plant Soil Environ. 2004. Vol. 50. No. 8. P. 339-345
- DOI: 10.17221/4041-PSE
- Farouk S., Mosa A.A., Taha A.A., Ibrahim Heba M., EL-Gahmery A.M. Protective effect of humic acid and chitosan on radish (Raphanus sativus, L. var. sativus) plants subjected to cadmium stress // Journal of Stress Physiology & Biochemistry. 2011. Vol. 7(2). P. 99-116.
- Halim M., Conte P., Piccolo A. Potential availability of heavy metals to phytoextraction from contaminated soils induced by exofenous humic substances//Chemosphere. 2003. Vol. 52. P. 265-275
- DOI: 10.1016/S0045-6535(03)00185-1
- Janoš P., Vávrová J., Herzogová L., Pilařová V. Effects of inorganic and organic amendments on the mobility (leachability) of heavy metals in contaminated soil: a sequential extraction study//Geoderma. 2010. Vol. 159. Issues (3-4). P. 335-341
- DOI: 10.1016/j.geoderma.2010.08.009
- McBride N.M. Reactions controlling heavy metal solubility in soils//Adv. Soil Sci. 1989. No. 10. P. 1-56.
- Panagos P., Van Liedekerke M., Yigini Y., Montanarella L. Contaminated sites in Europe: review of the current situation based on data collected through a European network. J Environ Public Health, 2013
- DOI: 10.1155/2013/158764
- Park J.H., Lamb D., Paneerselvam P., Choppala G., Bolan N., Chung J.W. Role of organic amendments on enhanced bioremediation of heavy metal (loid) contaminated soils//Journal of Hazardous Materials. 2011. Vol. 185. No. 2. P. 549-574
- DOI: 10.1016/j.jhazmat.2010.09.082
- Perminova I., Hatfield K., Hertkorn N. Use of humic substances to remediate polluted environments: from theory to practice. Van GodewijckStraat 30. Dordrecht. Netherlands. 2005. 506 p.
- Pukalchik M., Mercl, F., Terekhova V., Tlustoš P. Biochar, wood ash and humic substances mitigating trace elements stress in contaminated sandy loam soil: Evidence from an integrative approach//Chemosphere. 2018. Vol. 203. P. 228-238
- DOI: 10.1016/j.chemosphere.2018.03.181
- Tóth G., Hermann T., Da Silva M.R., Montanarella L. Heavy metals in agricultural soils of the European Union with implications for food safety//Environment international. 2016. Vol. 88. P. 299-309
- DOI: 10.1016/j.envint.2015.12.017
- Trevisan S., Francioso O., Quaggiotti S., Nardi S. Humic substances biological activity at the plant-soil interface//Plant Signaling Behav. 2010. Vol. 5. P. 635-643
- DOI: 10.4161/psb.5.6.11211
- Tyler G., Olsson T. Concentrations of 60 elements in the soil solution as related to the soil acidity//European Journal of Soil Science. 2001. Vol. 52(1). P. 151-165
- DOI: 10.1046/j.1365-2389.2001.t01-1-00360.x
- Vance E., Brookes P., Jenkinson D. An extraction method for measuring soil microbial biomass C//Soil Biol Biochemistry. 1987. Vol. 19. P. 703-707
- DOI: 10.1016/0038-0717(87)90052-6
- Yin Y., Impellitteri C.A., You S.J., Allen H.E. The importance of organic matter distribution and extract soil: solution ratio on the desorption of heavy metals from soils//Science of the Total Environment. 2002. Vol. 287 (1-2). P. 107-119
- DOI: 10.1016/S0048-9697(01)0100


