Влияние химической структуры фосфоновых кислот, меченных 188Re, на их поведение в организме лабораторных животных
Автор: Тищенко В.К., Петриев В.М., Сморызанова О.А., Михайловская А.А.
Рубрика: Научные статьи
Статья в выпуске: 1 т.26, 2017 года.
Бесплатный доступ
Данная работа посвящена изучению влияния химической структуры ряда фосфоновых кислот, меченных 188Re, на их фармакокинетические свойства в организме интактных крыс после внутривенного введения. Были исследованы свойства кислот с двумя фосфоновыми группами - 1-гидроксиэтилиден-1,1-дифосфоновая кислота (ОЭДФ), четырьмя фосфоновыми группами - N,N,N’,N’-этилендиаминтетракис(метиленфосфоновая кислота) (ЭДТМФ) и окса-бис(этиленнитрило)тетра(метиленфосфоновая кислота) (ОЭНТМФ), пятью фосфоновыми группами диэтилентриаминопентакис(метилфосфоновая кислота) (ПФК). Эффективность связывания 188Re с фосфоновыми кислотами составляет не менее 95%. Радиохимические примеси в растворе меченого препарата не превышают 5,0%. Все исследуемые соединения обладают высокой стабильностью in vivo и селективно накапливаются в костной ткани. Показано, что химическая структура фосфоновых кислот влияет на накопление меченых соединений в костной ткани. По уровню накопления активности в скелете препараты можно расположить в следующем порядке (в порядке убывания): 188Re-ПФК > 188Re-ОЭДФ > 188Re-ЭДТМФ > 188Re-ОЭНТМФ. Все препараты характеризуются быстрым выведением из крови и минимальным накоплением во внутренних органах и тканях. Выведение радиоактивности из организма происходит через мочевыводящие пути. В других органах и тканях - в лёгких, печени, селезёнке и мышечной ткани - максимальные значения активностей отмечаются сразу после введения препаратов, однако уже через 1 ч значительная часть активности выводится.
Фосфоновая кислота, фармакокинетика, радионуклидная терапия, 1-гидроксиэтилиден-1, 1-дифосфоновая кислота, n'-этилендиаминтетракис (метиленфосфоновая кислота), диэтилентриаминопентакис(метилфосфоновая кислота), окса-бис(этиленнитрило)тетра(метиленфосфоновая кислота), коэффициент дифференциального накопления, остеотропные препараты
Короткий адрес: https://sciup.org/170170286
IDR: 170170286 | DOI: 10.21870/0131-3878-2017-26-1-78-88
Effect of chemical structure of some phosphonic acids labeled with 188Re on their behavior in laboratory animals
The article considers effects of chemical structure of some phosphonic acids labeled with 188Re on their pharmacokinetic behavior in organisms of intact rats following intravenous injection. The properties of acids with two phoshonic groups - 1-hydroxyethylidene-1,1-diphosphonic acid (HEDP), four phosphonic groups - N,N,N’,N’-ethylenediaminetetrakis(methylenephosphonic acid) (EDTMP) and oxa-bis(ethylenenitrilo)tetra(methylenephosphonic acid) (OENTMP), five phosphonic groups diethylenetriaminopentakis(methylphosphonic acid) (PPA) were studied. Radiochemical yield of phosphonic acids labeled with 188Re, is not less than 95%, the radiochemical impurities do not exceed 5.0%. All compounds have high stability in vivo and selectively accumulate in osseous tissue. Accumulation of the above labeled compounds in osseous tissue depends on chemical structures of phosphonic acids. The level of accumulated radioactivity in skeleton following administration of the radiopharmaceticals can be arranged in the following descending order: 188Re-PPA > 188Re-HEDP > 188Re-EDTMP > 188Re-OENTMP. All compounds are rapidly excreted from blood with minimal accumulation in soft organs and tissues. The excretion of radioactivity from the bodies is occurred through the urinary routes. In other organs and tissues - the lungs, liver, spleen and muscle tissue - the maximum values of radioactivity detected immediately after injection of the preparations, however after 1 h a significant part of the activity is eliminated from these tissues.
Текст научной статьи Влияние химической структуры фосфоновых кислот, меченных 188Re, на их поведение в организме лабораторных животных
Одним из эффективных методов лечения костных метастазов является системная радионуклидная терапия. Наиболее перспективными для этой цели являются фосфоновые кислоты – идеальные соединения для доставки радиоактивных изотопов в костную ткань. Они характеризуются наличием Р–С–Р-связи, обеспечивающей биохимическую резистентность фосфонатов и их связывание с гидроксиапатитом костной ткани. Кроме того, фосфоновые кислоты оказывают прямое антирезорбтивное действие на костную ткань за счёт ингибирования остеокластов [1]. Химическая структура этих кислот характеризуется разным содержанием фосфоновых групп в составе молекулы (от одной до шести групп), а также фосфоновые кислоты бывают азотсодержащими и не содержащими азот.
Наиболее эффективными считаются азотсодержащие фосфонаты, механизм действия которых заключается в ингибировании фарнезилпирофосфатсинтазы – ключевого фермента, необходимого для посттрансляционной модификации внутриклеточных сигнальных белков остеокластов [1, 2]. Помимо антиостеолитического действия, фосфонаты могут подавлять проли-
Тищенко В.К. – с.н.с., к.б.н.; Петриев В.М.* – в.н.с., д.б.н., проф. НИЯУ МИФИ; Сморызанова О.А. – с.н.с., к.б.н.; Михайловская А.А. – с.н.с., к.б.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИРЦ» Минздрава России.
ферацию опухолевых клеток рака предстательной железы, молочной железы, колоректального рака, множественной миеломы и др. [3-7].
Радионуклид 188Re считается перспективным для создания терапевтических радиофармпрепаратов (РФП). Период полураспада 188Re составляет 17 ч, энергия гамма-квантов – 0,155 (15,2%) МэВ, максимальная энергия бета-частиц – 2,12 МэВ. Генераторная система 188W/188Re позволяет продуцировать радионуклид 188Re в течение 4-6 месяцев [8], поэтому проводить метку препаратов 188Re можно непосредственно перед применением РФП в клинике. Терапевтический эффект 188Re обусловлен преимущественно β--излучением, а наличие в спектре излучения гамма-квантов позволяет контролировать распределение РФП в организме с помощью гамма-камеры.
Целью настоящего исследования является изучение влияния химической структуры фосфоновых кислот, меченных 188Re, на их фармакокинетические свойства в организме интактных крыс после внутривенного введения.
Материалы и методы
Для изучения влияния химической структуры производных фосфоновых кислот на их фармакокинетику в организме лабораторных животных были получены четыре препарата, содержащие от двух до пяти фосфоновых групп: 1-гидроксиэтилиден-1,1-дифосфоновая кислота (188Re-ОЭДФ), окса-бис(этиленнитрило)тетра(метиленфосфоновая кислота) (188Re-ОЭНТМФ), N,N,N’,N’-этилендиаминтетракис(метиленфосфоновая кислота) (188Re-ЭДТМФ) и диэтилен-триаминопентакис(метилфосфоновая кислота) (188Re-ПФК). В структуре ОЭДФ содержится две фосфоновые группы, ОЭНТМФ и ЭДТМФ – четыре фосфоновые группы, ПФК – пять фосфоновых групп.
Для получения меченых препаратов использовали монокалиевую соль ОЭДФ (фармакопейное наименование – ксидифон) – 20% раствор, ФС 42-3184-95 (производства ОАО «Мосхим-фармпрепараты» им. Н.А. Семашко), ОЭНТМФ была получена в АО «НИФХИ им. Л.Я. Карпова», ЭДТМФ – производства компании Sigma-Aldrich, ПФК – производства компании Fluka (Германия). 188Re получали в виде раствора Na188ReO 4 путём элюирования изотоническим раствором (0,9% раствор NaCl) с колонки генератора 188W/188Re производства АО «ГНЦ РФ – ФЭИ».
Метку препаратов проводили по методике, описанной в работах [9, 10]. Для этого использовали лиофилизаты, содержащие наборы реагентов, необходимые для образования комплексных соединений 188Re с производными фосфоновых кислот. Во флакон с набором реагентов вводили элюат 188Re в виде раствора перрената натрия (Na188ReO 4 ) в изотоническом растворе объёмом 2,0-4,0 мл c объёмной активностью, равной 3,7-7,4 МБк/мл (0,1-0,2 мКи/мл). Эффективность связывания 188Re с лигандами фосфоновых кислот и радиохимические примеси в препаратах определяли с помощью бумажной хроматографии на ватмане-1 производства компании Sigma (Англия). В качестве подвижной фазы использовали ацетон и смесь EtOH: 25% раствор аммиака: H 2 O в соотношении 2:5:5. Количественное определение меченого препарата и радиохимических примесей в виде 188ReO 4 - и 188ReO 2 проводили с помощью радиометрии полосок хроматографической бумаги. Эффективность связывания 188Re с лигандами фосфоновых кислот составляла не менее 95%. Радиохимические примеси в растворе меченого препарата не превышали 5,0%.
Исследования фармакокинетики РФП проводили на белых беспородных крысах-самцах весом 180±40 г. Всего было использовано 80 животных, которые были поделены на четыре группы (по 20 крыс в каждой). На животных первой, второй, третьей и четвёртой групп исследовали фармакокинетику 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК соответственно. Введение меченых препаратов осуществлялось внутривенно (в хвостовую вену) по 0,37 МБк (0,01 мКи) в объёме 0,1 мл. Количество вводимого РФП составляло 2,27-3,57 мг/кг массы животного. Через определённые интервалы времени (5 мин, 1, 3, 24 и 48 ч) по 4 животных в каждый срок забивали под наркозом декапитацией, выделяли пробы органов и тканей, помещали в пластиковые пробирки, взвешивали на электронных весах «Sartorius» (Германия) и проводили радиометрию с помощью автоматического гамма-счётчика «Wizard» версии 2480 фирмы «PerkinElmer/Wallac» (Финляндия). По данным радиометрии на каждый срок наблюдения для каждого препарата рассчитывали удельную активность на 1 г ткани в процентах от введённого количества. Результаты радиометрии обрабатывали методом оценки среднеквадратичной ошибки средней величины (M±m).
Кроме того, были рассчитаны коэффициенты дифференциального накопления (КДН) как частное от деления величин концентрации меченых препаратов в костной ткани и других органах и тканях.
Результаты и обсуждение
Сравнительные данные фармакокинетических свойств РФП 188Re-ПФК, 188Re-ОЭДФ, 188Re-ОЭНТМФ и 188Re-ЭДТМФ приведены в табл. 1, из которой видно, что для исследуемых препаратов характерна выраженная аккумуляция в костной ткани. Значительное содержание препаратов в скелете отмечается сразу же после их внутривенного введения (рис. 1-4). Через 1-3 ч концентрации РФП достигают максимальных значений, что характерно для многих меченых фосфонатов [11-14]. В более поздние сроки (24-48 ч) происходит постепенное выведение активности из костной ткани.
Таблица 1
Распределение 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ, 188Re-ПФК в организме интактных крыс после внутривенного введения препаратов (в % на 1 г ткани)
|
№ |
Наименование |
Наименование |
Время после введения п |
репарата |
|||
|
п/п |
органа, ткани |
препарата |
5 мин |
1 ч |
3 ч |
24 ч |
48 ч |
|
1 |
Кровь |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
1,10±0,24 0,83±0,12 1,46±0,11 2,05±0,57 |
0,36±0,04 0,24±0,03 0,35±0,03 0,46±0,01 |
0,21±0,02 0,10±0,01 0,27±0,03 0,32±0,03 |
0,08±0,01 0,04±0,01 0,074±0,002 0,10±0,01 |
0,033±0,007 0,054±0,014 0,027±0,004 0,033±0,006 |
|
2 |
Щитовидная железа |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,64±0,23 1,32±0,20 0,68±0,12 1,44±0,21 |
0,63±0,15 1,81±0,24 0,51±0,09 0,45±0,14 |
0,74±0,09 1,16±0,17 0,81±0,13 0,85±0,21 |
0,45±0,02 0,50±0,15 0,18±0,02 0,23±0,05 |
0,17±0,03 1,28±0,30 0,16±0,05 0,26±0,07 |
|
3 |
Лёгкие |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,62±0,12 0,49±0,08 0,83±0,11 1,22±0,19 |
0,22±0,02 0,15±0,01 0,55±0,06 0,34±0,01 |
0,12±0,01 0,07±0,01 0,23±0,07 0,20±0,01 |
0,065±0,009 0,028±0,005 0,027±0,003 0,066±0,004 |
0,038±0,002 0,015±0,003 0,063±0,007 0,032±0,002 |
|
4 |
Печень |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,27±0,05 0,25±0,02 0,66±0,11 0,41±0,08 |
0,20±0,03 0,09±0,01 0,52±0,06 0,19±0,03 |
0,14±0,01 0,05±0,01 0,28±0,07 0,19±0,02 |
0,092±0,008 0,026±0,002 0,210±0,020 0,060±0,004 |
0,073±0,007 0,024±0,004 0,092±0,006 0,036±0,003 |
|
5 |
Почки |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
2,67±0,77 1,12±0,19 5,79±1,17 4,11±1,43 |
4,19±0,18 1,79±0,06 2,10±0,20 4,78±0,51 |
3,55±0,42 1,48±0,07 5,69±0,42 3,59±0,19 |
1,64±0,06 0,84±0,20 1,16±0,02 1,32±0,09 |
0,94±0,12 0,68±0,04 0,66±0,08 0,86±0,03 |
Продолжение таблицы 1
|
№ п/п |
Наименование органа, ткани |
Наименование препарата |
Время после введения препарата |
||||
|
5 мин |
1 ч |
3 ч |
24 ч |
48 ч |
|||
|
6 |
Селезёнка |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,19±0,04 0,17±0,01 0,33±0,07 0,30±0,06 |
0,11±0,01 0,05±0,01 0,07±0,01 0,12±0,01 |
0,09±0,01 0,04±0,01 0,11±0,03 0,10±0,01 |
0,050±0,006 0,019±0,005 0,048±0,012 0,049±0,002 |
0,039±0,004 0,014±0,001 0,140±0,020 0,022±0,002 |
|
7 |
Желудок без содержимого |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,44±0,10 0,20±0,03 0,49±0,04 0,72±0,11 |
0,47±0,11 0,36±0,05 0,34±0,03 0,49±0,06 |
0,50±0,09 0,34±0,01 0,88±0,07 0,63±0,07 |
0,16±0,04 0,06±0,02 0,13±0,03 0,11±0,01 |
0,058±0,004 0,022±0,002 0,033±0,004 0,034±0,004 |
|
8 |
Мышца бедра |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,28±0,10 0,10±0,02 0,21±0,04 0,42±0,07 |
0,078±0,013 0,027±0,004 0,048±0,006 0,096±0,015 |
0,040±0,005 0,018±0,007 0,045±0,011 0,047±0,006 |
0,023±0,007 0,007±0,002 0,009±0,002 0,019±0,002 |
0,011±0,002 0,006±0,001 0,012±0,003 0,009±0,001 |
|
9 |
Кость бедра |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
1,01±0,27 0,34±0,02 1,38±0,11 1,79±0,19 |
2,29±0,16 1,17±0,07 1,59±0,07 3,31±0,21 |
2,05±0,37 0,96±0,14 1,44±0,20 2,60±0,31 |
1,59±0,20 0,71±0,09 0,95±0,03 1,64±0,12 |
1,01±0,11 0,56±0,08 0,56±0,10 0,86±0,05 |
|
10 |
Кость черепа |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,66±0,15 0,33±0,04 0,70±0,11 1,40±0,14 |
1,19±0,11 0,88±0,05 0,90±0,03 1,91±0,30 |
1,05±0,12 0,72±0,08 0,71±0,07 1,77±0,15 |
0,86±0,08 0,63±0,07 0,50±0,02 1,09±0,14 |
0,79±0,06 0,40±0,06 0,27±0,03 0,65±0,05 |
|
11 |
Кость ребра |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,63±0,11 0,29±0,02 0,62±0,04 1,28±0,26 |
1,32±0,19 0,89±0,07 0,73±0,04 3,07±0,42 |
1,31±0,16 0,68±0,08 0,62±0,06 2,69±0,48 |
1,50±0,20 0,51±0,07 0,44±0,04 1,71±0,18 |
1,33±0,24 0,34±0,01 0,24±0,04 1,46±0,18 |
|
12 |
Кость позвоночника с костным мозгом |
188Re-ОЭДФ 188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
1,01±0,24 0,32±0,01 1,03±0,08 1,39±0,11 |
1,13±0,12 0,76±0,05 1,04±0,08 1,62±0,22 |
0,92±0,06 0,81±0,10 0,83±0,08 1,41±0,11 |
0,58±0,05 0,58±0,06 0,56±0,04 0,93±0,05 |
0,46±0,01 0,42±0,05 0,33±0,07 0,48±0,01 |
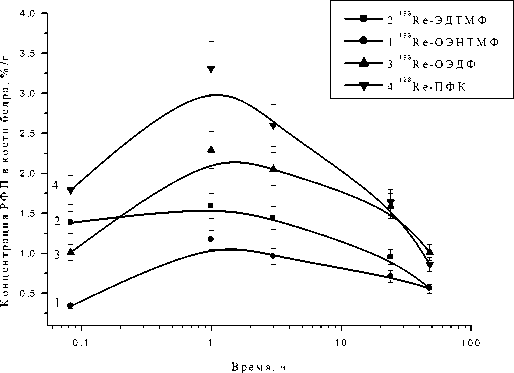
Рис. 1. Кинетика накопления и выведения 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК в костной ткани бедра интактных крыс.
Аналогичные тенденции в распределении активности отмечаются в костях черепа, рёбер и позвоночника (рис. 2-4). После введения препаратов их концентрация в костях постепенно увеличивается до максимальных значений через 1-3 ч. В дальнейшем концентрация всех РФП постепенно снижается, но, в связи с тем, что выведение активности из крови и других органов, тканей существенно интенсивнее, в костях этот показатель остаётся на относительно высоком уровне. Из исследованных четырёх препаратов наиболее высокая концентрация активности в костях характерна для 188Re-ПФК. Так, например, в костной ткани бедра и ребра его концентрация превышает 3%/г. Наиболее низкая концентрация активности отмечается в костях после внутривенного введения 188Re-ОЭНТМФ, которая не превышает 0,89%/г во все сроки исследования (рис. 2-4).
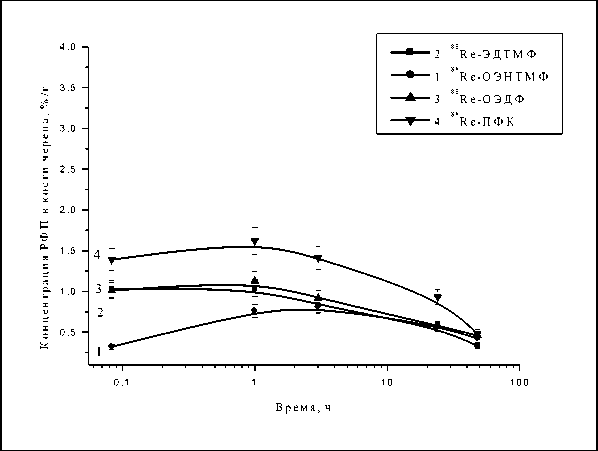
Рис. 2. Кинетика накопления и выведения 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК в костной ткани черепа интактных крыс.
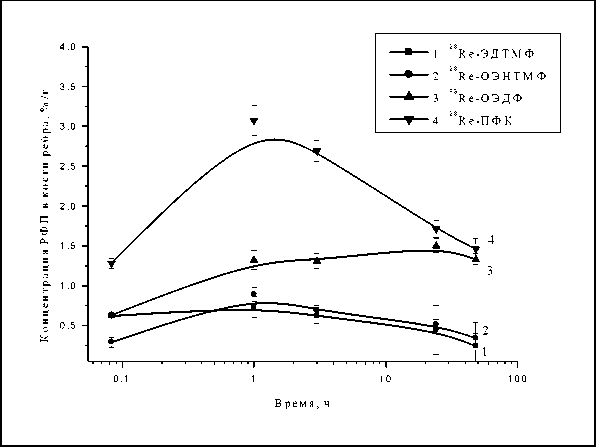
Рис. 3. Кинетика накопления и выведения 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК в костной ткани ребра интактных крыс.
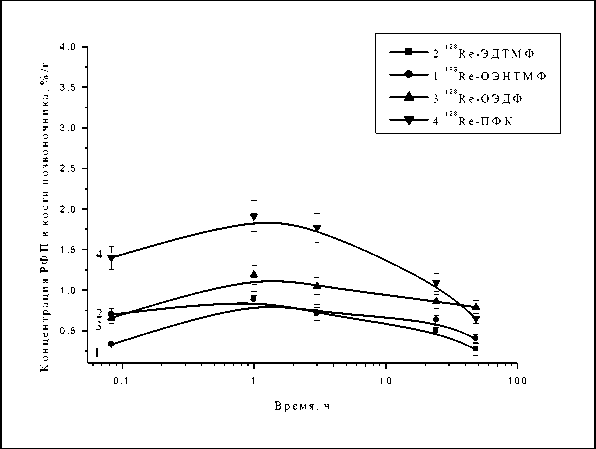
Рис. 4. Кинетика накопления и выведения 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК в костной ткани позвоночника интактных крыс.
Для более детальной оценки закономерностей накопления и выведения меченых препаратов из костной ткани по сравнению с окружающими мягкими тканями были рассчитаны величины отношения удельного содержания исследуемых РФП в костях к удельному содержанию его в крови и мышце (КДН) (табл. 2 и 3). Численные значения КДН для крови меньше единицы через 5 мин после инъекции препаратов, а в остальные сроки исследования эти величины больше единицы. Максимальные значения КДН отмечаются через 48 ч (табл. 2). Аналогичные показатели КДН для мышцы больше единицы во все сроки наблюдений (табл. 3). Это свидетельствует о более интенсивном выведении активности из крови и мышцы по сравнению с костной тканью. Следует отметить, что величины КДН по отношению к мышце существенно выше, чем по отношению к крови, т.е. накопление активности в мышечной ткани значительно ниже, чем в костной ткани и крови.
Таблица 2
Отношение удельного содержания 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ, 188Re-ПФК в костях к удельному содержанию в крови
|
№ п/п |
Наименование органа, ткани |
Наименование препарата |
Время после введения препарата |
||||
|
5 мин |
1 ч |
3 ч |
24 ч |
48 ч |
|||
|
1 |
Кость бедра/ |
188Re-ОЭДФ |
0,92±0,15 |
6,49±0,26 |
9,79±1,90 |
19,8±1,62 |
36,8±10,1 |
|
кровь |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,34±0,04 0,96±0,10 1,02±0,18 |
4,21±1,20 4,65±0,32 7,15±0,51 |
9,63±0,70 5,58±1,20 8,57±1,90 |
17,2±0,96 13,0±0,67 15,7±0,67 |
8,60±1,66 22,0±4,14 28,1±4,81 |
|
|
2 |
Кость черепа/ |
188Re-ОЭДФ |
0,61±0,07 |
3,37±0,29 |
5,00±0,40 |
11,1±1,62 |
29,1±7,66 |
|
кровь |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,31±0,02 0,48±0,07 0,81±0,15 |
3,18±0,89 2,63±0,17 4,15±0,68 |
7,33±0,62 2,66±0,23 5,58±0,46 |
15,4±1,10 6,86±0,35 10,6±1,62 |
6,70±2,17 11,0±2,82 20,9±3,07 |
|
|
3 |
Кость ребра/ |
188Re-ОЭДФ |
0,60±0,03 |
3,89±0,86 |
6,25±0,70 |
20,0±4,72 |
48,2±12,5 |
|
кровь |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
0,29±0,04 0,43±0,04 0,73±0,20 |
2,97±0,51 2,14±0,14 6,71±1,02 |
6,87±0,30 2,33±0,10 9,14±2,80 |
12,4±1,58 6,00±0,59 16,4±1,91 |
6,00±2,50 10,0±3,30 50,0±14,6 |
|
|
4 |
Кость |
188Re-ОЭДФ |
0,97±0,20 |
3,18±0,23 |
4,43±0,37 |
7,45±1,00 |
16,3±3,59 |
|
позвоночника/ |
188Re-ОЭНТМФ |
0,33±0,04 |
3,51±0,94 |
8,11±0,29 |
14,1±0,88 |
6,80±1,73 |
|
|
кровь |
188Re-ЭДТМФ 188Re-ПФК |
0,72±0,08 0,80±0,16 |
3,03±0,23 3,50±0,46 |
3,15±0,30 4,49±0,53 |
7,69±0,65 9,02±0,62 |
13,4±3,74 15,9±2,97 |
|
Таблица 3
Отношение удельного содержания 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ, 188Re-ПФК в костях к удельному содержанию в мышце
|
№ п/п |
Наименование органа, ткани |
Наименование препарата |
Время после введения препарата |
||||
|
5 мин |
1 ч |
3 ч |
24 ч |
48 ч |
|||
|
1 |
Кость бедра/ |
188Re-ОЭДФ |
4,28±1,04 |
31,1±3,26 |
57,3±16,9 |
78,70±9,50 |
100,8±23,5 |
|
мышца |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
2,60±0,38 8,30±1,15 4,49±0,44 |
36,1±9,10 34,6±3,70 38,3±8,25 |
66,7±16,8 38,5±10,3 58,6±11,0 |
168,9±63,8 127,7±33,6 86,8±7,80 |
69,7±18,8 54,7±8,03 97,2±14,08 |
|
|
2 |
Кость черепа/ |
188Re-ОЭДФ |
2,83±0,54 |
16,1±2,02 |
28,0±4,62 |
44,8±8,18 |
76,3±11,6 |
|
мышца |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
2,30±0,29 3,70±0,81 3,55±0,42 |
27,2±6,70 19,6±2,30 20,6±2,45 |
52,2±14,4 18,2±3,50 39,4±6,00 |
143,6±51,8 67,8±18,5 57,2±7,89 |
52,7±14,4 26,9±7,50 73,4±11,5 |
|
|
3 |
Кость ребра/ |
188Re-ОЭДФ |
3,00±0,78 |
18,0±4,89 |
35,6±7,53 |
80,5±18,8 |
131,0±32,0 |
|
мышца |
188Re-ОЭНТМФ 188Re-ЭДТМФ 188Re-ПФК |
2,20±0,40 3,30±0,60 3,10±0,52 |
25,6±3,90 16,1±2,40 32,6±2,18 |
47,9±11,7 15,6±2,40 60,3±14,0 |
110,8±34,7 58,5±14,7 94,6±20,3 |
41,3±0,90 24,4±7,20 161,3±19,8 |
|
|
4 |
Кость |
188Re-ОЭДФ |
4,72±1,69 |
15,1±1,63 |
25,0±4,70 |
30,0±5,17 |
44,4±5,90 |
|
позвоночника/ |
188Re-ОЭНТМФ |
2,50±0,35 |
30,0±7,00 |
56,1±12,9 |
145,4±62,0 |
53,2±11,7 |
|
|
мышца |
188Re-ЭДТМФ 188Re-ПФК |
6,30±1,40 3,58±0,56 |
22,3±1,40 19,8±5,99 |
21,6±4,38 31,0±3,67 |
77,5±23,7 50,0±5,83 |
34,8±12,3 54,7±8,62 |
|
Динамика выведения 188Re-ОЭДФ, 188Re-ОЭНТМФ, 188Re-ЭДТМФ и 188Re-ПФК из крови характеризуется интенсивным снижением активности в течение 48 ч (табл. 1). Через 5 мин после инъекции в крови отмечалось 0,83-2,05%/г от введённой активности. Через 1 ч в кровотоке сохранялось 0,24-0,46%/г от введённой активности, снижаясь до 0,027-0,054%/г через 48 ч (табл. 1).
Выведение активности происходит через мочевыделительную систему, обеспечивая, тем самым, высокое содержание РФП в почках [13-15]. 188Re-ЭДТМФ характеризуется наибольшим уровнем активности в почках: его содержание варьирует в диапазоне от 0,66 до 5,79%/г. Активность 188Re-ПФК в почках изменяется от 0,86 до 4,78%/г, 188Re-ОЭДФ – от 0,94 до 4,19%/г. Самый низкий уровень накопления активности в почках характерен для 188Re-ОЭНТМФ: от 0,68 до 1,79%/г.
Внутривенное введение РФП не приводило к значительному накоплению активности в других внутренних органах и тканях. В лёгких, печени, селезёнке и мышечной ткани максимальные значения активностей отмечаются сразу после введения препаратов, однако, уже через 1 ч значительная часть активности выводится (табл. 1). В дальнейшем концентрация препаратов в этих органах и тканях продолжает снижаться.
Заключение
Таким образом, все исследуемые РФП сразу же после их внутривенного введения в значительных количествах накапливаются в костной ткани и удерживаются в ней в течение 48 часов, однако максимальные значения активностей отмечаются через 1-3 ч. При этом содержание РФП в костной ткани неодинаково: наибольший уровень активности характерен для 188Re-ПФК, а наименьший – для 188Re-ОЭНТМФ, что свидетельствует о влиянии химической структуры фосфоновой кислоты на накопление активности в скелете. В остальных органах и тканях фармакокинетические свойства РФП практически одинаковы. Все препараты характеризуются быстрым выведением из крови и минимальным накоплением во внутренних органах и тканях, а также высокой стабильностью in vivo , оцениваемой по содержанию в щитовидной железе. Элиминация активности из организма осуществляется преимущественно выделительной системой почек.
Список литературы Влияние химической структуры фосфоновых кислот, меченных 188Re, на их поведение в организме лабораторных животных
- Russell R.G. Bisphosphonates: the first 40 years//Bone. 2011. V. 49, N 1. P. 2-19.
- Ebetino F.H., Hogan A.M., Sun S., Tsoumpra M.K., Duan X., Triffitt J.T., Kwaasi A.A., Dunford J.E., Barnett B.L., Oppermann U., Lundy M.W., Boyde A., Kashemirov B.A., McKenna C.E., Russell R.G. The relationship between the chemistry and biological activity of the bisphosphonates//Bone. 2011. V. 49, N 1. P. 20-33.
- Mani J., Vallo S., Barth K., Makarević J., Juengel E., Bartsch G., Wiesner C., Haferkamp A., Blaheta R.A. Zoledronic acid influences growth, migration and invasive activity of prostate cancer cells in vitro//Prostate Cancer Prostatic Dis. 2012. V. 15, N 3. P. 250-255.
- Iguchi K., Tatsuda Y., Usui S. Hirano K. Pamidronate inhibits antiapoptotic bcl-2 expression through inhibition of the mevalonate pathway in prostate cancer PC-3 cells//Eur. J. Pharmacol. 2010. V. 641, N 1. P. 35-40.
- Dedes P.G., Gialeli C., Tsonis A.I., Kanakis I., Theocharis A.D., Kletsas D., Tzanakakis G.N., Karamanos N.K. Expression of matrix macromolecules and functional properties of breast cancer cells are modulated by the bisphosphonate zoledronic acid//Biochim. Biophys. Acta. 2012. V. 1820, N 12. P. 1926-1939.
- Notarnicola M., Messa C., Cavallini A., Bifulco M., Tecce M.F., Eletto D., Di Leo A., Montemurro S., Laezza C., Caruso M.G. Higher farnesyl diphosphate synthase activity in human colorectal cancer inhibition of cellular apoptosis//Oncology. 2004. V. 67, N 5-6. P. 351-358.
- Morgan G.J., Davies F.E., Gregory W.M., Szubert A.J., Bell S.E., Drayson M.T., Owen R.G., Ashcrott A.J., Jackson G.H., Child J.A. National Cancer Research Institute Haematological Oncology Clinical Studies Group. Effects of induction and maintenance plus long-term bisphosphonates on bone disease in patients with multiple myeloma: the Medical Research Council Myeloma IX Trial//Blood. 2012. V. 119, N 23. P. 5374-5383.
- Pillai M.R., Dash A., Knapp F.F. Jr. Rhenium-188: availability from the (188)W/(188)Re generator and status of current applications//Curr. Radiopharm. 2012. V. 5, N 3. P. 228-243.
- Petriev V.M., Afanasieva E.L., Skvortsov V.G., Baranov N.G. Influence of the rhenium carrier in eluate of Re-188 on its binding with potassium-sodium salt of hydroxyethilidene biphosphonic acid//Czech. J. Phys. 2006. V. 56, Suppl. D. Part II. P. D731-D741.
- Petriev V.M. Influence of reactant concentrations and solution acidity on the complexation of 188Re with 1-hydroxyethane-1,1-diphosphonic acid//Radiochemistry. 2008. V. 50, N 2. P. 203-207.
- Shiryaeva V.K., Petriev V.M., Bryukhanova A.A., Smoryzanova O.A., Skvortsov V.G. Comparative analysis of pharmacokinetic characteristics of radiopharmaceuticals based on the monopotassium salt of 1-hydroxyethylidenediphosphonic acid labeled by 99mTc and 188Re//Pharm. Chem. J. 2011. V. 45, N 6. P. 333-340.
- Shiryaeva V.K., Petriev V.M., Smoryzanova O.A., Skvortsov V.G. Pharmacokinetics of 188Re-labeled pentaphosphonic acid in rats with experimental bone callosity//Pharm. Chem. J. 2013. V. 47, N 5. P. 251-256.
- Ширяева В.К., Петриев В.М., Сморызанова О.А., Скворцов В.Г. Изучение фармакокинетических характеристик радиофармпрепарата на основе монокалиевой соли 1-гидроксиэтилиден-дифосфоновой кислоты, меченной 188Re, в организме крыс с рабдомиосаркомой М-1//Вопросы биологической, медицинской и фармацевтической химии. 2012. № 5. С. 36-43.
- Lin W., Lin C., Yeh S., Hsieh B., Tsai Z., Ting G., Yen T., Wang S., Knapp F.F., Stabin M. Rhenium-188 HEDP: a new generator-produced radiotherapeutic drug of potential value for treatment of bone metastases//Eur. J. Nucl. Med. 1997. V. 24, N 6. P. 590-595.
- Lungu V., Niculae D., Bouziotis P. Pirmettis I., Podina C. Radiolabeled phosphonates for bone metastases therapy//J. Radioanal. Nucl. Chem. 2007. V. 273, N 3. P. 663-667.


