Влияние хорионического гонадотропина на фагоцитарную и окислительную активность моноцитов и нейтрофилов
Автор: Ширшев С.В., Куклина Е.М., Гугович А.М.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 9, 2008 года.
Бесплатный доступ
В ходе исследования было выявлено влияние хорионического гонадотропина (ХГ) в дозах, сопоставимых с концентрацией гормона в крови на I и III триместрах беременности, на окислительную и фагоцитарную активность моноцитов и нейтрофилов женщин in vitro. Установлено, что гормон оказывает супрессивное действие на фагоцитарную активность моноцитов и нейтрофилов. Также гормон угнетает спонтанную окислительную активность нейтрофилов, однако ингибирующее действие гормона на моноциты проявляется только при стимулировании окислительной активности и только высокой дозой гормона. Таким образом, конечный результат воздействия ХГ зависит не только от дозы гормона, но и от активационного статуса исследуемых клеток.
Короткий адрес: https://sciup.org/147204444
IDR: 147204444 | УДК: 612.018:612.017.1:611.018.53
The effect of the chorionic gonadotrophin on phagocytic and oxidative activity of neutrophils and monocytes
In the course of experimental work we have investigated the effect of human chorionic gonadotrophin (hCG), coresponding to I and III pregnancy trimesters, on phagocytic and oxidative activity of neutrophils and monocytes. It was shown that hormone renders the supressive action in monocyte and neutrophil phagocytic activity. Also, the hormone supresses spontaneous oxidative activity of neutrophils, however only high dose of the hormone was shown supressive action on oxidative activity of zimozan-induced monocytes. Thus, was installed that the result of the action of hCG depends on hormonal dose and also on activation state of the cells.
Текст научной статьи Влияние хорионического гонадотропина на фагоцитарную и окислительную активность моноцитов и нейтрофилов
Беременность является иммунологическим феноменом, уникальность которого заключается не только в преодолении трансплантатом иммунных механизмов, но и в становлении новых эндокринных взаимодействий, обеспечивающих на качественно новом уровне нормальное сосуществование и развитие двух организмов (Ширшев, 2002). Геном развивающегося плода в организме матери наполовину заимствован у отца, однако при физиологически протекающей беременности отторжения генетически чужеродного трансплантата не происходит.
Изучение факторов и механизмов, ответственных за изменения, происходящие с организмом матери во время беременности, является актуальной проблемой репродуктивной иммунологии. Важнейшим направлением в рамках данной проблемы является анализ роли репродуктивных гормонов в регуляции процессов иммунитета при беременности.
Основным пептидным гормоном плаценты, проектирующим развитие беременности, является хорионический гонадотропин (ХГ). В крови беременных женщин ХГ обнаруживается сразу после имплантации плодного яйца и далее его уровень интенсивно нарастает, достигая максимума к 7–10-й неделям. Затем концентрация ХГ существенно снижается и держится на таком уровне последующие II–III триместры (Benveniste, Scommegha, 1981).
Показано, что ХГ имеет специфические рецепторы на различных типах иммунокомпетентных клеток и оказывает существенное влияние как на адаптивные, так и на неспецифические защитные реакции организма (Fuchs et al., 1981; Ricketts, Jones, 1985). В период беременности супрессия адаптивного иммунного ответа матери компенсируется активацией системы естественного иммунитета. Основными клетками, которые определяют функционирование данной системы, являются мо-ноциты/макрофаги и нейтрофилы.
Помимо этого, ХГ стимулирует секрецию прогестерона и эстрадиола и свои иммуномодулирующие эффекты реализует в комплексе с этими гормонами. В то же время направленность имму-норегуляторного действия ХГ зависит не только от уровня концентрации половых стероидов, но и от активационного статуса клетки-мишени (Ширшев, Кеворков, 1993).
В силу перечисленных особенностей ХГ является в настоящее время объектом пристального внимания как фактор, тормозящий процессы отторжения плода, и основной претендент на роль антифертильной вакцины.
Целью данного исследования являлось изучение влияния ХГ в дозах, сопоставимых с концентрацией гормона в I и III триместрах беременности, на фагоцитарную и окислительную активность моноцитов и нейтрофилов женщин в крови in vitro.
Материалы и методы исследования
В работе использовали фракционированные лейкоциты периферической крови (моноциты и нейтрофилы) небеременных женщин репродуктивного возраста.
В эксперименте использовали ХГ («Profasi», Италия) в физиологических концентрациях, соответствующих их уровню в периферической крови в I и III триместрах беременности – 100 и 10 МЕ/мл соответственно (Benveniste, Scommegha, 1981). Для стимуляции клеток применяли зимозан (0,5 мг/мл), опсонизированный пулом сывороток. Для проведения люминолзависимой хемилюминесценции (ЛЗХЛ) использовали люминол («Sigma», США) в концентрации 5×10-4М.
Мононуклеарные клетки периферической крови (МНК) и нейтрофилы выделяли из гепаринизированной (25 МЕ/мл) венозной крови центрифугированием в двойном градиенте плотности фиколл-верографина («Pharmacia», Швеция; «Спофа», Чехия) с плотностью верхнего и нижнего градиентов 1,077 и 1,112 г/мл соответственно. С верхней интерфазы собирали МНК, с нижней – нейтрофилы. Затем из МНК путем адгезии выделяли моноциты с двух пассажей на чашки Петри («anumbra», Куба). Чистота выделения для моноцитов составляла 78–85% (по оценке моноклональных антител к CD14 (ICN Ph, США)), для нейтрофилов – 95% (гистологическая оценка).
При культивировании клеток использовалась среда 199 (НПО «Биомед», Россия) с добавлением 5% эмбриональной телячьей сыворотки («Serva», Германия), 0,01М HEPES («Serva», Германия), 300 мкг/мл L-глутамина («Serva», Германия), 100 мкг/мл гентамицина («Pharmacia», Швеция). Клетки (5×106/мл) инкубировали с гормоном в течение 6 часов при 37°С и 5% СО 2 , после чего определяли их фагоцитарную и окислительную активность. Затем вносили стимулятор и также оценивали фагоцитарную (в течение 30 мин) и окислительную (в течение 50 мин) активность клеток. Контроль культуры клеток инкубировали с растворителем гормона (NaCl – 0,9%) при аналогичных условиях. Жизнеспособность клеток оценивалась с помощью 5% эозина, она составила 95–97%.
Фагоцитарная активность оценивалась по степени гашения биолюминесценции лиофилизиро- ванной культуры люминесцентных бактерий генно-инженерного штамма E.coli Lum+ со спонтанным свечением (Патент 2292553 от 27.01.2007). Одну ампулу препарата разводили в 1 мл холодной дистиллированной воды, выдерживали 1 час при 4°С, 30 мин при комнатной температуре, затем еще 30 мин при 37°С и центрифугировали 10 мин (3000 об/мин), после чего доводили физиологическим раствором до 50 мл, получая рабочую концентрацию бактерий 5×106 /мл.
Готовую суспензию бактерий (180 мкл) вносили в лунки 96-луночного планшета, инкубировали в течение 3–5 мин при 37°С и снимали фоновый уровень свечения бактерии, затем, после внесения клеточной культуры в соотношении 1:10, измерялась степень гашения биолюминесценции в течении 30 мин с интервалом в 10 мин., при этом происходило полное поглощение E. coli Lum+ фагоцитирующими клетками. Измерение производилось на люминоскане «Аscent» (Финляндия) в относительных единицах свечения (RLU). Далее рассчитывался индекс фагоцитарной активности клеток (ИФА), отражающий процент гашения биолюминесценции по сравнению с исходным уровнем, по
Х 1 – Х 2
ИФА = -------х 100,
Х1 формуле где Х1 – интенсивность биолюминесценции контрольной пробы;
Х 2 – интенсивность биолюминесценции опытной пробы.
Окислительную активность оценивали по интенсивности ЛЗХЛ клеточной культуры (Dahigren, Sten-dahl, 1984). Для этого в планшет вносили 180 мкл раствора Хенкса без фенолового красного («Биолот», Россия), содержащего люминол (5×10-4М). После инкубации в течение 3-5 мин при 37 ° С и замера фонового свечения добавляли 20 мкл клеточной суспензии (5×106 /мл) и при непрерывном перемешивании измеряли интенсивность спонтанной хемилюминесценции для оценки исходного уровня окислительного метаболизма клеток. Затем в кювету вносили 20 мкл зимозана (0,5 мг/мл), опсонизированного пулом сывороток, и фиксировали интенсивность стимулированной хемилюминесценции в течение 50 мин с интервалом в 10 мин. Измерения производились также на люминоскане «Аscent» (Финляндия) в относительных единицах свечения (RLU).
При статистической обработке результатов вычислялись средняя арифметическая величина и ее стандартная ошибка. Достоверность различий между средними величинами оценивалась с помощью парного t -критерия Стьюдента, достоверными считались данные при р < 0,05.
Результаты исследований и их обсуждение
На первом этапе исследований оценивалась способность ХГ влиять на фагоцитарную активность нейтрофилов и моноцитов по степени гашения биолюминесценции.
Установлено, что низкая доза гормона, соответствующая ей в крови в III триместре беременности, оказывает статистически значимое угнетающее действие на нейтрофилы на 10 мин инкубации. Высокая же доза ХГ, характерная для крови в I триместре беременности, ингибирует фагоцитарную активность нейтрофилов как на 10, так и на 20 мин инкубации, что говорит о более эффективном действии высокой дозы гормона на нейтрофилы (рис. 1).
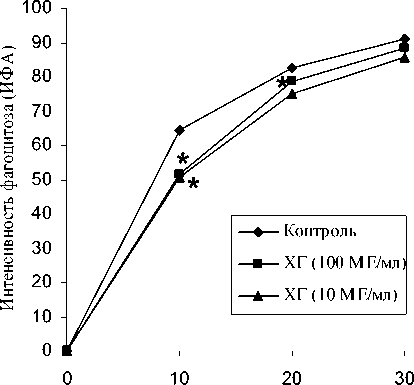
Инкубация с E. coli Lum+, мин.
Рис. 1. Изменение индекса фагоцитарной активности нейтрофилов
Примечание: здесь и далее * – р < 0,05 в сопоставлении с контролем
При расчете ИФА для моноцитов были получены статистически значимые данные (рис. 2), причем угнетение низкой дозой ХГ, характерной для крови в III триместре беременности, наблюдалось как на 10, так и на 20 мин инкубации, а ингибирование ХГ-100 МЕ/мл на 10, 20 и 30 мин инкубации моноцитов с E. coli Lum+.
Таким образом установлено, что ХГ в дозах, характерных для крови в I и III триместрах беременности, угнетает фагоцитарную активность нейтрофилов и моноцитов. Учитывая, что угнетение фагоцитарной активности нейтрофилов происходит только высокой дозой ХГ, можно предположить, что нейтрофилы менее чувствительны к действию гормона.
На втором этапе исследования изучалось влияние ХГ на спонтанную и зимозанстимулирован-ную ЛЗХЛ нейтрофилов и моноцитов. Для оценки исходного уровня окислительного метаболизма клеток исследовалась спонтанная ЛЗХЛ.
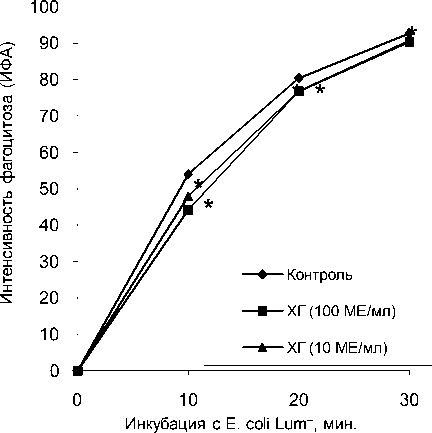
Рис. 2. Изменение индекса фагоцитарной активности моноцитов
Установлено, что ХГ как в низкой дозе, соответствующей ему в крови в III триместре беременности, так и в высокой дозе оказывает статистически значимое угнетающее действие на спонтанную ЛЗХЛ нейтрофилов (рис. 3).
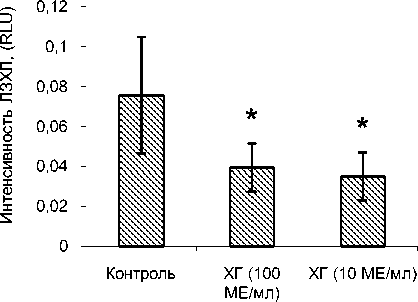
Экспериментальное воздействие
Рис. 3. Влияние ХГ на спонтанную ЛЗХЛ нейтрофилов
В то же время при оценке зимозанстимулиро-ванной ЛЗХЛ нейтрофилов гормон статистически достоверного влияния не оказывал (рис. 4).
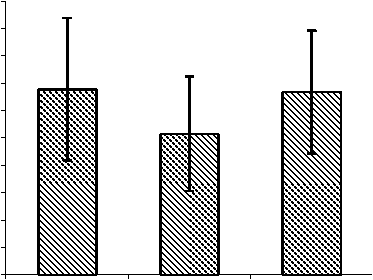
Аналогично исследовались и моноциты, однако был получен противоположный результат. При оценке влияния ХГ на спонтанную ЛЗХЛ моноцитов статистически значимых данных получено не было (рис. 5).
Но при внесении в суспензию, обогащенную моноцитами опсонизированного зимозана, интенсивность ЛЗХЛ достоверно угнеталась высокой дозой ХГ, соответствующей его содержанию в I триместре беременности, на всем протяжении эксперимента (рис. 6).
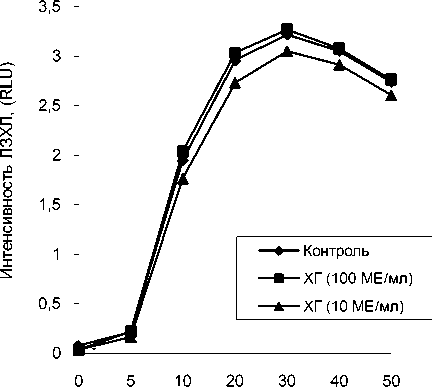
Продолжительность стимуляции, мин
Рис. 4. Влияние ХГ на динамику зимозанстимули-рованной ЛЗХЛ нейтрофилов
Таким образом, ХГ дифференцированно влияет на ЛЗХЛ нейтрофилов и моноцитов, угнетая спонтанную окислительную активность нейтрофилов, не влияя на стимулированную, а также оказывая ингибирующее действие на стимулированную ЛЗХЛ моноцитов.
0,02 s 0,018 £ 0,016 X 0,014 CO R 0,012 о 0,01
0,008 £ 0,006 = 0,004
0,002 0
Контроль ХГ (100 МЕ/мл) ХГ (10 МЕ/мл)
Экспериментальное воздействие
Рис. 5. Влияние ХГ на спонтанную ЛЗХЛ моноцитов
Представленные данные говорят об эффективном регуляторном действии ХГ на функции нейтрофилов и моноцитов периферической крови. Как правило, ХГ оказывает ингибирующее действие на процессы фагоцитоза и окислительной активности, что, по-видимому, способствует полноценному развитию физиологической беременности. Кроме того, установлено, что гормональная стимуляция окислительного метаболизма как нейтрофилов, так и моноцитов зависит от активационного статуса клетки. Литературные данные по регуляции окислительной активности нейтрофилов в крови во время беременности весьма противоречивы. С од- ной стороны, показано, что в этот период окислительный потенциал клеток повышен, причем данный эффект наблюдается только в III триместре (Selvaraj et al., 1982). С другой стороны, имеются работы, в которых отмечается его снижение (Krause et al., 1987; Crouch et al., 1995), наиболее выраженное также в III триместре (Crouch et al., 1995). Вероятно, такие противоречия можно объяснить разными методическими подходами к оценке окислительной активности клеток.
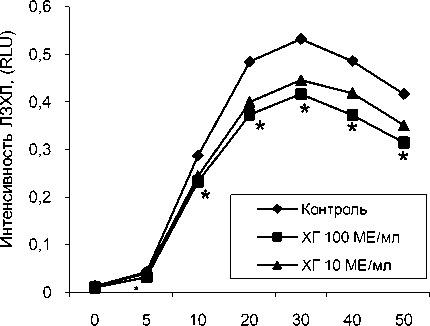
Продолжительность стимуляции, мин
Рис. 6. Влияние ХГ на динамику зимозанстимули-рованной ЛЗХЛ моноцитов
Таким образом, влияние ХГ на нейтрофилы и моноциты зависит от срока гестации. Так, в I триместре гормон угнетает фагоцитарную активность нейтрофилов и моноцитов и спонтанную окислительную активность нейтрофилов. В III триместре ХГ также оказывает угнетающее действие на фагоцитарную и окислительную активность данных клеток, что, по-видимому, способствует благополучному исходу беременности.
Список литературы Влияние хорионического гонадотропина на фагоцитарную и окислительную активность моноцитов и нейтрофилов
- Ширшев, С.В. Механизмы иммунноэндокринного контроля процессов репродукции: в 2 т./С.В. Ширшев. Екатеринбург: УрО РАН, 2002.
- Ширшев, С.В. Зависимость иммуномодулирующих эффектов хорионического гонадотропина от исходной функциональной активности спленоцитов, реализующих адаптивный иммунный ответ/С.В. Ширшев и Н.Н. Кеворков//Пробл. эндокринологии. 1993. Т. 39, № 1. С. 54-57.
- Пат. 2292553 Российская Федерация, МПК 7 G01N33/53. Способ определения фагоцитарной активности нейтрофилов периферической крови человека по степени гашения биолюминесценции./Ширшев С.В., Куклина Е.М., Заморина С.А., Никитина Н.М., Некрасова И.В. -заявитель и патентообладатель Ин-т экологии и генетики микроорганизмов УрО РАН (RU), Ширшев С.В. (RU) -№ 2005118124/15; заявл. 10.06.05; опубл. 27.01.07, Бюл. № 3.
- Benveniste, R. Human chorionic gonadotropin alphasubunit in pregnancy/R. Benveniste, A. Scommegha//Amer. J. Obstet. Gynecol. 1981. Vol. 141. P. 952-961.
- Crouch, S.P.M. The effect of pregnancy on polymorphonuclear leukocyte function/S.P.M. Crouch, I.P. Crocker, J. Fletcher//J. Immunol. 1995. Vol. 155. P. 5436-5443.
- Dahigren, C. Myeloperoxidase modulates the phagocytic activity of polymorphonuclear neutrophil leukocytes. Studies with cells from a myeloperoxidase deficient patient/C. Dahigren, O. Stendahl//J. Clin. Invest. 1984. Vol. 73. P. 366-373.
- Fuchs, T. In vitro induction of human suppressor Tcells by chorionic gonadotropin preparation/T. Fuchs, L. Hammarstrom, C.I. E. Smith, J. Brundin//J. Reprod. Immunol. 1981. Vol. 3. P. 75-84.
- Krause, P.J. Host defense during pregnancy: neutrophil chemotaxis and adherence/P.J. Krause, C.J. Ingardia, L.T. Pontius [et al.]//Acad. J. Obstet. Gynecol. 1987. Vol. 157. P. 274-281.
- Ricketts, R.M. Differential effect of human chorionic gonadotropin on lymphocyte proliferation induced by mitogens/R.M. Ricketts, D.B. Jones//J. Reprod. Immunol. 1985. Vol. 7. P. 225-232.
- Selvaraj, S.K. Mechanism of monocyte activation and expression of proinflammatory cytochemokines by placenta growth factor./S.K. Selvaraj, R.K. Giri, N.E. Perlman [et al.]//Endocrinol. 1982. Vol. 108. P. 1515.


