Влияние электроактивированных водных растворов на морфофункциональные показатели поджелудочной железы и почек крыс с экспериментальной моделью сахарного диабета
Автор: Гайдарова Анна Павловна, Хорина Юлия Александровна, Корощенко Галина Анатольевна, Серкина Оксана Александровна, Хачатрян Ашот Папикович, Ларионов Петр Михайлович, Айзман Роман Иделевич
Журнал: Science for Education Today @sciforedu
Рубрика: Биологические, химические, медицинские науки
Статья в выпуске: 4 (8), 2012 года.
Бесплатный доступ
В статье анализируется влияние электроактивированных водных растворов на морфофункциональные показатели поджелудочной железы и почек крыс с экспериментальной моделью сахарного диабета. Отмечается положительное влияние анолита на концентрацию глюкозы в плазме, морфофункциональные показатели поджелудочной железы и почек крыс с исследуемой патологией. Подчеркивается необходимость дальнейшего исследования биохимических процессов, определяющих гипогликемический эффект анолита.
Электроактивация, католит, анолит, водно-солевой обмен, сахарный диабет, почка, поджелудочная железа, крыса
Короткий адрес: https://sciup.org/147137409
IDR: 147137409 | УДК: 591.133
Effect of electroactivated water solutions on morphological and functional parameters of rats's pancreas and kidneys with experimental model of diabetes mellitus
The article devoted to study of electroactivated water solutions on morphological and functional parameters of pancreas and kidneys of rats with experimental diabetes mellitus model. It has been found a positive effect of anolyte on the concentration of glucose in plasma and morphological and functional parameters of pancreas and kidneys in rats with this pathology. There was indicated the necessity for further research on the biochemical processes that defined anolyte protective and hypoglycemic effects.
Текст научной статьи Влияние электроактивированных водных растворов на морфофункциональные показатели поджелудочной железы и почек крыс с экспериментальной моделью сахарного диабета
Электроактивация – сравнительно новая отрасль в медицине, открывающая широкие возможности применения водных растворов, обработанных электрическим током, в качестве лекарственных средств в эксперименте и в клинике [1, с. 88–91; 3, с. 54;
4, с. 26; 6, с. 23–25]. Электрохимически активные водные растворы (ЭВР) образуются при определенном режиме электрического воздействия в анодной или катодной камерах диафрагменных электротехнических установок [2, с. 36–107].
Серкина Оксана Александровна – старший лаборант кафедры анатомии, физиологии и безопасности жизнедеятельности ИЕСЭН, Новосибирский государственный педагогический университет.
Хачатрян Ашот Папикович – доктор медицинских наук, профессор кафедры анатомии, физиологии и безопасности жизнедеятельности ИЕСЭН, Новосибирский государственный педагогический университет Ларионов Петр Михайлович – доктор медицинских наук, профессор кафедры фундаментальной медицины, Новосибирский государственный университет.
Все права защищены

4(8) 2012 ISSN 2226-3365
При пропускании электрического постоянного тока через водный раствор в нем происходит электроактивация молекул, атомов, ионов и перераспределение ионов в электрическом поле [5, с. 93]. В результате вода, находящаяся в катодной зоне (ЭВР-К), приобретает восстановительные свойства и запасает потенциальную энергию. Католит обладает высокой биологической активностью, поскольку повышает интенсивность биохимических процессов, постоянно протекающих в живой клетке. Он обладает противовоспалительными и общетонизирующими свойствами, нормализует энергетический потенциал клеток и повышает интенсивность и эффективность тканевого дыхания. Анолит (ЭВР-А) обладает анальгезирующим, антиаллергическим, противовоспалительными свойствами, а также мощным антисептическим действием (противогрибковым, антивирусным и антибактериальным), что объясняется высокими окислительными свойствами раствора и содержанием химических соединений, выделяющих хлор, кислород и озон [2, с. 36–107; 3, с. 54; 4, с. 26; 6, с. 23–25].
В этой связи представлялось интересным изучить механизм влияния вышеперечисленных электрохимически активных водных растворов на организм при развитии сахарного диабета, как одной из наиболее распространенных и социально значимых патологий человека.
Методика . С этой целью был проведен эксперимент на взрослых крысах линии Wistar массой 200–250 г. Все животные были поделены на 2 группы – контрольную и экспериментальную, каждая из которых, в свою очередь, была разделена на три подгруппы: животные, получающие воду, раствор католита (ЭВР-К) или анолита (ЭВР-А) (рис.1).
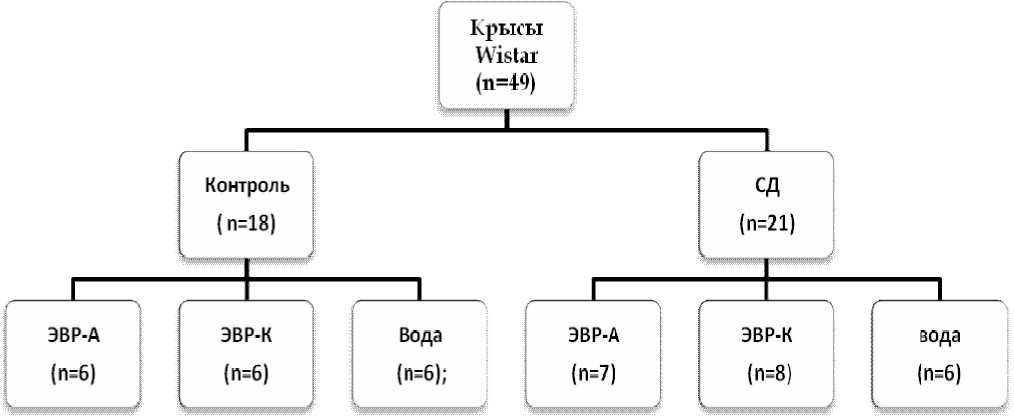
Рис. 1.
Распределение животных по группам наблюдения.
Для моделирования сахарного диабета животным подкожно вводили 10 % раствор аллоксана из расчета 0,1мл/100г массы тела.
На 1, 3 и 6 сутки эксперимента у животных
Все права защищены

4(8) 2012
ISSN 2226-3365
брали пробы крови путем надсечки хвоста для определения уровня глюкозы. На 6 сутки животных высаживали в обменные клетки для сбора мочи. В конце эксперимента у всех животных из нижней полой вены брали пробы крови для последующего определения ионноосмотических показателей, а также образцы тканей поджелудочной железы и почки.
Концентрацию глюкозы в плазме крови и моче определяли пикриновым методом на спектрофотоколориметре «Spekol» при длине волны 560 нм.
Концентрацию ионов натрия и калия в моче, плазме крови определяли методом пламенной фотометрии с использованием фотометра «BMW Technologies», производства США.
Для определения осмотической концентрации мочи и плазмы крови использовали метод криоскопии. Измерения выполняли на миллиосмометре «OSMOMAT», производство Германия в диапазоне от 300 до 2000 мосм/л.
Парциальные функции почек (табл.1) рассчитывали по общепринятым формулам [7, с. 293].
Для светооптического исследования образцы поджелудочной железы и почек фиксировали в 10 % растворе нейтрального формалина, обезвоживали в серии спиртов возрастающей концентрации и заключали в парафин. Срезы толщиной 5-6 микрон, окрашивали гематоксилином Майера, эозином, альциановым синим и заключали в канадский бальзам.
Таблица 1
Расчет парциальных функций почек
М- масса тела (г),
U cr и P cr – концентрация креатинина в моче и плазме (мг%);
U NA иP NA – концентрация натрия в моче и плазме (ммоль/л);
U K и P k – концентрация калия в моче и плазме (ммоль/л);
U osm и P osm – концентрация осмотически активных веществ в моче и плазме (мосмоль/л).

4(8) 2012
ISSN 2226-3365
Статистический анализ результатов исследования проводили на основе определения среднеарифметических (М) и их ошибок (±m). Различие показателей оценивали методами вариационной статистики по t-критерию Стьюдента и критерию ANOVA (для непараметрических данных) и считали достоверными при p≤0,05. Расчеты производили по общепринятым формулам с использованием стандартных программ пакета Microsoft Office (Statistica-6.0).
Все животные находились в стандартных условиях вивария при свободном доступе к воде или соответствующему раствору и пище.
Результаты. На первом этапе исследования был проведен анализ концентрации глюкозы в плазме крови крыс в динамике развития экспериментального сахарного диабета (табл.2).
Таблица 2
Концентрация глюкозы в плазме крови крыс (M±m), ммоль/л
|
Время эксперимента, сутки |
Контроль (интактные) |
СД |
||||
|
вода |
ЭВР-А |
ЭВР-К |
вода |
ЭВР-А |
ЭВР-К |
|
|
1 |
6,7±0,39 |
6,5±0,35 |
6,6±0,18 |
14,7±3,4* |
7,06±1,15 ▲ Δ |
23,06±4,03* |
|
3 |
18,1±4,0* |
9,3±1,4 ▲ Δ |
23,18±5,01* |
|||
|
6 |
16,1±5,3 |
11,2±3,2 |
12,05±2,8 |
|||
Примечание (здесь и далее):
* - достоверные отличия от аналогичных показателей контроля (р ≤0,05 ) ;
Δ – достоверные отличия между экспериментальными группами (католит, анолит) (р ≤0,05);
▲ - достоверные отличия по сравнению с группой «вода» (р ≤0,05 )
Из данных таблицы 2 видно, что у здоровых животных католит и анолит не вызывали изменения уровня глюкозы в крови на протяжении всего периода наблюдения. У животных экспериментальной группы уже на первые сутки после инъекции аллоксана уровень глюкозы был достоверно выше аналогичных показателей контроля, что свидетельствовало о развитии сахарного диабета. Только в группе «ЭВР-А» этот показатель был достоверно ниже показателей остальных групп и достоверно не отличался от контроля. Подобная ситуация сохранилась на 3 сутки эксперимента. На 6 сутки наблюдения уровень глюкозы у всех экспериментальных животных достоверно не различался между группами и был в 2 раза выше интактных животных.
Таким образом, можно заключить, что у здоровых животных электрохимически активные водные растворы не вызывали изменений уровня глюкозы в крови, тогда как на фоне сахарного диабета ЭВР-А оказывал выраженный гипогликемический эффект, вызывая задержку развития сахарного диабета, тогда как ЭВР-К не проявлял протективного сахаропонижающего эффекта.
При анализе ионно-осмотических показателей плазмы крови и мочи крыс было выявлено, что у интактных животных различные водные растворы не вызывали существенных изменений концентрации ионов и показателей функций почек, кроме
Все права защищены

4(8) 2012
ISSN 2226-3365
снижения мочевины в плазме крови после приема ЭВР-А. На фоне сахарного диабета концентрация натрия и калия не изменялись, а содержание мочевины имело тенденцию к повышению, и уровень креатинина был достоверно выше аналогичных показателей здоровых животных. Полученные изменения могут свидетельствовать о нарушении функционального состояния почек и развитии почечной недостаточности в условиях СД. При этом существенных отличий среди животных, принимавших разные электрохимически активированные водные растворы, не обнаружено, за исключением некоторого увеличения концентрации креатинина и гипокалиемии после приема ЭВР-К (табл. 3).
Таблица 3
Ионно-осмотические показатели плазмы крови крыс (M±m)
|
Концентрация, ммоль/л |
контроль |
СД |
||||
|
вода |
ЭВР-А |
ЭВР-К |
вода |
ЭВР-А |
ЭВР-К |
|
|
натрия |
139,4±13,5 |
138,3±12,1 |
129,7±13,0 |
148,0±23,7 |
124,0±8,6 |
131,0±34,1 |
|
калия |
4,1±0,2 |
3,9±0,2 |
4,0±0,3 |
3,8±0,2 |
3,6±0,3 |
3,0±0,3*▲ |
|
креатинина |
1,14±0,04 |
1,1±0,05 |
1,09±0,02 |
1,4±0,03* |
1,4±0,04* |
1,5±0,01*▲ Δ |
|
мочевины |
54,0±4,9 |
33,8±5,6▲ Δ |
49,8±4,8 |
60,0±7,7 |
64,8±7,2* |
63,6±8,7 |
Примечание: см. таблицу 2
Изучение гидро- и ионоуретической функций почек позволило выявить увеличение уровня диуреза на фоне сахарного диабета в группах животных, принимавших как анолит, так и католит (табл. 3). Скорость клубочковой фильтрации и уровень канальцевой реабсорбции не отличались между группами СД и контроля. Параллельно возрастала экскретируемая фракция калия, что, вероятнее всего, отражало увеличение секреции катиона. Указанные факты свидетельствуют в пользу усиления экскреции осмотически активных веществ (например, глюкозы) под влиянием ЭВР в условиях СД, в результате чего повышалась скорость мочеотделения и очищение калия.
Поскольку функциональные изменения органа обусловлены изменением его морфологической структуры, на следующем этапе нашего исследования был проведен анализ морфологической структуры поджелудочной железы и почек животных.
Таблица 4
Гидро- и ионоуретическая функции почек крыс (M±m)
|
Показатель |
контроль |
СД |
||||
|
вода |
ЭВР-А |
ЭВР-К |
вода |
ЭВР-А |
ЭВР-К |
|
|
V, мл/100г*час |
0,05±0,02 |
0,03±0,01 |
0,04±0,01 |
0,06±0,01 |
0,11±0,02*▲ |
0,11±0,03* |
|
СКФ, мл/100г*час |
13,7±3,4 |
20,6±2,12 |
12,2±2,5 Δ |
10,4±2,0 |
15,2±3,7 |
12,2±4,9 |
Все права защищены

4(8) 2012
ISSN 2226-3365
|
R H 2 O, % |
99,6±0,1 |
99,7±0,03 |
99,6±0,09 |
99,6±0,04 |
99,7±0,1 |
99,0±0,6 |
|
U Na *V, мкмоль/100г*ч ас |
4,0±1,5 |
13,7±0,6▲ Δ |
7,0±2,8 |
4,3±1,6 |
6,8±2,4* |
16,5±5,5 Δ |
|
U K *V, мкмоль/100г*ч ас |
15,6±6,4 |
12,0±1,5 |
8,9±3,1 |
17,1±8,6 |
16,6±1,07 |
17,1±6,7 |
|
EF Na , % |
0,2±0,1 |
0,4±0,05 |
0,4±0,2 |
0,3±0,09 |
0,3±0,10 |
2,11±0,97 |
|
EF K , % |
22,8±10,2 |
15,03±3,3 |
13,06±2,8 |
54,2±6,2 |
40,6±2,2* |
58,5±11,8* |
Примечание: см. таблицу 2
Анализ структурной организации поджелудочной железы крыс контрольной группы показал, что структура органа соответствует норме: клетки расположены довольно равномерно с хорошо контурируемыми ядрами.
Было установлено, что во всех экспериментальных группах по сравнению с контролем наблюдались некротические изменения, вызванные интоксикацией аллоксаном. При анализе структурной организации поджелудочной железы крыс после приема ЭВР-А обнаружена только кольцевидная трансформация ацинуса, гипертрофия островков Лангерганса, субнекроз. Иная картина наблюдалась в структурной организации поджелудочной железы крыс, употреблявших ЭВР-К при аллоксановой модели сахарного диабета. Наряду с кольцевидной трансформацией ацинуса, гипертрофией островков Лангерганса, субнекрозом, которые наблюдались в группе СД+ЭВР-А, отмечена также гипертрофия и гиперплазия островков Лангерганса, междольковый отек, очаговые некрозы ткани, псевдокистоз, а также соединительнотканное замещение ацинусов, элементы жировой атрофии, тяжелый протеолиз в сочетании с липолизом (рис.2). Таким образом, прием ЭВР-А на фоне СД способствовал минимальным структурным изменениям поджелудочной железы по сравнению с водой и ЭВР-К.
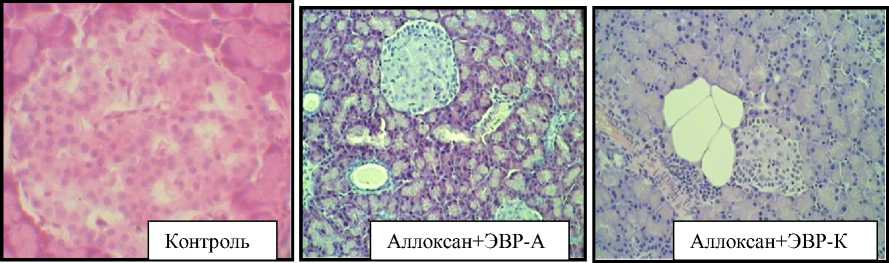
Рис. 2.
Морфологическая структура поджелудочной железы.
Все права защищены

4(8) 2012
ISSN 2226-3365
Почки практически всех животных контрольной группы имеют нормальную структурную организацию. Отчетливо обозначены корковое и мозговое вещество почечной паренхимы. Клубочки коры представлены капиллярными петлями, заключенными в эпителиальные капсулы со слегка различимыми просветами. Анализ структурной организации почек крыс с аллоксановой моделью сахарного диабета после приема ЭВР-А показал кистозную множественную трансформацию, гидрофическую дистрофию канальцев, выраженную полифибропластическую реакцию на уровне капилляров, канальцевые некрозы, начинающиеся фибропластические реакции.
В почках крыс после приема ЭВР-К обнаружен слабо выраженный кистоз, гидрофическая дистрофия, акцентированная на проксимальных канальцах, ячеистая структура на фоне тотальных некрозов, очаговый некроз с плазматическим пропитыванием интерстиция (рис. 3).
Следовательно, на фоне аллоксанового диабета в почках животных всех экспериментальных групп по сравнению со здоровыми животными обнаружены тяжелые последствия аллоксановой интоксикации. Регенерирующее действие ЭВР на почки в ходе эксперимента не установлено (рис.3).
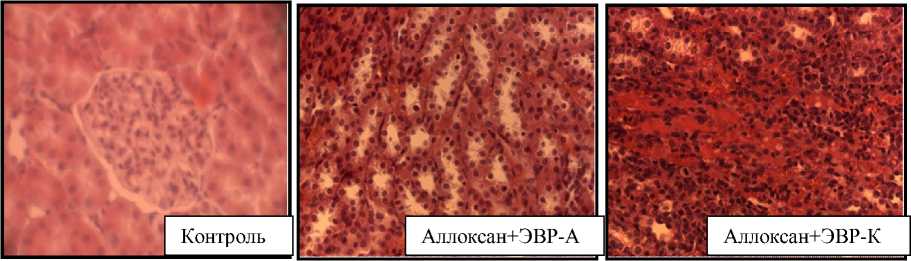
Рис. 3.
Морфологическая структура почки.
Таким образом, прием электрохимически активных водных растворов не вызывает изменений функций почек и водно-солевого обмена у здоровых животных, тогда как при сахарном диабете увеличение диуреза и экскретируемой фракции калия после приема ЭВР требует дальнейшего изучения. В то же время анолит на фоне изучаемой патологии способствует задержке развития данного заболевания, что проявляется в более низких показателях уровня глюкозы в крови, тогда как католит не оказывает подобного протективного эффекта. Гистологический анализ показал положительное влияние анолита на структуру поджелудочной железы крыс с аллоксановой моделью сахарного диабета. Полученные данные требуют исследования биохимических процессов, определяющих подобный гипогликемический и протективный эффекты анолита.
Все права защищены

4(8) 2012
ISSN 2226-3365
Список литературы Влияние электроактивированных водных растворов на морфофункциональные показатели поджелудочной железы и почек крыс с экспериментальной моделью сахарного диабета
- Зарезаев О. А., Корнева Т. К., Паничева С. А. Обработка рук хирурга электрохимическими активированными растворами и микробиологический контроль метода//Электрохимическая активация в медицине, сельском хозяйстве, промышленности: тезисы докл. всерос. конф. -М., 1994.
- Электрохимическая активация: История, состояние, перспективы. Академия медико-технических наук Российской Федерации/под ред. В. М. Бахира. -М.: ВНИИИМТ, 1999. -107 с.
- Петросян Э. А. Патогенетические принципы и обоснование лечения гнойной хирургической инфекции методом непрямого электрохимического окисления: автореферат на соискание ученой степени доктора мед. наук. -М.,1991. -54 с.
- Метод непрямой электрохимической детоксикации организма с использованием гипохлорита натрия в практической медицине//Добриянец А. И., Жидков С. А., Кузьмин Ю. В. Методические рекомендации. -Минск, 2000. -26 с.
- Вахидов В.В., Мамаджанов У. Д., Касымов А. Х. и др. Способ получения жидкости с биологически активными свойствами/Авторское свидетельство СССР. -М., 1982. -93 с.
- Гительман Д. С., Збрижер Э. Р. Исследование влияния электроактивированного раствора католита на иммунный ответ и кроветворение у сублетально облученных мышей//Электрохимическая активация в медицине, сельском хозяйстве, промышленности: тезисы докл. всерос. конф. -М., 1994.
- Лакин Г.Ф. Биометрия. -М.: Высшая школа, 1980. -293 с.


