Влияние электромагнитного излучения терагерцового диапазона частотой молекулярного спектра оксида азота 150+0,75 ГГц на морфофункциональные нарушения микроциркуляции у белых крыс в состоянии острого и длительного стресса
Автор: Бугаева И.О., Киричук Вячеслав Федорович, Иванов А.Н., Куртукова М.О.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Физиология и патофизиология
Статья в выпуске: 4 т.5, 2009 года.
Бесплатный доступ
Изучено влияние электромагнитного излучения терагерцового диапазона на частотах молекулярного спек- тра излучения и поглощения оксида азота 150+0,75 ГГц на морфофункциональные изменения микроциркуля- ции и структуры тканей у животных в состоянии острого и длительного иммобилизационного стресса. Показано, что воздействие электромагнитных волн на указанных частотах вызывает ограничение активности гипоталамо- гипофизарно-надпочечниковой и тиреоидной осей стрессорной реакции. Установлено, что волны терагерцового диапазона на частотах оксида азота способны восстанавливать нарушения внутрисосудистого, сосудистого и внесосудистого компонентов микроциркуляции, а также обладают гистопротекторным действием.
Микроциркуляция, электромагнитное излучение, терагерцовый диапазон, оксид азота, стресс
Короткий адрес: https://sciup.org/14916960
IDR: 14916960
Influence of terahertz range electromagnetic radiation at molecular spectrum frequency of 150+0,75 GHz nitric oxide on microcirculation morphofunctional disturbances in white rats in condition of acute and prolonged stress
The effect of electromagnetic radiation of terahertz range at frequency of emission and absorption molecular spectrum of 150+0,75GH z nitric oxide on morphofunctional changes of microcirculation and tissue structure in animals in condition of acute and prolonged immobilization stress has been studied. It has shown that the influence of electromagnetic waves at these frequencies causes activity decrease of hypothalamic-pituitary-adrenal and tireoyd axis of stress reaction. It has been determined that terahertz range waves at frequency of nitric oxide are liable to restore disturbances of intravascular, vascular and extravascular components of microcirculation and also have histoprotective effect.
Текст научной статьи Влияние электромагнитного излучения терагерцового диапазона частотой молекулярного спектра оксида азота 150+0,75 ГГц на морфофункциональные нарушения микроциркуляции у белых крыс в состоянии острого и длительного стресса
Изменения регионарного, в частности, коронарного, мозгового, почечного кровотока и системной гемодинамики, в том числе недостаточность кровообращения, связаны, прежде всего, с нарушениями микроциркуляции.
Для коррекции различных компонентов микро-циркуляторных нарушений используют широкий спектр препаратов: вазодилататоры, антиагреганты, дезагреганты, прямые и непрямые антикоагулянты, антиоксиданты и др. Однако фармакотерапия всегда сопровождается возникновением различной степени выраженности побочных эффектов. В связи с этим
в настоящее время ведутся поиски новых немедикаментозных методов коррекции указанных нарушений. Одним их таких методов является низкоинтенсивное излучение миллиметрового и субмиллиметрового диапазона частот [1].
Однако в доступной литературе представлены только исследования влияния ТГЧ-излучения на частотах оксида азота 150 + 0,75 ГГц на отдельные функциональные показатели различных составляющих микроциркуляции, в частности ее внутрисосудистого компонента [2]. При этом нет комплексных сведений о морфофункциональных изменениях в системе микроциркуляции под влиянием данного диапазона волн, и их роли в гистофизиологии тканей.
Цель работы: установить влияние электромагнитного излучения терагерцового диапазона частотой молекулярного спектра излучения и поглощения оксида азота 150+0,75 ГГц на морфофункциональ- ные нарушения микроциркуляции и структуры тканей в различных органах у белых крыс, находящихся в состоянии острого и длительного стресса.
Материалы и методы. Исследования проведены на 155 белых нелинейных крысах-самцах массой 180-220 г. В качестве модели нарушения микроциркуляции нами использовался острый иммобилизацион-ный стресс: жесткая фиксация животных на спине в течение 3-х часов. В качестве длительно действующего стрессора использовали ежедневную 3-часовую иммобилизацию животных в положении на спине в течение 5 суток [2].
Облучение животных проводилось малогабаритным медицинским аппаратом «КВЧ-ΝО», разработанным в Медикотехнической ассоциации КВЧ (г. Москва) совместно с ФГУП «НПП-Исток» (г. Фрязино) и ОАО ЦНИИИА (г. Саратов) [3].
Облучалась поверхность кожи площадью 3 см2 над областью мечевидного отростка грудины. Облучатель располагался на расстоянии 1,5 см над поверхностью тела животного. Мощность излучения генератора составляла 0,7 мВт, а плотность мощности, падающей на участок кожи размером 3 см2, составляла 0,2 мВт/см2. Продолжительность однократного облучения составляла 30 минут.
Исследование морфофункциональных изменений в тканях проведено на 5 группах животных по 15 особей в каждой: 1 группа – контрольная (15 интактных крыс-самцов); 2 группа – крысы-самцы, находящиеся в состоянии острого иммобилизационного стресса; 3 группа включала животных, подвергнутых облучению терагерцовыми волнами на частотах молекулярного спектра излучения и поглощения оксида азота 150 + 0,75ГГц в течение 30 минут на фоне острого стресса; 4 группа – крысы-самцы, находящиеся в состоянии длительного иммобилизационного стресса; 5 группа включала животных, подвергнутых ежедневному 30-минутному облучению терагерцо-выми волнами на частотах молекулярного спектра излучения и поглощения оксида азота 150 + 0,75ГГц в течение 5 дней, на фоне длительного стресса (облучение животных проводили после каждого сеанса иммобилизации).
Материал для гистологического исследования забирался после декапитации животных. В остром стрессе животных декапитировали через 24 часа от начала действия стрессора, а при длительном стрессе – через 24 часа после 5-й иммобилизации (на 6-е сутки эксперимента).
Ткани головного мозга, эндокринных желез (гипофиза, надпочечников, щитовидной железы), висцеральных органов (сердце, печень, легкие, желудок, брыжейка тонкой кишки, почки) фиксировались в 10% - м растворе нейтрального формалина, после чего доводились до парафиновых блоков. Окраску препаратов проводили гематоксилином и эозином, а для элективного выявления фибрина использовался гистохимический метод ОКГ (оранжевый Ж, красный 2С, водный голубой).
Результаты. Проведенные нами исследования показали, что у животных в состоянии острого иммо-билизационного стресса происходят морфофункциональные изменения гипофиза, надпочечников и щитовидной железы, сопровождающиеся повышенным кровенаполнением гипофиза, щитовидной железы и надпочечников. В щитовидной железе происходит изменение эпителия фолликулов и коллоида. Во многих фолликулах отмечалась повышенная митотическая активность интрафолликулярного эпителия.
В надпочечниках выявлено истончение клубочковой зоны, выраженное в различной степени истощение клеток пучковой зоны коры надпочечников, что проявлялось диффузным или очаговым обеднением этих клеток липидами.
У животных в состоянии длительного стресса также отмечалось повышенное кровенаполнение гипофиза. В щитовидной железе обнаружено, что большинство фолликулов не содержало коллоида, а эпителий фолликулов высокий, многорядный (рис. 1). В состоянии длительного стресса развивается гипертрофия коры надпочечников, происходит измене-
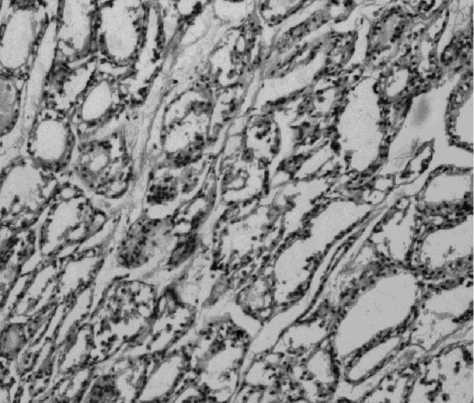
Рис. 1. Щитовидная железа крысы-самца, находящегося в состоянии длительного стресса. Разжижение коллоида и образование вакуолей, большинство фолликулов коллоида не содержат. Многорядный, высокий эпителий фолликулов. Окр. Г-Э. Ув. 200
ние соотношения между зонами (гипертрофируется пучковая зона коры надпочечников). Морфологические изменения, выявленные в надпочечниках у этой группы животных (уменьшение липидных включений, изменение соотношения между зонами коры за счет увеличения пучковой зоны), и выраженное полнокровие являются структурным эквивалентом усиления продукции кортикостероидов и их секреции в условиях стресс-реакции.
В центральной нервной системе и в висцеральных органах обнаружены нарушения всех компонентов микроциркуляции у животных в состоянии острого и длительного иммобилизационного стресса, которые возникают уже после однократной иммобилизации и прогрессируют в ходе длительного стресса.
У животных в состоянии острого и длительного стресса происходит также нарушение сосудистого компонента микроциркуляции, что проявляется изменением тонуса сосудов и кровенаполнения органов. Следует отметить, что у животных, подвергнутых однократной трехчасовой иммобилизации, во многих
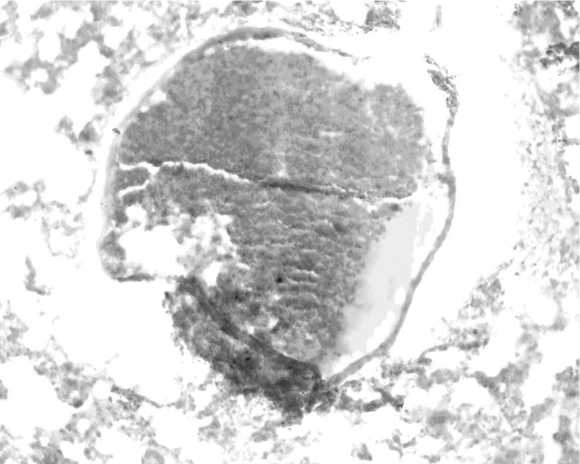
Рис. 2. Сепарация крови и образование пристеночных тромбов в просвете сосуда легкого крысы-самца, находящегося в состоянии длительного стресса. Окр. ОКГ. Ув. 400

Рис. 3. Фибриноидное набухание стенок артерий легких крысы-самца, находящегося в состоянии длительного стресса. Окр. ОКГ. Ув. 300
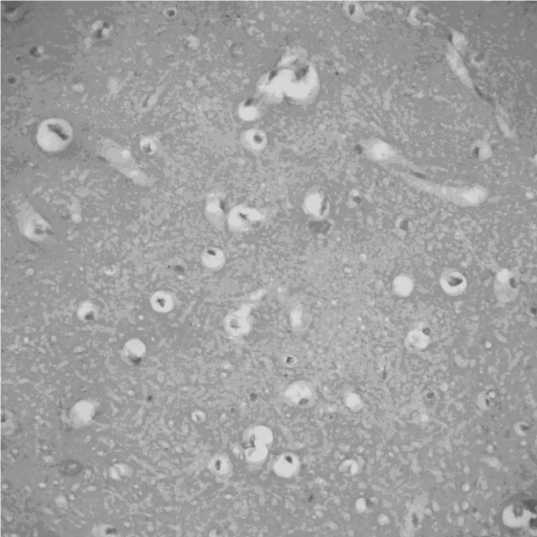
Рис. 4. Полнокровие сосудов, расширение периваскулярных и перицеллюлярных пространств ткани головного мозга крысы-самца, находящегося в состоянии длительного стресса. Окр. Г-Э. Ув. 200
органах (печень, почки, желудок, легкие) наблюдаются явления ишемии, что в целом организме отражает явления централизации кровотока. Нарушение сосудистого компонента микроциркуляции также проявляется увеличением проницаемости сосудов (фибриноидное набухание их стенок) и грубыми нарушениями целостности микрососудов (кровоизлияния в головном мозге и его мягкой оболочке, легких, брыжейке тонкого кишечника). Фибриноидное набухание стенок сосудов (рис. 3) и кровоизлияния (в мягкой мозговой оболочке, головном мозге, брюшине, легких) наиболее часто встречаются в гистологических препаратах органов животных, находящихся в состоянии длительного стресса.
Выявленные нами внесосудистые нарушения микроциркуляции, проявляющиеся отеками, отмечаются прежде всего в головном мозге и выражаются в увеличении периваскулярных и перицеллюлярных пространств (рис. 4). Они более выражены у животных в состоянии длительного стресса. Изменение внесосудистого компонента микроциркуляции еще больше усугубляют нарушения в других ее компонентах. В ряде органов (сердце, легкие, печень, почки, желудок) микроциркуляторные нарушения приводят к развитию дистрофических и некротических изменений.
Наши исследования показали, что нарушения микроциркуляции в головном мозге приводили к развитию дистрофических изменений нейронов у животных в состоянии длительного стресса. В сердце животных, подвергнутых однократной трехчасовой иммобилизации, обнаруживались признаки дистрофии миокарда: зернистость цитоплазмы, нечеткие ее контуры, отмечалась фрагментация мышечных волокон. При длительном стрессе признаки дистрофии миокарда нарастали: многие кардиомиоциты находились в состоянии зернисто-глыбчатого распада с исчезновением поперечно-полосатой исчерченности, в ряде случаев ядра не определялись (рис. 5).
У животных в состоянии острого иммобилизаци-онного стресса происходит нарушение внутрипече-ночной гемодинамики, приводящее к ишемии. При длительном стрессе нарушение внутрипеченочной гемодинамики проявляется застойными явлениями, при этом происходят дистрофия и некроз гепатоцитов.
В почках животных, подвергнутых однократной трехчасовой имообилизации, отмечены явления ишемии, которые приводят к дистрофическим изменениям в канальцах почек. При длительном стрессе у них развивается некроз эпителия почечных канальцев.
В результате проведенных исследований установлено, что электромагнитное излучение терагер-цового диапазона на частотах молекулярного спектра излучения и поглощения оксида азота 150+0,75 ГГц умеренно снижает активность гипоталамо-гипофизарно-надпочечниковой и тиреоидной осей стрессорной реакции, что проявляется отсутствием или уменьшением выраженности характерных для стресс-реакции морфо-функциональных изменений в гипофизе, надпочечниках и щитовидной железе. Так, у животных, подвергнутых ТГЧ-воздействию на фоне острого и длительного стресса, не обнаружены морфологические изменения гипофиза, снижается активность надпочечников, на что указывает отсутствие выраженной делипидизации их коры, и менее выражены изменения коллоида и эпителия фолликулов щитовидной железы (рис. 6), наблюдаемые соответственно при остром и длительном иммобилизаци-онном стрессе.
Электромагнитное излучение терагерцового диапазона на частотах молекулярного спектра излучения и поглощение оксида азота 150 + 0,75ГГц оказывает нормализующее влияние на микроциркуляцию и структуру тканей различных органов у белых крыс самцов, подвергнутых острому и длительному стрессу. Так, на фоне ТГЧ-воздействия восстанавливается внутрисосудистый компонент микроциркуляции у животных, подвергнутых ТГЧ-облучению на фоне острого и длительного стресса, при этом не обнаружено признаков сладжирования крови. У животных в состоянии острого стресса отмечается значительное уменьшение явлений ишемии многих висцеральных органов (печени, почек, легких), нормализация кровотока в головном мозге (рис. 7), снижение повышенной проницаемости сосудов и ломкости капилляров. Вышеуказанные факты свидетельствуют в пользу значительного влияния электромагнитных волн указанной частоты на сосудистый компонент микроциркуляции, в частности, на тонус сосудов.
Нами обнаружен ряд структурных изменений в тканях у крыс-самцов, находящихся в состоянии острого и длительного иммобилизационного стресса, под влиянием электромагнитного излучения терагер-цового диапазона на частотах молекулярного спектра излучения и поглощения оксида азота 150 + 0,75 ГГц. Следует отметить, что ТГЧ-воздействие не оказывает значительного влияния на грубые структурные нарушения. Так, ТГЧ-волны указанной частоты не оказывают эффективного влияния на дистрофические нарушения в сердце (рис. 8), однако способствуют значительному снижению частоты ишемического повреждения почек и печени у животных, подвергнутых однократной трехчасовой иммобилизации. В условиях длительного иммобилизационного стресса электромагнитное излучение терагерцового диапазона на частотах оксида азота способно препятствовать развитию дистрофических изменений нейронов головного мозга. Отсутствие дистрофических изменений нейронов, характерных для состояния длительного стресса у животных, подвергнутых курсовому ТГЧ-воздействию, свидетельствует о нейропротекторном эффекте волн указанной частоты.
Обсуждение результатов. Повышенное кровенаполнение гипофиза, щитовидной железы и надпочеч-

Рис. 5. Дистрофия миокарда крысы-самца, находящегося в состоянии длительного стресса. Окр. Г-Э. Ув. 400
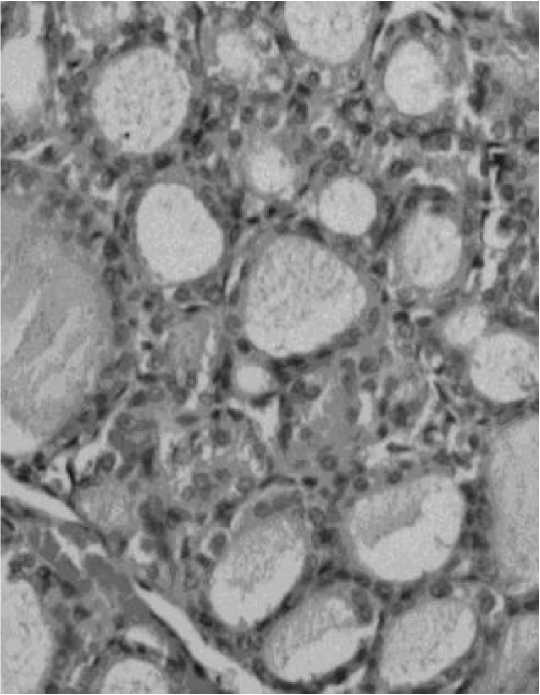
Рис. 6. Разжижение интрафолликулярного коллоида и высокий призматический эпителий фолликулов щитовидной железы крысы-самца, подвергнутого курсовому облучению ТГЧ-волнами на частотах МСИП оксида азота 150+0,75 ГГц на фоне длительного стресса. Окр. Г-Э. Ув. 200
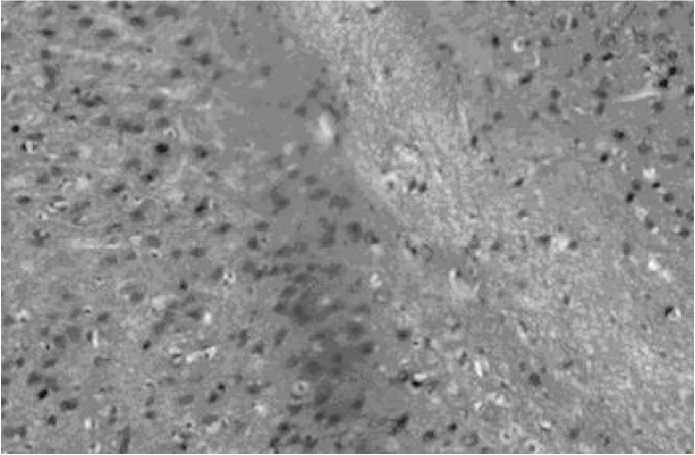
Рис. 7. Головной мозг крысы-самца, подвергнутого курсовому облучению ТГЧ-волнами на частотах МСИП оксида азота 150+0,75 ГГц на фоне длительного стресса. Окр. ГЭ х 200
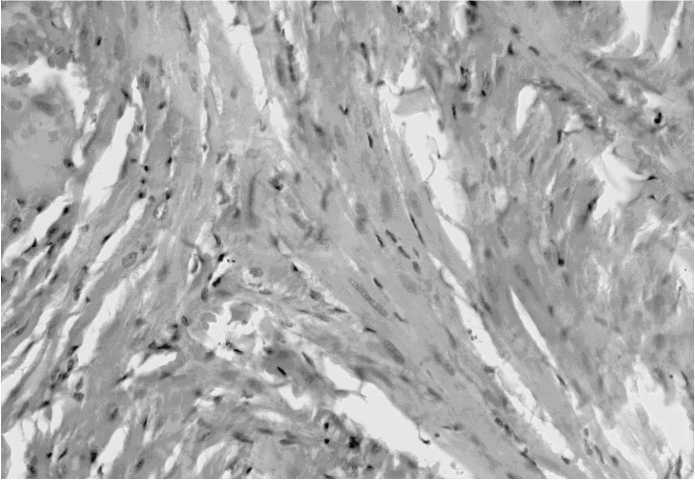
Рис. 8. Дистрофия отдельных волокон миокарда крысы-самца, подвергнутого курсовому облучению ТГЧ-волнами на частотах МСИП оксида азота 150+0,75 ГГц на фоне длительного стресса. Окр. ГЭ х 200
ников у животных в состоянии острого и длительного стресса свидетельствует о повышенной продукции гормонов [4]. Пролиферация клеток эпителия фолликулов, отсутствие коллоида в фолликулах щитовидной железы являются показателем ее гиперфункции [5]. Истощение клеток пучковой зоны коры надпочечников, что выражалось диффузным или очаговым обеднением этих клеток липидами, свидетельствует о значительном выделении глюкокортикоидов [6].
Таким образом, обнаруженные нами изменения эндокринных желез свидетельствуют о значительной активации основных стресс-реализующих систем, в частности гипоталамо-гипофизарно-надпочечниковой, тиреоидной осей стрессорной реакции. Изменения локального кровотока в этих железах можно рассматривать как функциональную гиперемию.
Выявленные в ряде органов нарушения внутрисосудистого компонента микроциркуляции у животных в состоянии острого и длительного стресса, проявляющиеся сепарацией крови на плазму и форменные элементы, характеризуют сладж-феномен, связанный с повышенной адгезией, агрегацией и агглютинацией форменных элементов крови, что обусловливает ее сепарацию на более или менее крупные конгломераты, состоящие из эритроцитов, тромбоцитов, лейкоцитов, и плазму крови [7].
Известно, что ключевое значение в регуляции сосудистого компонента микроциркуляции принадлежит эндотелию сосудов [8]. Повреждение эндотелия сосудов и обнажение субэндотелиальных слоев запускает реакции агрегации тромбоцитов, процесса свертывания крови, препятствующие кровопотере, вызывает спазм сосуда, прекращается образование антиагре-гантов [8]. Выявленные нами изменения сосудистого компонента микроциркуляции у животных в состоянии стресса можно объяснить повреждением эндотелия и развитием эндотелиальной дисфункции.
Обнаруженные изменения в структуре тканей различных органов животных, находящихся в состоянии острого и длительного стресса, объясняются длительным функционированием стресс-реализующих систем и повреждающим действим метаболитов этих систем [2].
Таким образом, у животных в состоянии острого стресса вследствие гиперфункции стресс-реализующих систем и повреждающего действия метаболитов этих систем возникают ярко выраженные нарушения внутрисосудистого, сосудистого и внесосудистого компонента микроциркуляции. Эти нарушения прогрессируют при длительном стрессе и приводят к развитию дистрофических и некротических изменений в тканях. Полученные нами данные согласуются с результатами многочисленных исследований, посвященных изучению морфофункциональных стрессорных изменений [4].
На основании ряда экспериментальных работ эффекты электромагнитного излучения терагерцового диапазона на частотах оксида азота150 + 0,75 ГГц тем или иным образом сопряжены с метаболическим циклом ΝО (преимущественно с ΝО-синтазной компонентой данного цикла).При облучении ТГЧ-волнами как на частотах МСИП ΝО, так и других терагерцовых частотах возможно увеличение реакционной способности и/или концентрации эндогенного оксида азота [9].
Условно можно выделить три уровня реализации эффектов повышения активности ΝО под влиянием ТГЧ-воздействия: непосредственное влияние на клетки – аутокринное действие; влияние на ткань в целом – паракринная регуляция деятельности соседних клеток и центральные эффекты – ΝО-зависимые изменения нервной и гуморальной регуляции [9].
В настоящее время обосновано представление о системе генерации оксида азота как об обособленной стресс-лимитирующей системе. Она активируется при действии на организм различных стресс-факторов и в процессе адаптации к повторным воздействиям факторов среды [10].
Активация ΝО-эргических нейронов в центральной нервной системе предупреждает гиперсекрецию таких гипоталамо-гипофизарных стрессорных гормонов, как кортикотропин, рилизинг-фактор кортикотропина и др. [11]. Этим фактом и объясняется отсутствие морфофункциональных изменений гипофиза у животных, подвергнутых ТГЧ-облучению на указанных частотах. Известно, что кортикотропин регулирует продукцию глюкокортикостероидов корой надпочечников [12]. Экспериментальные исследования показали, что ТГЧ-излучение на частотах МСИП оксида азота 150 + 0,75 ГГц белых крыс самцов способно предотвращать повышение уровня кортикостероидов при облучении до начала действия стрессора, то есть полученные данные указывают на ограничение активности гипоталамо-гипофизарно-надпочечниковой оси стрессорной реакции [9], что морфологически выражается в отсутствии делипи-дизации коры надпочечников у животных, подвергнутых ТГЧ-воздействию на фоне острого и длительного стресса.
Важную роль в регуляции микроциркуляции играет также симпато-адреналовая ось стрессорной реакции. Гиперкатехоламинемия вызывает спазм сосудов и ишемию ряда органов [12], что и было нами обнаружено у животных в состоянии острого и длительного стресса. Проведенные исследования показали, что при облучении животных, находящихся в состоянии острого иммобилизационного стресса, электромагнитными волнами терагерцового диапазона на частотах оксида азота 150 + 0,75 ГГц происходит статистически достоверное уменьшение концентрации катехоламинов в крови. Это свидетельствует об ограничении активности симпатоадреналовой оси стрессорной реакции [9].
Нормализацию внутрисосудистого компонента микроциркуляции у животных в состоянии острого и длительного стресса под влиянием терагерцовых волн указанной частоты можно объяснить аутокринным и паракринным механизмами действия оксида азота в системе форменных элементов крови (в частности тромбоцитов) [2].
Паракринные эффекты оксида азота, продуцируемого эндотелием оксида азота, объясняют нормализацию сосудитого компонента микроциркуляции, в частности тонуса сосудов [9].
Положительное влияние электромагнитного излучения на частотах оксида азота на нарушения внесо-судистого компонента микроциркуляции и структуры тканей реализуется, прежде всего, через изменение процессов липопероксидации. Показано, что при воздействии на животных, находящихся в состоянии острого иммобилизационного стресса, электромагнитными волнами терагерцового диапазона на частотах оксида азота 150,176-150,664 ГГц происходит нормализация процессов липопероксидации и активности антиоксидантов. Это проявляется в снижении концентрации токсических промежуточных продуктов перекисного окисления липидов – малонового диальдегида и гидроперекисей липидов. При воздействии терагерцового излучения на частотах молекулярного спектра излучения и поглощения оксида азота 150+0,75 ГГц в течение 30 минут наблюдается эффективная нормализация активности антиоксидантной системы – её ферментного и неферментного звеньев, что выражается в нормализации активности супероксиддисмутазы и каталазы в эритроцитах и восстановлении количества общих сульфгидрильных групп и витамина Е в сыворотке крови до уровня интактных животных [9].
Таким образом, электромагнитное излучение терагерцового диапазона на частотах молекулярного спектра излучения и поглощения оксида азота 150+0,75 ГГц обладает выраженным гистопротектор-ным действием на ряд органов, предохраняя ткани от повреждающего действия метаболитов стресс-реализующих систем и стимулируя процессы репарации. Вероятно, влияние излучения указанной частоты на тканевой метаболизм опосредуется через систему оксида азота и другие сопряженные с ней периферические стресс-лимитирующие системы.
Список литературы Влияние электромагнитного излучения терагерцового диапазона частотой молекулярного спектра оксида азота 150+0,75 ГГц на морфофункциональные нарушения микроциркуляции у белых крыс в состоянии острого и длительного стресса
- Киричук, В.Ф. КВЧ-терапия./В.Ф. Киричук, Т.В. Голова-чева, А.Г. Чиж. -Саратов: Изд-во СГМУ, 1999. -360 с.
- Электромагнитное излучение терагерцового диапазо-на на частотах оксида азота в коррекции и профилактике нарушений функциональной активности тромбоцитов у белых крыс при длительном стрессе/В.Ф. Киричук, А.Н. Иванов, О.Н. Антипова и др.//Цитология. -2007. -Т. 49. -№6. -С. 484-490.
- Аппарат для лечения электромагнитными волнами крайне высоких частот/О.В. Бецкий, А.П. Креницкий, А.В. Майбородин, В.Д. Тупикин. -Патент «Роспатента» на полезную модель №50835 от 27 января 2006.
- Половые различия адренокортикальной чувствительности и устойчивости к цереброваскулярным повреждениям у крыс при сильном стрессе/Т.Г. Анищенко, Г.Е. Брилль, Т.П. Романова, Н.Б. Игошева//Бюлл. эксперим. биол. мед. -1992. -Т. 114. -№ 10. -С. 353.
- Афанасьев, Ю.И. Гистология, цитология и эмбриология/Ю.И. Афанасьев, С.Л. Кузнецов, Н.А. Юрина. -М.: Медицина, 2004. -765 с.
- Колдышева, Е.В. Ультраструктурная реорганизация коры надпочечников при экстремальных воздействиях (общей гипоксии, гипертермии и генетически детерменирован-ных нарушениях метаболизма)/Автореф. дис. д-ра биол. наук/Е.В. Колдышева; НИИ региональной патологии и пато-морфологии СО РАМН. -Новосибирск, 2009. -48 с.
- Патологическая физиология/Н.Н. Зайко, Ю.В. Быць, А.В. Атаман и др. -Киев: «Логос», 2007. -640 с. 8. Киричук, В.Ф. Дисфункция эндотелия/В.Ф. Киричук, П.В. Глыбочко, А.И. Пономарева. -Саратов: Изд-во СГМУ, 2008. -112 с.
- Механизм действия терагерцовых волн на частотах оксида азота с физиологической точки зрения/В.Ф. Киричук, А.Н. Иванов, А.А. Цымбал, Е.В. Андронов//Миллиметровые волны в биологии и медицине. -2009. -№ 1-2. -С. 47-55.
- Манухина, Е.Б. Стресс-лимитирующая система оксида азота/Е.Б. Манухина, И.Ю. Малышев//Рос. физиол. журнал им. И.М. Сеченова. -2000. -Т. 86. -№. 10. -С. 1283-1292.
- Endotoxin stimulates an endogenous pathway regulating corticotrophin-releasing hormone and vasopressin release involving the generation of nitric oxide and carbon monoxide/I. Kostoglou-Athanassiou, A. Costa, P. Navarra et al.//J. Neuroimmunol. -1998. -V. 86. -P. 104-109.
- Киричук, В.Ф. Регуляция функций организма. Гуморальная регуляция/В.Ф. Киричук, А.Н. Иванов. -Саратов: Изд-во СГМУ, 2008. -99 с.


