Влияние электростимуляции на морфометрические характеристики реиннервируемой мышцы
Автор: Щудло Н.А., Филимонова Г.Н., Меньщикова И.А., Голобокова И.А.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2008 года.
Бесплатный доступ
В экспериментальных условиях на 21 взрослой беспородной собаке после перерезки и шва седалищного нерва проводили внутритканевую электростимуляцию сегментов спинного мозга и ствола нерва проксимальнее уровня повреждения. По результатам морфометрии диаметров мышечных волокон и стереологического анализа сделан вывод, что апробированный протокол электростимуляции оказывает отчѐтливое модулирующее действие на тканевую организацию реиннервируемой мышцы, способствуя развитию гипертрофии мышечных волокон; этот эффект сопровождается уменьшением васкуляризации мышцы по сравнению с нестимулированным контролем.
Мышечные волокна, реиннервация, электростимуляция, морфометрия
Короткий адрес: https://sciup.org/142121122
IDR: 142121122
The effect of electrical stimulation on the morphometric characteristics of the muscle being reinnervated
The interstitial electrical stimulation of the segments of spinal cord and those of nerve trunk proximal to the level of damage was performed experimentally in 21 adult mongrel dogs after sciatic nerve transection and suturing. By the morphometry results of muscular fiber diameters and those of stereological analysis the authors have come to a conclusion, that the approved protocol of electrical stimulation has a well-defined modulating effect on the tissue organization of the muscle being reinnervated, thereby contributing to developing hypertrophy of muscular fibers; this effect is accompanied by the decrease of muscle vascularization in comparison with non-stimulated control
Текст научной статьи Влияние электростимуляции на морфометрические характеристики реиннервируемой мышцы
Влияние электростимуляции на реиннервацию также было предметом исследований. K.C.B.G. Fernandes et al. [9] установили, что при использовании низкочастотной электротерапии для стимуляции регенерации нерва после его передавливания площадь поперечного сечения мышечных волокон реиннервируемых мышц повышалась, а доля соединительной ткани в них снижалась. После перерезки и шва двигательных нервов одни авторы получили данные об улучшении структуры и функции реиннервируемых мышц под воздействием электростимуляции [11], другие сделали вывод о супрессии реиннервации [12].
Цель – выявить эффекты электростимуляции на тканевую организацию и численно-размерный состав волокон реиннервируемой мышцы после перерезки и шва смешанного нерва.
МАТЕРИАЛЫ И МЕТОДЫ
Опыты проведены на 21 взрослой беспородной собаке. У 19 собак под внутривенным барбитуровым наркозом в асептических условиях выполнили полное пересечение и первичный микрохирургический шов седалищного нерва на уровне сред- ней трети бедра. Использовали инструментарий фирмы Aesculap, нить калибра 8/0 на атравматических иглах фирмы Ethicon и 8-кратное увеличение операционного микроскопа фирмы Opton.
В послеоперационном периоде у 4 животных не применяли воздействий на регенераторный процесс (нестимулированный контроль - Control). В опытной группе проводили курсы внутритканевой электростимуляции. Каждая процедура продолжительностью 40 минут состояла из двух частей: первая часть (20 минут) – внутритканевая электростимуляция сегментов спинного мозга, вторая часть (20 минут) – внутритканевая стимуляция ствола нерва проксимальнее уровня повреждения. Соответственно скелетотопии сегментов спинного мозга у собак [1], между остистыми отростками LI-LII, LII-LIII, LIII-LIV позвонков поочередно вводили игольчатый электрод. Его подключали к отрицательному полюсу аппарата, а положительный пластинчатый электрод кольцеобразно накладывали дистальнее уровня повреждения нерва – на область голени. Для внутритканевой электростимуляции [2] седалищного нерва игольчатый электрод отрицательной полярности вводили между большим вертелом бедренной кости и бугром седалищной кости. Положительный пластинчатый электрод также располагали в области голени. Процедуры проводили через день (понедельник, среда, пятница). Режим тока переменный, частота 50 Гц, длительность импульса -0,7 мс, длительность посылки 2 с; соотношение «посылка-пауза» 2:2. Силу тока подбирали индивидуально, до видимого мышечного ответа, в диапазоне от 4 до 20 мА. Для временного торможения двигательной активности собак перед каждым сеансом электростимуляции их вводили в медикаментозный сон с помощью стандартной комбинации минимальных доз препаратов, традиционно используемых в ветеринарии. Для выявления оптимальных режимов внутритканевой электростимуляции животных опытной группы разделили на две подгруппы: в первой через 4 недели после операции проводили курс из 18 сеансов (Stim 1), который заканчивался на сроке 2,5 месяца после операции (n=3); во второй (Stim 2) проводили два курса из 18 сеансов: первый – в те же сроки, что в первой подгруппе, а второй начинали через 6 ме- сяцев после операции и заканчивали в 8,5 месяцев (n=4). Через 12 месяцев после операции животных опытных групп и контрольной выводили из опыта введением летальной дозы барбитуратов.
Поскольку сроки появления первых электрофизиологических признаков реиннервации мышц голени у собак групп 1 и 2 индивидуально варьировали от 3 до 8 недель после операции [4], выполнены дополнительные 3 опыта по модели «предотвращённой регенерации» (Denerv): после резекции 3 см седалищного нерва изолировали его проксимальную и дистальную культи колпачками из биологически инертного материала. Группа Denerv выведена из опыта через 33 дня после операции. Это позволило получить однородные исходные данные по денервированной мышце в срок, непосредственно предшествующий реиннервации и началу сеансов электротерапии.
Содержание, кормление животных, операции и сеансы электростимуляции, а также выведение из опыта осуществляли согласно приказу МЗ СССР № 775 [5].
После эвтаназии для морфологических исследований забирали фрагменты передней большеберцовой мышцы из области брюшка на уроне его верхней, средней и нижней трети, монтировали на промаркированные этикетки площадью поперечного среза и погружали в жидкий азот. Изготавливали поперечные крио-статные срезы, выявляли активность миозиновой АТФ-азы по Padycula, Herman в модификации З. Лойда (3). Препараты оцифровывали на АПК «ДиаМорф» (Россия) и морфометрировали в программе “Medias”. Для двойного контроля использовали данные морфометрии мышц интактных собак (Intact). Статистическую обработку первичных данных осуществляли с использованием программных возможностей MS Excel-2000, вариационные ряды ранжировали с шагом 10,0 мкм и получали гистограммы распределения мышечных волокон по диаметрам.
РЕЗУЛЬТАТЫ
Визуальный анализ препаратов денервированной мышцы свидетельствует о значительной атрофии волокон уже через 1 месяц после резекции седалищного нерва. Кривая распределе- ния по диаметрам волокон по сравнению с интактной значительно смещена влево и вместо плато имеет высокий пик (рис. 1).
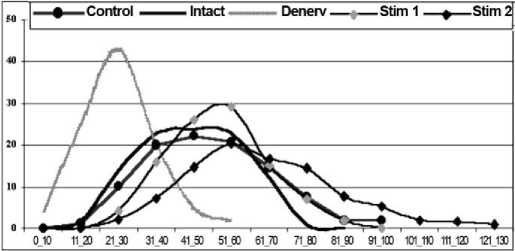
Рис. 1. Кривые распределения волокон передней большеберцовой мышцы собак по диаметрам в интактном состоянии и разных условиях эксперимента. Ось абсцисс – размерный класс волокон (0-10 мкм; 11-20 мкм и т.д.); ось ординат – процентная доля волокон каждого класса
Во всех опытах со швом нерва через год после операции формы и размеры профилей мышечных волокон в криостатных срезах свидетельствуют о компенсации денервационной атрофии, что подтверждают морфометрические данные. В контрольной группе усреднённая кривая распределения мышечных волокон по диаметру практически совпадает с интактной (рис. 1). В подгруппе Stim 1 она смещена вправо и имеет небольшой пик. В подгруппе Stim 2 смещение кривой вправо ещё более выражено, высота её пика снижается, а ширина основания значительно увеличивается. Изучение индивидуальных гистограмм животных этой группы показало, что у одной собаки из трёх распределение мышечных волокон по диаметру бимодально, что, предположительно, можно связать с неодинаковым влиянием электростимуляции на мышечные волокна разных метаболических типов.
По данным стереологического анализа, в контроле по сравнению с интактной мышцей в 1,5 раза уменьшена объёмная плотность микрососудов, в 1,2 уменьшена доля эндомизия и соответственно несколько увеличена объёмная плотность мышечных волокон (рис. 2). В подгруппе Stim 1 объёмная плотность мышечных волокон сопоставима с интактной мышцей, но объёмная плотность микрососудов уменьшена в 2,4 раза, а доля эндо-мизия увеличена в 1,2 раза. В подгруппе Stim 2 объёмная плотность микрососудов меньше, чем в контроле, но больше, чем в подгруппе Stim 1; объёмная доля эндомизия в этой группе наименьшая; даже по сравнению с интактной мышцей она уменьшена в 1,7 раза; объёмная плотность мышечных волокон несколько превышает соответствующий параметр других групп.
В контрольной группе по сравнению с интактной численная плотность мышечных волокон выше на 21 %, но на 38 % меньше численная плотность микрососудов, поэтому индекс васкуляризации снижен в 1,7 раза (рис. 3). В подгруппе Stim 1 численная плотность мышечных волокон прак- тически равна соответствующему параметру интактной мышцы, но численная плотность микрососудов уменьшена в 1,9 раза и в 2 раза уменьшен индекс васкуляризации. В подгруппе Stim 2 численная плотность мышечных волокон меньше, чем в интактной мышце в 1,3 раза, численная плотность микрососудов – в 1,8 раза, индекс васкуляризации уменьшен в 1,4 раза.
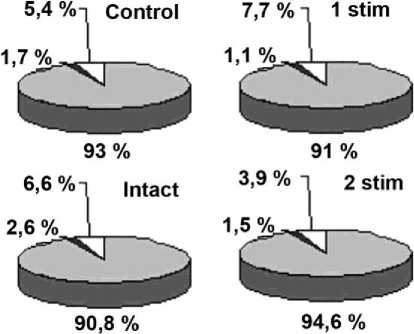
Рис. 2. Объёмные отношения мышечных волокон (серый цвет), эндомизия (белый) и микрососудов (чёрный) в передней большеберцовой мышце оперированных и интактных собак
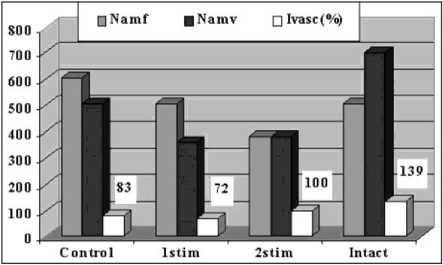
Рис. 3. Численные плотности мышечных волокон (Namf), микрососудов (Namv) и индекс васкуляризации (Ivasc %) в передней большеберцовой мышце оперированных и интактных собак
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Результаты нашего исследования свидетельствуют, что через 1 месяц денервации наступает выраженная атрофия передней большеберцовой мышцы собак. В процессе реиннервации размеры мышечных волокон восстанавливаются даже без применения электростимуляции, но тканевая организация мышцы через год после перерезки и шва нерва не является оптимальной. Во-первых, по сравнению с интактной мышцей объёмная доля микрососудов, их количество в единице площади поперечного сечения мышцы и среднее число, приходящееся на одно мышечное волокно, остаются сниженными. Во-вторых, повышенная объёмная и численная плотности мышечных волокон указывают на увеличение их численности в результате регенерационного миогенеза, который нередко приводит к формированию аномально ветвящихся мышечных волокон или мелких кластеров [6], что не способствует реституции мышцы.
В группе с одним курсом электростимуляции установлено её влияние на толщину мышечных волокон – судя по характеру кривой распределения, в среднем они становятся крупнее, чем в контроле и в интактной мышце. Объёмная и численная плотности мышечных волокон сопоставимы с интактной мышцей, но все параметры васкуляризации снижены не только по сравнению с интактной мышцей, но даже по сравнению с контролем. По-видимому, электро- стимуляция, проводимая в период от 1 до 2,5 месяцев после операции, поддерживает нормои индуцирует гипертрофию переживающих денервацию мышечных волокон, но оказывает тормозящее влияние не только на регенерационный миогенез, но и ангиогенез.
Проведение второго курса электростимуляции в сроки от 6 до 7,5 месяцев после шва нерва усиливает гипертрофию реиннервируемой мышцы. Индекс васкуляризации возрастает за счёт уменьшения численной плотности мышечных волокон, объёмная и численная плотности микрососудов остаются сниженными по сравнению с контролем и особенно интактной мышцей.
ВЫВОДЫ
Апробированный в наших экспериментах протокол электростимуляции оказывает отчётливое модулирующее действие на тканевую организацию реиннервируемой мышцы, способ- ствуя развитию гипертрофии мышечных волокон; этот эффект сопровождается уменьшением васкуляризации мышцы по сравнению с нести-мулированным контролем.


