Влияние картофельного сока на некоторые показатели иммунного профиля и микробиоту кишечника крыс
Автор: Черницкий А.Е., Оберюхтин Д.А., Опарина О.Ю., Лысова Я.Ю., Шанина Е.П.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Микробиота и иммунитет
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Исследования микробиоты кишечника и связанной с ней иммунной защиты относятся к важным направлениям в физиологии питания, поскольку все три фактора (пища-кишечная микробиота-иммунные клетки) непрерывно взаимодействуют между собой и участвуют в формировании резистентности макроорганизма к вирусным и бактериальным инфекциям. Введение в рацион растительных компонентов может заметно улучшить состав микробиоты кишечника и эффективность иммунной защиты. Картофель (Solanum tuberosum L.) - традиционный продукт питания, являющийся уникальным источником макро- (белки, жиры и углеводы) и микронутриентов (аскорбиновая кислота, ниацин, рибофлавин, тиамин, железо, фосфор, кальций, калий, антоцианы, каротиноиды). Одним из способов сохранить высокое содержание и биодоступность функциональных пищевых компонентов картофеля может стать его употребление в виде сока из неочищенных клубней, не подвергавшихся термической обработке. Состав клубней и получаемого из них сока значительно варьируются в зависимости от сортовых особенностей картофеля, окраски его мякоти и кожуры, содержания вторичных метаболитов. Ожидаемо, что различия в химическом составе сока определяют специфичность его действия на организм. Однако ранее эксперименты, подтверждающие эту гипотезу, не проводились. Цель исследования - сравнительная оценка влияния сока, полученного из неочищенных клубней картофеля сортов с разной пигментацией клубней, на иммунный профиль и микробиоту кишечника крыс. В эксперименте на шнековой соковыжималке получали сок из трех сортов картофеля: Багира (фиолетовый картофель), Лила (розовый картофель) и Аляска (белый картофель). Все сорта картофеля исследовали на содержание сухого вещества, крахмала, протеина, моно- и дисахаров, витамина С. Полученный сок выпаивали крысам в первой половине дня. В эксперименте использовали четыре группы нелинейных крыс-самцов по 9 особей в каждой (возраст 9-10 нед), три группы получали сок из фиолетового, розового и белого картофеля, одна (контроль) получала питьевую воду. В начале эксперимента (фон, 0-е сут) проводили взвешивание животных, отбирали образцы цельной крови для гематологических и иммунологических исследований, а также фекалий для бактериологического анализа. Далее в течение 4 нед экспериментальной диеты крыс всех групп еженедельно взвешивали. На 28-е сут отбирали образцы цельной крови и фекалий для проведения повторных лабораторных исследований. Гематологические показатели определяли на полуавтоматическом ветеринарном анализаторе Abacus Junior Vet («Diatron», Австрия). Лейкоцитарную формулу подсчитывали в мазках крови, окрашенных по Романовскому-Гимзе, по общепринятой методике. Подсчитывали Т- и В-лимфоциты, вычисляли Т/В-индекс, показатель фагоцитарной активности, фагоцитарный индекс, рассчитывали индекс системного воспаления, индекс системного воспалительного ответа, совокупный индекс системного воспаления, соотношение числа нейтрофилов и лимфоцитов, тромбоцитов и лимфоцитов, моноцитов и лимфоцитов. Бактериологические исследования проводили в соответствии с рекомендациями по выявлению условно-патогенных микроорганизмов в клинической микробиологии. Применяли методы описательной статистики, выполняли попарную оценку различий (U-критерий Манна-Уитни) и построение диаграмм (программы Jamovi, «The Jamovi Project», Австралия; https://www.jamovi.org/, Microsoft Office Excel 2023). Результаты считали статистически значимыми при p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Картофель, картофельный сок, крысы, микробиота кишечника, иммунный статус
Короткий адрес: https://sciup.org/142246205
IDR: 142246205 | УДК: 57.084:613.263:635.21:[619+612.017 | DOI: 10.15389/agrobiology.2025.4.664rus
Effects of potato juice on some indicators of immune profile and intestinal microbiota in rats
Research into the gut microbiota and the associated immune defense is an important area of nutritional physiology, as all three factors - food, gut microbiota and immune cells - interact continuously with each other and contribute to the macroorganism's resistance to viral and bacterial infections. The addition of plant-based components into the diet can significantly improve the composition of gut microbiota and immune defense effectiveness. Potatoes Solanum tuberosum L. are one of the traditional foods that are a unique source of macronutrients (proteins, fats, and carbohydrates) and micronutrients (ascorbic acid, niacin, riboflavin, thiamine, iron, phosphorus, calcium, potassium, anthocyanins, carotenoids). One way to preserve the high content and bioavailability of functional components in potatoes is to consume them in the form of juice from unpeeled tubers that have not undergone heat treatment. The composition of tubers and the juice obtained from them varies significantly depending on the varietal characteristics of the potato, the colour of the tuber flesh and peel, and the content of secondary metabolites. It is expected that differences in the chemical composition of the juice determine its specific effect on the body. However, no experiments confirming this hypothesis have been conducted previously. The aim of the study was to compare the effects of juice obtained from unpeeled tubers of different potato varieties on the immune profile and gut microbiota of rats. In an experiment using a screw juicer, juice was extracted from three varieties of potatoes: Bagira (purple potato), Lila (pink potato) and Alaska (white potato). All potato varieties were tested for dry matter, starch, protein, mono- and disaccharides, and vitamin C content. The juice obtained was left to settle for 30 minutes, and the supernatant was given to the animals to drink in the first half of the day. The experiment used four groups of male non-linear rats, 9 individuals in each (aged 9-10 weeks): three experimental groups that received juice from purple, pink and white potatoes, respectively, and one control group that was on a standard diet (mixed feed and drinking water). At the beginning of the experiment (background, day 0), the animals were weighed, whole blood samples were collected for hematological and immunological studies, and feces were collected for bacteriological analysis. Then, during the 4 weeks of the experimental diet, the rats in all groups were weighed weekly. On day 28, whole blood and fecal samples were collected for repeat laboratory tests. Hematological parameters were determined using a semi-automatic veterinary analyzer Abacus Junior Vet (Diatron, Austria). The leukocyte formula was calculated in blood slides stained according to Romanovsky-Giemsa, using the standard method. T- and B-lymphocytes, T/B index, phagocytic activity, and phagocytic index were determined using a modification of P.N. Smirnov et al. (2007). Additionally, the systemic inflammation index, systemic inflammatory response index, aggregate inflammation systemic index, neutrophil to lymphocyte ratio, platelet to lymphocyte ratio, and monocyte to lymphocyte ratio were calculated according to the formulas of V.A. Shvarts et al. (2024). Bacteriological studies of samples were performed in accordance with the Methodological Recommendations “Methods of bacteriological examination of conditionally pathogenic microorganisms in clinical microbiology”. Descriptive statistics, pairwise assessment of differences (Mann-Whitney U test) and diagram construction were performed using Jamovi software (The Jamovi Project, Australia; https://www.jamovi.org/) and Microsoft Office Excel 2023. Results were considered statistically significant at p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Влияние картофельного сока на некоторые показатели иммунного профиля и микробиоту кишечника крыс
Микробиота кишечника представляет собой динамичную экосистему, играющую ключевую роль как в физиологических процессах, так и в развитии заболеваний (1). Чем разнообразнее и обильнее индигенная микробиота кишечника, тем выше устойчивость организма к вирусным и бактериальным инфекциям (2). В кишечнике постоянно происходит взаимодействие между компонентами его содержимого — субстратами, бактериями и клетками иммунной системы (2).
Диета — один из факторов образа жизни, который поддается коррекции и может использоваться для профилактики и терапии многих социально значимых заболеваний (1). Растительная пища влияет на течение физиологических процессов в организме как непосредственно, изменяя состав микробиоты кишечника, так и опосредованно — через адсорбируемые малые биоактивные молекулы, образующиеся при утилизации ее компонентов микробиотой (3). Например, неперевариваемые углеводы (целлюлоза, гемицеллюлоза, инулин, галактоолиго- и фруктоолигосахариды), выступая в качестве субстрата для микробиоты, предотвращают адгезию вирусных и бактериальных патогенов, стимулируют иммунную систему и улучшают барьерную функцию кишечника (4). Кишечная микробиота находятся в постоянном взаимодействии с клетками иммунной системы. Пищевые волокна (инулин, пектин, резистентный крахмал) после метаболизации бифидо- и лактобактериями превращаются в короткоцепочечные жирные кислоты — сигнальные молекулы, посредством которых микроорганизмы обменивается информацией с иммунокомпетентными дендритными и T-регуляторными клетками (5). Другие вещества растительного происхождения, например полифенолы (флавоноиды, лигнаны и антоцианины) избирательно подавляют NF- к В-зависимый путь активации воспаления, пролиферации и апоптоза иммунных клеток (6) и стимулируют Nrf2-зависимый путь активации системы антиоксидантной защиты и детоксикации (7). Таким образом, иммунная защита организма зависит напрямую от типа пищи и состояния микробиоты кишечника.
Картофель относится к традиционным продуктам питания (8). Согласно официальным данным ФГБУН ФИЦ питания и биотехнологий о химическом составе используемых в Российской Федерации пищевых продуктов , в 100 г сырого картофеля содержится 2 г белка, 0,4 г жиров и 16,3 г углеводов, из которых 15 г при- ходится на крахмал. Кроме того, сырой картофель содержит высокие концентрации незаменимых микронутриентов: аскорбиновой кислоты, ниацина, рибофлавина, тиамина, железа, фосфора, кальция и калия (9). Сорта картофеля с пигментированной мякотью и кожурой обладают дополнительными функциональными свойствами за счет присутствия в них антоцианов и каротиноидов. Производные цианидина и пеларгонидина придают клубням красный цвет, а петунидин и дельфинидин — фиолетовый (10, 11). Одним из способов сохранить высокое содержание и биодоступность функциональных компонентов сырого картофеля может стать употребление картофельного сока, полученного из неочищенных клубней, не подвергавшихся термической обработке (12).
Интерес исследователей к биологическим свойствам сока из клубней картофеля насчитывает уже более ста лет (12, 13). На сегодняшний день в литературе описано влияние сырого картофеля (14) и некоторых продуктов его переработки — пищевых волокон (15), муки из синего картофеля, богатого антоцианами (16), картофельного крахмала (17) — на микробиоту кишечника. Упоминается способность антоцианов фиолетового картофеля и пептидного гидролизата непигментированного картофеля уменьшать воспаление при экспериментальном колите и метаболическом синдроме (18). Однако действие картофельного сока на иммунный профиль и микробиоту кишечника животных и человека ранее не изучалось.
В настоящей работе впервые выявлено влияние длительного (в течение 28 сут) применения сока из фиолетового, розового и белого картофеля на некоторые показатели иммунного профиля и микробиоту кишечника крыс и обнаружена зависимость наблюдаемых изменений от сортовых особенностей химического состава клубней и получаемого из них сока.
Целью исследования стала сравнительная оценка эффектов, оказываемых соком из неочищенных клубней картофеля разных сортов, на показатели иммунного профиля и кишечную микробиоту крыс.
Методика . В эксперименте использовали сок, полученный из неочищенных клубней картофеля трех сортов: Багира — с фиолетовой окраской мякоти (далее фиолетовый картофель), Лила — с розовой окраской мякоти (далее розовый картофель) и Аляска — с белой окраской мякоти (далее белый картофель). Перед получением сока в клубнях определяли массовую долю (%) сухого вещества, крахмала, протеина, моно-, дисахаров и витамина С (19). Образцы картофеля ( n = 5) анализировали два раза в условиях повторяемости в соответствии с требованиями ГОСТ Р ИСО 5725-1-2002 «Точность (правильность и прецизионность) методов и результатов измерений» (М., 2009). Сок получали с помощью шнековой соковыжималки (Hyundai HY-JS4322, Южная Корея), отстаивали его в течение 20-30 мин до отделения осадка, надосадочную жидкость переносили в поилки для крыс. В качестве контроля использовали питьевую воду (ООО «Чистогорье», Россия).
Все лабораторные животные до начала эксперимента находились на карантине в течение 14 сут, ранее в опытах не участвовали, содержались согласно ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» (M., 2019) и ГОСТ 33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур» (M., 2016). Все манипуляции на животных выполняли в соответствии с Рекомендацией Коллегии Евразийской экономической комиссии от 14.11.2023 № 33 «О Руководстве по работе с лабораторными (экспериментальными) животными при проведении доклинических (неклинических) исследований» (M., 2023).
В эксперимент отбирали только здоровых особей, используя в качестве критериев массу тела и результаты клинического осмотра. Взвешивание осуществляли на весах CAS SW-10 (Южная Корея). Формирование групп животных и их маркировку проводили за 5 сут до начала эксперимента. Всего в эксперименте использовали 36 нелинейных аутбредных крыс-самцов 9-10-недельного возраста, каждая группа (в том числе контрольная) включала 9 животных. До начала эксперимента средняя масса тела животных составляла 277 г, что соответствовало возрасту половозрелых крыс (20). Отклонение массы тела животных в пределах одной экспериментальной группы не превышало 10 % от средней величины. В течение эксперимента крыс взвешивали еженедельно. Рассчитывали относительный прирост массы крыс за 28 сут (%) и абсолютный прирост за 14 сут (г).
Животных содержали в виварии барьерного типа в пластиковых клетках (55,5x39x29 см) по 9 особей в каждой. Клетки были установлены на расстоянии 20-30 см от наружных стен и в 3 м от источника отопления, ширина проходов между клетками составила 1 м. При проведении эксперимента в помещении поддерживали следующие параметры микроклимата: влажность 40-60 %, температура 18-20 ° C, световой режим 12 ч (день)/12 ч (ночь).
Каждое утро в течение 28 сут крысы опытных групп получали картофельный сок, особи контрольной группы — питьевую воду. Вечером поилки с соком убирали, до утра следующего дня животные всех групп получали питьевую воду. Базовый рацион во всех группах включал корм для лабораторных крыс и мышей Дельта Фидс (АО «БиоПро», Россия), отвечающий требованиям ГОСТ 34566-2019 «Комбикорма полнорационные для лабораторных животных. Технические условия» (М., 2019), в соответствии с инструкцией производителя.
Образцы крови получали до начала (фон) и на 28-е сут после начала эксперимента из подъязычной вены в стерильные вакуумные пробирки Lab-Vac объемом 2 мл (антикоагулянт EDTA К3, «Shandong Chengwu Medical Products», Китай).
Биомаркеры системного воспаления — индекс системного воспаления (Systemic Inflammation Index, SII), индекс системного воспалительного ответа (Systemic Inflammation Response Index, SIRI), совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index, AISI), соотношение числа нейтрофилов и лимфоцитов (Neutrophil to Lymphocyte Ratio, NLR), тромбоцитов и лимфоцитов (Platelet to Lymphocyte Ratio, PLR) и моноцитов и лимфоцитам (Monocyte to Lymphocyte Ratio, MLR) рассчитывали по формулам, приведенным в работе В.А. Шварца с соавт. (23).
Пробы фекалий крыс отбирали во время дефекации в стерильные контейнеры для биологического материала до начала (фон) и на 28-е сут эксперимента. Бактериологическое исследование проб проводили согласно рекомендациям для клинической микробиологии по выявлению условнопатогенных микроорганизмов методом серийных разведений (24). Готовили 10-кратные разведений суспензий фекалий в физиологическом растворе с посевом на агаризованные (энтерококкагар, среда Эндо, среда № 10, среды Чапека, Плоскирева, Левина, висмут-сульфит агар, цетримидный агар, среды Сабуро, Вильсон-Блера, гектоеновый агар, XLD-агар, мясопептонный агар скошенный) и жидкие (мясопептонный бульон, среда Китта-Та-роци, бульон стрептококк, магниевая среда, среда Бифидум) питательные среды. Инкубировали при температуре 37±1 ° С в течение 16-18 ч (висмут-сульфит агар — до 48 ч), среды Чапека и Сабуро — 24±1 ° С в течение 3-5 сут. Из первого разведения материал высевали бактериологической петлей секторами на чашки Петри по Голду, из остальных разведений на чашки Петри высевали по 0,1 мл. После инкубации колонии микроорганизмов подсчитывали и выражали в виде десятичного логарифма числа колониеобразующих единиц в расчете на 1 г фекалий (lg КОЕ/г).
Обработку данных методами описательной статистики и попарные сравнения с помощью U-теста Манна-Уитни выполняли в программе Jamovi 2.6.13 , «The Jamovi Project», Австралия), статистически значимыми считали различия при p < 0,05. В таблицах результаты анализа химического состава клубней выражали как среднее арифметическое (М) со стандартной ошибкой среднего (±SEM), массы тела крыс — как среднее арифметическое (М) и стандартное отклонение (±SD), данные иммунологических исследований — в виде медианы (Me) и интерквартильного размаха (Q1-Q3). Построение диаграмм проводили в программе Microsoft Excel 2023 («Microsoft Corporation», США). Для визуализации изменений массы тела крыс строили графики типа «ящик с усами» (boxplot) по результатам еженедельных взвешиваний. Верхние и нижние границы каждого «ящика с усами» формируют соответственно квартили 3 (Q3) и 1 (Q1), демонстрируя интерквартильный размах, внутри которого лежит 50 % центральной половины данных. Горизонтальная линия внутри графика показывает медиану, поперечный крест — среднее арифметическое значение. «Усы» отображают диапазон данных и их разброс за пределами интерквартильного размаха. Достоверные различия между парой исследуемых признаков обозначали пунктирной линией, указывали точное значение p-value. Для визуализации показателей иммунного профиля строили скрипичные диаграммы (violin plot). Форма «скрипки» отображает плотность распределения данных: широкие участки указывают на высокую плотность значений, узкие — на низкую. Асимметрия формы отражает скошенность распределения. Среднее арифметическое значение представляли черным квадратом внутри графика, фактические значения — серыми кругами. Верхняя граница графика соответствует максимальным значениям, нижняя — минимальным. Достоверные различия между парой исследуемых признаков отмечали пунктирной линией и указывали точное значение p-value. Для визуализации результатов микробиологических исследований строили гистограммы (bar chart).
Результаты . Исследование химического состава клубней, используемых для получения сока, показало вариабельность признаков в зависимости 668
от сортовой принадлежности картофеля (табл. 1).
1. Химический состав клубней разной пигментации у трех сортов картофеля
( n = 5, M ±SEM, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года)
|
Сорт |
Сухое вещество, % |
Крахмал, % |
Протеин, % |
Сахара, % |
Витамин С, мг% |
|
|
моно- |
ди- |
|||||
|
Багира (фиолетовый) |
19,2±4,4 |
13,4±3,7* |
2,38±1,54 |
0,29±0,05 |
0,19±0,01 |
55,9±7,5* |
|
Лила (розовый) |
17,9±4,2 |
12,2±3,5* |
1,50±1,22* |
0,31±0,05 |
0,10±0,01 |
75,7±8,7* |
|
Аляска (белый) |
23,0±4,8 |
17,2±4,1 |
2,06±1,44 |
0,45±0,06 |
0,00±0,00 |
17,2±4,1 |
Примечание. Измерения проводили 2 раза в условиях аналитической повторности.
* Различия между пигментированными и непигментированным сортами статистически значимы при p < 0,05.
Обнаружено, что сорта картофеля с окрашенными клубнями (фиолетовые и розовые) накапливают на 22,1-29,1 % (р < 0,05) меньше крахмала, чем с непигментированными (белый картофель). Содержание протеина в клубнях фиолетового и белого картофеля было схожим, а у розового оказалось ниже на 27,2 % (р < 0,05). Содержание сухого вещества в розовых клубнях по сравнению с другими исследуемыми образцами было наименьшим. В клубнях фиолетового и розового картофеля свободные углеводы были распределены между моно- и дисахарами, а в белом представлены исключительно моносахарами.
Самым вариабельным признаком оказалось содержание витамина С, которое в окрашенных клубнях было в 3,25-4,40 раза выше, чем в непиг-ментированных (см. табл. 1). Вероятно, высокое содержание антоцианов с выраженными антиоксидантными свойствами в картофеле с пигментированной мякотью (11) способствовало лучшему накоплению и меньшему расходованию витамина С на нейтрализацию свободных радикалов (25).
Результаты еженедельных взвешиваний крыс, получавших и не получавших картофельный сок, представлены в таблице 2 и на рисунке 1. Попарные различия по U-тесту Манна-Уитни показали, что масса тела крыс опытной группы, получавших сок из розовых клубней картофеля, была достоверно ниже, чем в контрольной группе, на 8,72 % к 14-м сут (U = 131; р = 0,025) и на 5,31 % к 28-м сут (U = 152; р = 0,044). При этом у животных, получавших сок из фиолетовых клубней картофеля, она была выше, чем у особей, получавшими сок из розовых клубней, на 9,00 % к 7-м сут (U = 92,5; р = 0,047), на 12,01 % к 14-м сут (U = 71,0; р = 0,007), на 8,05 % к 21-м сут (U = 93,0; р = 0,049) и на 8,15 % к 28-м сут (U = 74,0; р = 0,009).
2. Масса тела нелинейных аутбредных крыс (г) в эксперименте по выпаиванию картофельного сока из клубней с разной пигментацией ( M ±SD, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года)
|
Группа животных |
| Фон (до эксперимента) | |
7-е сут |
114-е сут | |
121-е сут |28-е сут |
|
Контроль (вода, n = 9) |
274±34 |
286±33 |
321±37 |
346±39 452±49 |
|
Опыт: |
||||
|
сок из фиолетовых клубней ( n = 9) |
299±39 |
289±33B |
333±41B |
348±40B 466±43B |
|
сок из розовых клубней ( n = 9) |
261±50 |
263±44 |
293±46a |
320±45 428±43a |
|
сок из белых клубней ( n = 9) |
276±34 |
283±28 |
314±32 |
332±30 458±37 |
Примечание. Референсным значением массы тела половозрелых крыс, используемых в эксперименте, принято считать 180-300 г (15).
A — попарные различия по U-тесту Манна-Уитни между опытными и контрольной группами статистически значимы при р < 0,05. B — попарные различия по U-тесту Манна-Уитни между опытными группами животных, получавших сок соответственно из картофеля с фиолетовой и розовой мякотью, статистически значимы при р < 0,05.
Все четыре группы животных за время эксперимента демонстрировали прирост массы тела (рис. 1). В контрольной группе относительный прирост массы тела за 28 сут составил 39,4 %, в группе, получавшей сок из фиолетового картофеля, — 35,8 %, из розового — 39,0 %, из белого — 39,7 %. Можно сделать вывод, что сок из розового и белого картофеля не оказал заметного влияния на относительный прирост массы тела (показатель в этих группах не отличался от контрольных значений). В группе крыс, получавших сок из фиолетового картофеля, относительный прирост массы тела оказался на 6,18 % (р < 0,05) ниже, чем в контроле (см. рис. 1).
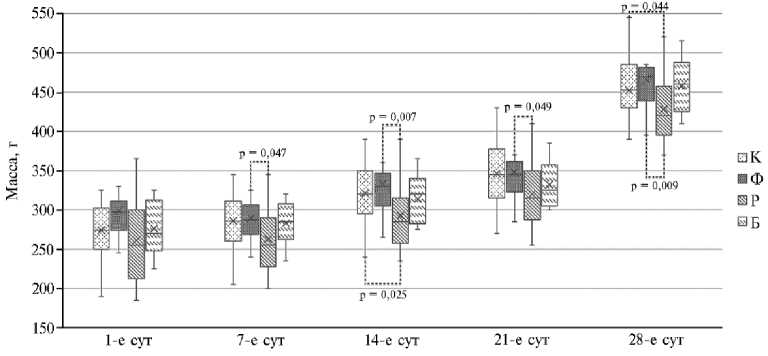
Рис. 1. Изменение массы тела у нелинейных аутбредных крыс в течение эксперимента по выпаиванию картофельного сока: К — контрольная группа, Ф, Р и Б — группы животных, получавших сок соответственно из фиолетового, розового и белого картофеля (все группы по n = 9, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года). Верхние и нижние границы каждого «ящика с усами» формируют квартили 3 (Q3) и 1 (Q1), соответственно, демонстрируя интерквартильный размах, внутри которого лежит 50 % центральной половины данных. Горизонтальная линия внутри графика показывает медиану, а поперечный крест — среднее арифметическое значение. «Усы» (от ящика вверх и вниз) отображают диапазон данных и их разброс за пределами интерквартильного размаха. Достоверные различия между парой исследуемых признаков по U-тесту Манна-Уитни обозначены пунктирной линией, указано точное значение p-value.
Однако, как сообщалось ранее (26), масса тела крыс — крайне вариабельный признак. Ретроспективный анализ результатов токсикологических испытаний с использованием лабораторных крыс, проведенный E. Gur с соавт. (26), показал, что при полной стандартизации содержания животных прирост массы различается даже между контрольными группами (26). В эксперименте по изучению влияния стандартного рациона (комбикорм Purina Chow 5001, Великобритания) на массу тела половозрелых крыс линии Sprague-Dawley были получены показатели абсолютного прироста от 13 до 102 г на 14-е сут и от 98 до 223 г на 50-е сут эксперимента (27). В нашем исследовании на 14-е сут отмечали абсолютный прирост 47 г в контрольной группе, 34 г в группе, получавшей сок из фиолетовых клубней, 32 г — из розовых и 38 г — из белых. Таким образом, наши результаты не позволяют говорить о заметном влиянии выпаивания картофельного сока на прирост массы тела животных и согласуются с опубликованными ранее данными (26, 27). Прирост массы тела у крыс всех четырех групп в настоящем исследовании можно считать естественным, без подозрения на гипертрофию жировой ткани.
Показатели иммунного профиля крыс до (фон) и в конце эксперимента представлены в таблице 3 и на рисунке 2.
Результаты бактериологических исследований фекалий крыс на 28-е сут эксперимента представлены на рисунках 3 и 4, соответственно. Важно отметить, что плесневые грибы, гемолизирующая Escherichia coli , Salmonella spp., Clostridium spp. и Pseudomonas aeruginosa в пробах не обнаружены.
3. Некоторые показатели иммунного профиля у нелинейных аутбредных крыс при выпаивании картофельного сока из фиолетовых (Ф) , розовых (Р) и белых (Б) клубней (группы по n = 9, Me [Q i ; Q 3 ], ФгБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года)
|
Показатель | |
Фон (до эксперимента) |
1 К | |
Ф |
1 Р 1 |
Б |
|
Лейкоциты, х109/л |
10,9 [9,39; 11,8] |
12,2 [10,5; 14,4] |
15,5 [13,6; 16,2] |
15,1 [12,7; 18,9] |
13,0 [11,7; 13,8] |
|
Лимфоциты, % |
68 [65; 71] |
64 [57; 75] |
70 [65; 71] |
64 [60; 75] |
68 [65; 69] |
|
Лимфоциты, х109/л |
5,9 [5,4; 6,2] |
8,4 [6,4; 9,4] |
9,3 [6,6; 10,7] |
8,2 [7,6; 10,3] |
7,5 [7,0; 8,2] |
|
Т-лимфоциты, % |
43 [40; 44] |
46 [43; 48] |
44 [42; 47] |
42 [35; 50] |
40 [37; 45] |
|
Т-лимфоциты, х109/л |
3,2 [2,9; 3,3] |
3,6 [3,0; 4,0] |
4,2 [3,5; 4,5] |
4,1 [3,0; 6,4] |
3,5 [3,0; 3,8] |
|
В-лимфоциты, % |
30 [24; 32] |
29 [22; 31] |
31 [30; 34] |
26 [25; 34] |
25 [24; 30] |
|
В-лимфоциты, *109/л |
1,8 [1,8; 2,4] |
2,2 [1,8; 2,4] |
2,7 [2,3; 3,8] |
2,7 [2,0; 3,4] |
2,2 [2,0; 2,5] |
|
Т/В-индекс |
1,5 [1,4; 1,8] |
1,6 [1,5; 1,9] |
1,3А [1,2; 1,5] |
1,6 [1,4; 1,7] |
1,5 [1,4; 1,6] |
|
Палочкоядерные нейтрофилы, % |
0 |
0 |
1 [0; 1] |
0 |
0,5 [0; 1,0] |
|
Сегментоядерные нейтрофилы, % |
22 [20; 24] |
24 [16; 32] |
26 [22; 28] |
28 [18; 32] |
25 [18; 27] |
|
Эозинофилы, % |
5,5 [3; 7,8] |
7,0 [5,0; 9,0] |
5,0 [4,0; 8,0] |
5,0 [2,0; 8,0] |
4,0 [2,0; 8,5] |
|
Базофилы, % |
0,50 [0; 1,0] |
0 |
0 |
0 |
0 |
|
Моноциты, % |
3,0 [2,3; 3,8] |
3,0 [2,0; 4,0] |
1,0 [0; 2,0]А , B |
2,0 [1,0; 2,0] |
4,0 [2,3; 4,3] |
|
Тромбоциты, *109/л |
977 [954; 1175] |
921 [865; 961] |
911 [867; 935] |
984 [941; 1110] |
901 [791; 1000] |
|
Фагоцитарная активность, % |
40 [37; 42] |
44 [42; 46] |
43 [41; 49] |
44 [39; 46] |
42 [39; 45] |
|
Фагоцитарный индекс, у.е. |
5,6 [5,1; 5,7] |
3,6 [3,5; 3,9] |
5,0 [4,2; 5,4]А |
4,5 [4,4; 4,9]А |
4,5А [4,0; 4,8] |
|
SIRI |
1,0 [0,6; 1,4] |
0,85 [0,48; 1,03] |
0,46 [0; 0,86] B |
0,62 [0,37; 1,31] |
1,5 [0,90; 1,6] |
|
SII |
334 [315; 364] |
347 [196; 503] |
334 [272; 468] |
430 [232; 553] |
287 [253; 330] |
|
AISI |
826 [664; 1272] |
786 [391; 988] |
468 [0; 778] B |
608 [430; 1169] |
1253 [613; 1535] |
|
NLR |
0,33 [0,30; 0,38] |
0,39 [0,21; 0,62] |
0,37 [0,31; 0,46] |
0,44 [0,23; 0,57] |
0,37 [0,28; 0,40] |
|
PLR |
169 [141; 212] |
119 [106; 145] |
93 [85; 131] |
129 [97; 139] |
121 [103; 145] |
|
MLR, х10 - 2 |
4,6 [3,0; 5,6] |
3,7 [3,1; 5,7] |
1,5 [0; 3,0] B |
2,6 [1,4; 4,4] |
5,9 [3,9; 6,6] |
Примечание. SIRI — systemic inflammation response index (индекс системного воспалительного ответа), SII — systemic inflammation index (индекс системного воспаления), AISI — aggregate inflammation systemic index (совокупный индекс системного воспаления), NLR — neutrophil to lymphocyte ratio — отношение нейтрофилов к лимфоцитам, PLR — platelet to lymphocyte ratio (соотношение числа тромбоцитов и лимфоцитов), MLR — monocyte to lymphocyte ratio (соотношение числа моноцитов и лимфоцитов). Фон — фоновые значения (до эксперимента), К — контрольная группа, Ф, Р и Б — опытные группы животных, получавших сок соответственно из фиолетового, розового и белого картофеля.
А — попарные различия по U-тесту Манна-Уитни между опытными и контрольной группами статистически значимы при p < 0,05. B — попарные различия по U-тесту Манна-Уитни между опытными группами животных, получавших сок соответственно из картофеля с пигментированный и непигментированной мякотью, статистически значимы при p < 0,05.
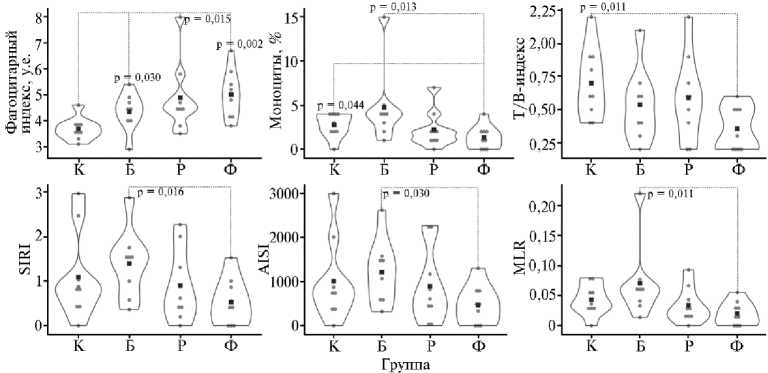
Рис. 2. Попарное сравнение некоторых показателей иммунного профиля у нелинейных аутбредных крыс (U-тест Манна-Уитни) на 28-е сут выпаивания картофельного сока между контрольной группой (К, вода) , группой, получавшей сок из белых (Б) , розовых (Р) и фиолетовых (Ф) клубней. Форма скрипичной диаграммы (violin plot) отражает плотность распределения данных. Верхняя граница диаграммы — максимальное значение в группе, нижняя граница — минимальное значение. Внутри диаграммы располагаются фактические значения (серые точки). Черный квадрат — среднее значение. Прерывистые линии связывают пары сравнения, в которых выявлены статистически значимые различия (р < 0,05) с точным значением p-value (группы по n = 9, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года).
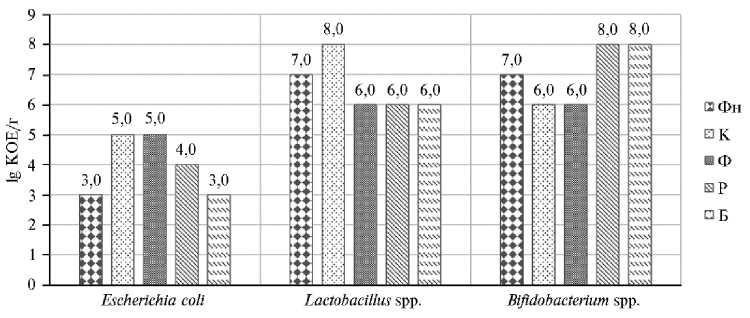
Рис. 3. Присутствие основных представителей нормофлоры в кишечнике нелинейных аутбредных крыс на 28-е сут выпаивания картофельного сока . Фн — фоновые значения (до эксперимента), К — контрольная группа (вода), Ф, Р, Б — группы крыс, получавшие сок соответственно из фиолетовых, розовых и белых клубней картофеля (группы по n = 9, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года). Референсные значения (lg КОЕ/г фекалий): E. coli — 7,0-8,0; Lactobacillus spp. — 5,0-8,0; Bifidobacterium spp. — 7,0-9,0 (29).
Установлено, что у животных, получавших картофельный сок, изменился состав нормальной микрофлоры кишечника (см. рис. 3). У крыс, которым выпаивали сок из фиолетового картофеля, содержание в фекалиях E. coli, относящейся к нормофлоре, выросло на 66,6 %, а Bifidobacterium spp. и Lactobacillus spp. снизилось относительно фоновых значений на 14,3 %, однако по сравнению с контролем существенно не изменилось, за исключением лактобактерий (снизилось на 33,3 %). Включение в рацион крыс сока из розового и белого картофеля привело к снижению численности Lactobacillus spp. по сравнению как с фоновыми (на 14,3 %), так и с контрольными значениями (на 25,0 %). В отношении Bifidobacterium spp. экспери- ментальная диета оказывала противоположное действие, существенно (соответственно на 14,3 и 33,3 % по сравнению с фоновыми и контрольными значениями) увеличивая популяцию этих бактерий к 28-м сут опыта. Применение сока из розового картофеля спровоцировало заметный (на 33,3 %) по сравнению с фоном рост популяции E. coli, относящейся к нормальной микрофлоре кишечника, но меньший, чем у особей из контрольной группы. В группе крыс, получавших сок из белого картофеля, такого эффекта не отмечали.
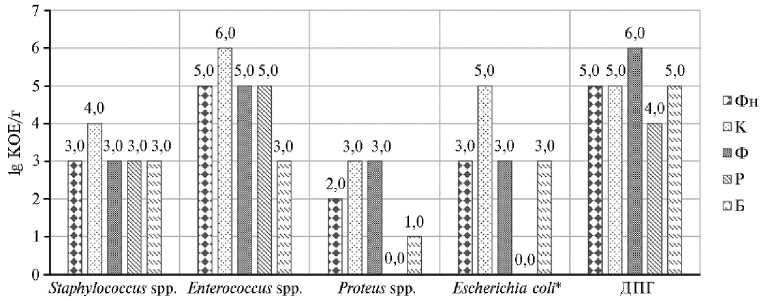
Рис. 4. Присутствие основных представителей условно-патогенных микроорганизмов в кишечнике нелинейных аутбредных крыс на 28-е сут выпаивания картофельного сока . Фн — фоновые значения (до эксперимента), К — контрольная группа (вода), Ф, Р, Б — группы, получавшие сок соответственно из фиолетовых, кишечника крыс (группы по n = 9, ФГБНУ УрФАНИЦ УрО РАН, октябрь-ноябрь 2023 года). Референсные значения (lg КОЕ/г фекалий): Staphylococcus spp. — 2,0-4,0; Enterococcus spp. — 5,0-7,0; Proteus spp. — 2,0-4,0; E. coli* — 2,0; ДПГ (дрожжеподобные грибы) — 2,0-5,0 (29).
Наши данные согласуются с результатами более ранних работ на мышах по изучению действия сырого картофеля (14) и картофельного крахмала (17). На фоне растительной диеты в фекалиях грызунов обычно одновременно повышается численность бифидо- и лактобактерий (28), однако для крыс более физиологичным считается преобладание Bifidobacterium spp. над Lactobacillus spp. (29).
Мы предполагаем, что относительное угнетение роста Lactobacillus spp. связано с низким содержанием в картофеле (см. табл. 1) и получаемом из него соке свободных моно- (глюкозы, фруктозы, галактозы) и дисахаридов (лактоза и сахароза) (30), которые необходимы для нормального энергетического обмена этих бактерий, но не высвобождаются из сырого крахмала, на долю которого приходится до 92,0 % всех углеводов картофеля (10) в процессе пищеварения (31). Известно, что бактерии рода Lactobacillus spp., присутствующие в кишечнике, участвуют в регуляции иммунного гомеостаза за счет поддержания популяции Т-регуляторных клеток (Treg), выделяющих противовоспалительные цитокины (IL-10, IL-17 и IL-22), в восстановлении баланса провоспалительных цитокинов и поддержании соотношения Th17/Treg (32). Помимо этого, лактобактерии ответственны за регулирование целостности эпителиального барьера кишечника, поддержание его муцинового слоя, а также выработку противомикробных пептидов (33).
Виды рода Bifidobacterium spp. являются представителями индиген-ной микрофлоры кишечника (29). В нашем исследовании их число не изменилось в группе, получавшей сок фиолетового картофеля, по сравнению с контролем, однако возросло в группах, получавших сок из розового и белого картофеля (см. рис. 3). В отличие от Lactobacillus spp. у Bifidobacterium spp. имеются гены, ответственные за метаболизм сложных углеводов, в том числе крахмала (34), чем объясняется увеличение их относительного содержания в кишечной микробиоте крыс из опытных групп. Более того, выявленные изменения в микробиоте кишечника крыс, получавших сок из картофеля с пигментированной мякотью клубней, могут быть связаны со способностью Bifidobacterium spp. к метаболизму антоцианов (35, 36). Поскольку в эксперименте для получения сока мы использовали два сорта картофеля с пигментированной мякотью клубней (фиолетовый и розовый), а рост обилия Bifidobacterium spp. в микробиоте кишечника удалось обнаружить лишь в группе крыс, которым выпаивали сок из розового картофеля, можно предположить, что не все антоцианы одинаково метаболизируются кишечной микробиотой. Увеличение доли бифидобактерий в микробиоте кишечника может опосредованно влиять на иммунный статус животных (5). Известно, что бактерии Bifidobacterium spp. ответственны за ингибирование энтеропатогенов за счет продукции органических кислот, антибактериальных пептидов, ингибиторов кворум-сенсинга (34). В экспериментальных исследованиях на новорожденных телятах рост представленности бифидобактерий сопровождался снижением численности условно-патогенных микроорганизмов (патогенной E. coli, Clostridium spp. и др.) и числа случаев диареи при повышении среднесуточных приростов массы тела животных (35). Более того, иммунная стимуляция с участием Bifidobacterium spp. осуществляется за счет их взаимодействия с дендритными клетками, что приводит к улучшению иммунного гомеостаза в кишечнике (32). Во всех экспериментальных группах в образцах периферической крови крыс было отмечено увеличение фагоцитарного индекса: на 20,0 % для групп, получавших сок из розового (U = 12,5; p = 0,015) и белого (U = 13,0; p = 0,030) картофеля, и на 25,0 % — из фиолетового картофеля (U = 5,50; p = 0,002), при этом без существенных изменений в лейкоцитарной формуле, за исключением численности моноцитов (см. табл. 3 и рис. 2). Их содержание у животных, получавших сок из фиолетового картофеля, уменьшилось по сравнению с контролем на 66,7 % (U = 18,0; p = 0,044). Также у них уменьшился Т/В-индекс на 18,5 % (U = 11,5; p = 0,011) за счет снижения относительного содержания Т-лимфоцитов и увеличения — В-лимфоцитов.
Известно, что при ферментации пищевых волокон продуцируемые Bifidobacterium spp. короткоцепочечные жирные кислоты (КЦЖК), к которым относятся пропионат, бутират и ацетат, усиливают способность тканевых макрофагов собственной пластинки кишечника к фагоцитозу патогенных бактерий (37). Также КЦЖК влияют на нейтрофилы периферической крови: они увеличивают их хемотаксис (способность мигрировать к участкам инфекции и воспаления) и фагоцитарную активность (38). В дополнение присутствующие в соке пигментированного картофеля антоцианы напрямую воздействуют на макрофаги и нейтрофилы: они дезактивируют избыточно продуцируемые активные формы кислорода и нетоз (выброс нейтрофильных клеточных ловушек) (39). Все это предотвращает повреждение тканей собственными иммунными клетками и воспаление (39).
Ось Bifidobacterium spp.—КЦЖК—иммунные клетки кишечника стала главным эффекторным звеном метаболизма, через которое свежевыжатый картофельный сок проявил иммуномодулирующее действие. На фоне длительного применения трех видов соков из картофеля были отмечены общие положительные тенденции в уменьшении численности условно-патогенных бактерий ( Staphylococcus spp., Enterococcus spp., Proteus spp., E. coli со слабо-выраженными ферментативными свойствами) (см. рис. 4). Сок из розового картофеля снизил содержание в фекалиях крыс Staphylococcus spp. на 15,0 %, 674
Enterococcus spp. на 16,7 %, дрожжеподобных грибов — на 20,0 %, при этом Proteus spp. и E. coli со слабовыраженными ферментативными свойствами в исследованных образцах выявить не удалось. Под действием сока из белого картофеля у экспериментальных животных также отмечалась тенденция к снижению представленности в фекалиях Staphylococcus spp. на 15,0 %, Enterococcus spp. на 40,0 %, Proteus spp. на 66,7 % и E. coli со слабовыраженными ферментативными свойствами на 40,0 %. Все описанные эффекты, вероятно, сформировались благодаря возросшей численности бактерий рода Bifidobacterium spp. в микробиоте кишечника крыс и, как следствие, увеличенной продукции КЦЖК, обладающих регулирующим действием на иммунные клетки кишечника (37-39). Их активация привела к подавлению роста условно-патогенной микрофлоры (см. рис. 4).
В группе крыс, получавших сок из фиолетового картофеля, также регистрировали уменьшение численности условно-патогенной микробиоты кишечника: Staphylococcus spp. на 15,0 %, Enterococcus spp. на 16,7 %, E. coli со слабовыраженными ферментативными свойствами на 40,0 %, при этом содержание в фекалиях Proteus spp. не изменилось, а дрожжеподобных грибов повысилось на 16,7 %. В этой группе животных изменения в численности условно-патогенной микробиоты кишечника связаны не с активацией оси Bifidobacterium s pp.—КЦЖК—иммунные клетки кишечника, а с прямым действием антоцианов сока картофеля на клетки иммунной системы. Как было указано выше, у картофеля с фиолетовой мякотью клубней их окраска обеспечивается за счет высокого содержания антоцианов петунидина и дельфинидина (10, 11). Последние обладают способностью изменять функциональную активность клеток иммунной системы (6). Так, в группе крыс, получавших сок из фиолетового картофеля, было отмечено снижение относительного содержания моноцитов. Этот эффект, отсутствующий у животных других групп, объясняется способностью петунидина и дельфинидина ингибировать транскрипцию фактора NF- k B за счет торможения деградации ингибитора 1 к В а , который сохраняет фактор NF- k B в неактивной форме (6, 40). В свою очередь, это приводит к уменьшению секреции провоспали-тельных цитокинов (TNF- a , IL-6, IL-1 e ) и медиаторов (COX-2, iNOS) (40). В дополнение оба антоциана потенцируют созревание дендритных клеток эпителия кишечника и снижают активацию Т-лимфоцитов макрофагами (40). Вероятно, из-за этого в группе крыс, получавших сок из фиолетового картофеля, было отмечено снижение Т/В-индекса за счет уменьшения относительного содержания Т-лимфоцитов и увеличения доли В-лимфоцитов (см. табл. 3, рис. 2). Ограничение размножения условно-патогенной микробиоты кишечника животных в эксперименте могло быть достигнуто за счет увеличения популяции зрелых дендритных клеток, способных захватывать живые условно-патогенные бактерии без нарушения целостности эпителиального барьера (41). При сравнительном анализе иммунного профиля крыс, получавших сок из белого и фиолетового картофеля, мы обнаружили, что у последних уровень моноцитов в крови был ниже на 75,0 % (U = 10,0; p = 0,013), как и значения биомаркеров системного воспаления: индекса системного воспалительного ответа SIRI на 69,3 % (U = 10,5; p = 0,016), совокупного индекса системного воспаления AISI на 62,3 % (U = 13,0; p = 0,030), отношения числа моноцитов к числу лимфоцитов MLR на 74,6 % (U = 9,0; p = 0,011) (см. табл. 3, рис. 2). Эти данные подтверждают противовоспалительные свойства сока из фиолетового картофеля.
В отношении бактерий E. coli, принадлежащих к нормальной микрофлоре, в группе, получавшей сок из фиолетового и белого картофеля, не отмечено какого-либо эффекта по сравнению с контролем. В то же время включение в рацион сока из розового картофеля стимулировало рост E. coli, относящейся к нормальной микрофлоре, в кишечнике крыс (см. рис. 3). Однако, как и в случае с Lactobacillus spp., рост относящейся к нормальной микрофлоре кишечника E. coli был ограничен отсутствием у этих бактерий ферментов гидролаз, способных к перевариванию полисахаридов (в том числе крахмала) (42). В качестве источников энергии такая E. coli использует моносахариды, дисахариды, некоторые полисахариды из муцинового слоя, многоатомные спирты и сахарные кислоты (42). Кроме того, коммен-сальные E. coli более консервативны в отношении питательных веществ, чем патогенные E. coli (43).
Обобщая результаты эксперимента и данные литературы (12, 44), можно говорить о том, что дополнение основного рациона лабораторных крыс картофельным соком не вызывало каких-либо негативных последствий. Животные набирали массу тела в пределах физиологических границ, у них отсутствовали признаки метаболических нарушений (44), дисбиоза кишечника (см. рис. 3 и 4), гематологические маркеры аллергии и воспаления (см. табл. 3). В настоящем исследовании в качестве модели мы использовали по одному сорту картофеля из каждой группы: с белой, розовой и фиолетовой окраской мякоти. Основные биологические эффекты, по-види-мому, были связаны не с макро- (см. табл. 1), а с микронутриентным составом клубней и получаемого из них сока (45). В дальнейшем целесообразно расширить сортовой состав каждой группы для выявления особенностей биологического действия соков с учетом индивидуальных сортовых характеристик картофеля (содержание сухого вещества, протеина, крахмала, сахаров и витаминов, макро- и микроэлементов).
Таким образом, в представленном исследовании впервые было изучено влияние сока из неочищенных клубней картофеля различных сортов (по одному сорту с фиолетовой, розовой и белой окраской мякоти) на иммунный профиль и микробиоту кишечника крыс. Установлено, что химический состав клубней картофеля определяет характер метабиотического и иммуномодулирующего действия получаемых из них соков. Соки из розового (сорт Лила) и белого (сорт Аляска) картофеля повышали представленность бактерий рода Bifidobacterium spp. в микробиоте кишечника на 25,0 %, способствовали снижению численности условно-патогенных микроорганизмов ( Staphylococcus spp. на 15,0 %, Enterococcus spp. на 16,7-40,0 %, Proteus spp. на 66,7 %, Escherichia coli со слабовыраженными ферментативными свойствами на 40,0 %, дрожжеподобных грибов на 20,0 %) и увеличивали фагоцитарную активность нейтрофилов крови на 20,0 % (U = 12,5; p = 0,015 и U = 13,0; p = 0,030 соответственно в группе крыс, получавших сок из розового и белого картофеля). Сок из фиолетового (сорт Багира) картофеля, богатый петунидином и дельфинидином, оказывал прямое действие на клетки иммунной системы: снижал число моноцитов в крови на 66,7 % (U = 18,0; p = 0,044) и Т/В-индекс на 18,5 % (U = 11,5; p = 0,011), что может быть связано с ингибированием провоспалительных путей через NF- к В-зависи-мые механизмы. Результаты исследования показали, что длительное (28 сут) применение соков из клубней картофеля, особенно с пигментированной мякотью, может рассматриваться как способ нутритивной коррекции иммунного профиля и кишечной микробиоты у моногастричных животных и человека. Перспективы предлагаемого нами подхода далее будут определяться исследованиями механизмов взаимодействия антоцианов и короткоцепочечных жирных кислот с клетками иммунной системы, а также результатами доклинических и клинических испытаний на других биологических объектах.
ËÈÒÅÐÀÒÓÐÀ
ФГБНУ Уральский федеральный аграрный Поступила в редакцию научно-исследовательский центр 4 июня 2024 года
Уральского отделения РАН, Принята к пубёикации
620142 Ðîññèÿ, ã. Åêàòåðèíáóðã, óë. Áåëèíñêîãî, 112à, 30 èþëÿ 2024 ãîäà
Sel’skokhozyaistvennaya biologiya [ Agricultural Biology ], 2025, V. 60, № 4, pp. 664-680
EFFECTS OF POTATO JUICE ON SOME INDICATORS OF IMMUNE PROFILE AND INTESTINAL MICROBIOTA IN RATS
The authors declare no conflict of interests
Acknowledgements:
Supported within the framework of the state assignment of the Ministry of Science and Higher Education of the Russian Federation (state registration No. 0532-2021-0008 and No. 0532-2021-0009)


