Влияние комплексообразователя пирокатехина на извлечение из гальваношлама никеля и гидроксида никеля и изучение характеристик электродов, изготовленных из Ni(OH)2
Автор: Ольшанская Л.Н., Лазарева Е.Н., Яковлева Е.В.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Экология - технические науки
Статья в выпуске: 5 т.23, 2021 года.
Бесплатный доступ
Рассмотрены проблемы предприятий химической и машиностроительной отраслей промышленности, оказывающих негативное воздействие на состояние окружающей природной среды. Имеющиеся в их структуре гальванические цеха и участки относятся к категориям 1-3 классов опасности вследствие использования растворов и образующихся сточных вод, содержащих различные тяжелые металлы. На территории этих цехов образуется и накапливается большое количество гальванических шламов (ГШ), содержащих такие токсичные компоненты, как никель, цинк, железо, медь, хром, свинец, кадмий и др., оказывающих высокое токсичное, канцерогенное и мутагенное воздействие на живые организмы. Однако при нахождении эффективного способа переработки, ГШ могут служить источником получения ценных компонентов, в частности металлов и их соединений. В работе проведено избирательное извлечение ионов никеля, содержащихся в гальваническом шламе, в раствор при добавках пирокатехина (ПК) в диапазоне концентраций 50-250 г/л (шаг 50 г/л). Установлено, что оптимальная концентрация пирокатехина для извлечения ионовNi2+составила Спк=50 г/л. С увеличением концентрации ПК концентрация извлеченных ионов никеля растет (от 12,4 до 18,2 мг/мл),однако при высоких концентрациях ПК (100 ÷ 250 г/л) образуется густая суспензия, практически не поддающаяся фильтрованию. При последующей обработке полученного раствора 40% NaOH в диапазоне рН=7,2 ÷9,5 был осажден гидроксид Ni(OH)2, который удовлетворял требованиям ТУ 4836390 «Никеля гидрат закиси». Он был использован в качестве компонента активной массы катодов никель- кадмиевых (железных) аккумуляторов. Изучены электрохимические характеристики полученных катодов и показано, что по своим рабочим параметрам они не уступают промышленным Ni(OH)2электродам. В результате проведенных экспериментов установлено, что предлагаемая технология извлечения гидроксида никеля из металлсодержащего гальваношлама может применяться для изготовления активной массы катодов никель-кадмиевых (железных) аккумуляторов и является перспективной.
Металлсодержащие гальванические шламы, комплексон пирокатехин, извлечение никеля, гидроксид никеля, характеристики катодного материала
Короткий адрес: https://sciup.org/148323597
IDR: 148323597 | УДК: 622.544 | DOI: 10.37313/1990-5378-2021-23-5-90-95
Influence of the pyrokatekhin complex forming agent on the extraction of nickel and nickel hydroxide from galvano slides and the study of characteristics of electrodes made from Ni(OH)2
The problems of enterprises of the chemical and machine-building industries, which have a negative impact on the state of the natural environment, are considered. The galvanic workshops and areas available in their structure belong to categories 1-3 of hazard classes due to the use of solutions and the resulting wastewater containing various heavy metals. On the territory of these workshops, a large amount of galvanic sludge (GS) is formed and accumulates, containing such toxic components as nickel, zinc, iron, copper, chromium, lead, cadmium, etc., which have a high toxic, carcinogenic and mutagenic effect on living organisms. However, when finding an effective method for processing, GS can serve as a source of obtaining valuable components, in particular metals and their compounds. The work carried out selective extraction of nickel ions contained in galvanic sludge into a solution with addition of pyrocatekhin (PC) in the concentration range of 50-250 g/l (step 50 g/l). It was found that the optimal concentration of catechol for the extraction of Ni2+ ions was Cpc = 50 g/l. With an increase in the concentration of PC, the concentration of extracted nickel ions increases (from 12.4 to 18.2 mg / ml), however, at high concentrations of PC (100-250 g / L), a thick suspension is formed, which is practically not amenable to filtration. During the subsequent processing of the resulting solution of 40% NaOH in the range of pH = 7.2 ÷ 9.5, Ni(OH)2 hydroxide was precipitated, which met the requirements of TU 48 3 63 90 “Nickel nitrous hydrate”. It was used as a component of the active mass of nickel-cadmium (iron) battery cathodes. The electrochemical characteristics of the obtained cathodes have been studied and it has been shown that, in terms of their operating parameters, they are not inferior to industrial Ni(OH)2 electrodes. As a result of the experiments, it was found that the proposed technology for extracting nickel hydroxide from metal-containing galvanic sludge can be used to manufacture the active mass of nickel-cadmium (iron) batteries cathodes and is promising.
Текст научной статьи Влияние комплексообразователя пирокатехина на извлечение из гальваношлама никеля и гидроксида никеля и изучение характеристик электродов, изготовленных из Ni(OH)2
В настоящее время все без исключения предприятия оказывают негативное воздействие на состояние окружающей природной среды. Особенно это касается химической отрасли и машиностроения, где имеются гальванические цеха и участки. Опасность обусловлена не только образованием и воздействием вредных по составам растворов и образующихся сточных вод, но и накоплением большого количества гальванических шламов (ГШ), содержащих такие токсичные компоненты, как
никель, цинк, железо, медь, хром, свинец, кадмий и др.
Вместе с тем при нахождении эффективной технологии утилизации эти компоненты могут стать источником необходимых производствам металлов и материалов. Оптимальной является утилизация ГШ, проводимая последовательно в две стадии:
Первая стадия - избирательное извлечение тяжелых металлов путем химического выщелачивания металлов из осадков и селективного осаждения соединений металлов при различных значениях кислотности растворов [2], электрохимического извлечения [3,4], а так же взаимодействием с комплексообразователями [5]. В дальнейшем извлеченные компоненты можно применять для получения металлов и сплавов, пигментов-наполнителей, стеклоизделий, глазурей, иммобилизировать в полимерную матрицу, использовать для изготовления полиоксидных катализаторов [6], электродов никель-кадмиевых (Ni-Cd) и никель-железных (Ni-Fe) аккумуляторов [7] и др.
На второй стадии осуществляется утилизация пустых шламов при изготовлении, строительных материалов, дорожных покрытий, новых композиционных материалов и сорбентов [8]. Двухэтапная технология переработки ГШ позволяет получить необходимое производству сырье и снизить класс опасности образующихся отходов. Таким образом, нахождение оптимального способа утилизации гальваношламов с получением полезных компонентов, а так же изучение оптимальных условий их проведения, является актуальной и своевременной задачей.
Целью настоящей работы явилось проведение поэтапного извлечения ионов никеля и Ni(OH)2 из раствора гальваношлама в присутствии ком-плексообразователя пирокатехина, получение Ni(OH)2-катодов, изготовленных на основе полученного гидроксида никеля для NiCd(Fe) аккумуляторов и изучение циклических характеристик этих электродов.
МЕТОДИКА ИССЛЕДОВАНИЙ
Объектом исследований явился ГШ, образующийся после ванн никелирования и активации имеющий состав, приведенный в таблице 1.
Предварительная обработка ГШ заключалась в разведении его водой. Полученная суспензия характеризовалась кислотностью со значением рН = 8,7,определенной с помощью ионометрического преобразователя марки И-500.Авторами [5] было показано, что для проведения селективного извлечения ионов никеля из гальваношламов в качестве ком-плексообразователя можно использовать комплексон пирокатехин (рис. 1). Комплексоны образуют прочные соединения с ионами металлов. В этом отношении они превосходят большинство других химических соединений, которые способны быть лигандами в комплексах металлов.C помощью комплексонов можно селективно извлекать ценные компоненты из ГШ с целью их возврата в промышленное производство или другие отрасли народного хозяйства, уменьшать степень и, соответственно, класс опасности ГШ за счет снижения содержания в них высокотоксичных металлов, получать водорастворимые комплексонаты металлов. Наибольшей избирательной способностью по отношению к ионам никеля характеризуется пирокатехин[5], который был выбран нами для проведения дальнейших исследований.
Рис. 1. Стехиометрическая формула пирокатехина С6Н4(ОН)2[9]
С6Н4(ОН)2 легко растворим в воде (43 г в 100 мл воды), это белые или бесцветные моноклинные кристаллы с запахом фенола. Пирокатехин имеет молекулярную массу (в а.е.м.): 110,12, температуру плавления tпл=105 оС, температуру кипения tкип.= 245,9оС[9]. На свету и воздухе окрашивается в коричневый цвет [10], поэтому хранили его в темной химической посуде ГОСТ 25336-82 [11].
Проведено извлечение ионов никеля при добавке пирокатехина (ПК) в количестве от 0 до 250 г/л. При этом кислотность растворов ГШ изменялась в диапазоне от 8,7 (без добавок) до 5,43 (250 г/л ПК). Полученные вытяжки исследовали фотоколориметрическим методом на спектрофотометре ПромЭкоЛаб ПЭ5300В. Состав выделенного из ГШ гидроксида никеля определяли согласно ТУ 4836390 «Никеля гидрат закиси» [12], содержание никеля определяли комплексонометрическим и титриметрическим (с трилоном Б) методами; содержание добавок железа и магния определяли атомно-адсорбционным методом.
Готовили катоды при добавлении необходимых компонентов в активную массу и изучали их циклическиезарядно-разрядные характеристики на потенциостате марки Р-30 при постоянных токах в трехэлектродной ячейке с разделенным фильтрами Шотта катодным и анодным пространствами, что позволяет предотвратить смешение продуктов реакции. В качестве рабочих электродов использованы изготовленные нами электроды; вспомогательными электродами служили пластины из легированной стали, электродом сравнения – нормальный хлорсеребряный электрод; рабочим электролитом –про-изводственный щелочной раствор КОН+10 г/л LiOH (плотность 1,191,21 г/см3), взятый с ПАО «Завод автономных источников тока» («ЗАИТ») г. Саратова.
Все эксперименты проведены в 3-5 параллельных измерениях, доверительный интервал не превышал 92-95 %.
Таблица 1 – Состав гальваношлама после ванн никелирования и активации
|
Состав ГШ |
Ионы никеля |
Ионы железа, |
Ионы цинка |
Ионы меди |
Сульфат - ионы |
|
Содержание, % |
44 |
0,67 |
0,58 |
0,003 |
6,4 |
ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ И ИХ ОБСУЖДЕНИЕ
На основании полученных данных по извлечению ионов никеля пирокатехином была определенаих концентрация в растворах. Результаты измерения оптической плотности растворов, приготовленных на основе ГШ при различных добавках пирокатехина, и концентрации ионов никеля в растворах приведены в таблице 2.
Выявлено, что повышение добавок пирокатехина от 50 до 250мг/мл приводит к увеличению концентрации ионов никеля в растворе от 12,4 мг/мл (Спк=50 г/л) до 18,2 мг/мл (Спк=250 г/л), однако при высоких концентрациях ПК(100 ÷ 250 г/л) образуется густая суспензия, практически не поддающаяся фильтрованию.
Известно, что все металлы различаются своими строго индивидуальными значениями рН (табл. 3), при которых они выпадают из растворов в виде нерастворимых в воде гидроксидов [13]. Для осаждения гидроксида никеля из растворов ГШ с различными добавками ПК проводили их щелочную обработку 40% раствором NaOH, в результате в диапазоне рН≈7,2-9,5 осаждался Ni(OH)2.
Полученные результаты анализа состава выделенного из гальваношлама гидроксида никеля и определенного согласно [12] приведены в таблице 4.
Установлено, что наибольшее количество ионов никеля (29,9 %) присутствует в Ni(OH)2, полученном при введении в водный раствор пирокатехина концентрации 50 г/л. Эта добавка (Спк=50 г/л) выбрана нами для последующего извлечения Ni(OH)2, используемого для изготовления катодов никель-кадмиевых (железных) аккумуляторов.
Состав активной массы изготовленных нами электродов соответствовал составу катодов промышленных аккумуляторных батарей ПАО «ЗАИТ» (табл. 5).
На следующем этапе проведено изучение электрохимических характеристик изготовленных катодов. Заряд электродов проводили в гальваностатическом режиме при постоянной плотности тока (при iЗ=10 мА/см2). Разряд сформированных электродов (рис. 2) осуществляли в диапазоне плотностей тока iр=40÷120мА/см2 (шаг 20 мА/см2).
На основании полученных данных построены графики зависимости изменения емкости сформированных электродов от времени разряда (рис. 3). Анализ полученной зависимости позволил выбрать ток разряда (iр=80мА/см2), при котором достигается наибольшая отдаваемая емкость. При больших и меньших плотностях тока наблюдаются скачкообразные изменения величины потенциала, свидетельствующие о неустойчивом состоянии и, возможно, возникновении дополнительных изменений в структуре электродов.
Для обоснования возможности использования катодов, изготовленных по технологии с пирокатехином, проводили сравнительное определение емкостных характеристик разработанных нами и промышленных (ПАО «ЗАИТ»)
Таблица 2 – Изменение концентрации ионов никеля в растворе при различных добавках ПК
|
Концентрация пирокатехина, г/л |
0 |
50 |
100 |
150 |
200 |
250 |
|
Оптическая плотность, А |
1,870 |
1,964 |
2,125 |
2,439 |
2,789 |
|
|
Концентрация №2М03, мг/мл |
12,4 |
13,2 |
14,2 |
16,1 |
18,2 |
Таблица 3 – Ряд осаждения гидроксидов металлов из кислого раствора [13]
|
Ион |
Fe (lll) |
Cr (lll) |
Cu (ll) |
Zn (ll) |
Fe (ll) |
Ni (ll) |
Mn (ll) |
Mg(ll) |
|
рН* |
1,5*-4,1** |
4,0-6,8 |
5,3-6,2 |
5,4-8,0 |
6,5-9,7 |
7,2-9,5 |
7,8-10,4 |
9,4-12,4 |
* первая цифра – начало осаждения; **вторая – полное осаждение гидроксида
Таблица 4 – Состав гидроксида, полученного из ГШ с различным содержанием ПК
|
Концентрация ионов металлов в Ni(OH) 2 , мг/мл |
С пк , г/л |
|||||
|
0 |
50 |
100 |
150 |
200 |
250 |
|
|
Ni2+ |
0,4 |
29,9 |
24,6 |
23,1 |
18,9 |
18,7 |
|
Fe2+ |
0,0 |
8,3 |
6,9 |
6,2 |
5,2 |
5,1 |
|
Mg2+ |
0,00 |
0,04 |
0,03 |
0,03 |
0,02 |
0,02 |
Таблица 5 – Состав активной массы для изготовления катода на основе Ni(OH)2
|
Вещество |
Ni(OH) 2 |
CoSO 4 |
Графит |
Ba(OH) 2 |
KOH |
|
Количество, % |
34,4 |
2,4 |
18,4 |
2,6 |
9,1 |
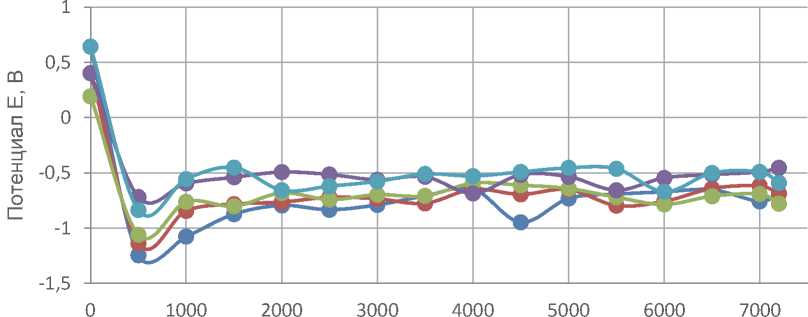
Время t, c
-120 -100 -80 -60 -40
Рис. 2. Зависимости E,t для электродов, изготовленных с использованием Ni(OH)2, полученного при добавке в раствор Спк=50 г/л при iр=40÷120мА/см2
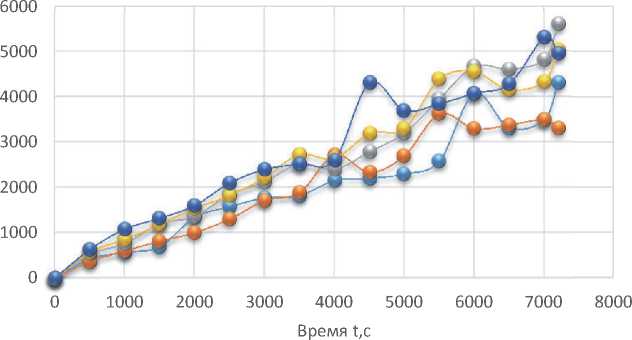
•—40 -в--60 -в—80 и -100 -в—120
Рис. 3. Зависимости Q-t для электродов, изготовленных с использованием Ni(OH)2, полученного при добавке Спк=50 г/л при iР=40÷120мА/см2
электродов. На основании полученных зависимостей был построен сводный график зависимости ёмкости электродов от времени разряда (рис. 4). Из рисунка видно, что электроды, изготовленные на основе гидроксида никеля, выделенного из раствора ПК с концентрацией 50 г/л, не уступают по своим емкостным характеристикам электродам, изготовленным на основе заводского материала.
Полученные результаты показывают, что предлагаемая методика извлечения ионов никеля в присутствии комплексона пирокатехина и далее получения гидроксида никеля из ГШ может быть рекомендована для изготовления активной массы катодов никель-кадмиевых (железных) аккумуляторов и является перспективной.
ЗАКЛЮЧЕНИЕ
Проведено избирательное извлечение ионов никеля, содержащихся в гальванических шламах в раствор при различных добавках пирокатехина (50-250 г/л). Выбрана оптимальная концентрация пирокатехина Спк=50 г/л для извлечения Ni2+ из растворов гальваношлама. Показано, что с увеличением содержания ПК концентрация извлеченных ионов никеля растет (от 12,4мг/мл (Спк=50 г/л) до 18,2 мг/мл (Спк=250 г/л)), однако при высоких концентрациях ПК (100÷250 г/л) образуется густая суспензия, практически не поддающаяся фильтрованию для отделения нерастворимых примесей (песок, глинистые минералы и др.), содержащихся в исходном гальваношламе.
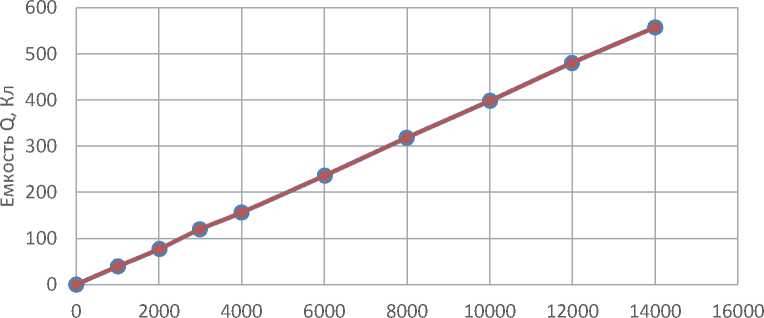
Время t, с
-•- ЗАИТ —•— Спк=50г/л
Рис. 4. Зависимости Q-t для катодов, изготовленных с использованием Ni(OH)2, извлеченного из ГШ при добавке Спк=50 г/ли промышленных катодов ПАО «ЗАИТ» при iР= 80мА/см2
При последующей обработке полученного раствора щелочью (40% NaOH) в диапазоне рН=7,2 ÷9,5 был осажден гидроксид Ni(OH)2, который удовлетворял требованиям ТУ 4836390 «Никеля гидрат закиси» для использования в качестве компонента активной массы катодов никель- кадмиевых (железных) аккумуляторов.
Изучены электрохимические характеристики полученныхNi(OH)2катодов и показано, что по своим рабочим параметрам они не уступают промышленным электродам.
В результате проведенных экспериментов установлена перспективность предлагаемой технологии использования комплексона пирокатехина для селективного извлечения в раствор ионов никеля из ГШ, далее получения гидроксида никеля и изготовления активной массы катодов Ni-Cd (Fe) аккумуляторов.
Список литературы Влияние комплексообразователя пирокатехина на извлечение из гальваношлама никеля и гидроксида никеля и изучение характеристик электродов, изготовленных из Ni(OH)2
- Рубанов, Ю.К., Токач Ю.Е. Утилизация отходов гальванического производства // Экология и промышленность России. 2010. Октябрь. С. 2-3.
- Исследование выщелачиваемости ионов тяжелых металлов из ферритизированных шламов гальванического производства / А.В. Пинаев, В.В. Семенов, В.В. Савиных, Е.С. Климов // Экология и промышленность России. 2006. Август. С. 24-25.
- Извлечение металлического никеля из никель-содержащего гальваношлама ОАО «Роберт-Бош-Саратов» / Л.Н. Ольшанская, Е.Н. Лазарева, В.В. Егоров, Т.М. Цечоев // Экологические проблемы промышленных городов: материалы Всероссийской конф. Саратов 4-6 апреля 2009 г. Часть 1. Саратов: СГТУ, 2009. С. 298-302.
- Хранилов, Ю.П., Еремеева Т.В., Бобров М.Н. Использование электрохимических технологий при переработке отходов гальванических производств с целью их утилизации // Актуальные проблемы электрохимической технологии. Сб. статей молодых ученых. Т.1. Саратов: ГАОУ ДПО «СарИПКиПРО», 2011. С. 240-244.
- Завальцева О.А. Комплектны для извлечения ионов тяжелых металлов из гальваношламов // Экология и промышленность России. 2010. Февраль. С. 36-38.
- Терещенко, А.Д.,Фарафонова И.А., Таратуто А.С. Катализаторы, полученные на основе отходов гальванических производств // Экотехнология и ресурсосбережение. 1999. № 3. С. 86 90.
- Ольшанская, Л.Н., Лазарева Е.Н., Булкина Л.А. Утилизация тяжелых металлов и их соединений из гальваношламов с получением пигментов-наполнителей и активной массы положительных электродов никель-железных (кадмиевых) аккумуляторов // Химическое и нефтегазовое машиностроение. 2016. № 2. С. 42-45.
- Патент 2590999 Российская Федерация, МПК B 01 J 20/26, B 01 J 20/30. Способ получения сорбционного материала для очистки сточных вод от нефтепродуктов / Бухарова Е.А., Татаринцева Е.А., Ольшанская Л.Н.; заявитель и патентообладатель Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Саратовский государственный технический университет имени Гагарина Ю.А.». № 2014154486/05; заявл.30 декабря 2014 г.; опубл.10.07.2016, Бюл. № 19. 2 с.
- Пирокатехин: Справочник химика / http://www. chem100.ru (дата обращения 1.06 2021).
- Применение пирокатехина // http:// www. wikipedia.ru (дата обращения 1.06 2021).
- ГОСТ 25336-82 «Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры» / М.: 2004. ИПК Издательство стандартов. 103 с.
- ТУ 48 3 63 90 «Никеля гидрат закиси» распространяются на никеля гидрат закиси, получаемый из растворов сернокислого никеля действием едкого натра и предназначенный для производства ще- 13. Лурье Ю.Ю. Справочник по аналитической химии. лочных аккумуляторов (pdf передан 02.10. 2019). М.: Химия, 1971.454 с. (С. 248).


