Влияние кортизола в комплексе с липопротеинами очень низкой плотности на развитие гепатомы НА-1 и карциномы Эрлиха
Автор: Панин Л.Е., Белоногова Ж.И., Князев Р.А., Чешенко И.О.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 3 (57), 2013 года.
Бесплатный доступ
Исследования проводились на клетках асцитной НА-1 гепатомы и асцитной карциномы Эрлиха. После пассажа клеток на мышах выделяли смешанную культуру клеток, содержащую опухоль-ассоциированные макрофаги. Показано, что в сокультуре комплекс ЛПОНП–кортизол значительно подавлял пролиферативную активность опухолевых клеток. Полученная константа связывания кортизола с ЛПОНП указывает на то, что в комплексообразовании принимает участие белковый компонент липопротеинов. Предполагается, что в образовании такого комплекса важную роль играют опухоль-ассоциированные макрофаги. Обнаружено, что механизм подавления роста опухолевых клеток связан с апоптозом.
Опухолевые клетки, липопротеины, кортизол, опухоль-ассоциированные макрофаги, биосинтез нуклеиновых кислот
Короткий адрес: https://sciup.org/14056331
IDR: 14056331 | УДК: 616.36-006.6:577.11]-092.9
Influence of cortisol and very low-density lipoproteines on the development of НА-1 hepatoma and Ehrlich’s carcinoma
Studies were conducted using ascetic HA-1 hepatomas and ascitic Ehrlich’s carcinoma cells. After passage of cells in mice, cell culture containing tumor-associated macrophages was studied. It was shown that the very low-density lipoprotein (VLDL)-cortisol complex significantly inhibited proliferative activity of tumor cells. The obtained constant of cortisol binding to VLDL indicated that the protein component of lipoproteins participated in the complex formation. Tumor-associated macrophages were suggested to play an important role in the formation of this complex. It was found that inhibition of tumor cell growth was related to apoptosis.
Текст научной статьи Влияние кортизола в комплексе с липопротеинами очень низкой плотности на развитие гепатомы НА-1 и карциномы Эрлиха
Применять липопротеины крови для лечения опухолевых заболеваний предложено давно [6, 12]. Обычно их используют как транспортную форму различных цитостатиков: рубомицина, актиномицина Д, циклофосфана и других препаратов. Чаще всего для этого берут липопротеины низкой плотности (ЛПНП). Они обладают достаточно высоким аффинитетом по отношению к цитостатикам. Так, константа диссоциации (Kд) для тамоксифена составляет 2,3×10-8 М [14]. Используется также способ ковалентной пришивки препарата к белковому компоненту ЛПНП [10]. Липопротеины высокой плотности (ЛПВП) для доставки в опухолевые клетки цитостатиков применяются редко. Существуют единичные работы по их доставке в клетки карциномы [5] и гепатомы [7]. Наблюдается разная степень связывания цитостатиков с липопротеинами крови. Так, циклоспорин G в плазме крови преимущественно связывается с ЛПВП (50–60 %) и в меньшей степени с ЛПНП (20–30 %) и ЛПОНП (10 %) [13].
Нам не встречались работы, в которых липопротеины плазмы крови использовались с целью запуска апоптоза опухолевых клеток. В этом отношении интерес представляет работа, в которой применялись липосомы, содержащие сфингомиелин и церамид, для стимуляции апоптоза в клетках гепатоцеллюлярной гепатомы крыс [1]. Показано, что оба соединения подавляют пролиферацию и усиливают апоптоз раковых клеток. Индукторами апоптоза являются не только сфингомиелин, фос-фатидилсерин, церамид, но и стероидные гормоны (глюкокортикоиды) [4].
В данном исследовании мы для стимуляции апоптоза опухолевых клеток использовали липопротеины очень низкой плотности (ЛПОНП)
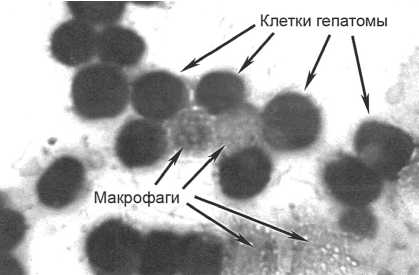
Рис. 1. Микрофото. Клетки асцитной НА-1 гепатомы с опухоль-ассоциированными макрофагами.
Окраска по Романовскому-Гимза, ×400
в комплексе с кортизолом. Это было обусловлено тем, что, во-первых, ЛПОНП достаточно богаты сфингомиелином [2] и, во-вторых, они активно связывают кортизол и кортикостерон. Константы связывания равны (5 ± 0,1) × 106М-1 и (8 ± 0,1) × 106М-1 соответственно [11].
Цель исследования – оценить кооперативный характер действия кортизола и липопротеинов очень низкой плотности в механизме запуска апоптоза опухолевых клеток.
Материал и методы
Исследования проводились на культурах клеток асцитной гепатомы НА-1, полученной в результате индукции мышей самцов линии A/Sn о-аминоазотолуолом (Институт цитологии и генетики СО РАН, г. Новосибирск). В экспериментах использовали клетки, выделенные на 10-е сут после перевивания их в брюшную полость мышей той же линии из расчёта 1 млн клеток на особь. Также в работе использовали мышей линии ICR с асцитной карциномой Эрлиха (Институт цитологии и генетики СО РАН). Клетки перитонеального экссудата получали на 10-е сут после пассажа опухоли для последующего культивирования. Свежевыделенные клетки ресу-спендировали в среде RPMI-1640 с L-глутамином, содержащую 20 мМ HEPES/NaOH (pH 7,4), 2 мM L-глутатиона, 100 ед/мл пенициллина, 50 мкг/мл гентамицина, 5,6 mM глюкозы, 10 нМ инсулина. Клетки наносили на 6-луночные планшеты («Orange Scientific», Бельгия), покрытые коллагеном первого типа. Инкубацию проводили при 37°С в атмосфере 5 % СО2 и 95 % воздуха при влажности 85 %. Конечная плотность клеток 5×106 на мм2. Продолжительность инкубации
Рис. 2. Электрофорез ДНК в агарозном геле.
Примечание: 1 – контроль; 2 –ЛПОНП; 3 – ЛПОНП–кортизол
24 ч. Пролиферативную активность клеток оценивали по скорости включения 3Н-тимидина в ДНК. Последний добавляли в среду инкубации в дозе 2 мкКи/мл за 2 ч до окончания эксперимента. Радиоактивность измеряли на сцинтилляционном счётчике «Mark-III»(США) и выражали в имп/ мин на 1 мг белка. Содержание белка в образцах определяли по Лоури [8]. Кортизол добавляли в среду инкубации в конечной концентрации 10–6 М, ЛПОНП – 200 мкг/мл. Содержание ДНК в образцах определяли полуколичественно с помощью электрофореза в агарозном геле. Апоптоз опухолевых клеток оценивали с помощью электронной микроскопии. Для этого образцы фиксировали в 2,5 % растворе глутарового альдегида в течение 1 ч, затем – в 0,1М ФСБ, содержащем 1 % OsO4. Образцы обезвоживали в спиртовых растворах с повышающейся концентрацией и заливали в аралдит. Срезы просматривали в электронном микроскопе YEM 100B (Япония).
Статистический анализ проводили с использованием программы Statistica 6.0 (StatSoft, USA, , достоверность значений определяли по t-критерию Стьюдента.
Результаты и обсуждение
Клетки асцитной гепатомы с опухоль-ассоциированными макрофагами (рис. 1) в организме мышей активно делятся, так что продолжительность жизни животных не превышает 2–3 нед. Ранее нами было показано, что пролиферативная активность клеток НА-1 гепатомы зависит от макрофагов. При стимуляции последних комплексом ЛПВП-кортизол отмечалось резкое усиление в сокультуре биосинтеза как ДНК, так и белка [3].
ВЛИЯНИЕ КОРТИЗОЛА В КОМПЛЕКСЕ С ЛИПОПРОТЕИНАМИ ОЧЕНЬ НИЗКОЙ ПЛОТНОСТИ ...
В данном исследовании мы оценивали влияние комплекса ЛПОНП-кортизол на скорость биосинтеза ДНК в сокультуре. Оказалось, что кортизол и ЛПОНП независимо друг от друга несколько тормозили скорость биосинтеза ДНК (разница с контролем недостоверна). Добавление к сокуль-туре комплекса ЛПОНП-кортизол вдвое снижало скорость биосинтеза ДНК (табл. 1). Принимая во внимание, что обмен липопротеинов связан в первую очередь с макрофагами, следует допустить, что именно последние запускают механизм подавления опухолевого роста.
Дальнейшие исследования мы проводили на культуре клеток асцитной карциномы Эрлиха в присутствии опухоль-ассоциированных макрофагов. Пролиферативную активность клеток также оценивали по скорости включения 3Н-тимидина в ДНК. Показано, что кортизол и ЛПОНП независимо друг от друга несколько снижали скорость биосинтеза ДНК (разница с контролем недостоверна). Комплекс ЛПОНП–кортизол снижал скорость биосинтеза в 1,7 раза (табл. 2). Полученные результаты аналогичны вышеуказанным. Эти результаты подтверждены данными электрофоретического анализа ДНК в образцах клеток асцитной карциномы Эрлиха (рис. 2). Значительное снижение содержания ДНК в образцах указывает на гибель клеток асцитной карциномы.
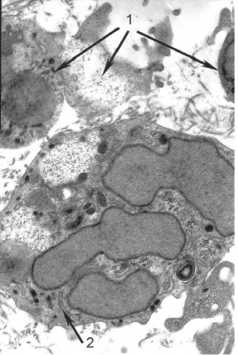
Рис. 3. Электронная микроскопия клеток асцитной карциномы Эрлиха. Действие комплекса ЛПОНП–кортизол.
Примечание: 1 – погибшая клетка;
2 – клетка в состоянии апоптоза, × 8000
Электронно-микроскопический анализ изменения структуры клеток выявил потерю микроворсин, секвестрацию цитоплазмы в среду инкубации и фрагментацию ядер (рис. 3). Обнаруженные признаки позволяют отнести механизм гибели опухолевых клеток под влиянием комплекса ЛПОНП–кортизол к апоптозу. Отсутствие выраженного эффекта подавления пролиферативной активности опухолевых клеток под влиянием
Таблица 1
Изменение скорости биосинтеза ДнК в сокультуре клеток на-1 гепатомы под влиянием комплекса ЛПонП-кортизол
|
Условия инкубации |
Имп/мин/мг белка M ± m, n=6 |
|
Контроль |
14233 ± 1802 |
|
ЛПОНП |
9647 ± 1613 |
|
Кортизол |
9903 ± 2644 |
|
ЛПОНП-кортизол |
6909 ± 565* |
Примечание: * – различия статистически значимы по сравнению с контролем (р<0,01).
Таблица 2
Изменение скорости биосинтеза ДнК в сокультуре клеток асцитной карциномы Эрлиха под влиянием комплекса ЛПонП-кортизол
|
Условия инкубации |
Имп/мин/мг белка M ± m, n=6 |
|
Контроль |
7805 ± 447 |
|
ЛПОНП |
5002 ± 298 |
|
Кортизол |
5939 ± 236 |
|
ЛПОНП-кортизол |
4176±376 * |
Примечание: * – различия статистически значимы по сравнению с контролем (р<0,05).
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2013. № 3 (57)
ЛПОНП или кортизола говорит о том, что мы имеем дело с кооперативным механизмом действия обоих компонентов комплекса. Полученная величина константы связывания гормона с ЛПОНП указывает на то, что в комплексообразовании принимает участие белковый компонент последних. Однако какой белок ЛПОНП принимает в этом участие – пока нами не установлено.
Заключение
Описан новый механизм подавления роста опухолевых клеток НА-1 гепатомы и карциномы Эрлиха, обусловленный кооперативным эффектом действия кортизола и ЛПОНП. Результаты электронной микроскопии позволяют утверждать, что данный механизм связан с апоптозом клеток.


