Влияние липополисахарида из клеток Salmonella typhi на кровообращение и дыхание анестезированной крысы
Автор: Туманова Татьяна Сергеевна, Губаревич Елена Алексеевна, Александров Вячеслав Георгиевич
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Исследование механизмов, реализующих кардиореспираторные эффекты повышенного системного уровня бактериальных липополисахаридов (ЛПС), необходимо для понимания процессов, приводящих к нарушению дыхания и кровообращения при развитии системного воспалительного ответа. ЛПС разных видов бактерий отличаются по составу компонента, определяющего их активность. Цель настоящего исследования состояла в экспериментальной проверке предположения о том, что ЛПС, выделенный из клеток бактерии Salmonella tуphi, может оказывать влияние на рефлексы, участвующие в контроле кровообращения и дыхания. Материалы и методы. В острых экспериментах на крысах линии «Вистар» (n=23, масса 200-225 г), анестезированных уретаном (1800 мг/кг, в/б), регистрировали артериальное давление, пневмотахограмму и электромиограмму диафрагмы. Определяли среднее артериальное давление, частоту сердечных сокращений, дыхательный объём и минутный объём дыхания. Барорефлекс тестировали путем внутривенного введения раствора фенилэфрина, который вызывал дозозависимое повышение артериального давления и, как следствие, рефлекторное снижение частоты сердечных сокращений. Силу инспираторно-тормозящего рефлекса оценивали методом функциональной ваготомии. Величину учитываемых параметров определяли до и после внутривенного введения раствора, содержащего 100 мкг ЛПС или физиологического раствора. Отличия параметров от их исходных и контрольных значений оценивали по критерию Манна-Уитни и считали достоверными при p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Бактериальный липополисахарид, salmonella tуphi, кровообращение, дыхание, артериальный барорефлекс, инспираторно-тормозящий рефлекс
Короткий адрес: https://sciup.org/14117548
IDR: 14117548 | УДК: 612.1+612.2+612.017 | DOI: 10.34014/2227-1848-2020-1-138-149
Effect of lipopolysaccharide from Salmonella typhi cells on blood circulation and respiration of anesthetized rats
In order to understand the processes, which cause respiration disturbance and impaired circulation during the development of a systemic inflammatory response (SIR) it is necessary to study the mechanisms which implement the cardiorespiratory effects of an increased systemic level of bacterial lipopolysaccharides (LPS). LPS obtained from various bacteria differ in the composition that determines their toxicity. The aim of the present study was to experimentally test the hypothesis that LPS isolated from bacterium Salmonella typhi (S. typhi) cells could affect reflexes involved in circulation and breathing control. Materials and Methods. The authors recorded blood pressure, pneumotachogram and diaphragm electro-myogram in acute experiments on Wistar rats (n=23, weight 200-225 g), anesthetized with urethane (1800 mg/kg, i.p.). They also calculated mean arterial pressure, heart rate, breathing capacity and respiratory minute volume. Baroreflex was tested by intravenous phenylephrine administration, which caused a dose-dependent blood pressure rise and, as a result, a reflex heart rate fall. The strength of the inspiratory inhibitory reflex (IIR) was evaluated by functional vagotomy. The values of the studied parameters were evaluated before and after intravenous administration of the physiologic saline, or the saline containing 100 pg of LPS. Parameter differences from the initial and control values were evaluated according to Mann-Whitney criterion and considered relevant at p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Влияние липополисахарида из клеток Salmonella typhi на кровообращение и дыхание анестезированной крысы
Введение. Клеточная стенка грамотрица-тельных бактерий, входящих в состав микрофлоры кишечника, является источником липополисахарида (ЛПС), который постоянно присутствует в системном кровотоке и в нормальных условиях эффективно нейтрализуется антиэндотоксическими системами. Нарушение барьерной функции кишечника и массовое разрушение бактерий приводят к повышению системного уровня ЛПС. При попадании в системный кровоток ЛПС взаимодействует с циркулирующим ЛПС-связывающим белком, а затем с рецепторным комплексом
CD14/TLR4/MD-2, расположенным на поверхности иммунокомпетентных клеток. Это приводит к быстрой активации внутриклеточного сигнального пути, включению генов ядерного фактора каппа В (NF-kB) и усиленному синтезу провоспалительных цитокинов IL-1 и ФНО [1, 2]. В клинической картине развивающегося системного воспалительного ответа (СВО) доминируют сердечно-сосудистая и дыхательная дисфункции, которые проявляются, в частности, в изменении АД, тахикардии и гипервентиляции [3, 4]. Считается, что эндотоксическая активность ЛПС определя- ется главным образом одним из его компонентов, липидом А, который у разных видов бактерий отличается длиной, положением и количеством цепей жирных кислот. В частности, липиды А, входящие в состав ЛПС клеточной стенки Escherichia и Salmonella, являются бифосфорилированными, имеют асимметричное распределение жирных кислот, но различаются по их количеству. В состав липида А из Escherichia coli (E. coli) входит 6 жирных кислот, а в состав липида А из Salmonella typhi (S. tуfi) – 7 жирных кислот. MD-2 различает эту особенность структуры липида А и, в зависимости от неё, по-разному активирует TLR4 [2, 5, 6]. Кроме того, установлено, что и другие структурные компоненты ЛПС, которые отличаются у разных бактерий, могут влиять на эндотоксическую активность ЛПС [7]. Эти данные позволяют предполагать, что повышение системного уровня ЛПС, происходящего из разных видов бактерий, может по-разному воздействовать на продукцию цитокинов и, как следствие, оказывать различное влияние на функции систем дыхания и кровообращения при развитии СВО.
К настоящему времени установлено, что системное введение ЛПС приводит к повышению уровня провоспалительных цитокинов, в частности ФНО [8–12], и вызывает изменение артериального давления и повышение ЧСС [11, 12]. Кроме того, показано, что провоспа-лительные цитокины при повышении их системного и церебрального уровня изменяют паттерн внешнего дыхания, оказывают угнетающее действие на рефлекторные механизмы системы дыхания [13–18]. Установлено также, что эти эффекты реализуются посредством NO-ергических и простаноидзави-симых механизмов [16–18].
Таким образом, кардиореспираторные эффекты ЛПС, а также механизмы их реализации изучены достаточно подробно. Вместе с тем анализ литературных данных показывает, что особенности кардиореспираторных эффектов, которые могут проявляться в результате отличий в структуре ЛПС, выделенного из разных видов бактерий, практически не исследовались.
Цель исследования. Экспериментальная проверка предположения о том, что ЛПС, вы- деленный из клеток бактерии S. tуfi, может оказывать влияние на рефлексы, участвующие в контроле кровообращения и дыхания.
Материалы и методы. Эксперименты были проведены на 23 самцах крыс линии Wistar массой 200–225 г из ЦКП «Биоколлекция» ИФ РАН, анестезированных внутрибрюшинным введением уретана в дозировке 1800 мг/кг. Температура тела животных в ходе опытов поддерживалась на уровне 37±0,5 ºC. Содержание лабораторных животных, уход за ними, а также организация всех экспериментальных процедур осуществлялись в соответствии с Приложением А к Европейской конвенции о защите позвоночных животных, используемых в экспериментах и в других научных целях (ETS N 123).
Животные были разделены на две группы: контрольную (n=11) и экспериментальную (n=12). Хирургическая подготовка животного к эксперименту включала трахеостомию, катетеризацию бедренной артерии и вены, а также установку электромиографиче-ских электродов на реберную часть диафрагмы. К трахеостоме присоединялась пнев-мометрическая трубка, к артериальному катетеру – переходная камера датчика давления. Электроды, трубка и датчик подключались к предусилителям, которые формировали сигналы электромиограммы, пневмотахограммы и артериального давления. Cигналы поступали на вход устройства сбора данных PowerLab 8/32, работавшего под управлением пакета программ LabChart 7. Этот аппаратнопрограммный комплекс (AD Instruments, New Zealand) обеспечивал мониторинг и регистрацию артериального давления (АД), пневмотахограммы (ПТГ) и электромиограммы диафрагмы (ЭМГди). Кроме того, с его помощью производился расчёт и регистрация среднего артериального давления (АДср), частоты сердечных сокращений (ЧСС), дыхательного объема (ДО), частоты дыхания (ЧД), длительности вдохов (Тi) и минутного объема дыхания (МОД) в режимах on- и offline. Инспираторно-тормозящий рефлекс Геринга–Брейера (ИТР) оценивался методом функциональной ваготомии, который реализуется путем окклюзии верхних дыхательных путей в конце выдоха. Сила ИТР характеризовалась про- центным соотношением длительности первого окклюзионного «вдоха» и длительности последнего свободного вдоха перед окклюзией [18, 19], причем длительности вдохов определялись по ЭМГди. Тестирование артериального барорефлекса (БР) осуществлялось путем болюсного введения α-адреномиметика фенилэфрина в дозировке 0,05 мг/кг. Затем средствами программного пакета MS Excel определялся угловой коэффициент а в уравнении линейной функции y=ax+k, аппроксимирующей зависимость между ростом АДср и падением ЧСС. Величина a определяет наклон аппроксимирующей прямой линии и отражает силу БР: коэффициент увеличивается при усилении и уменьшается при ослаблении БР. Через час после начала эксперимента контрольным животным вводилось 2 мл физиологического раствора. Животным основной группы также через час вводилось 2 мл раствора, содержащего ЛПС, выделенный из клеток бактерии S. typhi (препарат «Пирогенал», пр-во «Медгамал», Россия), в дозировке 0,9 мг/кг. Общая длительность эксперимента составляла 3 ч. По завершении эксперимента животные усыплялись передозировкой анестетика. Значения величин определялись с интервалом 10 мин и нормировались относительно их фоновых значений на 60-й мин эксперимента, перед введением раствора. Тестирование БР производилось каждые 30 мин и нормировалось относительно 40-й мин.
Статистическая обработка данных производилась при помощи пакетов программ MS Excel и Statistica for Windows. Рассчитывались средние значения абсолютных и нормированных величин и ошибки средних. Полученные величины сводились в таблицы и использовались для построения графиков. Значения учитываемых параметров после введения ЛПС сравнивались со значениями, полученными непосредственно перед введением ЛПС (фоновые значения), а также со значениями, полученными в контрольных экспериментах. Для определения достоверности наблюдавшихся изменений использовался непараметрический критерий Манна–Уитни. Различия считались достоверными при р<0,05.
Результаты. Эксперименты показали, что к 60-й мин от начала регистрации показа- тели, характеризующие состояние систем кровообращения и дыхания, стабилизировались, поскольку не было обнаружено достоверных различий между их значениями на 20-й, 40-й и 60-й мин. Кроме того, не было обнаружено достоверных различий между их значениями, полученными в контрольных экспериментах и в экспериментах с введением ЛПС (табл. 1).
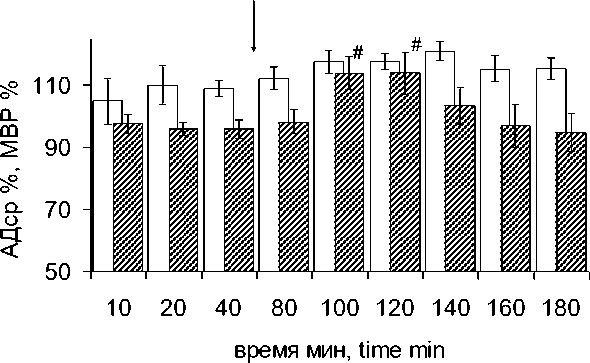
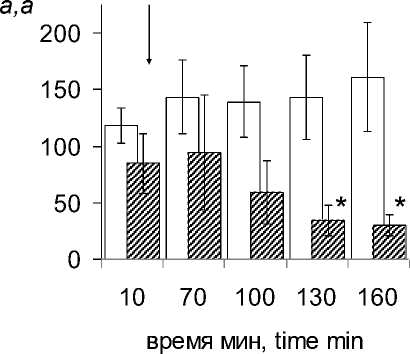
Полученные результаты свидетельствуют о том, что введение физиологического раствора не оказывало статистически значимого влияния на величину АД ср (рис. 1а). Вместе с тем через 40 мин после введения раствора, содержащего ЛПС, наблюдалось статистически значимое увеличение величины АД ср по сравнению с его фоновыми показателями, которое сохранялось и на 120-й мин. Затем значения АД ср возвращались к исходным величинам и не отличались от значений, полученных в контрольных экспериментах.
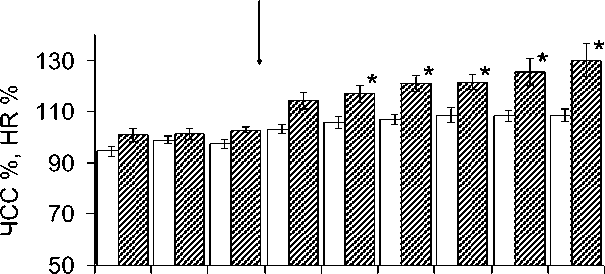
ЧСС была стабильна в контрольных экспериментах и начинала возрастать после введения ЛПС (рис. 1б). На 120-й мин ЧСС была достоверно выше фоновых и контрольных значений и продолжала расти до конца эксперимента.
Таким образом, полученные результаты свидетельствуют о том, что ЛПС при его внутривенном введении оказывает влияние на систему кровообращения, повышая ЧСС.
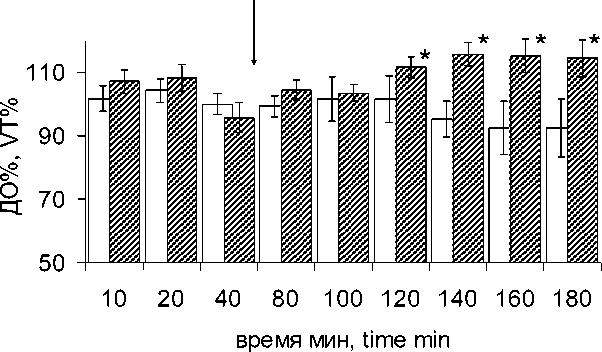
В контрольных экспериментах ДО оставался относительно стабильным, не обнаруживая каких-то определенных изменений (рис. 2а). В то же время ЛПС вызывал небольшое, но статистически значимое увеличение ДО начиная со 120-й мин эксперимента, т.е. через 60 мин после введения вещества (рис. 2а). При этом достоверных отличий между величинами ЧД, полученными в этих сериях экспериментов, получено не было. МОД в контрольной серии экспериментов был стабилен, несколько снижаясь к концу эксперимента (рис. 2б). Напротив, после введения ЛПС наблюдался постепенный рост МОД. На 140-й мин и до конца эксперимента величина МОД была достоверно больше его фоновых и контрольных значений. Очевидно, что введение ЛПС приводило к увеличению вентиляции, главным образом за счет роста ДО.
Таблица 1
Table 1
Абсолютные величины учитываемых показателей до введения контрольного и экспериментального растворов
Absolute values of relevant indicators before control and experimental solution administration
|
Показатели Parameters |
Группа Group |
10-я мин 10th min |
20-я мин 20th min |
40-я мин 40th min |
60-я мин 60th min |
|
АД ср , мм рт. ст. Mean ABP, mm Hg |
контрольная control |
76±4 |
73±4 |
72±2,8 |
73±3 |
|
экспериментальная experimental |
67±4 |
66±3 |
62±34 |
68±3 |
|
|
ЧСС, уд./мин HR, BPMs |
контрольная control |
359±15 |
362±12 |
375±12 |
385±14 |
|
экспериментальная experimental |
397±14 |
400±13 |
404±10 |
407±14 |
|
|
ЧД, ц/мин RF, min-1 |
контрольная control |
114±5 |
108±6 |
109±5 |
111±6 |
|
экспериментальная experimental |
120±6 |
122±7 |
123±10 |
122±6 |
|
|
ДО, мл TVe, ml |
контрольная control |
1,5±0,2 |
1,6±0,2 |
1,5±0,2 |
1,5±0,2 |
|
экспериментальная experimental |
1,9±0,3 |
2,0±0,4 |
1,8±0,2 |
1,9±0,3 |
|
|
МОД, мл/мин RMVe, ml/min |
контрольная control |
157±21 |
168±19 |
160±17 |
164±17 |
|
экспериментальная experimental |
235±53 |
241±55 |
221±60 |
236±53 |
|
|
Тi оккл, % Ti occl, % |
контрольная control |
142±6 |
140±6 |
140±3 |
148±4 |
|
экспериментальная experimental |
150±7 |
159±9 |
143±4 |
153±5 |
|
|
Коэффициент а Coefficient a |
контрольная control |
1,6±0,12 |
- |
1,6±0,19 |
- |
|
экспериментальная experimental |
1,5±0,18 |
- |
1,5±0,12 |
- |
а
а
б b
10 20 40 80 100 120 140 160 180время мин, time min
□ Контрольная группа Сontrol group^ Экспериментальная группа Еxperimental group
Рис. 1. Изменения АД ср (а) и ЧСС (б) в экспериментальной и контрольной группах. Стрелка – момент введения растворов.
-
# – достоверные отличия от фоновых значений при p<0,05;
* – достоверные отличия от фоновых и контрольных значений при p<0,05.
На рис. 2 и 3 обозначения те же
Fig. 1. Changes in mean blood pressure (a) and heart rate (b) in experimental and control groups. Arrow points the moment of injection.
-
# – the differences from the background values are significant at p<0.05;
-
* – the differences from the background and control values are significant at p<0.05 The designations in Fig. 2 and 3 are the same
а
а
б b
ш
О
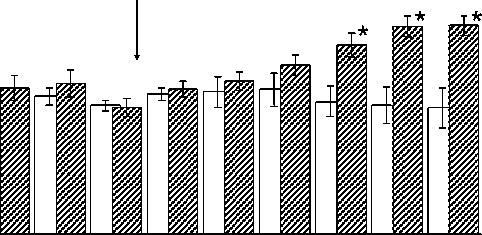
10 20 40 80 100 120 140 160 180время мин, time min
□ Контрольная группа Control groupЭкспериментальная группа Experimental group
Рис. 2. Изменение ДО (а) и МОД (б) в контрольных экспериментах и в экспериментах с введением ЛПС
Fig. 2. Changes in tidal volume (TVe) (a) and respiratory minute volume (RMVe) (b) in control experiments and in experiments with LPS administration
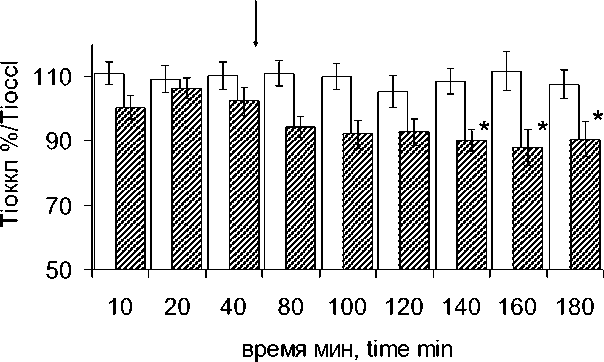
Тестирование БР в контрольных экспериментах и в экспериментах с введением ЛПС показало, что начальные значения показателя силы этого рефлекса, определенные до введения раствора, на 40-й мин эксперимента, составляли соответственно 1,6±0,2 и 1,4±0,4. Эти величины не имели достоверных отличий между собой; при нормировании данных, полученных в соответствующих сериях экспериментов, они были приняты за 100 % (рис. 3а). После введения физиологического раствора наблюдалось усиление барорефлекса, которое не было, однако, статистически значимым. Под влиянием ЛПС про- исходило достоверное ослабление барорефлекса (рис. 3а).
Тестирование ИТР показало его стабильность в контрольных экспериментах и постепенное ослабление после введения ЛПС (рис. 3б). Через 40 мин после введения показатель силы ИТР уменьшался до величины, статистически значимо отличавшейся от фоновых и контрольных значений, и продолжал постепенно снижаться вплоть до конца эксперимента. Таким образом, полученные результаты показали, что влияние ЛПС на рефлекторные механизмы регуляции систем кровообращения и дыхания проявляется в их ослаблении.
а
а
б b
Контрольная группа/Control groupЭкспериментальная группа/Experimental group
Рис. 3. Изменение силы БР (а) и ИТР (б) в контрольных экспериментах и экспериментах с введением ЛПС
Fig. 3. Changes in the power of baroreflex (a) and inspiratory-inhibitory reflex (IIR) (b) in control experiments and in experiments with LPS administration.
Обсуждение. Итак, в результате проведенных экспериментов было установлено, что системное введение ЛПС, выделенного из клеток бактерии S. typhi , вызывает повышение ЧСС и МОД у крыс, анестезированных уретаном. Кроме того, происходит ослабление двух важных рефлекторных механизмов, участвующих в контроле функций кровообращения и дыхания, а именно БР и ИТР. Нашими предыдущими исследованиями было установлено, что подобные эффекты вызывает введение
ЛПС, выделенного из клеток E. coli [21]. При системном введении этого вещества анестезированным крысам происходило повышение ЧСС, увеличение ДО и МОД, а также ослабление барорефлекса и инспираторно-тормозящего рефлекса. Вместе с тем следует отметить, что ЛПС из E. coli вызывал снижение АД, а в экспериментах с ЛПС из S. typhi мы не наблюдали снижения АД. Напротив, через 40 мин после введения вещества отмечалось временное увеличение АД ср , а ещё через
40 мин уровень АД ср возвращался к исходным значениям. Это различие могло быть вызвано разницей в дозировках, применявшихся при исследовании ЛПС разного происхождения. По-видимому, следует признать, что по основным параметрам, ЧСС и вентиляции, а также по рефлекторным механизмам циркуляторная и респираторная системы крысы, анестезированной уретаном, сходным образом реагируют на ЛПС, выделенный из разных видов бактерий.
С одной стороны, известно, что несмотря на то что механизмы действия липополисахаридов на иммунокомпетентные клетки могут изменяться в зависимости изменений в структуре их молекулы, конечным результатом будет выделение провоспалительных цитокинов, в частности ФНО [8]. С другой стороны, в предыдущих экспериментах на крысах, анестезированных уретаном, нами было установлено, что экзогенное повышение системного уровня ФНО усиливает вентиляцию за счет роста ДО и ослабляет инспираторно-тормозящий рефлекс [18]. Было показано, что эти эффекты устраняются диклофенаком, который оказывает ингибирующее действие на проста-гландин-эндопероксид синтазу (КФ 1.14.99.1, циклооксигеназа (ЦОГ)). Поскольку, кроме того, известно, что ФНО вызывает экспрессию ряда белков, включая ЦОГ, был сделан вывод о том, что респираторные эффекты, которые наблюдаются при повышении его системного уровня, являются следствием повышения системного уровня простагландинов и их действия на нервные механизмы регуляции дыхания. Таким образом, представляется вполне вероятным, что те изменения в функциях сердечно-сосудистой и респираторной систем, которые наблюдались в наших экспериментах в результате введения ЛПС из клеток S. tуfi , являются следствием повышения системного уровня ФНО, усиления синтеза ЦОГ и повышения уровня простагландинов.
Возможны и другие пути реализации наблюдавшихся нами эффектов, поскольку введение ЛПС вызывает продукцию не только ФНО, но и других провоспалительных цитокинов, в частности интерлейкина-1-бета (ИЛ-1β). Установлено, что экзогенное повышение системного уровня ИЛ-1β приводит к изменению состояния респираторной системы анестезированной крысы, причем его эффекты также реализуются посредством простаноид-зависимых механизмов [15, 16]. В свою очередь простагландины выступают в роли ингибирующих модуляторов, оказывающих своё действие на уровне продолговатого мозга, в цепях нейронов, осуществляющих контроль дыхания и кровообращения [21, 22].
Заключение. Полученные результаты свидетельствуют о том, что экзогенное повышение системного уровня ЛПС, выделенного из бактерии S. tуfi , взывает изменения в состоянии систем дыхания и кровообращения крысы, анестезированной уретаном. Эти изменения проявляются в тахикардии, усилении вентиляции и ослаблении рефлекторных механизмов регуляции систем дыхания и кровообращения. Подобные изменения наблюдались при моделировании СВО путем введения ЛПС из клеток E. coli , а также при экзогенном повышении системного уровня ФНО на том же объекте в аналогичных экспериментальных условиях. Поэтому вероятно, что обнаруженные эффекты ЛПС, выделенного из S. tуfi , также реализуются при посредничестве ФНО, который вызывает рост циклооксигеназной активности и, соответственно, усиление синтеза простагландинов. Таким образом, можно полагать, что в условиях модельных экспериментов на анестезированных животных ЛПС, выделенные из разных источников, несмотря на разницу в тонком строении их молекул, оказывают сходное действие на функции дыхания и кровообращения, в т.ч. на рефлекторные механизмы их регуляции.
Список литературы Влияние липополисахарида из клеток Salmonella typhi на кровообращение и дыхание анестезированной крысы
- Heumann D., Roger T. Initial responses to endotoxins and Gram-negative bacteria. Clin. Chim. Acta. 2002; 323 (1-2): 59-72.
- Yang H. Cellular events mediated by lipopolysaccharide-stimulated toll-like receptor 4MD-2 is required for activation of mitogen-activated protein kinases and Elk-1. J. Biol. Chem. 2000; 275 (27): 2086120866.
- Singer M., Deutschman C.S., Seymour C. W. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA. 2016; 315 (8): 801-810. DOI: 10.1001/jama.2016.0287
- Marik P.E., Taeb A.M. SIRS, qSOFA and new sepsis definition. J. Thorac. Dis. 2017. 9 (4): 943-945. DOI: 10.21037/jtd.2017.03.125
- Simpson B.W., Trent M.S. Pushing the envelope: LPS modifications and their consequences. Nat. Rev. Microbiol. 2019; 17 (7): 403-416. DOI: 10.1038/s41579-019-0201-x
- Tsukamoto H. Lipopolysaccharide-binding protein-mediated Toll-like receptor 4 dimerization enables rapid signal transduction against lipopolysaccharide stimulation on membrane-associated CD14-express-ing cells. Int. Immunol. 2010; 22 (4): 271-280.
- Steven S. Time response of oxidative/nitrosative S-stress and inflammation in LPS-induced endotoxe-mia - a comparative study of mice and rats. Int. J. Mol. Sci. 2017; 18 (10): 2176.
- Волошина Е.В., Зубова С.В., Прохоренко С.В. Сравнение эффектов разных хемотипов липополиса-харидов из Escherichia Coli и Salmonella на синтез TNF-а и IL-6 макрофаго-подобными клетками ТНР-1. Медицинская иммунология. 2009; 11 (6): 509-514.
- Shangze G. Histidine rich glycoprotein ameliorates endothelial barrier dysfunction through regulation of NFkB and MAPK signal pathway. Br. J. Pharmacol. 2019; 176 (15): 2808-2824.
- Koike-Kiriyama N., Adachi Y., Iwasaki M. High mortality rate of (NZWxBXSB) F1 mice induced by administration of lipopolysaccharide attributes to high production of tumor necrosis factor-alpha by increased numbers of dendritic cells. Clin. Exp. Immunol. 2008; 154: 285-293.
- Stahl O. Mimicry of human sepsis in a rat model - prospects and limitations. J. Surg. Res. 2013; 179 (1): e167-e175.
- Altavilla D., Squadrito G., MinutoliL. Inhibition of nuclear factor-kappaB activation by IRFI 042, protects against endotoxin-induced shock. Cardiovasc. Res. 2002; 54: 684-693.
- Aleksandrova N.P., Danilova G.A. Effect of intracerebroventricular injection of interleukin-1beta on the ventilatory response to hyperoxic hypercapnia. Eur. J. Med. Res. 2010; 15 (II): 3-6.
- Александрова Н.П. Цитокины и резистивное дыхание. Физиология человека. 2012; 38 (2): 119-129.
- Александрова Н.П., Меркурьев В.А., Александров В.Г. Влияние интерлейкина-1 на паттерн дыхания и инспираторно-тормозящий рефлекс Геринга-Брейера. Вестник ТвГУ. Сер. Биология и экология. 2013; 2: 9-17.
- Александрова Н.П., Меркурьев В.А., Туманова Т.С., Александров В.Г. Механизмы модуляции рефлекторного контроля дыхания при повышении системного уровня провоспалительного цитокина интерлейкина-1ß. Российский физиологический журнал им. И.М. Сеченова. 2015; 101 (10): 1158-1168.
- Александров В.Г., Александрова Н.П., Туманова Т.С., Евсеева А.Д., Меркурьев В.А. Участие NO-ер-гических механизмов в реализации респираторных эффектов провоспалительного цитокина интерлейкина-1бета. Российский физиологический журнал им. И.М. Сеченова. 2015; 101 (12): 1373-1385.
- Александров В.Г., Туманова Т.С., Александрова Н.П. Диклофенак устраняет дыхательные эффекты фактора некроза опухоли у крыс. Журнал эволюционной биохимии и физиологии. 2018; 54 (4): 298-300.
- Mortola J.P., Trippenbach T., Rezzonico R. Hering-Breuer reflexes in high-altitude infants. Clin. Sci. 1995; 88: 345-350.
- Aleksandrova N.P., Aleksandrov V.G., Ivanova T.G. Effects of Gamma-Aminobutyric Acid on the Hering-Breuer Inspiration-Inhibiting Reflex. Neurosci. Behav. Physiol. 2010; 40 (2): 165-171.
- Туманова Т.С., Александров В.Г. Влияние бактериального липополисахарида на рефлекторные механизмы кардиореспираторной системы анестезированной крысы. Научные труды V съезда физиологов СНГ. 4-8 октября 2016. Сочи - Дагомыс; 2016: 158.
- Forsberg D., Ringstedt T., Herlenius E. Astrocytes release prostaglandin E2 to modify respiratory network activity. Elife. 2017; 6. URL: https://elifesciences.org/articles/29566 (дата обращения: 24.11.2019).
- DOI: 10.7554/eLife.29566


