Влияние липосомальной формы полиненасыщенных жирных кислот на процессы перекисного окисления липидов
Автор: Ламажапова Г.П., Жамсаранова С.Д., Бурнашева Е.В.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 4 (49), 2014 года.
Бесплатный доступ
Изучены некоторые показатели перекисного окисления липидов и суммарное содержание антиоксидантов (CCA) в сыворотке крови и печени экспериментальных животных при гиперлипидемии, вызванной детергентом Твин-80. В работе установлено, что введение липосомальной формы полиненасыщенных жирных кислот вызывало снижение продуктов перекисного окисления липидов в тканях экспериментальных животных. Существенного изменения уровня CCA в анализируемых объектах не наблюдалось.
Полиненасыщенные жирные кислоты, перекисное окисление липидов, малоновый диальдегид, суммарное содержание антиоксидантов, липосомы, дислипидемия
Короткий адрес: https://sciup.org/142148186
IDR: 142148186 | УДК: 577.125.33:
The impact of liposomal forms of polyunsaturated fatty acids on lipid peroxidation
Some indicators of lipid peroxidation and toal content of antioxidants in serum and liver of experimental animals with hyperlipidaemia caused by detergent Tween-80 were studied. It is ^ found that the intake of liposomal form of polyunsaturated. fatty acids is resulted in decrease of lipid peroxidation products in tissues of experimental animals. Significant changes in the level of total content of antioxidants in the analyzed objects are not observed.
Текст научной статьи Влияние липосомальной формы полиненасыщенных жирных кислот на процессы перекисного окисления липидов
Характерной особенностью утвержденных «Норм физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации» (МР 2.3.1.24.32-08) является установление нормативных уровней потребления целого ряда ранее не нормируемых, но очень важных минорных компонентов пищи, обладающих высокой биологической активностью. К числу таких компонентов относятся и полиненасыщенные жирные кислоты (ПНЖК).
Потребность в ПНЖК определена от 6 до 10% от энергетической ценности суточного рациона, при этом потребность в ω-3 ПНЖК от 1 до 2% от суммы ккал. При этом важно, чтобы соотношение ω-6/ω-3 ПНЖК в рационе здорового человека составляло 10:1, а в случае болезни – 5:1 и даже 3:1. В питании населения России реальное соотношение ω-6/ω-3 ПНЖК составляет от 10:1 до 30:1, таким образом, испытывается постоянный острый дефицит в ω-3 ПНЖК и, прежде всего, в эйкозапентаеновой (ЭПК) и докозогексаеновой (ДГК) кислотах. Известно, что ПНЖК оказывают выраженное влияние на липидный состав и атерогенный потенциал крови и других тканей организма.
Наличие большого числа двойных связей в структуре ПНЖК делает их главной мишенью для активных форм кислорода, что приводит к усилению процессов перекисного окисления липидов (ПОЛ) и развитию процессов, реализующих так называемый окислительный стресс. Однако наряду с данными о прооксидантных свойствах ПНЖК появляются сообщения и об их антиоксидантном действии [1].
Целью работы было изучение влияния липосомальной формы ПНЖК на некоторые показатели перекисного окисления липидов на модели гиперлипидемии, вызванной детергентами.
Материал и методы исследования
В работе были использованы липосомы, полученные из фосфолипидов печени байкальской нерпы с добавлением жира нерпы в концентрации 3 мг/мл по разработанному методу [2]. В качестве антиоксиданта был использован α-токоферол ацетат в концентрации 1% (по отношению к липидному компоненту), соответствующий требованиям ФС 42-2654-898.10. Жир байкальской нерпы получали согласно ТИ 9281-017-02069473-2001.
Экспериментальная работа выполнена на половозрелых крысах-самцах Вистар массой 220-280 г, полученных из питомника НИИ Биофизики Ангарской государственной технической академии. Животные находились в индивидуальных клетках. При этом все животные получали стандартный рацион питания.
Эксперименты выполнены с соблюдением всех правил и рекомендаций Европейской конвенции по защите позвоночных животных, используемых в экспериментальных работах (Страсбург, 1986).
Все животные были разделены на 3 группы: 1-я интактная группа крыс, содержащаяся на обычном режиме питания; 2-я контрольная группа, у которой была вызвана гиперлипидемия введением Твина-80; 3-я группа – опытная группа, которая в течение 14 дней получала липосомальную суспензию и Твин-80.
Гиперлипидемию у крыс вызывали по ускоренной методике внутрибрюшинным введением Твина-80 в дозе 250 мг на 100 г массы тела в 1 мл дистиллированной воды.
Степень выраженности окислительных процессов в организме экспериментальных животных определяли по содержанию малонового диальдегида (МДА) как вторичного продукта ПОЛ в сыворотке крови [3] и печени животных [4].
Определение суммарного содержания антиоксидантов (ССА) в сыворотке крови и печени экспериментальных животных проводилось на проточно-инжекционной системе «ЦветЯуза-01-АА» с амперометрическим детектированием в Биотехнологическом центре Восточно-Сибирского государственного университета технологий и управления.
Статистическую обработку результатов исследования выполняли в MS Excel 6.0 с использованием функции t-распределения Стьюдента. Полученные результаты считали достоверными при p≤0,05.
Результаты исследования
На рисунке 1 представлены данные по содержанию МДА в сыворотке крови экспериментальных животных.
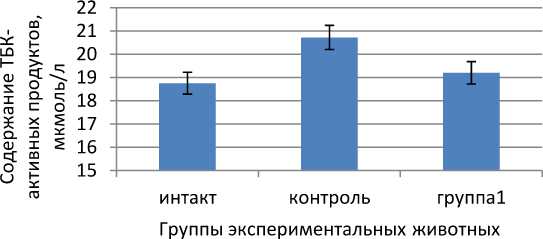
Рис. 1. Показатель уровня малонового диальдегида в сыворотке крови экспериментальных животных, получавших Твин-80 и липосомальную суспензию
Как следует из рисунка 1, введение детергента Твин-80 вызывало увеличение данного показателя по отношению к интактной группе, которое составило 10,5%, в то время как при введении липосом показатель в опытной группе животных снизился на 7,9% по отношению к контролю.
На рисунке 2 показаны изменения показателя МДА в печени экспериментальных животных.
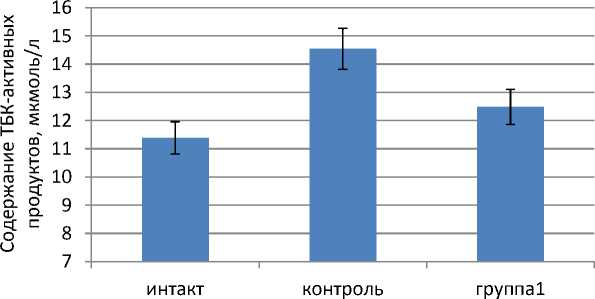
Группы экспериментальных животных
Рис. 2. Показатель уровня малонового диальдегида в печени экспериментальных животных, получавших Твин-80 и липосомальную суспензию
Как видно из рисунка 2, при введении Твина-80 контрольной группе животных уровень содержания малонового диальдегида в печени достоверно увеличился на 38,4%. Это напрямую может быть связано с полученными нами данными по увеличению общего холестерина (ОХС) в крови. Можно полагать, что активация ПОЛ на фоне увеличения содержания ОХС связана с компенсаторной реакцией организма, направленной на сохранение исходной микровязкости мембран. Известно, что накопление ацилгидроперекисей в микросомальных мембранах гепацитов при гиперхолестеринемии сопровождается изменением активности ряда микросомальных ферментов и, в частности, ингибированием ключевого фермента катаболизма ОХС и образования желчных кислот микросомальной 7α-гидроксилазой ХС [5].
На рисунке 3 представлены данные суммарного содержания антиоксидантов в сыворотке крови экспериментальных животных.
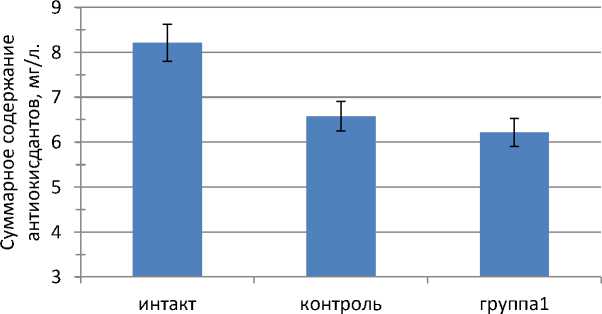
Группы экспериментальных животных
Рис. 3. Суммарное содержание антиоксидантов в сыворотке крови экспериментальных животных
Полученные данные указывают на то, что в контрольной группе животных ССА достоверно снизилось на 24,7% по отношению к интакту. В то время как в группе животных, получавших липосомальную форму ПНЖК, суммарное содержание антиоксидантов также снизилось на 31,9%. Установлено, что снижение суммарного содержания антиоксидантов кор- релирует с уровнем малонового диальдегида в сыворотке крови экспериментальных животных. Данные результаты, по-видимому, указывают на участие липосомальной формы ПНЖК в процессах ингибирования процессов ПОЛ.
На рисунке 4 представлены данные суммарного содержания антиоксидантов в печени животных.
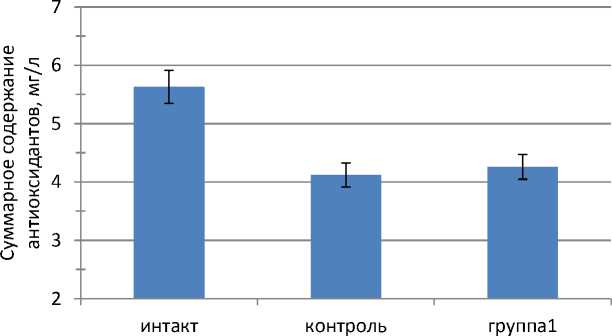
Группы экспериментальных животных
Рис. 4. Суммарное содержание антиоксидантов в печени экспериментальных животных
Из рисунка 4 следует, что суммарное содержание антиоксидантов в печени контрольной группы животных также снизилось на 36,6% в отличие от интактной группы животных. В 1-й группе животных ССА снизилось на 32,1% по отношению к интакту.
Развитие перекисного окисления липидов напрямую связано с содержанием антиоксидантов. Перекисное окисление липидов, развивающееся при накоплении активных форм кислорода, приводит к развитию оксидативной модификации макромолекул, которые способствуют развитию очень многих заболеваний и синдромов. Соотношение антиоксидантов и прооксидантов определяет, будет ли развиваться и прогрессировать оксидативный стресс [6]. Это соотношение участвует в регуляции многих очень важных биологических процессов.
Заключение
Поскольку первичные и вторичные продукты ПОЛ оказывают выраженное повреждающее действие, в организме существуют регуляторные механизмы, ограничивающие накопление высокотоксичных продуктов. Реакции автоокисления ПНЖК в биомембранах могут подавлять природные антиоксиданты, важнейшим из которых является а-токоферол.
Витамин Е (а-токоферол ацетат) - наиболее распространенный антиоксидант в природе - является липофильной молекулой, способной инактивировать свободные радикалы непосредственно в гидрофобном слое мембран и таким образом предотвращать развитие цепи перекисного окисления.
Ведущую роль в регуляции процессов ПОЛ в организме играют «антиоксидантные» ферменты, способные утилизировать анион-радикалы кислорода (супероксиддисмутаза -СОД), Н2О2 (каталаза) и глутатионпероксидаза (ГП), глутатион-8-трансфераза.
Антиоксидантное действие ПНЖК, по мнению авторов [7], объясняется результатом как их радикалсвязывающей способности, или «экранирующим» эффектом последних, так и влиянием на активность антиоксидантных ферментов.
Таким образом, при воспроизведении дислипопротеинемии, вызванной введением индуктора, отмечалось усиление свободнорадикальных процессов, выражавшихся в повышении уровня продуктов ПОЛ и снижении суммарного содержания антиоксидантов в тканях экспериментальных крыс. Превентивное применение ПНЖК в липосомальной форме приводило к достоверному понижению уровня продуктов ПОЛ как в крови, так и в печени живот- ных, но при этом существенно не изменяло уровня ССА в анализируемых тканях гиперли-пидемированных крыс.


