Влияние лорноксикама на системную воспалительную реакцию у больных острым панкреатитом. Клиническое рандомизированное исследование
Автор: Галлямов Э.А., Агапов М.А., Малахов П.С., Какоткин В.В.
Журнал: Хирургическая практика @spractice
Статья в выпуске: 4, 2019 года.
Бесплатный доступ
Пусковым патогенетическим механизмом локальных и системных воспалительных изменений при остром панкреатите является продукция медиаторов воспаления и, в частности, цитокинов. Всё это обуславливает позиционирование системной воспалительной реакции как мишени для терапевтического воздействия.Целью исследования явилось оценить анальгетический эффект терапии лорноксикамом, а также изучить влияние препарата на системную воспалительную реакцию у больных острым панкреатитом.Материалы и методы: в рандомизированное проспективное исследование включены 334 пациента с острым панкреатитом в возрасте от 25 до 68 лет. Больные были разделены на две группы. Пациентам 1 группы (n = 246) проводилась только стандартная консервативная терапия; 88 пациентов 2 группы дополнительно получали препарат лорноксикам. Производилась оценка выраженности болевого синдрома и частоты послеоперационных осложнений.Результаты: Во второй группе больных системные осложнения развивались статистически значимо реже (р = 0,00034), летальность была также статистически значимо меньше (р = 0,006)...
Острый панкреатит, лорноксикам, обезболивание, цитокины
Короткий адрес: https://sciup.org/142224490
IDR: 142224490 | УДК: 617-089.844 | DOI: 10.17238/issn2223-2427.2019.4.32-39
The effect of lornoxicam on the systemic inflammatory response in patients with acute pancreatitis. Clinical randomized trial
The trigger pathogenetic mechanism of local and systemic inflammatory changes in acute pancreatitis is the production of inflammatory mediators and, in particular, cytokines. It determines the positioning of the systemic inflammatory response as a target for therapeutic action.The aim of research: evaluation of the analgesic effect of lornoxicam therapy, as well as studying the effect of the drug on the systemic inflammatory response in patients with acute pancreatitis.Materials and methods: the randomized prospective study included 334 patients with acute pancreatitis aged 25 to 68 years. The patients were divided into two groups. Patients in group 1 (n = 246) were treated only with standard conservative OP therapy; 88 patients in group 2 were additionally treated with lornoxicam. The severity of the pain syndrome and the frequency of postoperative complications were evaluated. Results: In the second group of patients, systemic complications developed statistically significantly less frequently (p = 0...
Текст научной статьи Влияние лорноксикама на системную воспалительную реакцию у больных острым панкреатитом. Клиническое рандомизированное исследование
Тяжелый острый панкреатит (ТОП) остается одной из самых актуальных проблем ургентной хирургии. Проведенные эпидемиологические исследования свидетельствуют о том, что заболеваемость ОП составляет от 48 до 238 случаев на миллион населения, из них ТОП составляет 10–25 %, а общая летальность — 9–20 %. Причиной смертности в первые 6 суток являются в большинстве случаев легочные осложнения и, в частности, респираторный дистресс-синдром. Большинство летальных исходов после первой недели заболевания вызваны инфицированным панкреонекрозом и сепсисом. Таким образом, в настоящий момент отчетливо вырисовывается высокая медико-социальная значимость проблемы ОП [1]. При ОП в результате гибели большого количества собственных клеток организма происходит высвобождение значительных концентраций продуктов деградации тканей, что приводит к активации различных сигнальных путей, активации клеток иммунной системы и запуску выработки провоспалительных цитокинов [2]. В настоящее время доказана роль интерлейкинов (ИЛ): ИЛ-1, ИЛ-6, ИЛ-8, фактора некроза опухолей альфа (ФНОa), а также циклооксигеназы (ЦОГ). Последние занимают ведущее значение в патогенезе острого панкреатита [2]. Результатами их влияния является: увеличение сосудистой проницаемости, миграция лейкоцитов, локальное повреждение тканей, генерализация воспалительной реакции, повреждение почек, легких и других органов и в особо тяжелых случаях — развитие полиор-ганной недостаточности [3].
Патофизиология боли при ОП еще не до конца изучена. Тем не менее в настоящее время известен ряд основополагающих механизмов. Локальное высвобождение из поврежденных тканей медиаторов воспаления (в том числе цитокинов) стимулирует общую воспалительную реактивность [4]. Эти медиаторы непосредственно включаются в стрессовые реакции, так как, циркулируя в крови, они вызывают гормональные сдвиги в отдаленных «пусковых» органах (в том числе и в гипофизе). Эти медиаторы включаются в течение стрессовых реакций также и опосредованно, усиливая ноцицептивную афферентную трансмиссию, вызывая или потенцируя при этом высвобождение гипоталамических гормонов. То есть происходит и опосредованный запуск невральных стимулов, которые остаются ведущими в механизмах развития боли при ОП. Таким образом, природа реакций, приводящих к развитию болевого синдрома при ОП, сложна. Она включает невральные, гуморальные и воспалительные механизмы [5]. Пока еще невозможно выделить одну группу механизмов, которые бы в определенном соотношении были бы применимы к каждому из компонентов взаимосвязанного комплекса реакций [6, 7].
Учитывая вышесказанное, применение НПВС в комплексном лечении ТОП выглядит патогенетически обоснованным как с позиций контроля над выраженной воспалительной реакцией, так и с точки зрения адекватного обезболивания. Поэтому в данной работе мы проанализировали эффект терапии лорноксикамом на интенсивность болевого синдрома и уровень секреции цитокинов у больных ТОП.
Материалы и методы
В рандомизированное проспективное исследование включены 334 пациента с острым панкреатитом в возрасте от 25 до 68 лет, находившиеся на лечении с 2012 по 2018 г. в ГКБ имени И.В. Давыдовского Департамента здравоохранения г. Москвы. Мужчин было 211 (63,2 %), женщин — 123 (36,8%). Больные были разделены на две группы. Пациентам 1 группы (n = 246) проводилась только стандартная консервативная терапия ОП; 88 пациентов 2 группы дополнительно получали препарат лорноксикам. Последний вводили внутривенно капельно два раза в сутки в течение пяти суток от момента поступления.
Консервативная терапия ОП включала следующие компоненты: анальгетическую, спазмолитическую терапию, обеспечение функционального покоя поджелудочной железы путем медикаментозного подавление внешней секреции с использованием октреотида по 100–300 мкг 3 раза в сутки и ингибиторов протоновой помпы (контролок 40 мг два раза в/в), инфузионную корригирующую терапию. Всем больным проводилась комбинированная нутритивная поддержка (внутривенно и энтерально сбалансированные смеси через установленный назоинтестинальный зонд) с первых суток стационарного периода.
Интенсивность болевого синдрома в обеих группах мы оценивали каждые восемь часов с использованием визуальной аналоговой шкалы боли (ВАШ) [8], масштабируемой от нуля до десяти (где ноль означает отсутствие боли, а десять — сильную, но терпимую боль). В нашей клинике рутинное лечение болевого синдрома при ОП складывалось из нескольких ступеней. В случае неинтенсивного болевого синдрома использовали НПВС. При более выраженной боли к НПВС добавляли анальгетики из группы опиоидов. Интенсивный болевой синдром являлся показанием к постановке эпидурального катетера. В группе сравнения базовым препа- ратом из группы НПВС был кеторолак (30 мг два раза в сутки в/м).
Для определения эффективности противовоспалительного эффекта оценивали следующие показатели: частоту системных осложнений ОП, общую летальность, продукцию цитокинов: ИЛ-6, ИЛ-8, ФНОa. Содержание цитокинов определяли методом ИФА с использованием коммерческих наборов для иммуноферментного анализа (e-Biosciences). Для определения всех вышеописанных параметров забор крови производили у пациентов на 1, 3, 7 и 12-е сутки стационарного лечения.
Статистическую обработку результатов исследований производили в программном пакете StatSoft Statistica 6.0 с использованием непараметрических критериев. Для сравне- ния групп по количественным признакам использовали U-критерий Манна-Уитни и критерий Вилкоксона. Различия показателей в группах считали статистически значимым при р < 0,05.
Результаты
Системные осложнения ОП развились у 172 (51,5 %) из 334 пациентов (Таблица 1). У большинства больных в обеих группах зафиксировано сочетание нескольких системных осложнений ОП. Самым частым осложнением была недостаточность желудочно-кишечного тракта, проявляющаяся парезом кишечника. Во второй группе больных ОП системные осложнения развивались статистически значимо реже (р = 0,00034), летальность была также статистически значимо меньше (р = 0,006).
Таблица 1.
Системные осложнения у больных ОП
|
Вид осложнения панкреатогенной токсемии |
Группа 1 (n=246), n (%) |
Группа 2 (n=88), n (%) |
p |
Итого (n=334), n (%) |
|
Панкреатогенный шок |
30 (12,2) |
6 (6,8) |
0,276 |
36 (10,8) |
|
Острая сердечно-сосудистая недостаточность |
49 (19,9) |
12 (13,6) |
0,191 |
61 (18,3) |
|
Острая почечная недостаточность |
99 (40,2) |
28 (31,8) |
0,163 |
127 (38) |
|
Интоксикационные расстройства сознания |
42 (17,1) |
9 (10,2) |
0,126 |
51 (15,3) |
|
Недостаточность желудочно-кишечного тракта |
116 (47,2) |
30 (34,1) |
0,034 |
146 (43,7) |
|
Острая дыхательная недостаточность |
28 (11,4) |
9 (10,2) |
0,767 |
37 (11,1) |
|
Острая печеночная недостаточность |
61 (24,8) |
19 (21,6) |
0,546 |
80 (24) |
|
Всего |
141 (57,3) |
31 (35,2) |
0,00034 |
172 (51,5) |
|
Летальность |
47 (19,1) |
6 (6,8) |
0,006 |
53 (15,9) |
Оценка анальгетического эффекта лорноксикама
Анализ данных ВАШ показал, что в определенные временные промежутки существовала статистически значимая разница в интенсивности болевого синдрома между двумя группами пациентов. Первое измерение проводилось сразу при поступлении больного в стационар перед началом лечения. Средние значения баллов ВАШ в группах составили 6,53 (группа 1) против 7,28 (группа 2), р = 0,57. Таким образом, перед началом исследования статистически значимых различий в интенсивности болевого синдрома между группами не было. После первого введения 16 мг лорноксикама в первой группе средний бал ВАШ составил 1,8 против 3,5 во второй группе (р = 0,02).
После второго введения НПВС в первой группе бал ВАШ составил 0,53 против 1,1 (р = 0,86).
На третий день стационарного лечения средний бал ВАШ в первой группе был 1,38 против 1,86 (р = 0,69), на 7-й день — 0,2 против 2,33 (р = 0,034), на 12-й день — 1,0 против 2,8 (р = 0,053) (Рисунок 1).
Анализ синтеза цитокинов у пациентов с системными осложнениями ОП
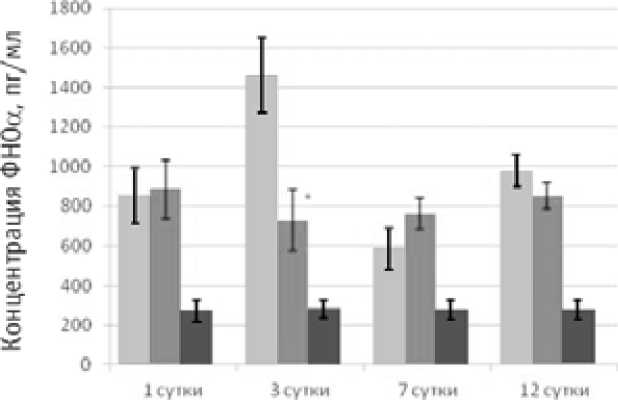
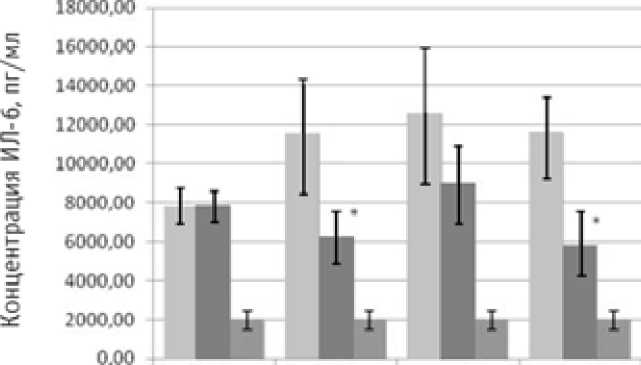
У пациентов с различными осложнениями панкреатогенной токсемии мы проанализировали секрецию ФНОa, ИЛ-6 и ИЛ-8 в динамике. У больных обеих групп в первые сутки отмечается значительное увеличение выработки про-воспалительных цитокинов ФНОa, ИЛ-6 и ИЛ-8 в перифе- рической крови по сравнению с группой здоровых доноров. У пациентов группы 1 на третьи сутки стационарного периода отмечается повышение уровня продукции ФНОa,
ИЛ-6 и ИЛ-8, тогда как у пациентов группы 2 секреция цитокинов снижается и статистически значимо отличается от уровня цитокинов у больных группы 1 (Рисунок 2–4).

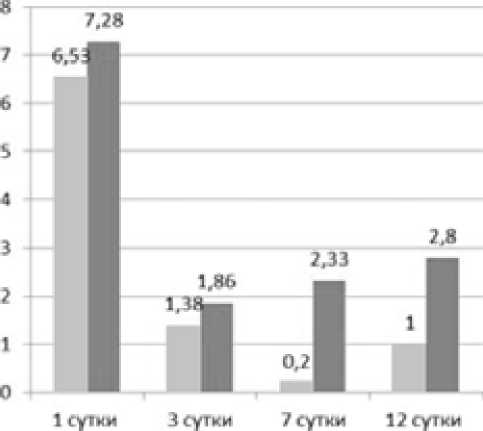
Рисунок 1. Динамика интенсивности болевого синдрома по ВАШ
больные группы 1
■ рольные группы 2
Больны? Группу 1
-
■ Больные группы 2
-
■ Здорп вые доноры
Рисунок 2. Секреция ФНОa у больных ОП.
*Статистически значимые различия значений между группами, р < 0,05
ItyiKW З-п'тня 7^утнн IltYitiH
Больные группы 1
-
■ Больные группы 2
-
■ Здоровые доноры
Рисунок 3. Секреция ИЛ-6 у здоровых доноров и больных с системными осложнениями ОП.
*Статистически значимые различия значений между группами больных
■ Больные группы 1■ Больные группы 2
Здоровые доноры
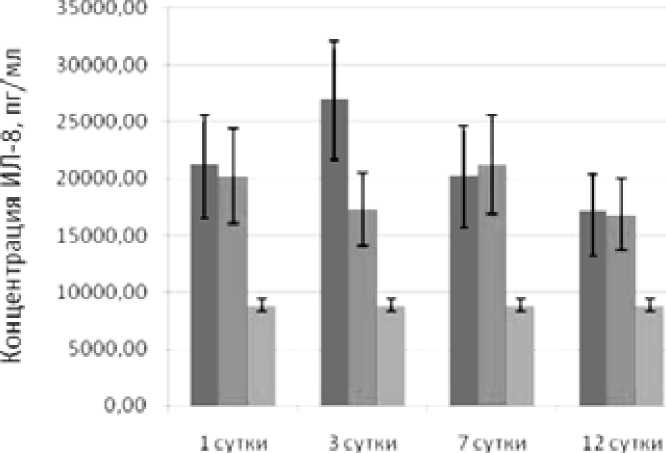
Рисунок 4. Секреция ИЛ-8 у здоровых доноров и больных с системными осложнениями ОП
В первые сутки в обеих группах уровень секреции ИЛ-8 значительно превосходит показатели, полученные в группе здоровых доноров. На третьи сутки ИЛ-8 во группе 2 снижается, в то время как в группе 1 данный показатель продолжает увеличиваться.
На 7-е сутки в группе 2 мы наблюдали некоторое повышение выработки цитокинов по сравнению с показателями в этой группе больных на третьи сутки, что может быть обусловлено прекращением проведения терапии лорноксика-мом.
Обсуждение
В нашем исследовании у больных отсутствовали осложнения, связанные с приемом лорноксикама, что говорит о безопасности препарата и выбранных режимов дозирования. Возрастание тяжести и частоты осложнений панкреатогенной токсемии происходит по мере увеличения распространенности деструктивного процесса в поджелудочной железе [9]. В свою очередь системные проявления в виде легочной, сердечно-сосудистой, почечной и печеночной недостаточности патогенетически обусловлены в основном массивным выбросом и циркуляцией медиаторов воспаления, в которых доминирующим пулом выступают провоспалительные цитокины (ИЛ-6, ИЛ-8, ФНОa) [10].
В нашем исследовании мы выявили повышенную выработку ФНОa, ИЛ-6 и ИЛ-8 у больных ОП на первой неделе заболевания. ФНОa — один из медиаторов системной прогрессии и разрушения тканей при тяжелых заболеваниях. Он участвует в индукции генов провоспалительных молекул, клеточной гибели, вовлечении и активации клеток иммунной системы. Чрезмерная продукция ФНОa приводит к развитию системного воспаления. В связи с этим ФНОa играет важную роль в развитии системных проявлений ОП и по-лиорганной дисфункции. Существуют противоречивые данные о продукции ФНОa при ОП. В работах исследователей показано, что уровень ФНОa, продуцируемый выделенными МНК больных ОП, не отличался от значений в контрольной группе и не коррелировал с тяжестью заболевания. В других исследованиях повышенные уровни ФНОa, вырабатываемые МНК больных ОП на первой неделе заболевания, коррелировали с развитием системного воспаления [11].
Известно, что у больных ОП важное прогностическое значение имеют уровни ИЛ-6 и ИЛ-8, которые коррелируют с тяжестью заболевания [12,13]. При анализе оцениваемых показателей в группе пациентов, получавших лорноксикам, выявили, что у больных этой группы происходит достоверное снижение выработки провоспалительных цитокинов на третьи сутки заболевания по сравнению с больными, находящимися на стандартной терапии. Наличие статистически значимого снижения секреции ФНОa, ИЛ-6 на третьи сутки в группе 2 может являться следствием проводимой терапии лорноксикамом. Снижение секреции ИЛ-8 в группе
-
1 на третьи сутки может являться следствием проведения терапии лорноксикамом.
Известно, что ИЛ-8 играет ключевую роль в механизмах развития повреждения тканей при гипоксии с последующей реперфузией [13]. На третьи сутки при ОП после коррекции нарушений центральной гемодинамики происходит реперфузия тканей после временной ишемии. При этом восстановление кровотока в тканях вызывает более значительные повреждения, чем это происходит в период ишемии. Механизм этого явления во многом связан с повышенной секрецией ИЛ-8. Последняя приводит к активации нейтрофильных лейкоцитов, генерации свободных радикалов кислорода и повреждению тканей. Поэтому в нашем исследовании пик продукции ИЛ-8 в группе сравнения зафиксирован на третьи сутки, т.е. повышенная экспрессия ИЛ-8 в начале заболевания может служить доказательством процессов реперфузионного повреждения тканей, усугубляющих течение ОП.
В 1986 г. ВОЗ представила пошаговую стратегию лечения боли, где вначале целесообразно использование монотерапии ПНВС, а при более выраженном болевом синдроме — комбинаций с опиоидами [14]. Ранее считалось, что использование производных морфина в лечении ОП является небезопасным из-за влияния последнего на сфинктер Одди [15]. Новейшие исследования, в том числе метаанализы, показали, что опиоидные анальгетики могут назначаться при ОП и выражение «опиоидам нет места в лечении ОП» следует считать устаревшим [16]. Тем не менее существует целый ряд неблагоприятных эффектов опиоидов (угнетение дыхания в первую очередь), что ограничивает их применение при ОП [17]. Более интенсивный болевой синдром является показанием к проведению эпидуральной анальгезии. Такой способ введения локальных анестетиков при ОП обеспечивает хорошее обезболивание, но не оказывает ингибирующего действия на стрессовые реакции, запущенные патологическим процессом, хотя в последнее время появляются данные об улучшении процессов микроциркуляции и окисгенации тканей зоны первичного повреждения [18].
Патофизиология болевого синдрома при ОП сложна, и в этом каскаде между местом повреждения и моментом восприятия боли лежит целая серия сложных электрохимических явлений, которые и рассматриваются как мишени терапевтического воздействия. Изначально воспалительный процесс в поджелудочной железе и парапанкреатической клетчатке трансформируется в виде электрической активности на окончаниях чувствительных нервов, затем по проводящим путям попадает в ЦНС. Таким образом, становятся понятны все точки приложения обезболивания при ОП. На проведение нервного импульса можно влиять при помощи эпидурального введения местных анестетиков, на процессы модуляции в ЦНС — системным введением опиоидов. Зона же первичного повреждения является точкой приложения НПВС, и в данном контексте применение последних выглядит как патогенетически обусловленное воздействие не только на болевой синдром, но и на зону первичного аффекта.
В нашем исследовании лорноксикам пациентам первой группы вводили как в качестве монотерапии (83 %), так и в комбинации с опиоидами (5,7 %) и эпидуральным обезболиванием (11,3 %). То есть лорноксикам в лечении ОП является эффективным анальгетиком как самостоятельно, так и в комбинации схем мультимодального обезболивания и обладает выраженным противовоспалительным эффектом, который, учитывая снижение концентрации цитокинов, носит системный характер.
Заключение
Боль в животе является самым ранним и ведущим симптомом у больных ОП. Существуют также веские доказательства того, что выраженность боли может являться прогностическим признаком дальнейшего клинического течения ОП. Купирование болевого синдрома при ОП по-прежнему остается сложной задачей и предполагает системное воздействие на все звенья патогенеза болевого синдрома.
В нашем исследовании применение лорноксикама на начальных этапах развития ОП снижало чрезмерную выработку провоспалительных цитокинов и риск развития ССВР, а также приводило к адекватному купированию боли. Таким образом, включение в комплекс консервативных мероприятий терапии лорноксикамом у больных ОП позволило добиться снижения не только интенсивности болевого синдрома, но и частоты развития осложнений панкреатогенной токсемии и уменьшить летальность у данной категории пациентов.
Список литературы Влияние лорноксикама на системную воспалительную реакцию у больных острым панкреатитом. Клиническое рандомизированное исследование
- Cartmell M.T., Kingsnorth A.N. Acute pancreatitis. Hosp Med. 2000 Jun; 61(6):382-5. [] DOI: 10.12968/hosp.2000.61.6.1350
- Guillaumes S., Blanco I., Villanueva A., Sans M.D., Clave P., Chabes A. et al. Chloroquine stabilizes pancreatic lysosomes and improves survival of mice with diet-induced acute pancreatitis.Pancreas. Pancreas. 1997 Apr; 14(3):262-6. [] DOI: 10.1097/00006676-199704000-00007
- Sawa H., Ueda T., Takeyama Y., Yasuda T., Shinzeki M., Nakajima T. et al. Role of Toll-like receptor 4 in the pathophysiology of severe acute pancreatitis in mice. Surg Today. 2007; 37(10):867-73. [10.1007/ s00595-007-3520-x] DOI: 10.1007/s00595-007-3520-x
- Carr D.B., Ballantyne J.C., Osgood P.F., Kemp J.W., Szyfelbein S.K. Pituitary-adrenal stress response in the absence of brain-pituitary connections. Anesth Analg. 1989 Aug; 69(2):197-201
- Hurgreaves K.M., Dionne R.A. Evaluating endogenous mediators of pain and analgesia in clinical studies, p. 579. In: Max MB, Portenoy RK, Laska EM (cds): The Design of Analgesic Clinical Trials. Advances in Pain Research and Therapy. Vol. 18. Raven Press, New York, 1991
- Factors determining the pattern of stress responses, p.17. In Usdin E., Kvetnansky R., Axelrod J. (eds): Stress. The Role of Catecholamines and Other Neurotransmitters. Gordon and Breach Science Publishers, New York, 1983
- Smelik P.G. Summary of panel discussions on stress, p. 69. In Usdin E., Kvetnansky R., Axelrod J. (eds): Stress. The Role of Catecholamines and Other Neurotransmitters. Gordon and Breach Science Publishers, New York, 1983
- Williamson A., Hoggart B. Pain: a review of three commonly used pain rating scales. J Clin Nurs. 2005 Aug; 14(7):798-804. [https://doi. org/.x]
- DOI: 10.1111/j.1365-2702.2005.01121
- Cruz-Santamaria D.M., Taxonera C., Giner M. Update on pathogenesis and clinical management of acute pancreatitis. World J Gastrointest Pathophysiol. 2012 Jun 15; 3(3):60-70. [10.4291/wjgp. v3.i3.60.]
- DOI: 10.4291/wjgp.v3.i3.60
- Kylanpaa M.L., Repo H., Puolakkainen P.A. Inflammation and immunosuppression in severe acute pancreatitis. World J Gastroenterol. 2010 Jun 21; 16(23):2867-72. []
- DOI: 10.3748/wjg.v16.i23.2867
- Malleo G., Mazzon E., Siriwardena A.K., Cuzzocrea S. Role of tumor necrosis factor alpha in acute pancreatitis: from biological basis to clinical evidence. Shock. 2007 Aug; 28(2):130-40. [10.1097/ shk.0b013e3180487ba1]
- DOI: 10.1097/shk.0b013e3180487ba1
- Inagaki T., Hoshino M., Hayakawa T., Ohara H., Yamada T., Yamada H. et al. Interleukin-6 is a useful marker for early prediction of the severity of acute pancreatitis. Pancreas. 1997 Jan; 14(1):1-8. [https://doi. org/]
- DOI: 10.1097/00006676-199701000-00001
- Novovic S., Andersen A.M., Ersboll A.K., Nielsen O.H., Jorgensen L.N., Hansen M.B. Proinflammatory cytokines in alcohol or gallstone induced acute pancreatitis. A prospective study. JOP. 20.09 May 18; 10(3):256-62.
- Helm J.F., Venu R.P., Geenen J.E., Hogan W.J., Dodds W.J., Toouli J et al. Effects of morphine on the human sphincter of Oddi. Gut. 1988 Oct; 29(10):1402-7. []
- DOI: 10.1136/gut.29.10.1402
- Jakobs R., Adamek M.U., von Bubnoff A.C., Riemann J.F. Buprenorphine or procaine for pain relief in acute pancreatitis. A prospective randomized study. Scand J Gastroenterol. 2000 Dec; 35(12):1319-23. [https:// ]
- DOI: 10.1080/003655200453692
- Mitchell R.W.D., Smith G. The control of acute postoperatice. Br J Anaesth. 1989 Aug; 63(2):147-58. []
- DOI: 10.1093/bja/63.2.147
- Bachmann K.A., Trepte C.J., Tomkotter L., Hinsch A., Stork J., Bergmann W. et al. Effects of thoracic epidural anesthesia on survival and microcirculation in severe acute pancreatitis: a randomized experimental trial. Crit Care. 2013 Dec 5; 17(6):R281.. [10.1186/ cc13142]
- DOI: 10.1186/cc13142
- Organization W.H. Traitement de la douleur cancereuse. Geneva, Switz: World Health Organization, 1987


