Влияние меди на образование биопленок у штаммов рода Enterococcus, выделенных из водной экосистемы с антропогенной нагрузкой
Автор: Ускова С.С., Мартынова А.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2025 года.
Бесплатный доступ
Для выживания в неблагоприятных условиях внешней среды бактерии рода Enterococcus инициируют различные оборонительные стратегии. Например, они способны переходить в некультивируемое, но жизнеспособное состояние (VBNC – viable but noncultivable) или образовывать биопленки. Биопленка представляет собой пористую и сложную структуру, образованную микроорганизмами одного или нескольких видов, организованную в несколько слоев клеток, необратимо прикрепленных к биотической или абиотической поверхностям и заключенную в матрицу, состоящую из внеклеточных полимерных веществ. Цель настоящего исследования − изучить влияние меди на образование биопленок представителями рода Enterococcus, выделенных в период с 10 марта 2018 г. по 24 сентября 2020 г. из водной экосистемы с антропогенной нагрузкой. В результате исследования процесса формирования биопленок установлено изменение морфологии биопленок в зависимости от присутствия меди, концентрации и конкретного вида энтерококков.
Медь, биопленки, Enterococcus, E. faecalis, E. faecium
Короткий адрес: https://sciup.org/147250954
IDR: 147250954 | УДК: 579.86 | DOI: 10.17072/1994-9952-2025-2-196-203
Effects of copper on biofilm formation in strains of the genus Enterococcus iso-lated from an aquatic ecosystem under anthropogenic stress
Bacteria of the genus Enterococcus can enter an uncultivated but viable state or form biofilms in order to survive in adverse conditions. A biofilm is a porous and complex structure formed by one or more spe-cies of microorganisms, organized into several layers irreversibly attached to a biotic or abiotic surface and en-closed in a matrix consisting of extracellular polymeric substances. The aim of this study is to investigate the effects of copper on biofilm formation in strains of the genus Enterococcus isolated from an aquatic ecosystem under anthropogenic stress. A study of biofilm formation in 30 strains of the genus Enterococcus isolated from anthropogenic aquatic ecosystems from March 10, 2018 to September 24, 2020 revealed that the morphology of biofilms varies depending on the presence of copper, their concentration and the type of enterococci (E. faecalis and E. faecium).
Текст научной статьи Влияние меди на образование биопленок у штаммов рода Enterococcus, выделенных из водной экосистемы с антропогенной нагрузкой
В настоящее время существует серьезная проблема, связанная с устойчивостью энтерококков к клинически важным антибиотикам, в частности к аминогликозидам, гликопептидам, включая ванкомицин, и хинолонам [Tacconelli, Cataldo, 2008]. Энтерококки склонны к генетическому обмену через транспозоны и плазмиды, что привело к распространению генов устойчивости к антибиотикам [Witte, 2004]. Кроме того, в недавнем отчете [Warnes et al., 2010] подчеркивается разрыв между разработкой новых антибиотиков и растущим числом инфекций, вызываемых множественными устойчивыми к антибиотикам микроорганизмами.
Энтерококки являются кишечными комменсалами и могут выдерживать высокие концентрации соли и значения рН, типичные для кишечника человека. Известно, что они могут выживать в окружающей среде в течение длительного времени. Они также могут выживать на мягких поверхностях, включая больничные постельные принадлежности и пластмассы [Neely, Maley, 2000], обивку мебели, напольные и настенные покрытия, и могут быть устойчивыми к воздействию широко применяемых чистящих средств, включая гипохлорит натрия [Warnes et al., 2010].
Присутствие неподвижных микроорганизмов на абиотических поверхностях может вызвать серьезные проблемы, приводящие к значительным затратам и негативным последствиям в различных областях, таких как здравоохранение и лечебные учреждения, системы водного транспорта, судоходство и морская промышленность, а также теплообменники и системы охлаждения [Gomes, Simoes, Simoes, 2020].
Биопленка представляет собой многоклеточную структуру, образованную микроорганизмами. Помимо микробных клеток, в ее состав входят вода и внеклеточное полимерное вещество, известное как экзо-полисахаридный матрикс. Это вещество состоит из полисахаридов, белков, нуклеиновых кислот и поверхностно-активных веществ [Liu et al., 2019]. Биопленка служит защитой от повреждений, особенно при воздействии неблагоприятных факторов окружающей среды. Она позволяет микроорганизмам прочно прикрепляться как к биотическим, так и к абиотическим поверхностям [Lange et al., 2021]. Экзополи-сахаридный матрикс может быть непроницаемым для противомикробных препаратов, что затрудняет проникновение последних в биопленку [Mah, O’Toole, 2001].
«Чувство кворума» является основным средством коммуникации в бактериальных скоплениях. Каждая клетка вырабатывает химические соединения, такие как бактериоцины, и экспрессирует определенные гены. Это явление считается механизмом устойчивости. Чем выше плотность популяции микроорганизмов, тем больше выделяется самоиндуцирующих соединений. Происходят изменения в экспрессии генов, и в итоге меняется вся популяция [Liu et al., 2019]. Преобладание устойчивых к лекарствам бактерий в биопленках является одной из причин, по которой бактериальные инфекции трудно поддаются лечению. Лекарства также могут быть неэффективны против бактерий, находящихся в биопленке [Lange et al., 2021].
Для борьбы с образованием биопленки могут быть использованы различные подходы, зависящие от условий окружающей среды и области применения [Gomes, Simoes, Simoes, 2020]. Наиболее распространенные методы борьбы с биопленками включают использование противомикробных средств, таких как дезинфицирующие средства и биоциды для обработки поверхности, или антибиотиков для борьбы с биопленками, связанными со здоровьем человека. Однако использование химических веществ часто неэффективно и способствует развитию резистентности бактерий. Для удаления биопленок с различных поверхностей могут использоваться механические методы, которые основаны на воздействии механической нагрузки, способной преодолеть силы, удерживающие биопленку на поверхности тела. Это приводит к ее отсоединению [Boudarel et al., 2018].
Механические методы используются в различных областях медицины. Например, для контроля зубных биопленок используют зубную щетку или нагнетают жидкость высокоскоростными струями воды. В медицинских приборах используется водяная щетка под давлением, а в системах распределения питьевой воды используется промывка труб. Для контроля биопленок на поверхностях, контактирующих с пищевыми продуктами, в основном используется ультразвук в сочетании с химическими методами [Yu et al., 2020]. Ультразвук способствует физическому разрушению биопленок, создавая лучшие условия для антимикробного действия химических веществ. Использование поверхностных материалов с антимикробными и антиадгезивными свойствами является важной стратегией развития. Они широко изучаются в качестве профилактической меры и альтернативы традиционным протоколам дезинфекции или антибактериальной терапии. Антимикробные поверхности можно разделить на те, которые используются для предотвращения адгезии и не влияют на жизнедеятельность микроорганизмов, и те, которые препятствуют их адгезии [Boudarel et al., 2018].
Медь – это микроэлемент, необходимый для нормального функционирования метаболизма большинства прокариотических и эукариотических организмов. В природе медь может находиться в окисленном (Cu+2) или восстановленном (Cu+1) состоянии. Она может действовать как донор или акцептор электронов при восстановлении или окислении различных субстратов [Latorre et al., 2011]. Благодаря таким свойствам этот переходный элемент оказывается необходимым для нормального протекания ряда биохимических процессов. С другой стороны, избыток меди может вызывать образование свободных радикалов в результате реакций Габера — Вейса и Фентона, которые способны повреждать клеточные мембраны, белки и ДНК. Такая двойственная природа меди объясняет необходимость в специальных системах регуляции, которые поддерживают клеточный гомеостаз этого металла [Gomes, Simoes, Simoes, 2020].
Поступление, перемещение внутри клетки, хранение и выведение — вот четыре основных этапа, необходимых для работы с этим металлом в клеточной среде. У бактерий одна из наиболее изученных систем, контролирующих содержание меди, кодируется опероном cop . Этот оперон кодирует белки, которые могут контролировать внутриклеточное перемещение меди, регулировать поглощение и выведение металла, а также экспрессию самого оперона [Li et al., 2010]. Другой группой белков, которая также играет важную роль в поддержании уровня меди в клетке, является семейство cut . Одним из наиболее изученных представителей этого семейства является белок CutC. Хотя его роль в гомеостазе меди до конца не изучена, появляется все больше свидетельств того, что этот ген может экспрессироваться по-разному в ответ на воздействие меди, поскольку он может быть прямо или косвенно вовлечен в защиту от избытка этого металла [Latorre et al., 2011].
Существует несколько механизмов, приводящих к гибели бактерий при контакте с медью, они могут различаться в зависимости от вида микроорганизма и условий окружающей среды. Например, планктонные клетки, прикрепленные к поверхности или образующие биопленки, могут по-разному реагировать на взаимодействие с медью. При взаимодействии меди с микроорганизмами могут происходить различные процессы, такие как повреждение клеточной стенки, окислительное повреждение, вызванное образованием активных форм кислорода, ингибирование ферментов и деградация нуклеиновых кислот. Эти процессы могут привести к повреждению клеток и снижению клеточной активности [Hans et al., 2016]. Цель: изучить влияния меди на образование биопленок у штаммов рода Enterococcus, выделенных из водной экосистемы с антропогенной нагрузкой.
Материалы и методы исследования
Для исследования чувствительности штаммов рода Enterococcus к тяжелым металлам было изучено 18 образцов воды из устья р. Вторая Речка (43°16'045" с. ш., 131°54'05" в. д.), т. к. река находится в черте города и подвержена загрязнению тяжелыми металлами [Шулькин, Богданова, Киселев, 2007].
Было выделено 30 штаммов бактерий рода Enterococcus , идентификация которых проводилась методом полимеразной цепной реакции. Штаммы идентифицировали с помощью ПЦР с использованием известных праймеров гена 16S РНК: 5'-AACGCGAAGAACCTTAC-3' и 5'-CGGTGTGTACAAGACCC-3'. Размер амплифицированного фрагмента составил 440 п. о. [Skowron et al., 2016]. Синтез праймеров был осуществлен компанией «Синтол» (Москва, Россия).
Изучение устойчивости бактерий рода Enterococcus к меди проводилось на питательной среде для морских микроорганизмов (СММ), содержащей: CaCO₃ – 1.0 г/л, MgSO₄ – 1.0 г/л, пептон – 5.0 г/л, дрожжевой экстракт – 5.0 г/л, K₂HPO₄ – 0.2 г/л, глюкозу – 0.2 г/л, агар – 15.0 г/л и дистиллированную воду – 1 000 мл. В качестве селективной добавки добавляли соли меди CuSO₄ в возрастающих концентрациях. Автоклавирование проводили при 121°C в течение 15 мин. Суточную культуру бактерий засевали на чашки Петри с питательной средой СММ. Посев проводили в трех повторах. Культуру выращивали при комнатной температуре в течение 2–3 суток. Результаты учитывали по наличию или отсутствию роста на чашках с металлами [Бузолева, 2011].
Исследование устойчивости биопленок к меди проводился на жидкой питательной среде ГРМ (ФБУН ГНЦ ПМБ, Оболенск, Россия) с добавлением возрастающей концентрации соли меди CuSO₄. Из суточной культуры бактерий делали суспензию мутностью 0.5 по стандарту МакФарланда и засевали по 50 мкл в одноразовую чашку Петри с жидкой питательной средой ГРМ. Посев проводили в трех повторах. Культуру выращивали при температуре 37ºС в течение 2–3 суток. Результаты учитывали по наличию или отсутствию роста на чашках с металлами после окрашивания 1% раствором генциан фиолетовым [Мар-данова и др., 2016].
Морфологию бактериальных клеток оценивали методом окраски по Граму [Прунтова, 2005]. Биопленки окрашивали 1% раствором генциан фиолетовым [Марданова и др., 2016]. Исследование проводили с помощью микроскопа марки Primo Start производства Zeiss. Отмечали окраску мазка, а также размер, форму и способ расположения бактерий на предметном стекле.
Статистическая обработка данных проводилась в программе STATISTICA 10. Графики и таблицы формировались в программе Excel.
Результаты и обсуждение
При исследовании чувствительности бактерий рода Enterococcus , выделенных из р. Вторая Речка, было выявлено, что все изученные штаммы способны к росту при концентрациях меди, превышающих предельно допустимые значения (ПДК). ПДК для меди в морской воде составляет 0.05 мг/л, а в пресной — 0.01 мг/л [Коршенко, 2020].
При концентрации меди в среде 1 450 мг/л рост 43% (13) штаммов Enterococcus spp. значительно снижался, что позволяет классифицировать эти штаммы как чувствительные. Однако 17% (5) штаммов демонстрировали рост при концентрации 1 500 мг/л. Концентрация 1 550 мг/л являлась минимально ингибирующей концентрацией (рис. 1). Также были зафиксированы изменения в культуральных свойствах бактерий. При увеличении концентрации меди в среде культивирования бактерий до 1 400 мг/л формировались непрозрачные колонии оранжевого цвета с металлическим блеском. В то же время другие колонии становились прозрачными. Кроме того, наблюдались изменения в морфологии бактериальных клеток . При концентрации 800 мг/л клетки располагались парами. При концентрации 1 400 мг/л клетки также располагались парами, при этом размер клеток незначительно увеличивался. При концентрации 1 500 мг/л клетки располагались парами и короткими цепочками, а также становились более круглыми по сравнению с клетками, выращенными в присутствии более низких концентраций меди в среде [Ускова, Мартынова, 2024].
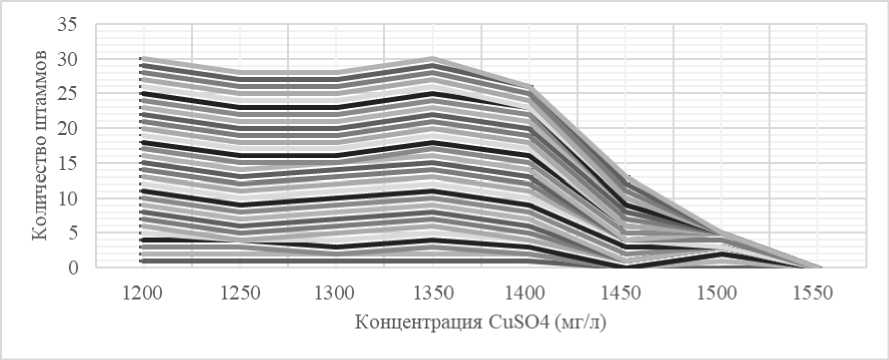
Рис. 1. . Влияние различных концентраций меди на рост бактерий Enterococcus [Ускова, Мартынова, 2024]
[Effect of different copper concentrations on the growth of Enterococcus bacteria [Ускова, Мартынова, 2024] ]
Биопленки, образованные представителями E. faecalis , состоят из плотных скоплений овальных кокков, объединенных внеклеточным матриксом. С увеличением концентрации меди до 800 мг/л клетки образуют менее плотные скопления, размер бактериальных клеток уменьшается. При концентрации 1 500 мг/л клетки также образуют менее плотные скопления, но появляются клетки разных размеров (рис. 2).
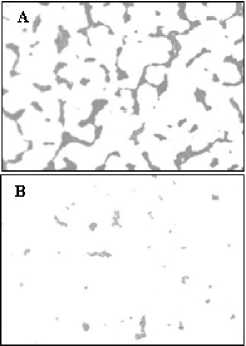
Рис. 2. Влияние различных концентраций меди на формирование биопленки E. faecalis (микроскоп Primo Start, 100x).
Концентрация CuSO 4 : А – контроль (среда ГРМ без добавления солей металлов), Б - 800 мг/л, В – 1 500 мг/л
[Effect of various copper concentrations on the formation of biofilm of E. faecalis (Primo Start microscope, 100x).
CuSO 4 concentration: A – control (timing medium without addition of metal salts),
B - 800 mg/l, C – 1 500 mg/L]
Биопленки штаммов E. faecium 1 состоят из плотных скоплений овальных кокков, объединенных внеклеточным матриксом. С увеличением концентрации меди до 800 мг/л значительные изменения не наблюдаются. При концентрации 1 500 мг/л клетки образуют менее плотные скопления, размер клеток увеличивается (рис. 3).
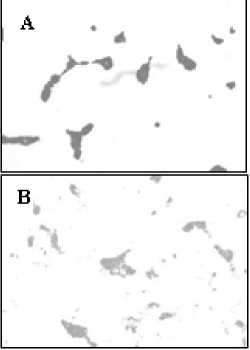

Рис. 3. Влияние различных концентраций меди на формирование биопленок штамма E. faecium 1 (микроскоп Primo Start, 100x). Концентрация CuSO 4 : А – контроль (среда ГРМ без добавления солей металлов), Б - 800 мг/л, В – 1 500 мг/л
[Effect of various copper concentrations on the formation of biofilms of E. faecium 1 strain (Primo Start microscope, 100x).
CuSO 4 concentration: A – control (timing medium without addition of metal salts), B -800 mg/l, C – 1 500 mg/L]
Биопленки штаммов E. faecium 2 состоят из плотных скоплений овальных кокков, объединенных внеклеточным матриксом. С увеличением концентрации меди до 800 мг/л образуются ромбовидные образования, в которых клетки расположены от одного края до противоположного. При концентрации 1 500 мг/л ромбовидные образования уменьшаются, а вокруг них образуется рыхлая биопленка, состоящая из небольших круглых кокков (рис. 4).
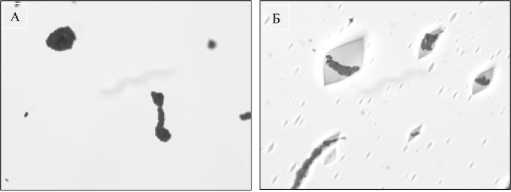
Рис. 4. Влияние различных концентраций меди на формирование биопленки штамма E. faecium 2 (микроскоп Primo Start, 100x). Концентрация CuSO 4 : А – контроль (среда ГРМ без добавления солей металлов), Б - 800 мг/л, В – 1 500 мг/л
[Effect of various copper concentrations on the formation of biofilms of E. faecium 2 strain (Primo Start microscope, 100x).
CuSO 4 concentration: A – control (timing medium without addition of metal salts), B - 800 mg/l, C – 1 500 mg/L]

Образование таких структур может быть связано с тем, что соли меди оказывают сильное окислительное воздействие на микроорганизмы. Это воздействие часто приводит к повреждению клеточных мембран, белков и ДНК. В ответ на это бактерии пытаются адаптироваться, что приводит к образованию биопленок. Внеклеточный матрикс биопленки может связывать ионы меди, снижая их концентрацию в окружающей среде. Внутри биопленки могут образовываться локальные области с разной концентрацией меди. Некоторые микроорганизмы способны выделять вещества, которые нейтрализуют токсичное действие меди.
Взаимодействие меди с биопленками отличается от взаимодействия с планктонными клетками. Процесс формирования биопленки включает в себя несколько этапов: первоначальное обратимое и необратимое прикрепление, созревание и дисперсию. Последний этап имеет решающее значение для закрепления биопленки в новых местах за счет отделения планктонных форм, которые инициируют формирование новых биопленок в других местах [Rabin et al., 2015].
Структура биопленки всегда одинакова, независимо от ее формы. Внутри бактериального сообщества находятся мелкие клетки с ограниченным потенциалом размножения, в то время как внешние области заняты метаболически активными клетками. Это связано с недостатком кислорода и питательных веществ в центре структуры биопленки [Lange et al., 2021]. Бактериальная неоднородность может способствовать развитию различных устойчивых свойств, которые могут распространяться на все бактериальное сообщество [Mah, O’Toole, 2001]. Бактерии, не обладающие устойчивостью, становятся менее чувствительными к про-тивомикробным препаратам при выращивании в структуре биопленки [Stewart, 2002].
В биопленках микроорганизмы защищены матрицей из экзополисахаридов. Следовательно, действие меди направлено не только на взаимодействие с микроорганизмами, но и нарушение структуры экзопо-лисахаридов. Однако влияние меди на образование экзополисахаридов изучено недостаточно [Lin et al., 2020]. Показано, что ионы меди в биопленках Pseudomonas aeruginosa в основном находятся в матрице экзополисахаридов, и лишь небольшая часть обнаруживается внутри клеток или в клеточной мембране и/или клеточной стенке [Gomes, Simoes, Simoes, 2020].
Однако механизмы действия меди могут варьироваться в зависимости от условий окружающей среды, таких как присутствие воды, температура, рН, присутствие других металлов или ионов, степень окисления, шероховатость поверхности и присутствие микроорганизмов на поверхности металла. Антимикробные свойства меди обычно связаны с высвобождением ионов меди, которые могут повреждать микробные клетки из-за изменения структуры и активности белков и ферментов.
Образование биопленки является эффективной стратегией для выживания и сохранения микробов в условиях стресса, например, в присутствии противомикробных препаратов и тяжелых металлов. Структура биопленки может быть связана с защитным механизмом, который позволяет бактериям выживать и сохраняться в средах с высокой концентрацией металлов [Muller, Medigue, Koechler, 2007]. Исследования показали, что субингибиторные концентрации тяжелых металлов могут вызывать образование биопленки [Kaplan et al., 2012], что изучалось на примере кадмия [Wu, Santos, Fink-Gremmels, 2015] и других металлов.
Заключение
Изучение влияния солей меди (CuSO 4 ) на штаммы бактерий рода Enterococcus , выделенных из водной экосистемы с антропогенной нагрузкой, показало, что концентрация меди 1 550 мг/л являлась минимально ингибирующей. С увеличением концентрации CuSO 4 изменялись морфология бактериальных клеток, культуральные свойства и форма биопленок. При концентрации CuSO 4 1 400 мг/л колонии приобретали оранжевый цвет и становились непрозрачными, а при 800 мг/л CuSO 4 клетки располагались попарно. При концентрациях CuSO 4 1 400 и 1 500 мг/л размер клеток увеличивался, клетки формировали пары и цепочки. Биопленки E. faecalis при 800 мг/л становились менее плотными, а при 1 500 мг/л в них появлялись клетки различных размеров. Биопленки E. faecium 1 в присутствии 1 500 мг/л CuSO 4 увеличивались в размере. У E. faecium 2 при 800 мг/л образовывались ромбовидные структуры, которые при концентрации CuSO 4 1 500 мг/л уменьшались, а вокруг формировалась рыхлая биопленка.


