Влияние мелатонина на макрофаги и клетки дисперсной эндокринной системы селезенки
Автор: Лузикова Елена Михайловна, Московский Александр Владимирович, Московская Олеся Игоревна, Ефремова Ольга Александровна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Краткие сообщения
Статья в выпуске: 1 т.24, 2016 года.
Бесплатный доступ
Изучена реакция Iba-I-позитивных клеток селезенки на введение мелатонина. Установлено, что введение мелатонина (препарат «Мелаксен») с водой перорально (раствор 4 мг препарата на 1 л Н2О) в течение 4 недель приводит к морфологическим изменениям: уменьшению среднего количества клеток макрофагального ряда (Iba-1+), увеличению количества лимфоидных узелков; уменьшению содержания катехоламинов и серотонина во всех иммунокомпетентных клетках красной и белой пульпы; снижению содержания гистамина в люминесцирующих гранулярных клетках красной пульпы.
Селезенка, мелатонин, макрофаги, нейроаминсодержащие клетки
Короткий адрес: https://sciup.org/143177079
IDR: 143177079
The effect of melatonin on macrophages and cells of the diffuse endocrine system of the spleen
Reaction of Iba-I positive cells in the spleen was studied on the introduction of melatonin. It was detected that oral administration of melatonin (drug «Melaxen») with water (solution 4 mg of the drug per 1 l H2O) for 4 weeks leads to morphological changes in the spleen: increase in quantity of lymphoid nodules, more pronounced in the spleen of animals kept by artificial darkening; decrease in the quantity of cells of the macrophage series (Iba-1+). Exogenous melatonin causes an increase in the number of lymphoid nodules, reducing the levels of catecholamines and serotonin in all immunocompetent spleen cells, reducing histamine content in luminescent cells of red pulp.
Текст научной статьи Влияние мелатонина на макрофаги и клетки дисперсной эндокринной системы селезенки
Введение. Мелатонин — нейропептид и нейротрансмиттер участвующий в синхронизации циркадных ритмов, оказывающий онкопротектор-ное [1], геропротекторное [5, 8] и иммуностимулирующее действие [5, 8, 9, 12]. Экстрапинеальный мелатонин играет ключевую роль в координации клеточных функций и межклеточных связей при иммунном ответе [14]. Одни исследователи считают, что мелатонин не оказывает ни прямого, ни опосредованного Т-лимфоцитами влияния на активированные макрофаги [16]. Результаты других исследований показывают, что количество натуральных киллеров и макрофагов в селезенке под влиянием мелатонина возрастает [11].
Ионизирующая кальций связывающая адапторная молекула (Iba-1) идентифицирована как кальций-связывающий белок, экспрессирующийся клетками моноцитарно-макрофагального происхождения [4]. Iba-1 принимает участие в реорганизации актинового скелета и образовании мембранных складок макрофагов при индуцированном фагоцитозе [13].
C помощью люминесцентно-гистохимических методов в селезенке обнаруживаются люминесцирующие гранулярные клетки (ЛГК), обладающие функцией синтеза и накопления и секреции биогенных аминов: ЛГК лимфоидных узелков, ЛГК на границе лимфоидного узелка (береговые ЛГК) и ЛГК красной пульпы (2, 3). ЛГК селезенки относятся к клеткам дисперсной эндокринной системы (APUD–серии) (9), которые играют большую роль в формировании местного гомеостаза Часть клеток диффузной эндокринной системы относится к макрофагальному ряду, например, дендритные клетки (3).
Цель исследования - выявить реакцию клеток макрофагального ряда и биоаминсодержащих клеток селезенки на экзогенный мелатонин.
Материал и методы исследования. Объектом исследования служила селезенки 60 двухмесячных мышей-самцов одной массы (18 - 22 г), содержавшихся при сбалансированном рационе питания и в различных условиях освещения.
Животные были разделены на 2 группы:
I - (n = 30) – животные, которые содержались в обычных условиях вивария в течение 4 недель эксперимента (естественное освещение; продолжительность светового дня 8 – 9 часов; освещенность на уровне клеток в утренние часы 50 – 150 люкс, днем в пасмурный день – до 500 люкс, в ясный день – до 1000 люкс, вечером 100 – 200
люкс; влажность воздуха 40 – 60%, свободный доступ к питьевой воде и корму);
II - (n = 30) – животные получали препарат мелаксен ad libium в концентрации 4 мг/литр с питьевой водой в течение 4 недель и находились в условиях обычного освещения (естественное освещение; продолжительность светового дня 8 – 9 часов; освещенность на уровне клеток в утренние часы 50 – 150 люкс, днем в пасмурный день – до 500 люкс, в ясный день – до 1000 люкс, вечером 100 – 200 люкс; влажность воздуха 50 – 70%);
Селезенка у животных забиралась после декапитации на 28-е сутки эксперимента во второй половине дня (1500 – 1700). Все действия, предусматривавшие контакт с лабораторными животными, осуществлялись с учетом требований «Правил проведения работ с использованием экспериментальных животных» («Приказ МЗ РФ от 19.06.2003 г. №267) и в соответствии с «Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях».
Криостатные срезы селезенки толщиной 5 мкм обрабатывались следующими методами: непрямым иммунофлуоресцентным методом по стандартному протоколу:
эндогенная пероксидазная активность подавлялась путем инкубации срезов в 3% растворе H2O2 в течении 30 минут с последующей трехкратной промывкой 0,1 М фосфатным буфером. Блок неспецифического связывания проводился преинкубацией срезов с 10% козьей сывороткой и 0,05% тритоном Х-100. В качестве первичных антител были использованы анти-Iba-1 (1:1000; rabbit polyclonal anti-Iba-1,Wako Chemicals GmbH, Neuss, Germany). Для визуализации Iba-1 использованы меченные флуорохромом вторичные антитела Alexa Fluor 488 (1:250; goat anti rat IgG; Invitrogen) [15]. Препараты анализировались при помощи светового микроскопа Микмед 5, подсчет структур проводился при увеличении 1500; люминесцентно-гистохимическим методом Фалька – Хилларпа (В. Falk, N.A. Hillarp et al., 1962.) в модификации Е.М. Крохиной (Е.М. Крохина, П.Н. Александров 1969) для избирательного выявления катехоламинов и серотонина в морфо-функциональных структурах тимуса. Срезы органов толщиной 10-15 мкм обрабатывались в параформальдегидной камере в течение 60 минут при температурном режиме термостата 80°С. При обработке тканей парами формальдегида моноамины превращаются в сильнофлуоресцирующие вещества (флуорофоры). При облучении видимым сине-фиолетовым светом низкие концентрации флюорофоров светятся изумрудно-зеленым, высокие – желтым светом. Серотонин под воздействием паров формальдегида превращается в 3,4-дигидро- ß-карболин – флюорофор, дающий желтое свечение;
методом цитоспектрофлуориметрии: уровень биоаминов в ТК определялся на микроскопе ЛЮМАМ-4 с помощью спектрофлуорометрической насадки ФМЭЛ –1А (В.Н. Карнаухов, 1978; В.Л. Калмыков, 1982) при выходном напряжении 900 В. Принцип данной процедуры заключается в следующем: ультрафиолетовые лучи определенной длины (390 нм), проходя через специальное отверстие – зонд диаметром 0,5 мм, направляются на препарат в темном поле. Зонд вырезает в плоскости препарата область, свет от которой идет на интерференционный светофильтр с определенной длиной волны. Для выявления интенсивности свечения гистамина используется сетофильтр № 7 (длина волны 515 нм). Флуорофоры катехоламинов в срезах образца начинают светиться с максимумом эмиссии 480 нм (фильтр № 6), свечение серотонина регистрируется на длине волны 525 нм (фильтр № 8). Замер интенсивности свечения производился в единицах флуоресценции (условные единицы по шкале регистрирующего прибора-усилителя У-5);
определением серотонинового индекса (Js)– безразменной величины, являющейся средней величиной от суммы частных соотношений содержания серотонина и катехоламинов в одной и той же клетке.
Js = [С]/[КА ] x N, где [С] – уровень серотонина, [КА] – уровень катехоламинов, N – число наблюдений. По динамике уровней биогенных аминов не всегда можно достоверно судить об их влиянии на интегральную биоаминную обеспеченность органа и на иммуногенез. Даже при нарастании концентрации серотонина влияние его может уменьшаться, в зависимости от динамики катехоламинов. Статистическая обработка полученных цифровых данных проводилась с использованием пакета программ Microsoft office (Word и Exсel). Оценка статистической значимости производилась по критерию Манна-Уитни.
Результаты исследования и их обсуждение. Введение мелатонина в течение 4-х недель приводит к увеличению среднего веса селезенки от 0,19 ± 0,02 г в контрольной группе до 0,21 ± 0,05 г. (p = 0,01) и увеличению первичных лимфоидных узелков во II-й экспериментальной группе.
Исследование клеток моноцитарно-макрофагального происхождения показывает, что ежедневный введение мелатонина в течение 4 недель животным, находящимся в условиях естественного освещения приводит к уменьшению среднего количества Iba-1-позитивных клеток в 2 раза (p = 0,0006). Наблюдается уменьшение количества Iba-1-позитивных клеток в ПАЛМ и во всех зонах лимфоидных узелков. Исследование
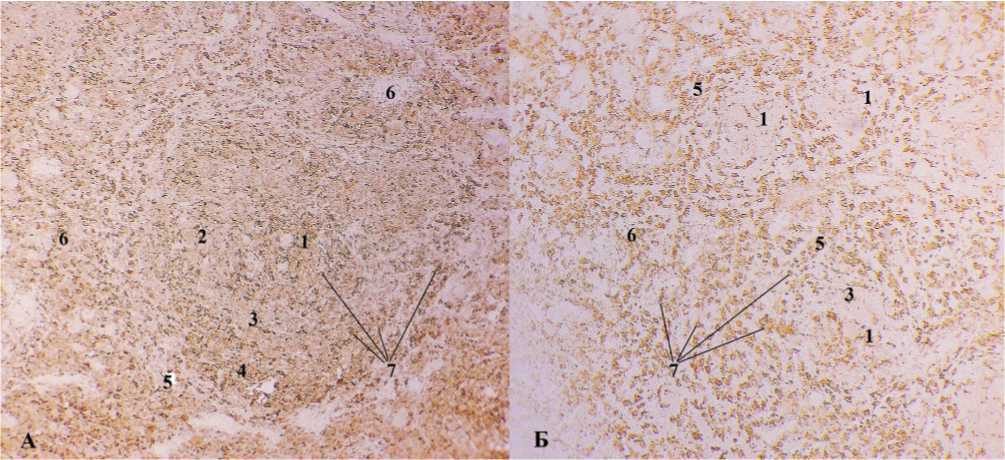
Рис. 1. Влияние мелатонина на Iba-1-позитивные клетки селезенки. Ув.100. А – лимфоидный узелок селезенки контрольных животных, Б – лимфоидные узелки селезенки животных, получавших мелатонин. 1 – периартериальная зона, 2 – зона размножения, 3 – мантийная зона, 4 – маргинальная зона, 5 – маргинальный синус, 6 – красная пульпа, 7 - Iba-1-позитивные клетки.
А
Б
контроль мелатонин
контроль мелатонин
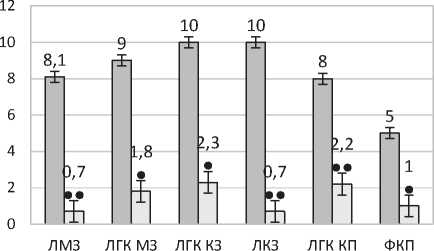
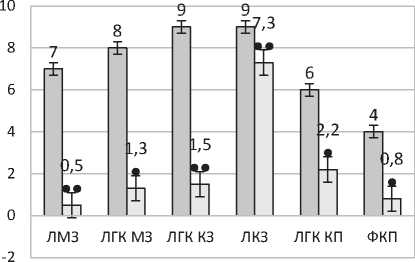
Рис. 2. Влияние мелатонина на содержание биоаминов (А — катехоламинов, Б серотонина) в иммунокомпетентных структурах селезенки: ЛМЗ — лимфоцитах мантийной зоны лимфоидного узелка, ЛГК МЗ — люминесцирующих гранулярных клетках мантийной зоны лимфоидного узелка, ЛГК КЗ — люминесцирующих гранулярных клетках маргинальной зоны лимфоидного узелка, ЛКЗ — лимфоцитах маргинальной зоны; ЛГК КП — люминесцирующих гранулярных клетках красной пульпы, ФКП — микроокружении ЛГК красной пульпы. • – p ≤ 0,01; •• - – p ≤ 0,001
красной пульпы селезенки животных, получавших мелатонин, показало уменьшение количества Iba-1-позитивных клеток в маргинальных синусах и увеличение в субкапсулярных синусах красной пульпы (рис. 1).
Изучение биоаминсодержащих иммунокомпетентных клеток селезенки показало, что под действием мелатонина содержание серотонина и катехоламинов во всех изученных структурах снижается.
По динамике уровней биогенных аминов не всегда можно достоверно судить об их влиянии на интегральную биоаминную обеспеченность органа и на иммуногенез. По серотониновому индексу (коэффициенту реципрокности) можно судить о преобладании серотонина в клетке (Js> 1), либо катхоламинов (Js < 1), что косвенно указывает о наличие процессов иммуносупрессии, либо об их отсутствии (Л.В. Девойно, 1972-1983).
В нашем эксперименте даже при снижении концентраций серотонина (рис. 2Б) и катехоламинов (рис. 2Б) во всех исследуемых структурах, их соотношение в клетках значимо не меняется: преимущественно наблюдается преобладание катехоламинов. Серотониновый индекс (Js) в структурах селезенки контрольных животных колеблется в пределах от 0,8 до 0,9 а в структурах селезенки животных, получавших мелатонин от 0,3 до 7,0. Под влиянием мелатонина Js лимфоцитов мантийной зоны увеличивается до 2, а Js лимфоцитов маргинальной зоны увеличивается до 7, что свидетельствует о преобладании серотонина в этих зонах. Таким образом, мы наблюдаем перераспределение биоаминов в лимфоидном узелке. Наиболее чувствительными к мелатонину являются ПАЛМ, маргинальные и субкапсулярные синусы красной пульпы селезенки.
Выводы. Мелатонин, вводимый перорально в течение четырех недель вызывает морфологические изменения в селезенке:
увеличение количества лимфоидных узелков;
уменьшение среднего количества клеток макрофагального ряда (Iba-1+) во всех зонах селезенки, за исключением зоны красной пульпы, прилегающей к капсуле.
снижение содержания катехоламинов и серотонина во всех иммунокомпетентных клетках красной и белой пульпы.
Список литературы Влияние мелатонина на макрофаги и клетки дисперсной эндокринной системы селезенки
- Арушанян, Э. Б. Гормон мозговой железы эпиф иза мелатонин - универсальный естественный адаптоген / Э. Б. Арушанян, Э. В. Бейер // Успехи физиологических наук. - 2012. - Т. 43. - № 3. - С. 82 - 100.
- Воронкова, О.В. Серотониновый индекс в биоаминсодержащих структурах селезенки при водном воздействии кальция / О.В. Воробьева. // Материалы Всероссийской конференции «Морфология в теории и практике». Чебоксары, 2008. - С. 59-60.
- Гордон, Д.С. Нейромедиаторы лимфоидных органов/Д.С. Гордон, В.Е. Сергеева, И.Г. Зеленова//Л.: Наука, 1982. -128 с.
- Кирик О.В. Кальций-связывающий белок Iba-1/ AIF1 в клетках головного мозга крысы /О.В. Кирик, Е.Г. Сухорукова, Д.Э. Коржевский //Морфология. 2010. Т. 136, № 2. С. 5 -7.
- Князькин, И. В. Экстрапинеальный мелатонин в процессах ускоренного и преждевременного старения у крыс / И. В. Князькин // Успехи геронтологии. - 2008. - Т. 21. - № 1. - С. 80 - 82.
- Маянский Н.А. Номенклатура и функции главного комплекса гистосовместимости человека /Н. А Маянский., А.Н. Маянский //Иммунология. 2006. Т. 27, № 1. С. 43-46.
- Сарилова И.Л. Эффект тестэктомии на структуры вилочковой железы, экспрессирующие главный комплекс гистосовместимости II класса /И.Л. Сарилова, В.Е. Сергеева, А.Т. Смородченко// Бюлл. Эксп. Биол. Мед. 2008. Т. 146, № 1. С. 103 - 106.
- Baeza, I. Improvement of leucocyte functions in ovariectomised aged rats after treatment with growth hormone, melatonin, oestrogens or phyto-oestrogens /I. Baeza, C. Alvarado, P. Alvarez, V. Salazar, C. Castillo, C. Ariznavarreta, J. A. Fdez-Tresguerres // J Reprod Immunol. - 2009. - V. 80. - № 1-2. - P. 70 - 79.
- Bugorkova S.A. Morphofunctional evaluation of the state of cells of APUD-system biomodel during anti-plague vaccine process /S.A. Bugorkova, V.V. Kutyreva // Zh Mikrobiol Epidemiol Immunobiol. - 2013. - № 4. - P. 49-55
- Cernysiov, V. Expression of melatonin receptors in the cells of immune system /V. Cernysiov, R. Bozaite, M. Mauricas, I. Girkontaite //Immunology. - 2012. - V. 137. - № 1. - P. 296.
- Currier, N. L. Exogenous melatonin: quantitative enhancement in vivo of cells mediating non-specific immunity /N. L. Currier, L. Z. Sun, S. C. Miller // J Neuroimmunol. -2000. V. 104. - № 2. - P. 101 - 108.
- Gupta, S. Photoperiodic regulation of nuclear melatonin receptor RORa in lymphoid organs of a tropical rodent Funambulus pennanti: role in seasonal oxidative stress [Электронный ресурс] /S. Gupta, C. Haldar, R. J. Ahmad// Photochem Photobiol B. - 2014. - Режим доступа: http://www.10.1016/j. jphotobiol.2014.11.013.
- DOI: 10.1016/j.jphotobiol.2014.11.013
- Ohsawa K. Microglia / macrophage-specific protein Iba1 binds to fimbrin and enhances its actin-binding activity / K. Ohsaw, Y. Imai, Y. Sasaki,S. Kohsaka // J. Neurochem. 2004. Vol. 88. P. 844 - 856.
- Ozkanlar, S. Melatonin Modulates the Immune System Response and Inflammation in Diabetic Rats Experimentally-Induced by Alloxan [Электронный ресурс]/S. Ozkanlar, A. Kara, E. Sengul, N. Simsek, A. Karadeniz, N. Kurt// Horm Metab Res. - 2015. -V. 47. - P. 1 - 8.
- Smorodchenko A. CNS - irrelevant T-cells enter the brain, cause blood-brain barrier disruption but no glial pathology/A. Smorodchenko, I. Wuerfel, E. Pohl, I. Vogt // Eur J. Neurosci. - 2007. V. 26. - № 6. - P. 1387-1398.
- Shafer, L.L. Assessment of melatonin's ability to regulate cytokine production by macrophage and microglia cell types / L. L. Shafer, J. A. McNulty, M. R. Young // J Neuroimmunol. - 2001. - V. 120. - №


