Влияние мультидисциплинарного подхода и маршрутизации пациентов на результаты лечения больных гепатоцеллюлярным раком
Автор: Петкау В. В., Бессонова Е. Н., Бредер В. В., Тарханов А. А., Киселева К. Е.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Собственные исследования
Статья в выпуске: 2 т.13, 2023 года.
Бесплатный доступ
Введение: Гепатоцеллюлярный рак (ГЦР) является шестой наиболее распространенной формой рака во всем мире и третьей наиболее распространенной причиной смертности от рака. На отдаленные результаты лечения влияют организационные решения, направленные на повышение доступности специализированной помощи. Цель нашего исследования - оценка влияния изменения маршрутизации и внедрения мультидисциплинарного подхода на общую выживаемость (ОВ) пациентов с ГЦР.Материалы и методы: Проведено ретроспективное исследование по изучению лечебной тактики и результатов лечения у всех пациентов с ГЦР, поставленных на учет в Свердловский областной онкологический канцер-регистр с диагнозом ГЦР с 2015 г. по 2021 г. Проведен сравнительный анализ в 3 группах пациентов: группа контроля (до изменений в маршрутизации), группа пациентов после изменений в маршрутизации и группа больных с мультидисциплинарным подходом с подключением гастроэнтеролога/гепатолога и интервенционного онколога.Результаты: Отмечается увеличение числа пациентов, получивших консультацию онколога и направленных на специализированное лечение: 12,0%, 19,5% и 34,9% соответственно (р
Гепатоцеллюлярный рак, мультидисциплинарный подход, маршрутизация, общая выживаемость
Короткий адрес: https://sciup.org/140300126
IDR: 140300126 | DOI: 10.18027/2224-5057-2023-13-2-1
Impact of a multidisciplinary approach and patient routing on the outcomes of treatment of patients with hepatocellular cancer
Introduction: Hepatocellular cancer (HCC) is the sixth most common form of cancer worldwide and the third most common cause of cancer death. The long-term results of treatment are influenced by organizational decisions aimed at increasing the availability of specialized care. The purpose of our study is to evaluate the impact of rerouting and the introduction of a multidisciplinary approach on overall survival (OS) of patients with HCC. Materials and methods. A retrospective study was conducted to study the treatment tactics and results of treatment in all patients with HCC registered in the Sverdlovsk Regional Oncological Cancer Registry with a diagnosis of HCC from 2015 to 2021. A comparative analysis was carried out in 3 groups of patients: the control group, before changes, group of patients after changes in routing, and a group of patients with multidisciplinary approach involving a gastroenterologist/hepatologist and an interventional oncologist.Results: There is an increase in the number of patients who received advice from an oncologist and referred for specialized treatment: 12.0 %, 19.5 % and 34.9 %, respectively (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Влияние мультидисциплинарного подхода и маршрутизации пациентов на результаты лечения больных гепатоцеллюлярным раком
Гепатоцеллюлярный рак (ГЦР) является шестой наиболее распространенной формой рака во всем мире и третьей наиболее распространенной причиной смертности от рака [1]. На основании базы данных о пациентах в США «Течение, распространенность и исходы злокачественных новообразований» (SEER) был построен прогноз эпидемиологии злокачественных новообразований (ЗН) до 2040 г. Авторы указывают на то, что ГЦР является лидером по скорости роста среди причин онкологической летальности. Рак печени станет третьей самой распространенной причиной смерти от ЗН в США [2]. Согласно данным НМИЦ им. А.П. Герцена, прирост заболеваемости ЗН печени и внутрипеченочных желчных протоков за 10 лет составил 49,9%. Заболеваемость ГЦР в Российской Федерации за 2020 год составила 6,12 на 100 тыс. населения [3].
Больные ГЦР представляют собой сложную группу пациентов. Во-первых, злокачественный процесс у них развивается на фоне хронических заболеваний печени, часто сопровождающихся нарушением функции печени, при этом 80–90% случаев ГЦР возникает в результате цирроза печени [1]. В такой ситуации ЗН и фоновое заболевание становятся конкурирующими в плане влияния на продолжительность жизни. Во-вторых, спектр лечебных опций ГЦР включает хирургию, рентген-хирургию, лучевую терапию и системное лечение [4]. Это требует многостороннего подхода к ведению таких пациентов, подключения к выработке тактики как онкологов, так и интервенционных онкологов (рентген-хирургов) и гастроэнтерологов (гепатологов).
В 2009 г. правительством Дании была утверждена программа «быстрого пути» (Fast Track Clinical Pathways) для пациентов с ГЦР. При этом срок от подозрения на ЗН печени до начала специализированного лечения был определен в 47 календарных дней. После успешной реализации проекта Villadsen с коллегами проанализировали влияние ускоренной маршрутизации на общую выживаемость (ОВ). Внедрение программы привело к сокращению сроков до начала лечения с 53,2 до 35,9 дней (р < 0,001). Однако изменение медианы ОВ было недостоверным: 231 против 293 дня (p = 0,11) [5].
Об улучшении результатов лечения больных ГЦР после внедрения мультидисциплинарного подхода говорит ряд зарубежных исследований. Yopp с соавторами на основании наблюдения за 355 пациентами с ГЦР из одного клинического центра отметили рост числа ранней стадии BCLC A с 26% до 44% (p = 0,0003) и увеличение медианы ОВ с 4,8 мес. до 13,2 мес. (ОР 2,5, 95% ДИ 2–3) [6].
В крупном многоцентровом Южнокорейском исследовании, в котором приняли участие 6619 больных ГЦР, пятилетняя ОВ при мультидисциплинарном подходе была значительно больше 71,2 % против 49,4% (р < 0,001), отношение рисков— 0,47 (95% ДИ 0,41–0,53). Увеличение выживаемости было особенно значимо у пациентов со сниженной функцией печени (ALBI 2 или 3), с промежуточной или распространенной стадией опухоли (BCLC стадия B или C), с уровнем АФП более 200 нг/мл [7].
Мультидисциплинарный подход считается оптимальным механизмом оказания помощи больным ГЦР и внесен в клинические рекомендации [8, 9]. При этом доказательная база по данному вопросу плохо представлена как в зарубежной, так и в отечественной литературе. Найденные на PubMed. gov и eLIBRARY.ru публикации чаще посвящены когортным исследованиям с подбором пациентов по определенным критериям, а не всех больных ГЦР в регионе [6, 7]. Также не представлены данные российских исследований по сравнению результатов лечения после введения мультидисци-плинарных консилиумов.
Целью нашего исследования послужила оценка влияния изменения маршрутизации и введения мультидисци-плинарного подхода на ОВ пациентов с ГЦР.
МАТЕРИАЛЫ И МЕТОДЫ
Нами было проведено ретроспективное исследование непосредственных и отдаленных результатов диагностики, маршрутизации, лечебной тактики у пациентов с ГЦР. В исследование включены пациенты, поставленные на учет в онкологический канцер-регистр с диагнозом ГЦР с 2015 г. по 2021 г.
Для формирования баз данных использовались данные Свердловского областного канцер-регистра, информационной базы Региональной онкологической системы
(ОНКОР), истории болезни и амбулаторные карты пациентов, поставленных на учет в 2015–2021 годах с кодом диагноза С22 по МКБ-10, протоколы аутопсий и записи о регистрации летальных исходов в областной информационной системе «Танатос».
Результаты обрабатывались при помощи статистического пакета SPSS Statistics 26.0. Обработка полученного материала проведена с использованием стандартных математических методов. Количественные данные представлены в виде среднее ± стандартное отклонение, качественные и категориальные признаки — в абсолютных и относительных величинах (N, %). Хи-квадрат, точный критерий Фишера и Z-критерий использовали для анализа различий между пропорциями в изучаемых подгруппах. Достоверность различий между средними величинам количественных переменных в подгруппах оценивали методом однофакторного дисперсионного анализа. Для преодоления проблемы множественных сравнений применяли поправку Бонферрони (вычисление порогового уровня статистической значимости с учетом числа проверенных гипотез). Общую выживаемость (ОВ) определяли в интервале от даты установления диагноза до даты смерти или окончания срока наблюдения. Медианы ОВ и их стандартные ошибки рассчитывали методом Каплана-Майера. Сравнение показателей ОВ в группах осуществляли с помощью лог-рангового теста. В ряде таблиц приведены также доверительные интервалы для медианы ОВ. В процессе проверки гипотезы вычисляли значение статистического критерия и уровень статистической значимости р, который сравнивали с заданным априори пороговым уровнем значимости 0,05. Красным шрифтом выделены достоверные показатели.
Все больные с ГЦР разделены на 3 группы:
-
1. Группа контроля, до внедрения изменений в маршрутизацию и до внедрения мультидисциплинарного подхода;
-
2. Группа пациентов после изменений в маршрутизации, сокращения сроков попадания в онкологический диспансер, разрешения прямого направления гастроэнтерологами в онкологический диспансер;
-
3. Группа больных ГЦР с внедрением маршрутизации и мультидисциплинарного подхода, с подключением к ведению пациентов врача гастроэнтеролога/гепато-лога и интервенционного онколога.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
С 2015 г. по 2021 г. в Свердловской области было выявлено 1917 случаев ГЦР, из них 800 женщин (41,7%) и 1117 мужчин (58,3%). Посмертно диагноз был поставлен в 888 случаев (46,3%) и прижизненно — в 1029 (53,7%). Средний возраст 69 ± 12 лет. Чаще всего заболевание выявлялось на поздних стадиях: более чем у половины пациентов была стадия BCLC D — 59,3% (табл. 1).
В 2015 г. в Свердловской области только 25 пациентов с ГЦР обратились к онкологам. Однако официальная
Таблица 1. Характеристика пациентов
При стандартной маршрутизации врач любой специальности сначала направляет пациента к районному онкологу, затем проводится дообследование в межмуниципальном центре или центре амбулаторной онкологической помощи. Далее пациент направляется в онкологический диспансер. Однако процесс дообследования часто затягивался из-за наличия сопутствующей патологии у большинства
|
■ Посмертный диагноз |
126 |
120 |
130 |
73 |
122 |
163 |
154 |
|
■ Направлен на симптоматическую терапию с места жительства |
117 |
49 |
54 |
24 |
33 |
28 |
32 |
|
■ Направлен на симптоматическую терапию из онкологического диспансера |
8 |
68 |
73 |
58 |
75 |
62 |
84 |
|
■ Специализированное лечение |
17 |
23 |
19 |
37 |
47 |
46 |
75 |
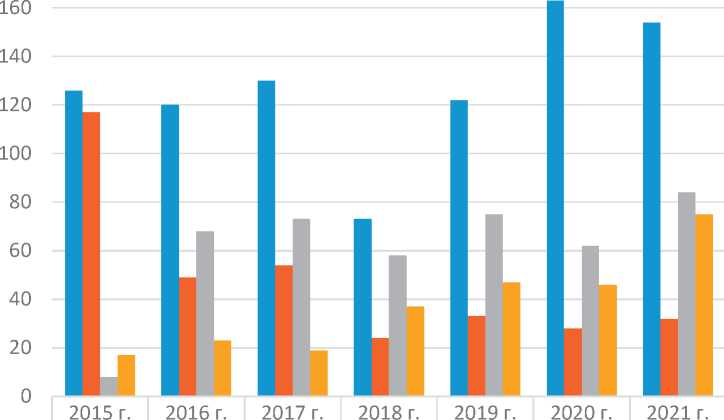
Рисунок 1. Распределение по тактике ведения всех впервые выявленных случаев ГЦР в Свердловской области в 2015–2021 годах.
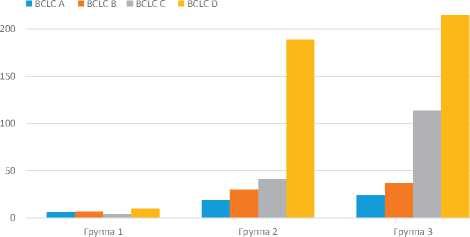
Рисунок 2. Распределение пациентов по стадиям BCLC пациентов с ГЦР, что требовало дополнительных консультации и обследований. Предполагалось, что упрощение направления пациентов в онкодиспансер сократит путь пациентов до диспансера и увеличит число больных ГЦР у онкологов. Также в общей лечебной сети проводились образовательные мероприятия с целью повышения онкологической настороженности и актуализации знаний по диагностике и лечению ГЦР. Среднее время от подозрения на ЗН в медицинской организации по месту жительства до первичного консультативного приема в областном онкологическом диспансере сократилось с 34,7 ± 3,4 до 23,4 ± 3,7 дней.
Следующим этапом в 2018 г. стало введение междисциплинарного подхода к лечению пациентов с ГЦР. Было запрещено направлять больных на симптоматическую терапию без коллегиального решения. В консилиумах по решению вопроса о лечении ГЦР кроме онколога-химиотерапевта, онколога-хирурга и онколога-химиотерапевта стали принимать участие гастроэнтеролог-гепатолог и интервенционный онколог.
При анализе динамики за 2015–2021 гг. можно отметить увеличение числа пациентов, направленных на специализированное лечение. Выросла доля пациентов, получивших специализированное лечение: 12,0%, 19,5%, 34,9% соответственно (р < 0,001). Выросло число пациентов, получивших консультацию в онкологическом диспансере с 17,6% в первой группе до 68,6% во второй и до 80,7% в третьей. Однако проведенные организационные мероприятия не повлияли на частоту посмертной диагностики,
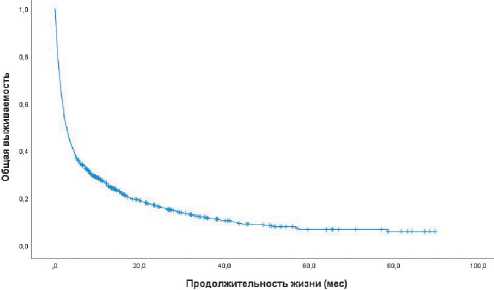
Рисунок 3. Общая выживаемость пациентов с ГЦР в Свердловской области (n = 1917).
которая в трех группах составила 47,0%, 44,4% и 47,7 % соответственно (рис. 1).
Анализ распределения по стадиям проводился только среди пациентов, получивших консультацию в СООД. Применялись система TNM и Барселонская система стадиро-вания [10]. Следует отметить резкое увеличение пациентов со стадией BCLC D после ускорения маршрутизации пациентов. Также увеличилось количество пациентов со стадией BCLC C во 2 и 3 группах (рис. 2).
Медиана ОВ составила 2,77 мес. (95% ДИ 2,39–3,15) (рис. 3), а при анализе в группах 2,8, 2,2 и 3,1 месяца соответственно. Значимое отличие было только между группами 3 и 2. Такие низкие показатели общей выживаемости связаны с большим удельным весом поздних стадий. Для нивелирования влияния стадии на вклад маршрутизации и мультидисциплинарного подхода в изменение ОВ был проведен подгрупповой анализ с разделением пациентов по системе BCLC. Выяснилось, что при нивелировании влияния стадии, общая выживаемость значимо увеличилась только в группе пациентов BCLC C, с 3,4 мес. до 12,5 мес. (р = 0,046).
Таблица 2. Отдаленные результаты лечения пациентов с ГЦР
|
1-группа контроля, до внедрения изменений |
2-группа после изменений в маршрутизацию |
3-группа после внедрения МДК |
Достоверность различия между группами |
|
|
Медиана общей выживаемости у выявленных при жизни (мес.) |
2,83 ± 0,53 |
2,20 ± 0,22 |
3,07 ± 0,32 |
Р 12 = 0,724 Р 13 = 0,064 Р 23 = 0,002 |
|
Стадия а |
78,5 ± N/A |
57,6 ± N/A |
N/A |
Не достоверно |
|
Стадия b |
34,8 ± 19,6 |
31,7 ± 5,14 |
N/A |
Не достоверно |
|
Стадия с |
3,40 ± 0,30 |
6,47 ± 2,01 |
12,5 ± 1,76 |
Р 23 = 0,046 |
|
Стадия d |
5,20 ± 1,77 |
2,10 ± 0,12 |
1,90 ± 0,14 |
Р 23 = 0,001 |
ОБСУЖДЕНИЕ
Ускорение начала лечения в нашем исследовании не оказало существенного влияния на медиану ОВ. Подтверждение этому факту мы находим и у ряда других авторов, которые указывают, что сокращение срока до начала лечения до 60 и даже до 48 дней не оказывает влияния на ОВ [5, 11].
Улучшение показателей ОВ наблюдается только после внедрения мультидисциплинарного подхода. К аналогичному увеличению ОВ при такой тактике — с 4,5 мес. до 9,5 мес. (p < 0,05) — пришли Chang et al. [12]. А в исследовании Charriere et al. отношение рисков по ОВ также было статистически значимым и составило 0,39 (95%ДИ 0,27– 0,54, р < 0,001) [11].
Увеличение ОВ в группе BCLC С могло быть связано с внедрением современных методов лечения, а не с подходами в диагностике и обследовании на ранних этапах. До 2018 г. единственной опцией таргетной системной терапии был сорафениб. С 2019 г. арсенал расширился за счет ленватиниба в первой линии и регорафениба во второй линии. Однако в регистрационном исследовании REFLECT ленватиниб не превосходил сорафениб по медиане общей выживаемости: 13,6 мес. против 12,3 мес. на сорафенибе (ОР 0,92; 95% ДИ 0,79–1,06) [13]. Схожие результаты в отношении медианы ОВ были получены при изучении ленватиниба в российской реальной практике: 14,6 месяцев (95%ДИ 10,6–18,6) [14].
Низкую медиану общей выживаемости можно связать с выявлением ГЦР на поздних стадиях. Похожие данные можно увидеть и в зарубежных исследованиях. Serper et al. фиксируют медиану ОВ в 1,1 год. В группе паци- ентов со стадией D — выживаемость 0,3 года, в группе С — 0,4 года [15].
Недостаточно высокая медиана ОВ в группе BCLC C и статистически достоверное снижение ОВ в группе BCLC D после внедрения мультидисциплинарного подхода, вероятно, связаны с тем, что у части пациентов «занижался» ECOG статус и устанавливалась распространенная стадия, что позволяло взять их на специализированное лечение. Такой эффект описан при анализе данных по применению сорафениба в реальной клинической практике в США [16].
ВЫВОДЫ
Упрощение маршрута пациента от гастроэнтеролога до онколога сокращает сроки до начала лечения, увеличивает число больных, которые получают консультативную помощь в онкологическом диспансере, но не влияет на ОВ. Мультидисциплинарный подход позволяет большему числу больных получить специализированную помощь. При этом максимальное влияние на ОВ отмечается при стадии BCLC C.
Несмотря на изменение маршрутизации и введение муль-тидисциплинарного подхода результаты лечения пациентов с ГЦР остаются неудовлетворительными. Целесообразным представляется максимальное воздействие на посмертную диагностику и сокращение запущенных стадий. Данные цели достижимы только путем внедрения скрининговых программ на уровне региона в целом.
Список литературы Влияние мультидисциплинарного подхода и маршрутизации пациентов на результаты лечения больных гепатоцеллюлярным раком
- Salgia R., & Mendiratta V. The Multidisciplinary Management of Hepatocellular Carcinoma// Clinical liver disease -2021 - Vol. 17№ 6 - P. 405-408. https://doi.org/10.1002/cld. 1068.
- Rahib L., Wehner M.R., Matrisian L.M., Nead K.T. Estimated Projection of US Cancer Incidence and Death to 2040 // JAMA Netw Open. 2021 - Vol. 4 №4 : e214708. doi: 10.1001/jamanetworkopen. 2021.4708. PMID : 33825840 ; PM-CID : PMC8027914.
- Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой Злокачественные новообразования в России в 2020 году (заболеваемость и смертность) - М. : МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, - 2021 .- илл .- 252 с.
- Llovet J.M., Kelley R.K., Villanueva A., Singal A.G., Pikarsky E., Roayaie S., et al. Hepatocellular carcinoma.// Nat Rev Dis Primers - 2021 - Vol. 7№ 1 : 6. doi: 10.1038/s41572-020-00240-3. PMID : 33479224.
- Villadsen G. E., Simonsen K., Ott P., Vilstrup H., Granb^k H. Effects of implementation of a national fast track clinical pathway for hepatocellular carcinoma in Western Denmark// J Gastrointestin Liver Dis .- 2019 - Vol. 28 №1 - P. 83-88. doi: 10.15403/jgld. 2014.1121.281. dnk. PMID : 30851176.
- Yopp A. C., Mansour J. C., Beg M. S., Arenas J., Trimmer C., Reddick M et al. Establishment of a multidisciplinary hepatocellular carcinoma clinic is associated with improved clinical outcome // Ann Surg Oncol - 2014 Apr Vol. 21 -№4 - P. 1287-95. doi: 10.1245/s10434-013-3413-8. Epub 2013 Dec 7. PMID : 24318095 ; PMCID : PMC5612826.
- Sinn D. H., Choi G. S., Park H. C., Kim J. M., Kim H., Song K. D. et al. Multidisciplinary approach is associated with improved survival of hepatocellular carcinoma patients // PLoS One - 2019 - Vol. 14 - №1 : e0210730. Published 2019 Jan 14. doi: 10.1371/journal.pone. 0210730.
- Бредер В. В., Базин И. С., Балахнин П. В., Виршке Э. Р., Косырев В. Ю., Ледин Е. В. и соавт. Практические рекомендации по лекарственному лечению больных злокачественными опухолями печени и желчевыводящей системы. Злокачественные опухоли : Практические рекомендации RUSSCO #3s2, 2022 (том 12). 467-529.
- Benson A. B., D'Angelica M. I., Abbott D. E., Anaya D.A., Anders R., Are C et al. Hepatobiliary Cancers, Version 2.2021, NCCN Clinical Practice Guidelines in Oncology// J Natl Compr Canc Netw - 2021 - Vol. 19 № 5 : 541-565. doi: 10.6004/jnccn. 2021.0022. PMID : 34030131.
- Reig M., Forner A., Rimola J., Ferrer-Fabrega J., Burrel M, Garcia-Criado A. et al. BCLC strategy for prognosis prediction and treatment recommendation : The 2022 update// J Hepatol - 2022 - Vol. 76 №3 : 681-693. doi: 10.1016/j. jhep. 2021.11.018. Epub 2021 Nov 19. PMID : 34801630 ; PMCID : PMC8866082.
- Charriere B., Muscari F., Maulat C., Bournet B., Bonnet D. et al. Outcomes of patients with hepatocellular carcinoma are determined in multidisciplinary team meetings// J Surg Oncol - 2017 - vol. 115 № 3 : 330-336. doi: 10.1002/jso. 24500. Epub 2016 Nov 4. PMID : 27813094.
- Chang T. T., Sawhney R., Monto A., Davoren J. B., Kirkland J. G., Stewart L. et al. Implementation of a multidisciplinary treatment team for hepatocellular cancer at a Veterans Affairs Medical Center improves survival// HPB (Oxford) -2008 - Vol 10 № 6 : 405-11. doi: 10.1080/13651820802356572. PMID : 19088925 ; PMCID : PMC2597312.
- Kudo M., Finn R. S., Qin S., Han, K. H., Ikeda, K., Piscaglia, F. et al. Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma : a randomised phase 3 non-inferiority trial // Lancet - 2018 -vol. 391,10126 : 1163-1173 : 1163-1173. doi: 10.1016/S0140-6736 (18) 30207.
- Петкау В. В., Султанбаев А. В., Меньшиков К. В. и др. Ленватиниб у пациентов с нерезектабельной гепатоцеллю-лярной карциномой в реальной клинической практике. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2022 ; 32 (4) : https://doi.org/10.22416/1382-4376-2022-20-35.
- Serper M., Taddei T.H., Mehta R., D'Addeo K., Dai F., Aytaman A. et al. VOCAL Study Group. Association of Provider Specialty and Multidisciplinary Care With Hepatocellular Carcinoma Treatment and Mortality// Gastroenterology. 2017 Vol. 152 № 8 : 1954-1964. doi: 10.1053/j.gastro. 2017.02.040. Epub 2017 Mar 7. PMID : 28283421 ; PMCID : PMC5664153.
- Sanoff H.K., Chang Y., Lund J.L., O'Neil B.H., Dusetzina S.B. Sorafenib Effectiveness in Advanced Hepatocellular Carcinoma// Oncologist - 2016 Vol. 21 №9 : 1113-20. doi: 10.1634/theoncologist. 2015-0478. Epub 2016 May 16. PMID : 27185615 ; PMCID : PMC5016063.


