Влияние натриевых солей пирроло[3,4-с]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета в экспериментальных моделях патологических состояний у мышей
Автор: Гейн О.Н., Бобровская О.В., Ибатуллин М.В., Гейн В.Л., Гейн С.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 4, 2025 года.
Бесплатный доступ
Основная функция клеток-эффекторов врожденного иммунитета – элиминация экзогенных и эндогенных патогенов. Однако в ряде случаев поглотительная и микробицидная активность фагоцитов может быть нарушена, что ведет к развитию патологических состояний. В связи с этим создание иммунотропных препаратов с мягкой модулирующей активностью в отношении фагоцитарной функции лейкоцитов актуально. В этом плане перспективными являются натриевые соли пирроло[3,4-с]-пиразол-3-онов (1а-б) и 1-фенилпиразол-3-карбоксамида (2а), которые в ранее проводимых исследованиях проявили модулирующее влияние на функции фагоцитирующих клеток. В данном исследовании нами было изучено влияние натриевых солей пирроло[3,4-с]-пиразол-3-онов (1а-б) и 1-фенилпиразол-3-карбоксамида (2а) на изменение поглотительной активности перитонеальных лейкоцитов и их микробицидный потенциал в условиях двух- и шестичасового иммобилизационного стресса и острого воспаления. В ходе исследования были получены следующие результаты: натриевые соли пирроло[3,4-с]-пиразол-3-онов (1а-б) и 1-фенилпиразол-3-карбоксамида (2а) нивелировали вызванное шестичасовой иммобилизацией угнетение поглотительной активности лейкоцитов, а также угнетение продукции активных кислородных радикалов, вызванное двух- и шестичасовым иммобилизационным стрессом. Исследуемые соединения (1а-б, 2а), введенные на фоне зимозана, отменяли стимулирующее влияние последнего на поглотительную активность лейкоцитов, однако не вызывали модуляции продукции активных радикалов лейкоцитами в стимулированных зимозаном культурах.
Фагоцитоз, микробицидный потенциал, стресс, зимозановый перитонит, натриевые соли пирроло[3, 4-с]-пиразол-3-онов, натриевые соли 1-фенилпиразол-3-карбоксамида
Короткий адрес: https://sciup.org/147252652
IDR: 147252652 | УДК: 612.017 | DOI: 10.17072/1994-9952-2025-4-445-453
The effect of sodium salts of pyrrolo[3,4-c]-pyrazol-3-ones and 1-phenylpyrazole-3-carboxamides on the functional activity of innate immune cells in experimental models of pathological conditions in mice
The primary function of innate immune effector cells is the elimination of exogenous and endogenous pathogens. However, in some cases, the absorptive and microbicidal activity of phagocytes can be impaired, leading to the development of pathological conditions. In this regard, the creation of immunotropic drugs with mild modulating activity in relation to the phagocytic function of leukocytes is relevant. In this regard, sodium salts of pyrrolo[3,4-c]-pyrazol-3-ones (1a-b) and 1-phenylpyrazole-3-carboxamide (2a) are promising; in previous studies, they showed a modulating effect on the functions of phagocytic cells. In this study, we investigated the effect of sodium salts of pyrrolo[3,4-c]-pyrazol-3-ones (1a-b) and 1-phenylpyrazole-3-carboxamide (2a) on changes in the absorptive activity of peritoneal leukocytes and their microbicidal potential under conditions of two- and six-hour immobilization stress and acute inflammation. The following results were obtained during the study: sodium salts of pyrrolo[3,4-c]-pyrazol-3-ones (1a-b) and 1-phenylpyrazole-3-carboxamide (2a) neutralized the inhibition of leukocyte scavenging activity caused by six-hour immobilization, as well as the inhibition of the production of active oxygen radicals caused by two- and six-hour immobilization stress. The studied compounds (1a-b, 2a), introduced against the background of zymosan, abolished the stimulating effect of the latter on the absorptive activity of leukocytes, but did not cause modulation of the production of active radicals by leukocytes in zymosan-stimulated cultures.
Текст научной статьи Влияние натриевых солей пирроло[3,4-с]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета в экспериментальных моделях патологических состояний у мышей
Как известно, нейтрофильные гранулоциты, а также моноциты, макрофаги являются основными эффекторами врожденного иммунитета, участвующими в элиминации экзогенных и эндогенных патогенов. Нейтрофилы, моноциты, макрофаги являются основными участниками и модуляторами воспалительной реакции. Привлекаемые хемоаттрактантами, они мигрируют в очаг воспаления, участвуют в фагоцитозе разрушенных клеток организма, а также проникших в организм патогенов, выделяя в окружающие ткани провоспалительные медиаторы, активные радикалы. Результатом чрезмерной активации провоспали-тельных механизмов может явиться генерализация воспалительного процесса. Однако снижение функциональной активности эффекторов воспаления может приводить к хронизации течения воспалительной реакции [Черешнев, Гусев, 2012].
Функциональная активность эффекторов врожденного иммунитета может быть детерминирована как генетически, так и изменяться под воздействием ряда экзогенных и эндогенных факторов. Известно, что различные стрессорные воздействия оказывают значимое влияние на функциональную активность лейкоцитов, как на поглотительную активность, так и на микробицидный потенциал, что обусловлено присутствием на мембране лейкоцитов рецепторов для основных гормонов стресса – катехоламинов и глюкокортикоидов [Szefler, 1987; Stern, Kunos, 1988; Шилов, Орлова, 2001].
Снижение функциональной активности фагоцитирующих клеток несет в себе риск развития вторичных иммунодефицитных состояний, сопровождающихся хроническими инфекционными осложнениями. Снижение функциональной активности фагоцитирующих клеток и, прежде всего, механизмов микроби-цидности наблюдается при хронической гранулематозной болезни, при которой вследствие дефекта фермента НАДН-оксидазы лейкоциты не способны образовывать активные формы кислорода [Шарапова и др., 2011]. Также установлено, что при туберкулезе значительно снижаются такие показатели, как процент активных нейтрофилов и завершенность фагоцитоза [Филинюк и др., 2005].
В связи с этим присутствует необходимость в создании иммунотропных препаратов, обладающих мягкой корригирующей направленностью в отношении поглотительной способности лейкоцитов и их микробицидного потенциала. Также важно, чтобы, помимо фармакологической эффективности, препараты не являлись бы токсичными, и получение их активных субстанций было бы возможно с помощью простых методов. В этом плане перспективными являются натриевые соли пирроло[3,4- с ]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида, которые в ранее проводимых исследованиях проявили иммуно-тропную активность в отношении функций фагоцитирующих клеток [Гейн и др., 2022; Гейн и др., 2025].
Цель работы – исследование влияния натриевых солей пирроло[3,4- с ]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета в экспериментальных моделях патологических состояний у мышей.
Материалы и методы исследования
Для оценки влияния натриевых солей пирроло[3,4- с ]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета при иммобилизационном стрессе были взяты 3 соединения (рис. 1), которые по ранее проведенным исследованиям оказывали влияние на поглотительную активность лейкоцитов и их микробицидный потенциал [Гейн и др., 2022].
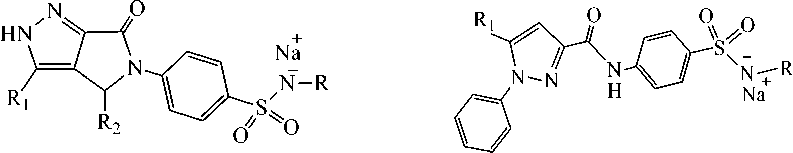
1а-б 2а
Рис. 1. Структурные формулы изучаемых соединений.
Натриевые соли пирроло[3,4- с ]-пиразол-3-онов: R1=4-BrC 6 H 4 , R2=3-CH 3 OC 6 H 4 , R= MeCO ( 1а) ;
R1 = 4-BrC 6 H 4 , R2 = 2-NO 2 C 6 H 4, R= MeCO ( 1б ); натриевая соль 1-фенилпиразол-3-карбоксамида:
R1 = 4-CH 3 OС 6 H 4 , R=С 3 H 2 NS ( 2а)
[Structural formulas of the compounds studied]
Эксперименты в системе in vivo проведены на белых нелинейных половозрелых мышах массой 21–26 г. Все исследовательские работы с лабораторными животными выполнялись в соответствии с общепринятыми этическими нормами обращения с животными, принятыми Европейской конвенцией по защите позвоночных животных, используемых для исследовательских и иных научных целей [Европейская …, 1986].
В качестве моделей патологических состояний использовали двух- и шестичасовой иммобилизацион-ный стресс и острое воспаление. Иммобилизацию животных проводили на спине, за 30 мин до начала иммобилизации вводили внутрибрюшинно соединения натриевых солей пирроло[3,4- с ]-пиразол-3-онов (1а-б) и 1-фенилпиразол-3-карбоксамида (2а) в дозе 100 мг/кг. Острую воспалительную реакцию индуцировали внутрибрюшинным введением мышам стерильной суспензии опсонизированного зимозана А (нерастворимый полисахарид клеточной стенки грибов Saccharomyces cerevisiae ) в дозе 50 мг/кг. Исследуемые соединения вводились внутрибрюшинно за 1 ч до введения зимозана.
Для оценки поглотительной активности перитонеальных лейкоцитов мышей к 80 мкл клеток добавляли 10 мкл суспензии FITC-меченого St. cohnii в конечной концентрации 108 кл/мл, пробы инкубировали 30 мин при температуре 37°C. Затем к клеткам добавляли лизирующий раствор (0.15М NH 4 Cl; 0.01М NaHCO 3 ; 0.0001М ЭДТА (этилендиаминтетрауксусная кислота)) и после 5 мин инкубации центрифугировали 5 мин при 250 g с охлаждением при температуре 4°C. После снимали супернатант, добавляли 0.02% ЭДТА в PBS (phosphate buffered saline – фосфатно-буферный солевой раствор) и снова центрифугировали 5 мин при 250 g с охлаждением при температуре 4°C. Далее вновь снимали супернатант, добавляли 100 мкл 0.02% ЭДТА в PBS. После этого пробы анализировали на проточно-лазерном цитометре («Bio Sino», Китай) [Nielsen et al., 1995].
Микробицидный потенциал перитонеальных лейкоцитов оценивался на основании продукции ими активных кислородных радикалов, оценку которых производили с помощью реакции люминолзависимой хемилюминесценции (ЛЗХЛ). Реакцию проводили в 96-луночных плоскодонных планшетах («Greiner», Германия), каждая лунка содержала клетки в концентрации 2 x 10 5 клеток/0.2 мл р-ра Хенкса. Индуктором ЛЗХЛ был выбран опсонизированный зимозан в концентрации 150 мкг/мл. В качестве маркера выраженности реакции ЛХЗЛ использовался люминол 10–5М. Регистрация результатов велась в течение 1 часа с интервалом в 5 мин с помощью люминометра («Tecan Trading AG», Швейцария) [Фримель, 1987].
Статистическую обработку данных проводили методами вариационной статистики с помощью t -критерия Стьюдента. Эффект считали достоверным при p < 0.05 по сравнению с контролем. Результаты представляли в виде средней и ее стандартной ошибки (М±m).
Результаты и их обсуждение
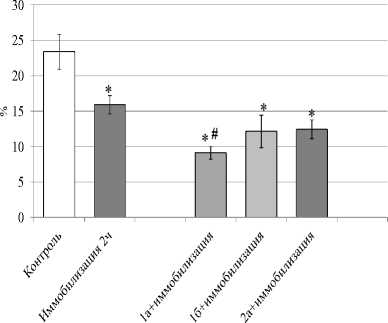
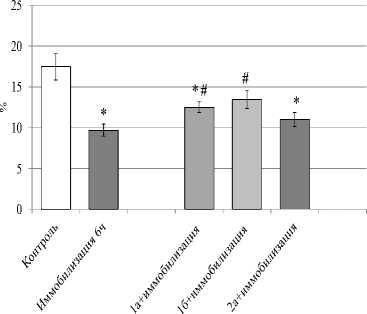
В ходе исследований было установлено, что двухчасовая иммоблизация приводила к угнетению поглотительной активности лейкоцитов. Исследуемые соединения 1а , 1б и 2а не отменяли угнетающего влияния двухчасового иммобилизационного воздействия на поглотительрную активность лейкоцитов (рис. 2А). Угнетение поглотительной активности лейкоцитов было выявлено и на фоне шестичасовой иммобилизации, и это угнетение носило более выраженный характер по сравнению с двухчасовым стрессом. Снижение поглотительной активности лейкоцитов относительно контроля при двухчасовом стрессорном воздействии составило 31%, а при шестичасовом – около 48%. Соединения 1а и 1б , являющиеся натриевыми солями пирроло[3,4- с ]-пиразол-3-онов, нивелировали выраженное угнетение поглотительной активности лейкоцитов, вызванное шестичасовым стрессорным воздействием (рис.2Б). В ранее проведенных исследованиях было показано что при самостоятельном введении натриевые соли пирроло[3,4-с]-пиразол-3-онов (la-б) и 1-фенилпиразол-З-карбоксамида (2а) стимулировали поглотительную активность лейкоцитов и прежде всего нейтрофильных гранулоцитов, увеличивая количество активных нейтрофилов в среднем более чем на 50%, а количество поглощенных ими объектов - на 8.6% и более [Гейн и др., 2022].
А
Б
Рис. 2. Влияние соединений 1а, 1б, 2а на фагоцитарную активность лейкоцитов (процент фагоцитоза) в условиях двухчасовой (А) и шестичасовой (Б) иммобилизации.
* - р <0.05 по сравнению с контролем, # - р <0.05 по сравнению иммобилизацией, количество животных в группах: n=7 (для 2-часовой иммобилизации) и n=8 (для 6-часовой иммобилизации)
[The effect of compounds 1a, 1b, 2a on the phagocytic activity of leukocytes (percentage of phagocytosis) under conditions of two-hour (A) and six-hour (B) immobilization]
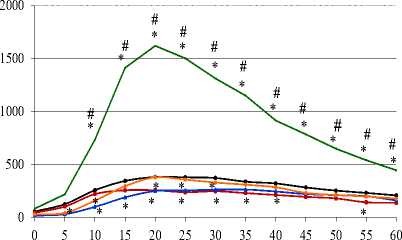
Оценивая стимулированную продукцию активных форм кислорода (АФК), было выявлено угнетение микробицидного потенциала лейкоцитов в условиях двухчасовой иммобилизации, начиная с 20-й мин и до 40-й мин включительно, а также на 55-й мин наблюдения. Соединение 1б на фоне 2-часового стрес-сорного воздействия ингибировало продукцию АФК лейкоцитами только в первые 10 мин, отменяя в последующем угнетающий эффект стресса на продукцию активных радикалов. Соединение 1а на фоне 2-часовой иммобилизации приводило к более ранней и продолжительной депрессии микробицидного потенциала лейкоцитов – с 5-й по 30-ю мин наблюдения по сравнению со стрессом. Введение 2а на фоне 2-часовой иммобилизации оказывало стимулирующее влияние на выраженность и пролонгированность продукции активных форм кислорода лейкоцитами как по сравнению с контролем, так и по сравнению со стрессорным воздействием (рис. 3А).
Шестичасовой иммобилизационный стресс, как и 2-часовой стресс, приводил к угнетению стимулированной зимозаном продукции АФК лейкоцитами. Угнетение продукции активных радикалов было более продолжительным и регистрировалось с 25 мин по 60 мин наблюдения. Исследуемые соединения ( 1а , 1б , 2а ), введенные на фоне шестичасовой иммобилизации, значительно увеличивали интенсивность продукции активных радикалов, начиная с 5-й мин и до конца наблюдения. Интенсивность продукции активных радикалов возрастала как по сравнению с животными, которые подвергались только стрессор-ному воздействию, так и по сравнению с контролем. Пик продукции АФК при введении на фоне стресса соединений 1а , 1б приходился на период с 15 по 25 мин эксперимента, в то время как у соединения 2а он был несколько смещен и регистрировался с 25 по 35 мин эксперимента (рис. 3Б).
Контроль Иммобилизация 2ч 1а+иммобили
1б+иммобилизация 2а+иммобилизацияС
* # * #
* #
# *
# *
## #
#
#
* #
# *
* #
#
*
*
#
##
# **
*
* #
# # * #
* * # * #
#
#
* # #
* # *
# # *
*
0 5 10
#
*
**** ****
15 20 25 30 35 40 45 50 55 60
Контроль
Иммобилизация 6ч 1а+иммобилизация
1б+иммобилизация 2а+иммобилизация
А
Б
Рис. 3. Влияние соединений 1а, 1б, 2а на стимулированную продукцию активных форм кислорода лейкоцитами в условиях двухчасовой (А) и шестичасовой (Б) иммобилизации.
* - p <0.05 к контролю, # - p <0.05 к стрессу, количество животных: в контрольной при двухчасовой иммобилизации n=8, в остальных группах n=9. По оси y – относительные единицы люминисценции, по оси x – время
[The effect of compounds 1a, 1b, 2a on the stimulated production of reactive oxygen species by leukocytes under conditions of two-hour (A) and six-hour (B) immobilization]
Таким образом, введение натриевых солей пирроло[3,4- с ]-пиразол-3-онов ( 1а-б ) и 1-фенилпиразол-3-карбоксамида ( 2а ) нивелировало вызванное шестичасовой иммобилизацией угнетение поглотительной активности лейкоцитов и отменяло угнетение продукции АФК, вызванное двух- и шестичасовым иммо-билизационным воздействием.
Через 15 б а количество активных фагоцитов увеличивалось по сравнению с контролем. Исследуемые соединения (1а-б , 2а ), введенные на ф ю активность лейкоцитов ис. 4).
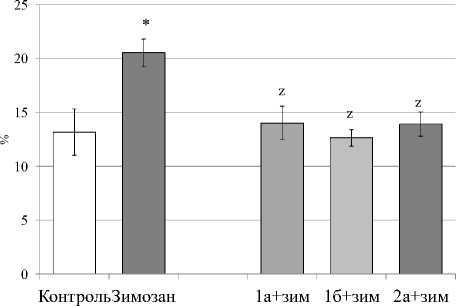
Рис. 4. Влияние соединений 1а, 1б, 2а на поглотительную активность перитонеальных лейкоцитов в модели острого воспаления.
По оси ординат – процент лейкоцитарного фагоцитоза, * - p <0.05 к контролю, z - p <0.05 к группе «зимозан», a - p <0.05 к группе «1б+зимозан», количество животных в каждой группе n=10
[Effect of compounds 1a, 1b, 2a on the absorptive activity of peritoneal leukocytes in an acute inflammation model]
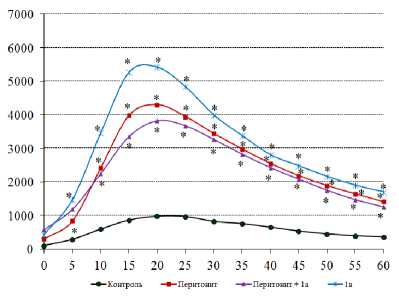
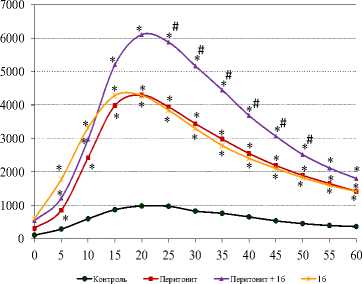
На фоне зимозанового перитонита продукция активных форм кислорода повышалась, что вполне объяснимо и связано со стимулирующим влиянием введенного зимозана на функциональную активность фагоцитирующих клеток [Шилов и др., 2021]. Соединение 1б , введенное на фоне зимозанового перитонита, не отменяло стимулирующего эффекта последнего и, начиная с 25 мин наблюдения, усиливало активирующее влияние зимозана на продукцию АФК. На фоне самостоятельного введения 1б продукция активных кислородных радикалов была выше значений контроля (рис. 5А). Натриевая соль пирроло[3,4- с ]-пиразол-3-она 1а как при самостоятельном введении, так и при введении на фоне зимозанового перитонита стимулировала продукцию активных радикалов по сравнению с контролем (рис. 5Б). Соединение
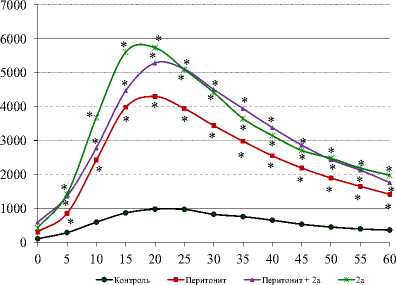
2а проявляло сходную с 1а и 1б направ кислородных радикалов лейкоцитами (ри
A
Б
В
Рис. 5. Влияние соединений 1а (А), 1б (Б), 2а (В) на стимулированную продукцию активных форм кислорода лейкоцитами в модели острого воспаления.
* - p < 0,05 к контролю, # - р < 0,05 к стрессу; количество животных в группах: контрольной - 8, с зимозановым перитонитом – 10, в опытных для 1а, 1б – 10, в опытных для 2а – 7. По оси y – относительные единицы люминисценции, по оси x – время
[The effect of compounds 1a (A), 1b (B), 2a (C) on the stimulated production of reactive oxygen species by leukocytes in a model of acute inflammation]
Таким образом, в модели острого воспаления натриевые соли пирроло[3,4- с ]-пиразол-3-онов ( 1а-б ) и 1-фенилпиразол-3-карбоксамида ( 2а ) отменяли стимулирующий эффект зимозана на поглотительную активность лейкоцитов и не приводили к изменению повышенной продукции активных радикалов.

![Влияние натриевых солей пирроло[3,4-с]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета в экспериментальных моделях патологических состояний у мышей Влияние натриевых солей пирроло[3,4-с]-пиразол-3-онов и 1-фенилпиразол-3-карбоксамида на функциональную активность клеток врожденного иммунитета в экспериментальных моделях патологических состояний у мышей](/file/cover/147252652/vlijanie-natrievyh-solej-pirrolo-34-spirazol-3-onov-i.png)
