Влияние некоторых параметров растворителей на растворимость производных сульфонилмочевины
Автор: Денисов Н.С., Угланова В.З., Денисов С.Н.
Журнал: Теория и практика современной науки @modern-j
Рубрика: Основной раздел
Статья в выпуске: 6 (6), 2015 года.
Бесплатный доступ
Рассмотрено влияние параметров растворителей на растворимость производных сульфонилмочевины.
Растворимость, растворители, производные сульфонилмочевины
Короткий адрес: https://sciup.org/140266979
IDR: 140266979
Текст научной статьи Влияние некоторых параметров растворителей на растворимость производных сульфонилмочевины
Широкое изучение сульфонилмочевинных препаратов началось с 80-х годов прошлого столетия всвязи с возможностью их широкого применения в сельском хозяйстве, экологии, медицине. Исследования этих веществ, направленные на увеличение сферы применения и улучшение их препаративных форм, актуальны и в настоящее время [1, 2].
Важным свойством производных сульфонилмочевины является их растворимость. Для рационального выбора направлений исследования межмолекулярных взаимодействий в жидкостях, необходимы знания о природе жидкого состояния. Анализ литературы, посвященной исследованиям жидких систем, свидетельствует о том, что большинство исследователей пользуются квазикристаллическим подходом [3-4]. Целесообразность данного подхода подтверждается многочисленными результатами, полученными с использованием рентгеноструктурного анализа. Данный подход, по-видимому, наиболее пригоден и для исследования смесей растворителей, используемых нами в качестве подвижных фаз, так как известно, что в данных системах при растворении различных соединений происходит процесс сольватации.
Для изучения влияния межмолекулярных взаимодействий в объеме подвижной фазы (ПФ) на хроматографирование производных сульфонилмочевины, нам представлялось целесообразным выделить следующие направления исследований:
изучение растворимости соединений исследуемого ряда в смесях растворителей используемых в качестве ПФ с различным содержанием полярных компонентов, для определения комплексного проявления происходящих межмолекулярных взаимодействий;
проведение исследований изменения концентрации ассоциативных образований различной стехиометрии при добавлении полярного растворителя, вследствие процесса сольватации;
проведение исследований роли локальных и объемных межмолекулярных взаимодействий, исходя из квазикристаллических представлений о структуре жидкостей.
Изучение растворимости производных сульфонилмочевины проводилось для смесей растворителей с одним неполярным апротонным растворителем – гексаном, являющимся универсальным сольватирующим компонентом с относительно слабым взаимодействием. Предполагалось, что между гексаном, с одной стороны, и компонентами смеси, с другой, полностью отсутствуют какие-либо специфические взаимодействия. Растворимость производных сульфонилмочевины изучалась методом изотермического насыщения при температуре 293 К, с жидкостнохроматографическим контролем концентрации исследуемых соединений [5-
6]. Погрешность измерения составляла ≤ 5%. Полученные зависимости растворимости производных сульфонилмочевины от содержания полярного компонента в смесях ПФ представлены на рис. 1.
Установлено, что растворимость производных сульфонилмочевины в спиртах примерно на порядок меньше, чем в остальных растворителях. Кроме того, полученные зависимости при использовании спиртов имеют линейный характер (кроме н-бутанола), а для остальных растворителей отличаются от линейности (табл. 1 и рис. 1).
Таблица 1. Статистические параметры линейной зависимости растворимости сульфонилмочевин от содержания полярного компонента в
ПФ. ( n=3, P=0,95 )
|
Соединение |
Полярный компонент |
Коэф-фициент детерми-нации |
Значение F-критерия |
Уро-вень значимости |
|
O O CH 3 O CH OO N 3 OS N ON N S CH3 N O 3 CH (трибенурон-метил) |
метилэтилкетон |
0,90 |
66,5 |
0,00 |
|
диоксан |
0,84 |
15,8 |
0,03 |
|
|
хлороформ |
0,67 |
16,4 |
0,00 |
|
|
метиленхлорид |
0,68 |
8,5 |
0,04 |
|
|
тетрагидрофуран |
0,95 |
55,8 |
0,01 |
|
|
изопропанол |
0,97 |
154,1 |
0,00 |
|
|
изоамиловый спирт |
0,98 |
148,4 |
0,00 |
|
|
н-бутанол |
0,77 |
9,9 |
0,05 |
|
|
O O CH 3 CH а SO NNSN CH 3 H SH HN O CH (сульфомету-ронметил) |
хлороформ |
0,95 |
110,3 |
0,00 |
|
метиленхлорид |
0,78 |
18,1 |
0,00 |
|
|
изоамиловый спирт |
0,96 |
53,6 |
0,02 |
|
|
н-бутанол |
0,77 |
10,4 |
0,05 |
|
|
Cl O CH 3 ON OS ON^ „N SH HN O CH (хлорсульфурон) |
метилэтилкетон |
0,85 |
11,8 |
0,07 |
|
диоксан |
0,89 |
16,5 |
0,05 |
|
|
изопропанол |
0,93 |
27,3 |
0,03 |
При изучении влияния на растворимость свойств среды, использовался подход, предложенный Коппелем И.А. и Пальмом В.А [7-8]. Согласно их положениям, при определенном упрощении процесса, происходящие сольватационные явления обусловлены разными независимыми свойствами среды. Специфическая сольватация между молекулами растворителя и растворенного вещества обусловлена двумя свойствами – общими кислотностью и основностью растворителей.
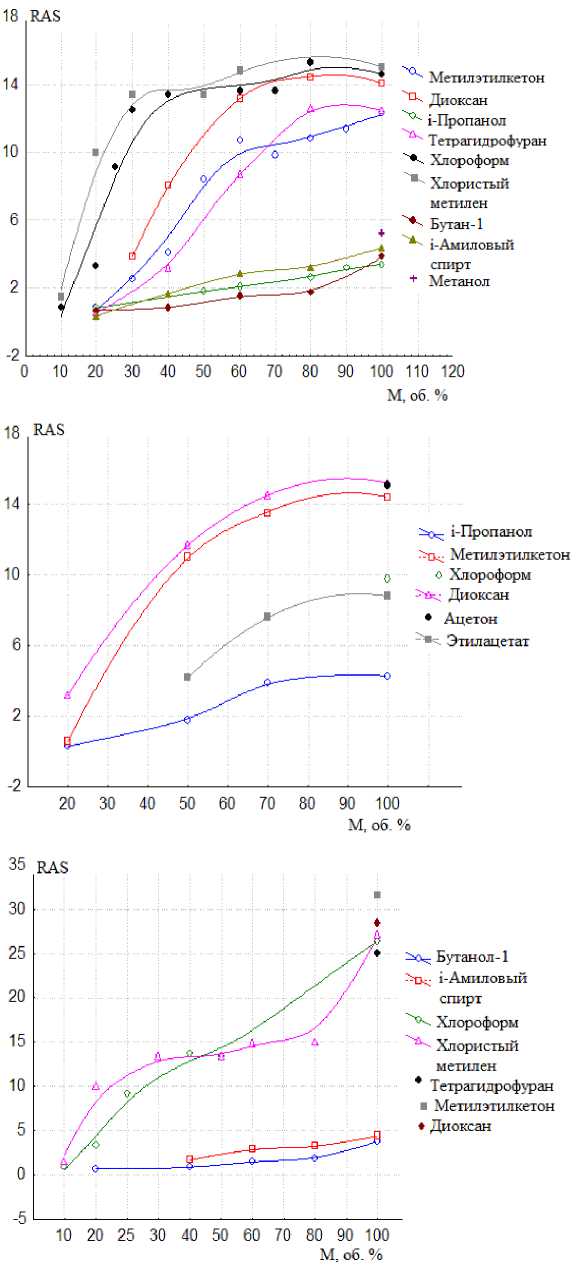
Рис. 1. Зависимость растворимости трибенуронметила (а), хлорсульфурона (б) и сульфометуронметила (в) от содержания полярного компонента в смесях растворителей гексан – п лярный компонент (Т=293 К)
Неспецифическая сольватация, с точки зрения электростатического подхода, определяется зависимостями от диэлектрической проницаемости и
а
б
в
показателя преломления. Постоянные использованных растворителей представлены в табл. 2.
Таблица 2. Физико-химические параметры растворителей (полярность ( Y ), поляризуемость ( Р ), параметр общей кислотности (электрофильности) ( Е ), общей основности (нуклеофильности) ( В ) растворителей) [9]
|
Растворитель |
Y |
Р |
Е |
В |
|
метанол |
0,4774 |
0,27671 |
14,90 |
218 |
|
этанол |
0,4698 |
0,29909 |
11,60 |
235 |
|
бутанол |
0,4574 |
0,32381 |
10,30 |
231 |
|
изопропанол |
0,4601 |
0,30961 |
8,70 |
236 |
|
изобутанол |
0,4588 |
0,32163 |
7,40 |
230 |
|
метиленхлорид |
0,4217 |
0,33982 |
2,70 |
23 |
|
хлороформ |
0,3587 |
0,33570 |
3,28 |
14 |
|
диоксан |
0,2231 |
0,33845 |
4,20 |
237 |
|
тетрагидрофуран |
0,4049 |
0,32916 |
0 |
287 |
|
метилэтилкетон |
0,4605 |
0,31040 |
2,00 |
209 |
|
ацетонитрилл |
0,4803 |
0,28568 |
5,20 |
160 |
|
гексан |
0,1862 |
0,30810 |
0 |
0 |
Для исследования влияния на величину растворимости, представленных в табл. 2 свойств, использован метод пошаговой регрессии. В качестве зависимых переменных использовались значения растворимости в индивидуальных растворителях. В результате установлено отсутствие значимой регрессии (для всех зависимостей уровень значимости критерия F-Фишера больше 0,05) растворимости производных сульфонилмочевины, по отношению ко всем исследуемым растворителям. По-видимому, это свидетельствует о различных механизмах сольватации. В связи с этим, протонные растворители были выделены в отдельную группу. Для определения степени влияния параметров независимых переменных, входящих в корреляционные уравнения, проведена стандартизация их значений. В результате расчетов определены наиболее значимые факторы, представленные в регрессионных уравнениях:
RAS (трибенуронметил)= 12,67 + 2,17Р (r=0,944; F=24,7; р=0,016; n=6),
RAS (хлорсульфурон)= 13,63 + 2,48B (r=0,998; F=689,8; р=0,001; n=4), ( 2 ) RAS (сульфометуронметил) спирты = 0,80 +1,18Y (r=0,994; F=239,8; р=0,001; n=5), ( 3 )
RAS (сульфометуронметил) спирты = 1,16 + 0,77 Е (r=0,936; F=21,4; р=0,019; n=5), ( 4 )
RAS (хлорсульфурон) спирты = 7,48 + 1,68 ⋅ Е (r=0,946; F=25,7; р=0,015; n=5),
RAS (хлорсульфурон)спирты= 5,38 + 6,78⋅Y (r=0,945; F=25,2; р=0,015; n=5), (6), где: RAS – растворимость анализируемого соединения;
E – кислотность растворителя;
-
Y - полярность растворителя;
Р – поляризуемость растворителя;
В – основность растворителя;
р – уровень значимости критерия F-Фишера.
Уравнения ( 1-6) показывают, что величину растворимости производных сульфонилмочевины определяют процессы как специфической, так и неспецифической сольватации. При специфической сольватации в исследованных растворителях, соединениям исследуемого ряда свойственно проявление как электрофильных, так и нуклеофильных свойств.
Растворимость производных сульфонилмочевины в спиртах, определяется параметрами кислотности и полярности данных растворителей ( 1-6 ) (рис. 2). Видно (рис. 2), что специфическая сольватация производных сульфонилмочевины, достаточно хорошо описывается изменением параметра кислотности спиртов, то есть в данных растворителях исследуемые соединения выступают, в основном, в качестве нуклеофильных
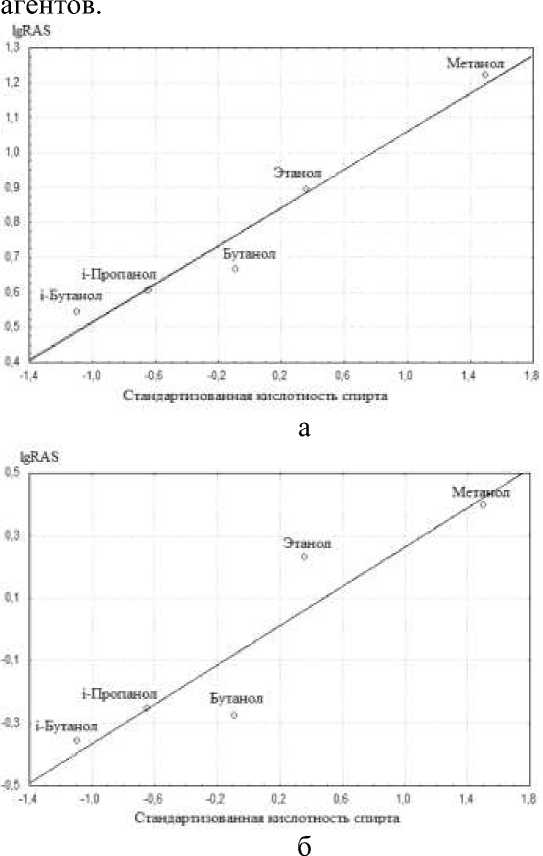
Рис. 2. Зависимость растворимости хлорсульфурона ( а ) и сульфометуронметила ( б ) от кислотности спирта
Таким образом, результаты проведенных исследований влияния свойств среды не противоречат тому, что величину растворимости производных сульфонилмочевины определяют процессы как специфической, так и неспецифической сольватации. Специфическая сольватация соединений исследуемого ряда в спиртах, обусловлена общей кислотностью растворителя.
Список литературы Влияние некоторых параметров растворителей на растворимость производных сульфонилмочевины
- Куликова Н.А., Лебедева Г.Ф. Гербициды и экологические аспекты их применения. Учебное пособие. М.: Либроком, 2010. 152 с.
- Спиридонов Ю.Я., Шестаков В.Г., Никитин Н.В. Технические средства и технологические особенности применения гербицидов и арборицидов. Научно-практическое руководство. М.: РАСХН ГНУ ВНИИФ, 2009. 68 с.
- Дуров В.А., Шилов И.Ю. Надмолекулярная организация и физико-химические свойства растворов циклогексанон - циклогексанол // Журн. физич. химии. 1996. Том 70. № 12. С. 2180-2186.
- Панченков Г.Н. Теория вязкости жидкостей. М.: Гостоптехиздат, 1947. 156 с.
- Государственная фармакопея СССР. Общие методы анализа. М.: Медицина, 1987. 334 с.
- Арзамасцев А.П., Сенов П.Л. Стандартные образцы лекарственных веществ. М.: Медицина, 1978. 448 с.
- Коппель И.А., Пальм В.А. // Реакционная способность органических соединений. 1971. Т. 8. № 1 (27). С. 291-295.
- Shorter J., Chapman N.B. Advances in linear free energy relationships. London - N.Y.: Plenum press, 1972. 486 p.
- Пальм В.А. Основы количественной теории органических реакций. Л.: Химия, 1977. 359 с.


