Влияние низкочастотного магнитного поля на растворимость органоминералов человека оксалатного типа в воде in vitro
Автор: Попков В.М., Усанов Д.А., Усанов А.Д., Ребров В.Г., Верхов Д.Г., Буланов В.М.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Урология
Статья в выпуске: 3 т.8, 2012 года.
Бесплатный доступ
Цель: выяснение влияния низкочастотного ПМП, действующего на воду с помещенным в нее мочевым камнем человека (оксалатного типа), на эффективность растворения вещества камня in vitro. В состав камня входили органические компоненты (63,1%), приводящие к уменьшению плотности раствора; мочевина (18,8%), напротив, приводящая к ее увеличению, и щавелевая кислота (19,7%). Материал и методы. При воздействии низкочастотных переменных магнитных полей могут возникать структурные изменения водных растворов, проявление которых зависит от химического состава исследуемых растворов. Результаты. Уменьшение величины коэффициента пропускания Т (%) от времени растворения образца камня свидетельствует об увеличении концентрации растворенного вещества камня в водном растворе, обработанного ПМП в диапазоне частот 2-9 Гц на фоне контрольного, тогда как рост этой зависимости с увеличением частоты ПМП в интервале 11-22 Гц свидетельствует о меньшей концентрации в опытном растворе, чем в контрольном. Заключение. Результаты эксперимента по определению влияния ПМП в диапазоне 2-22 Гц на растворимость образца мочевого камня, диспергированного и находящегося в воде, при действующем ПМП в течение часа свидетельствуют о максимальной растворимости камня при частоте 2 Гц на 14% больше, чем в контрольном растворе. Эффективность влияния ПМП на растворимость органоминерала падает с ростом частоты, что подтверждают результаты спек-трофотометрических и ареометрических измерений.
Коэффициент пропускания, мочевина, переменное магнитное поле, плотность, растворимость органоминералов
Короткий адрес: https://sciup.org/14917632
IDR: 14917632
Текст научной статьи Влияние низкочастотного магнитного поля на растворимость органоминералов человека оксалатного типа в воде in vitro
Адрес: 410056, г. Саратов, ул. Чапаева, 19/27, кв. 97.
Тел.: +79272772758.
частотных магнитных полей [1]. Под влиянием низкоинтенсивных переменных магнитных полей (ПМП) могут возникать структурные изменения водных растворов, проявление которых зависит от химического состава исследуемых растворов [2]. Целью исследо- ваний, результаты которых изложены в настоящей работе, было выяснение влияния низкочастотного ПМП, действующего на воду с помещенным в нее мочевым камнем человека (оксалатного типа), на эффективность его растворения в воде in vitro. Такого рода исследования проводились для случая, когда мочевые камни (ураты) помещались в предварительно обработанную ПМП воду [3].
Методы. В каждом эксперименте использовали минералы оксалатного типа из коллекции мочевых камней, предоставленной кафедрой урологии Саратовского государственного медицинского университета.
Опыты проводились на водных растворах диспергированного до размера фракции 0,1-0,5 мм мочевого камня из указанной коллекции. Рабочий объем растворов составлял 8 мл. Источником магнитного поля служила установка, детальное описание которой приведено в работе [4]. В качестве контроля использовали растворы того же образца в дистиллированной воде, которые находились в той же лаборатории при фоновых уровнях магнитных полей, характерных для места проведения опытов.
Растворимость органоминерала в опыте определяли:
-
1) спектрофотометрическим методом в величинах на пропускание T (%). Регистрацию проводили через каждые 15 мин воздействия ПМП в течение часа на спектрофотометре Shimadzu-MRS-5000 (Япония) при комнатной температуре в кварцевых кюветах размером 1×1×4,5 см. Спектры анализировали как в максимумах поглощения матричных белков мочевых камней при λ=290 нм [5], так и в видимой области спектра при длине волны λ=560 нм. Оптическая плотность раствора и концентрация растворенного в нем вещества в исследуемом объекте связаны прямой пропорциональной зависимостью, что используется для количественных определений содержания компонентов [6];
-
2) ареометрическим методом по изменению величины плотности растворов от времени растворения минералов непосредственно в процессе магнитной обработки его в течение часа.
В предварительном опыте был проведен анализ фазового состава мочевого камня методом ИК-спектроскопии. Исходный материал готовился способом прессования таблеток с KBr (5 мг образца и 300 мг KBr). Спектры материала регистрировали на ИК-спектрометре Infralum FT-801.
Результаты. Для определения элементного состава отобранного для опыта мочевого камня был проведен его анализ на рентгенофлуоресцентном спектрометре (спектроскан МАКС-GV). Отобранный над осадком раствор прокачивали через сорбционный фильтр ДЭТАТА. После прокачивания рабочего раствора фильтр тщательно промывали дистиллированной водой. Фильтр слегка подсушивался, затем регистрировались спектры рентгеновской флуоресценции вещества, сорбированного на фильтре. Полученные спектры для определения концентрации элементов обрабатывались по методу фундаментальных параметров. Результаты этого анализа представлены в таблице.
Элементный состав минеральной части органоминерала, используемого в опыте (0,2% от общей массы органоминерала)
|
Компонента |
Концентрация, % |
|
SiO2 |
7,48 |
|
PO 4 |
7,92 |
|
SO 4 |
15,75 |
|
Cl |
14,03 |
|
K |
10,70 |
|
CaO |
20,11 |
|
Fe |
2,10 |
|
Cu |
18,91 |
|
Zn |
3,00 |
Как видно из таблицы, основная доля исследуемого образца состоит из силикатов, фосфатов,
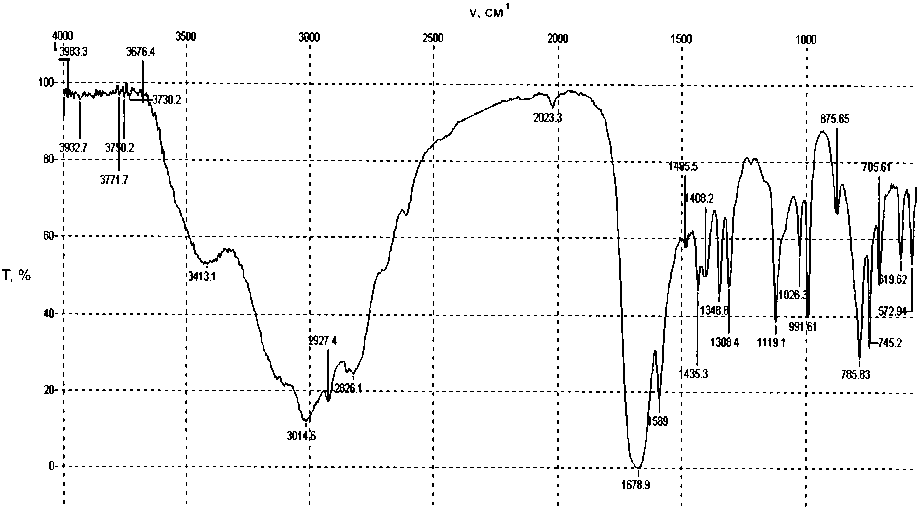
Рис. 1. ИК-спектр исходного органоминерала, использованного в опыте
кальцитов. Анализ ИК-спектра этого образца, представленного на рис. 1, показал, что в его составе обнаруживаются белковые компоненты (63,1%), мочевина (18,8%) и щавелевая кислота (19,7%). Чтобы выяснить, каким образом ПМП влияет на процесс растворения мочевого камня исследуемого типа, был проведен модельный эксперимент по растворению отдельных компонент, входящих в его состав.
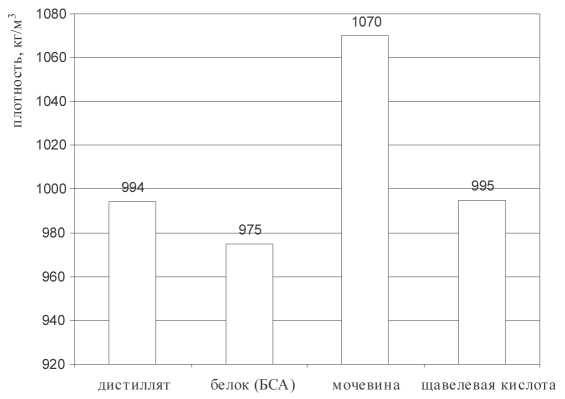
Рис. 2. Измерение плотности дистиллированной воды в присутствии белка, мочевины и щавелевой кислоты: белок (БСА) 0,05 г / 8 мл воды; мочевина 0,014 г / 8 мл воды; щавелевая кислота 0,015 г / 8 мл воды
Как следует из рис. 2, присутствие органической компоненты в воде приводит к уменьшению плотности раствора, а присутствие мочевины приводит к ее увеличению. В растворе щавелевой кислоты изменение плотности по сравнению с дистиллированной водой было незначительным, что связано с плохой ее растворимостью в воде (8% при нормальных условиях).
Таким образом, при растворении образца мочевого камня необходимо учитывать несколько процессов: растворение органической компоненты камня вместе с минеральной его составляющей, выход в раствор мочевины и щавелевой кислоты (слабо растворимой в воде).
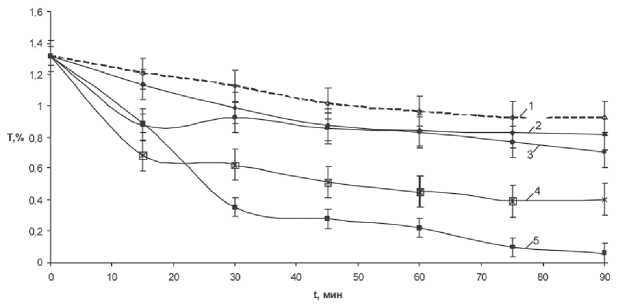
Рис. 3. Зависимость изменения коэффициента пропускания Т растворов от времени воздействия ПМП: кривая 1 — без магнитного поля; кривая 2 — частота ПМП 4 Гц; кривая 3 — частота ПМП 9 Гц; кривая 4 — частота ПМП 6 Гц; кривая 5 — частота ПМП 2 Гц
Обсуждение. Настоящее обсуждение полученных результатов относится к области фотометрии растворов на длине волны 290 нм, для которой наиболее выражено белковое поглощение. В видимой области (560 нм) различие в величине T (%) между контрольным и опытным растворами образца мочевого камня было незначительным и в данной работе не обсуждается.
На рис. 3 представлены зависимости коэффициента пропускания Т на длине волны 290 нм от времени растворения образца мочевого камня в дистиллированной воде, находящегося в ПМП в течение 60 минут c частотами из диапазона 2-9 Гц, а на рис. 4 — с частотами 11 и 22 Гц.
Уменьшение величины Т (%) с ростом времени растворения свидетельствует об увеличении концентрации растворенного образца, обработанного ПМП, на фоне контрольного, тогда как рост данной зависимости с увеличением частоты ПМП в интервале 11 -22 Гц (рис. 4) свидетельствует о меньшей концентрации растворенного образца в опытном растворе относительно контроля.
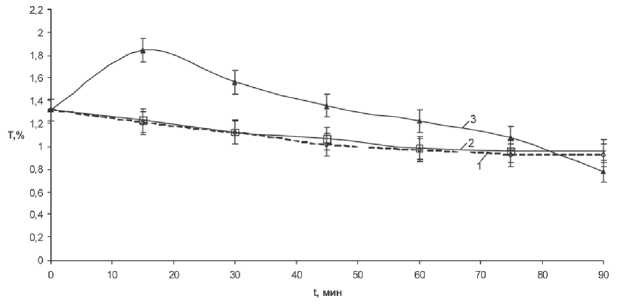
Рис. 4. Зависимость изменения коэффициента пропускания Т (%) растворов от времени воздействия ПМП: кривая 1 — без магнитного поля; кривая 2 — частота ПМП 11 Гц; кривая 3 — частота ПМП 22 Гц
Результаты по измерению плотности исследуемых растворов при действующем ПМП ареометриче-ским методом представлены на рис. 5 и 6.
Из приведенных на рис. 5 результатов следует, что для частоты 2 Гц в течение 15 минут наблюдается резкое уменьшение плотности раствора, после чего зависимость плотность раствора от времени растворения возрастает до значений несколько меньших, чем исходная перед включением ПМП. При частоте ПМП 6 и 9 Гц наблюдается сходная зависимость: уменьшение плотности раствора до 45-й минуты, после чего происходит ее возрастание. Для частот 4 и 9 Гц плотность уменьшается и начинает возрастать лишь при выключении ПМП на 60-й минуте. В отсутствие ПМП (кривая 1) наблюдается монотонный спад плотности раствора в течение 45 минут. Можно сделать вывод о том, что уменьшение плотности как опытного, так и контрольного раствора, связано с выходом в воду органической фракции, тогда как ее последующий рост в опытных растворах связан с выходом в воду мочевины, что хорошо соответствует модельному эксперименту, результаты которого приведены на рис. 2.
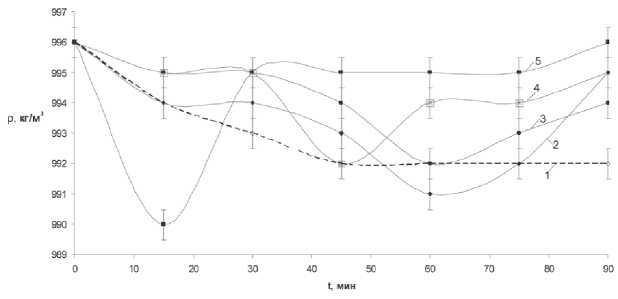
Рис. 5. Зависимость плотности раствора мочевого камня от времени растворения при воздействии ПМП из диапазона частот 2-9 Гц: кривая 1 — без магнитного поля; кривая 2 — частота ПМП 4 Гц; кривая 3 — частота ПМП 9 Гц;
кривая 4 — частота ПМП 6 Гц; кривая 5 — частота ПМП 2 Гц
На рис. 6 представлены результаты измерения плотности растворов того же образца мочевого кам-
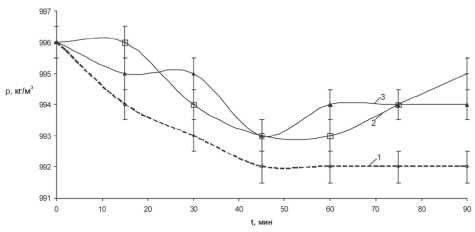
Рис. 6. Зависимость плотности раствора мочевого камня от времени растворения при воздействии ПМП: кривая 1 — без магнитного поля; кривая 2 — частота ПМП 11 Гц; кривая 3 — частота ПМП 22 Гц ня в зависимости от времени растворения при частотах ПМП 11, 22 Гц.
Исходя из полученных результатов (как фотометрических, так и ареометрических), можно предположить, что растворение мочевых камней непосредственно в ПМП в составе готового раствора идет в несколько стадий, и значение частоты ПМП существенным образом влияет на этот процесс. Результаты настоящего эксперимента отличаются от полученных нами ранее результатов [3], где использовали мочевые камни (уратного типа), в состав которых входила в основном мочевина (99,9%), хорошо растворимая в воде. В настоящем опыте образец мочевого камня по большей части состоит из малорастворимых и нерастворимых соединений (см. таблицу). Помимо этого, вся минеральная часть исследуемого мочевого камня связана большим количеством органической фазы.
Наблюдаемое уменьшение плотности раствора происходит при растворении органической фракции за счет гидратации белковых остатков [ 7 ]. Одновременно с этим происходит и увеличение концентрации мочевины в растворе. Следовательно, уменьшение плотности раствора за счет гидратированных органических компонент продолжается до тех пор, пока концентрация мочевины не достигнет того уровня, когда она начнет растворяться в связанной белками воде, что и влияет на увеличение плотности раствора.
Отметим, что, как было показано в [3], помещение в предварительно обработанную ПМП воду мочевых камней, относящихся к уратам, имело большую растворимость (примерно 27%), чем в контрольном растворе, которая была максимальной при частоте ПМП 22 Гц. Нами было также определено количество растворенного мочевого камня весовым методом, что составляло 22%, тогда как в контрольном растворе 8,1 % при воздействии ПМП с частотой 2 Гц.
Заключение. Таким образом, можно сделать вывод о том, что наблюдаемые изменения плотности раствора (см. рис. 5, 6), а именно падение плотности в интервале времени (15 мин — 2 Гц, 50 мин — 6 Гц, 60 мин — 9 Гц, см. рис. 5) связаны с растворением органической компоненты мочевого камня, а ее последующий рост объясняется выходом в раствор мочевины, в то время как в контрольном растворе происходит только растворение органической оболочки камня. Растворимость образца минерала оксалатного типа максимальна при ПМП с частотой 2 Гц и на 14% больше, чем в контрольном растворе. Эффективность влияния ПМП на растворимость органоминерала падает с ростом частоты.
Список литературы Влияние низкочастотного магнитного поля на растворимость органоминералов человека оксалатного типа в воде in vitro
- Аксенов С. И. Вода и ее роль в регуляции биологических процессов. М.: Наука, 1990. 118 с.
- Яблокова Е.В., Новиков В.В., Фесенко Е.Е. Действие слабых магнитных полей на флуоресценцию воды и водно-солевых растворов. Выделение и частичная характеристика флуоресцирующих фракций//Биофизика. 2007. Т. 52, № 2. С. 197-204
- Попков В.М., Усанов Д. А., Ребров В. Г., Уса-нов А.Д. Влияние низкочастотного магнитного поля на растворимость органоминералов человека in vitro//Урология. 2012. Вып. 2. С. 17-19
- Усанов Д.А., Шишкин ГГ., Скрипаль А. В., Усанов А.Д. Влияние внешнего переменного магнитного поля на частоту сердцебиений пресноводного рачка -дафнию//Биомедицинская радиоэлектроника. 2001. Вып. 8. С. 57-61
- Демченко А. П. Ультрафиолетовая спектофотометрия и структура белков. Киев: Наук, думка. 1981. 208 с.
- Кеслер И. Методы инфракрасной спектроскопии в химическом анализе. М.: Мир, 1964. 257 с.
- Гильберт Линг. Физическая теория живой клетки: незамеченная революция. СПб.: Наука, 2008. 376 с.


