Влияние нового ингибитора GSK-3B на процессы адгезии, активации, секреции и агрегации тромбоцитов
Автор: Сиротенко Виктор Сергеевич, Бабков Денис Александрович, Осман Элиас, Спасов Александр Алексеевич
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 т.20, 2023 года.
Бесплатный доступ
Тромбообразование - сложный многостадийный процесс, состоящий из последовательных фаз адгезии, активации и агрегации тромбоцитов. Рецепторный ландшафт тромбоцитов представлен множеством подтипом рецепторов и сигнальных путей, связанных с их активацией. Одним из участников этих путей является киназа GSK3P, однако ее роль и функции в регуляции активности тромбоцитов остаются сложным и не до конца выясненным вопросом. Изучение антиагрегантной активности ингибитора GSK3P соединения К-167 показало отсутствие влияния на адгезию и P2Y1-активацию тромбоцитов. В то же время К-167 ингибирует агрегацию, опосредованную GPVI и P2Y12 рецепторами с IC50 3,0 и 7,9 мкМ соответственно. Влияние на тромбоксан А2 и тромбин-индуцированную агрегацию слабое или отсутствует, что подтверждает GSK3p-опосредованный механизм действия. Показано, что важным аспектом антиагрегантной активности данного вещества является ингибирование синтеза тромбоксана А2 in vivo и подавление секреции содержимого гранул тромбоцитов.
Антиагрегантное действие, адгезия, активация, агрегация, 2-оксиндолы, gsk3fi
Короткий адрес: https://sciup.org/142238798
IDR: 142238798 | УДК: 615.273
The effect of the new GSK-3B inhibitor on the processes of platelet adhesion, activation, secretion and aggregation
Thrombosis is a complex multi-stage process consisting of successive phases of adhesion, activation and aggregation of platelets. The platelet receptor landscape is represented by many subtypes of receptors and signaling pathways associated with their activation. One of the participants in these pathways is the GSK3P kinase, but its role and functions in the regulation of platelet activity remain a complex and not fully elucidated issue. The study of the antiplatelet activity of the GSK3G inhibitor of the K-167 compound showed no effect on platelet adhesion and P2Y1 activation. At the same time, K-167 inhibits aggregation mediated by GPVI and P2Y12 receptors with IC50 3.0 and 7.9 pM, respectively. The effect on thromboxane A2 and thrombin-induced aggregation is weak or absent, which confirms the GSK3li-mediated mechanism of action. It has been shown that an important aspect of the antiplatelet activity of this substance is the inhibition of the synthesis of thromboxane A2 in vivo and the suppression of the secretion of the contents of platelet granules.
Текст научной статьи Влияние нового ингибитора GSK-3B на процессы адгезии, активации, секреции и агрегации тромбоцитов
Сердечно-сосудистые заболевания занимают лидирующие позиции среди причин смертности во всем мире [1]. Причиной большинства сердечнососудистых заболеваний является патологический тромбоз артерий, образующийся вследствие разрыва атеросклеротической бляшки или повреждения сосуда. Стратегия лечения и профилактики атеро-тромботических состояний включает использование антиагрегантных средств. У существующих средств из данной группы препаратов описаны нежелатель- ные реакции, существенно ограничивающие их применение: резистентность, отсутствие эффективности при использовании двойных доз, а в случае применения двойной/тройной антитромбоцитарной терапии значительно возрастает риск кровотечений, гастропатий и т. п. [2]. Стадии агрегации кровяных пластинок сопровождаются реализацией множества механизмов, включающих активность рецепторного ландшафта тромбоцитов и их систему вторичных сигнальных мессенджеров. Адгезия и агрегация тромбоцитов на открытом внеклеточном матриксе требует скоординированного взаимодействия гликопротеиновых рецепторов поверхности тромбоцитов с адгезивными макромолекулами. В условиях высокого сдвига первоначальное привлечение тромбоцитов к «реактивной поверхности» опосредовано обратимым взаимодействием между гликопротеиновым рецептором тромбоцитов GP Ib и связанным с коллагеном фактором фон Виллебранда. Это взаимодействие позволяет клеткам устанавливать контакты с коллагеном посредством гликопротеинового рецептора GP VI. Такое взаимодействие приводит к запуску outsidein механизма активации и распространения сигнала с участием комплекса PI3K-Akt-GSK-3β и ведущего к клеточной активации и высвобождению вторичных медиаторов АДФ и тромбоксана А2 (ТхА2) [3]. Эти агонисты вместе с локально продуцируемым тромбином вносят вклад в клеточную активацию, стимулируя рецепторы, связанные с гетеротримерными G-белками, которые индуцируют различные сигнальные события и действуют синергетически, вызывая полную активацию тромбоцитов [4]. В связи с этим является обязательным изучение механизма антиагрегантного действия оригинальных молекул. Согласно множественным исследованиям сигнальный комплекс PI3K-Akt-GSK-3β в тромбоцитах представляет особый интерес, как потенциальная мишень для более селективной фармакотерапии патологической активации тромбоцитарного звена гемостаза [5–7]. В ранее проведенных исследованиях было выявлено новое производное 2-оксиндола соединение К-167, проявляющее выраженную антиагрегантную активность по сравнению ацетилсалициловой кислотой, а также установлено, что соединение К-167 дозозависимо ингибирует фермент GSK-3β [8].
ЦЕЛЬ РАБОТЫ
Изучить влияние данного вещества на процессы адгезии, активации, секреции и агрегации тромбоцитов.
МЕТОДИКА ИССЛЕДОВАНИЯ
Эксперименты выполнены на 12 кроликах-самцах массой 2,5–3,0 кг и 42 нелинейных крысах-самцах (ФГБУН НЦБМТ ФМБА Росии).
3-Пиридин-2-ил-2-оксиндол К-167 синтезирован на кафедре медицинской химии и тонкого органического синтеза МГУ им. М. В. Ломоносова под руководством канд. хим. наук Н. А. Лозинской.
Исследование антиадгезивных свойств проводили в условиях in vitro при добавлении к цельной крови кроликов с помощью двухканального люмиагрегометра Chronolog-700. Образцы цельной крови получали методом свободного падения капли из ушной краевой вены кролика в пробирку, содержащую 3,8%-й раствор натрия цитрата. Активацию рецепторов адгезии тромбоцитов GP VI инициировали раствором коллагена I типа (50 мкг/мл). Об уровне адгезии тромбоцитов к микрофибриллам коллагена судили по значению импеданса [9].
Влияние на активацию тромбоцитов кроликов изучали в условиях in vitro методом малоуглового светорассеяния с помощью лазерного анализатора Лайт-Скан (НПФ «Люмэкс», Россия) (Патент РФ № 2391665, 29.12.2008). В качестве вещества сравнения был использован селективный антагонист P2Y 1 рецепторов тромбоцитов соединение MRS-2179 (Sigma, США).
Определение влияния на секрецию АТФ из плотных гранул тромбоцитов кроликов проводили на двухканальном люмиагрегометре Chronolog-700 с использованием люциферин-люциферазы. Уровень АТФ при этом определялся количественно путем измерения биолюминисценции. В качестве стимулятора тромбоцитов использовали АДФ (5 мкМ) [10].
Антиагрегантные свойства были изучены после стимуляции растворами АДФ (5 мкМ), коллагена (4 мкг/мл), агониста тромбоксановых рецепторов U46619 (3 мкМ) и тромбина (0,5 ЕД/мл) в качестве стимуляторов процессов агрегации тромбоцитов. Исследования проводили в плазме богатой тромбоцитами (при стимуляции АДФ и коллагеном) и суспензии отмытых тромбоцитов (при стимуляции U46619 и тромбином) при помощи двухканального люмиагрегометра Chronolog-700. Для получения суспензии отмытых тромбоцитов производили забор цельной крови кроликов с последующим центрифугированием (250 g, 10 мин). Полученный супернатант (богатая тромбоцитами плазма) повторно центрифугировали (850 g, 20 мин) для осаждения кровяных пластинок. Осадок подвергали ресуспензированию с использованием Tyrode буфера состава: 12,0 мМ NaHCO 3 , 138,0 мМ NaCl, 0,1 мМ CaCl 2 5,5 мМ глюкоза, 2,9 мМ KCl, 2,0 мМ MgCl 2 , 0,4 мМ NaH 2 PO 4 , 10,0 мМ HEPES (pH 7,4) [11].
Определение уровня синтеза TxB 2 в тромбоцитах осуществляли методом ИФА при стимуляции тромбоцитов арахидоновой кислотой (50 мкМ). Исследуемое соединение и препарат сравнения ацетилсалициловую кислоту вводили внутрижелудочно однократно за 2 часа до забора крови из брюшной аорты крыс в дозах ED50 антиагрегантной активности in vivo . Образцы цельной крови получали после наркотизации животных хлоралгидратом (400 мг/кг). Забранную кровь стабилизировали 3,8%-м цитратом натрия (9 : 1). Для исследования получали плазму, богатую тромбоцитами, путем центрифугирования цельной крови крыс при 250 g в течение 10 мин.
Исследование одобрено региональным этическим комитетом IRB 00005839 IORG 0004900 (OHRP) протокол № 2021/10 от 15.02.2021.
Статистическую обработку данных проводили с использованием встроенных функций MS Excel 2019 (расчет значений M, SEM и IC 50 методом линейной регрессии) и программы GraphPad Prism 8.0. Анализ достоверности проводили с применением критерия множественного сравнения 1-сторонний ANOVA с поправкой Тьюки. Данные считали достоверными при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
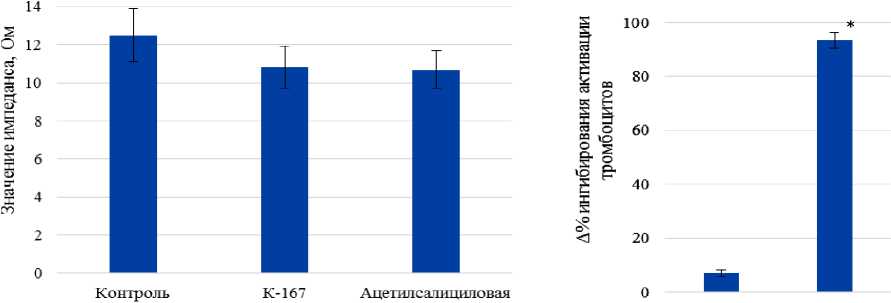
Первоначальная адгезия тромбоцитов к месту повреждения опосредуется связыванием коллагена, экспонированного на стенке поврежденного сосуда, с поверхностным GP VI [12]. При добавлении раствора коллагена в больших концентрациях к цельной крови происходит немедленная адгезия тромбоцитов к микрофибриллам коллагена и изменение значения импеданса. В контрольных образцах крови кроликов уровень импеданса составил 12,5 Ом. При добавлении раствора соединения К-167 к цельной крови в концентрации 100 мкМ наблюдалось снижение процессов адгезии тромбоцитов на 13,6 %, сопоставимое с действием ацетилсалициловой кислоты (рис. 1 а). Изучение процессов адгезии кровяных пластинок к коллагену позволило выявить недостоверное влияние соединения К-167 на данный процесс. Наряду с адгезией тромбоцитов происходит немедленная их активация. Одним из ключевых механизмов активации тромбоцитов является стимуляция P2Y1 рецепторов [13]. Селективный антагонист P2Y1 рецепторов тромбоцитов соединение MRS-2179 способствовало достоверному подавлению активации на 93,4 % (p < 0,05), в то время как исследуемое вещество К-167 имело незначительное влияние на данный процесс (рис. 1 б).
16 120
кислота К-167 MRS-2179
а б
Рис. 1. Влияние соединения К-167 на адгезию (а) и активацию (б) тромбоцитов:
* - данные достоверны относительно контроля, критерий 1 -сторонний ANOVA с поправкой Тьюки (р < 0,05)
С целью рекрутинга циркулирующих кровяных пластинок в процесс тромбообразования активированные тромбоциты высвобождают содержимое гранул хранения (АТФ, АДФ, Ca2+, P-селектин, цитокины и др.). Так, при стимуляции интактных тромбоцитов АДФ наблюдалось увеличение секреции АТФ до 65,9 нМ. Соединение К-167 в концентрации 100 мкМ способствовало достоверному снижению уровня секретируемой АТФ до 8,9 нМ (p < 0,05), что на 86,2% ниже контрольных значений. Такой уровень эффекта позволил провести дозозависимое изучение влияния соединения К-167. В концентрациях 10 и 1 мкМ исследуемое вещество способствовало подавлению секреции тромбоцитов до 22,5 нМ (p < 0,05) и 57,1 нМ соответственно. Значение IC50 при этом составило 6,7 мкМ (рис. 2). Ацетилсалициловая кислота в этих условиях показала меньшее по размеру эффекта подавление секреции АТФ с IC50 68,2 мкМ.
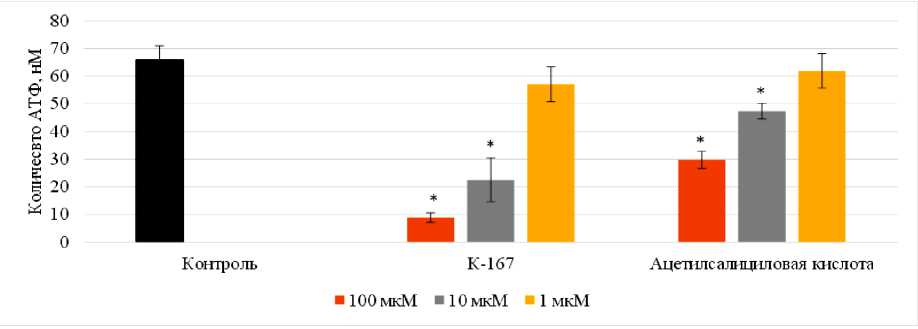
Рис. 2. Влияние соединения К-167 на секрецию АТФ из гранул тромбоцитов in vitro
Примечание: * - данные достоверны относительно контроля, критерий 1-сторонний ANOVA с поправкой Тьюки (р < 0,05)
Секрецию кровяных пластинок способны стимулировать различные агонисты, через множество путей внутриклеточного сигнального каскада. Как видно из рис. 3 наибольшую концентрационно-зависимую активность соединение К-167 проявило в отношении таких индукторов, как АДФ и коллаген. Показатели IC 50 при этом составили 7,9 и 3,0 мкМ соответственно.
В ходе исследований на суспензии отмытых тромбоцитов было установлено, что соединение К-167 дозозависимо предотвращало процессы агрегации тромбоцитов при стимуляции селективным агонистом тромбоксановых рецепторов U46619 (IC 50 43,7 мкМ). При этом вещество К-167 не способствовало снижению агрегации тромбоцитов, индуцированной тромбином.
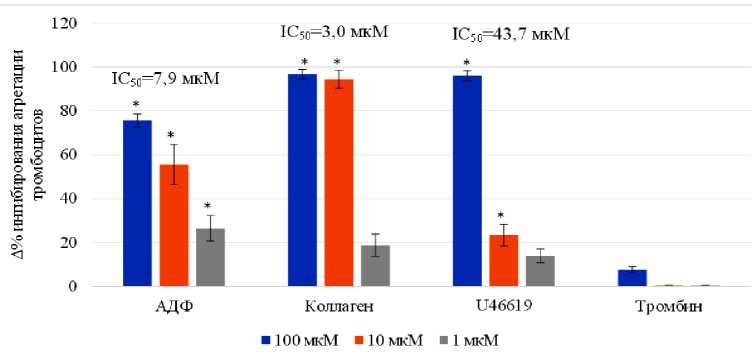
Рис. 3. Влияние соединения К-167 в концентрациях 100, 10 и 1 мкМ на агрегацию тромбоцитов, индуцированную различными агонистами: * - данные достоверны относительно контроля, критерий 1-сторонний ANOVA с поправкой Тьюки (р < 0,05)
Для более полной оценки действия соединения К-167 на систему гемостаза и, в частности, на тромбоксан-простациклиновую систему, было проведено исследование в условиях целостного организма при однократном внутрижелудочном введении. При стимуляции тромбоцитов крыс контрольной группы арахидоновой кислотой среднее количество TxB 2 составило 172,8 пкг/мл. Препарат сравнения – ацетилсалициловая кислота – при однократном внутрижелудочном введении способствовала дозозависимому ингибированию синтеза TxB 2 . Так, в дозе 92,3 мг/кг наблюдалось достоверное снижение количества TxB 2 до 20,6 пкг/мл ( p < 0,05), что на 88,1% ниже значений контрольной группы. Снижение вводимой дозы до 46,2 и 23,1 мг/кг позволило установить, что уровень
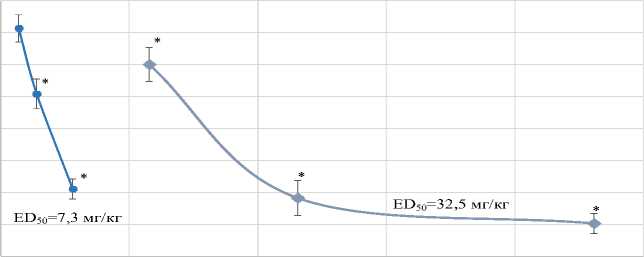
TxB 2 достоверно снижался до 36,5 ( p < 0,05) и 120,1 ( p < 0,05) пкг/мл соответственно. Значение ED 50 при этом для ацетилсалициловой кислоты составило 32,5 мг/кг (рис. 4). Для исследуемого соединения К167 также была установлена способность дозозависимо ингибировать синтез TxB 2 при однократном внутрижелудочном введении. В дозе 11,2 мг/кг соединение К-167 достоверно способствовало снижению уровня TxB 2 ( p < 0,05) до 42,2 пкг/мл, что на 75,6% ниже значений контрольной группы. При снижении дозы до 5,6 мг/кг наблюдалось достоверное ингибирование уровня TxB 2 до 101,7 пкг/мл ( p < 0,05).
В дозе 2,8 мг/кг соединение К-167 способствовало снижению синтеза TxB 2 до 142,7 пкг/мл. Показатель ED 50 при этом составил 7,3 мг/кг.
140 в
а
100 m
X
80 о
20 40 60 80 100
Доза, мг/кг
К-167 Ацетилсалициловая кислота
Рис. 4. Влияние соединения К-167 на уровень TxB2 в тромбоцитах крыс при однократном внутрижелудочном введении: * - данные достоверны относительно контроля, критерий 1 -сторонний ANOVA с поправкой Тьюки (р < 0,05)
При действии на тромбоциты АДФ происходит последовательная активация семейства пуриновых рецепторов (P2Y i и P2Y 12 ) на поверхности кровяных пластинок для достижения полной, необратимой агрегации тромбоцитов [14]. Степень влияния соединения К-167 на активацию тромбоцитов позволяет сделать вывод об отсутствии Р2Ү 1 -зависимого механизма антиагрегантного действия у исследуемого вещества.
Важным этапом является дальнейшая передача сигнала внутрь клетки ( outside-in ) и активация пути PI3K-Akt-GSK3e. Результирующим эффектом активации данного комплекса является стимуляция и стабилизация экспрессии гликопротеинов на поверхности тромбоцитов (GP Ib-IX-V, GP VI и др.) [15], а также высвобождение ионов Ca2+ из внутриклеточного депо, необходимых для активности PLA 2 [16].
Коллаген является лигандом для тромбоцитарного GP VI, экспрессируемого исключительно на тромбоцитах и мегакариоцитах [17]. Сигнальный путь активации GPVI сопровождается увеличением активности PLCy2, которая, в свою очередь, катализирует образование инозитол-1,4,5-трифосфата (IP3) и диацилглицерола (DAG). Образующиеся DAG и IP3 активируют протеинкиназу C (PKC) и высвобождение Ca2+ из внутриклеточных депо соответственно [18]. При этом происходит усиление активности цитозольной PLA2, катализирующей превращение арахидоновой кислоты. Последняя, в свою очередь, подверга ется воздействию ЦОГ-1 и ТхА2-синтазы с образованием мощного проагрегантного вещества тромбоксана А2 [19].
Мы показали, что К-167 обладает различной антиагрегантной активностью в зависимости от природы использованного агониста: коллаген > АДФ >> U46619 >> тромбин. Таким образом, наиболее чувствительными к действию К-167 являются рецепторные каскады GPVI и P2Y 12 , сходящиеся в активации пути PI3K-Akt-GSK3e [20]. GSK3в-опосредованный механизм действия К-167 также подтверждается его способностью подавлять секрецию АТФ из а-гранул (рис. 5). Кроме того, АДФ и коллаген при действии на тромбоциты имеют общие, перекликающиеся пути в системе сигнальных мессенджеров, нацеленные на синтез TxA 2 . Ингибирование процессов агрегации тромбоцитов, вызванных данными агонистами, косвенно может свидетельствовать о способности соединения К-167 оказывать влияние на снижение продукции TxA 2 .
Данная способность для исследуемого соединения была подтверждена в эксперименте по определению уровня TxB 2 в плазме крови крыс методом ИФА. Кроме того, дозозависимое ингибирование агрегации отмытых тромбоцитов, стимулированных агонистом рецепторов TxA 2 U46619, может указывать на наличие антагонистического влияния соединения К-167 на тромбоксановые рецепторы, их экспрессию или сигнальный каскад этих рецепторов.
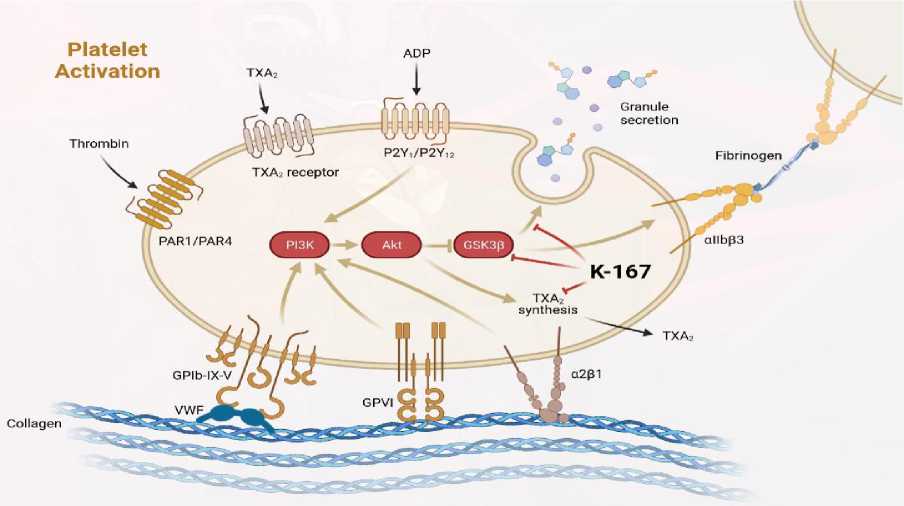
Рис. 5. Предполагаемый механизм антиагрегантного действия соединения К-167
При действии на отмытые тромбоциты раствора тромбина происходит классическая активация PARs-рецепторов на поверхности тромбоцитов, что указывает на функции этого фактора свертывания крови, выходящие за рамки коагуляционного каскада [21].
Тромбин протеолитически расщепляет часть внеклеточной петли этих рецепторов. Являясь мощным индуктором, он опосредует агрегацию тромбоцитов, мобилизацию кальция и изменение формы тромбоцитов, что в итоге приводит к активации рецептора
GP IIb/IIIa и развитию стойкой, необратимой агрегации тромбоцитов [22].
Отсутствие влияния соединения К-167 на тром-бин-индуцированную агрегацию тромбоцитов можно объяснить разнообразием сигнальных каскадов при активации разных подтипов PARs-рецепторов.
На ряду с классическим вариантом активации PAR-рецепторов, сопровождающимся передачей сигнала через G αq/11 , G α12/13 и G αi/o белки, существует дополнительный β-арристиновый путь, связанный с повышением активности Rho-киназы.
ЗАКЛЮЧЕНИЕ
Таким образом, проведенное нами исследование позволяет предположить, что соединение К-167 проявляет антиагрегантные свойства за счет подавления активности сигнальных каскадов рецепторов коллагена и АДФ, а также нарушает секрецию содержимого гранул тромбоцитов при их активации, что, вероятно, опосредовано ингибированием GSK3β. Механизм снижения продукции TxA 2 и подавления TxA 2 -зависимой активации тромбоцитов неясен и требует дополнительного изучения. Также представляется интересным изучение влияния К-167 на стабильность тромба в условиях высоких скоростей сдвига как следствие GSK3β-опосредованной активации ин-тегрина αIIbβ3.
Список литературы Влияние нового ингибитора GSK-3B на процессы адгезии, активации, секреции и агрегации тромбоцитов
- Wang, X., Ziegler, M. et al. Molecular imaging of arte-rial and venous thrombosis. British Journal of Pharmacology. 2021;178(21):4246–4269. https://doi.org/10.1111/bph.15635
- Setiabakti, N. M., Larsson, P., Hamilton, J. R. Phos-phoinositide 3-Kinases as Potential Targets for Thrombosis Prevention. International Journal of Molecular Sciences. 2022;23(9):4840. https://doi.org/10.3390/ijms23094840.
- O’Brien K. A., Stojanovic-Terpo A., Hay N., Du X. An important role for Akt3 in platelet activation and thrombosis. Blood. 2011;118(15):4215–4223. https://doi.org/10.1182/blood-2010-12-323204.
- Nieswandt B., Varga-Szabo D., Elvers, M. Integrins in platelet activation. Journal of Thrombosis and Haemostasis. 2009;7:206–209. https://doi.org/10.1111/j.1538-7836.2009.03370.x
- Chen H., Zhang S. et al.. Fruitflow inhibits platelet function by suppressing Akt/GSK3β, Syk/PLCγ2 and p38 MAPK phosphorylation in collagen-stimulated platelets. BMC Com-plementary Medicine and Therapies. 2022; 22(1):75. https://doi.org/10.1186/s12906-022-03558-5.
- Laurent P.-A., Séverin S. et al. Platelet PI3Kβ and GSK3 regulate thrombus stability at a high shear rate. Blood. 2015;125(5):881–888. https://doi.org/10.1182/blood-2014-07-588335
- Wei G., Xu X. et al. Salidroside inhibits platelet func-tion and thrombus formation through AKT/GSK3β signaling pathway. 2020;12(9):8151–8166. https://doi.org/10.18632/ ag-ing.103131.
- Lozinskaya N. A., Babkov D. A. et al. Synthesis and biological evaluation of 3-substituted 2-oxindole derivatives as new glycogen synthase kinase 3β inhibitors. Bioorganic & Me-dicinal Chemistry. 2019;27(9):1804–1817. https://doi.org/ 10.1016/j.bmc.2019.03.028.
- Perrella, G., Nagy, M., Watson, S. P., Heemskerk, J. W. M. Platelet GPVI (Glycoprotein VI) and Thrombotic Complications in the Venous System. Arteriosclerosis, Thrombosis, and Vas-cular Biology. 2021;41(11):2681–2692. https://doi.org/10.1161/ ATVBAHA.121.316108.
- Ushiki, T., Mochizuki, T. et al. Modulation of ATP Production Influences Inorganic Polyphosphate Levels in Non-Athletes’ Platelets at the Resting State. International Journal of Molecular Sciences. 2022;23(19):11293. https://doi.org/ 10.3390/ijms231911293.
- Zhao J., Xu Y. et al. Roxadustat Does Not Affect Platelet Production, Activation, and Thrombosis Formation. Arteriosclerosis, Thrombosis, and Vascular Biology. 2021;41(10):2523–2537. https://doi.org/10.1161/ATVBAHA.121.316495.
- Koltai K., Kesmarky G. et al. Platelet Aggregometry Testing: Molecular Mechanisms, Techniques and Clinical Im-plications. International Journal of Molecular Sciences. 2017;18(8):1803. https://doi.org/10.3390/ijms18081803.
- Gremmel T., Yanachkov I. B. et al. Synergistic Inhibi-tion of Both P2Y 1 and P2Y 12 Adenosine Diphosphate Recep-tors As Novel Approach to Rapidly Attenuate Platelet-Mediated Thrombosis. Arteriosclerosis, Thrombosis, and Vascular Biolo-gy. 2016;36(3):501–509. https://doi.org/10.1161/ATVBAHA. 115.306885.
- Suzuki T. Hetero-oligomerization and Functional Inter-action between Purinergic Receptors Expressed in Platelets to Regulate Platelet Shape Change. Yakugaku zasshi. 2015;135(12):1335–1340. https://doi.org/10.1248/yakushi.15-00178.
- O’Brien K. A., Gartner T. K. et al. ADP-Stimulated Ac-tivation of Akt During Integrin Outside-In Signaling Promotes Platelet Spreading by Inhibiting Glycogen Synthase Kinase-3β. Arteriosclerosis, Thrombosis, and Vascular Biology. 2012;32(9): 2232–2240. https://doi.org/10.1161/ATVBAHA.112.254680.
- Burke, J. E., Dennis, E. A. Phospholipase A2 struc-ture/function, mechanism, and signaling. Journal of Lipid Re-search. 2009;50:237–S242. https://doi.org/10.1194/jlr.R800033-JLR200.
- Qiao J., Arthur J. F. et al. Regulation of platelet acti-vation and thrombus formation by reactive oxygen species. Re-dox Biology. 2018;14:126–130. https://doi.org/10.1016/ j.redox.2017.08.021.
- Amelirad A., Shamsasenjan K. et al. Signaling Path-ways of Receptors Involved in Platelet Activation andShedding of These Receptors in Stored Platelets. Advanced Pharmaceu-tical Bulletin. 2019;9(1):38–47. https://doi.org/10.15171/apb. 2019.005.
- Lucotti, S. Cerutti, C. et al.. Aspirin blocks formation of metastatic intravascular niches by inhibiting platelet-derived COX-1/thromboxane A2. Journal of Clinical Investigation. 2019;129(5):1845–1862. https://doi.org/10.1172/JCI121985.
- Moroi, A. J., Watson, S. P. Impact of the PI3-kinase/Akt pathway on ITAM and hemITAM receptors: Haemo-stasis, platelet activation and antithrombotic therapy. Biochemi-cal Pharmacology. 2015;94(3):186–194. https://doi.org/ 10.1016/j.bcp.2015.02.004.
- Chandrabalan, A., Ramachandran, R. Molecular mechanisms regulating Proteinase‐Activated Receptors (PARs). The FEBS Journal. 2021;288(8);2697–2726. https://doi.org/ 10.1111/febs.15829.
- Nehaj, F., Sokol, J. et al. Thrombin Receptor Agonist Peptide–Induced Platelet Aggregation Is Reduced in Pa-tients Receiving Dabigatran. Clinical and Applied Throm-bosis/Hemostasis. 2018;24(2):268–272. https://doi.org/ 10.1177/1076029617713871.


