Влияние оксидов 3d-элементов на фазовое превращение анатаз - рутил
Автор: Белая Елена Александровна, Викторов Валерий Викторович, Жеребцов Дмитрий Анатольевич, Колмогорцев Алексей Михайлович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.10, 2018 года.
Бесплатный доступ
Изучено влияние оксидов 3d-элементов на фазовые превращения анатаза в рутил. Показано, что добавки соответствующих оксидов являются рутилирующими, независимо от способа синтеза исходного диоксида титана анатазной модификации. Оксид никеля эффективнее снижает начальную температуру фазообразования и оказывает более сильный рутилирующий эффект, чем оксид хрома. Температура полиморфного превращения зависит от предыстории как оксида никеля (II), так и оксида титана (IV).
Фазовые превращения, твердые растворы, диоксид титана, анатаз, рутил, оксид хрома, оксид никеля
Короткий адрес: https://sciup.org/147160419
IDR: 147160419 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem180101
Effect of 3d-element oxides on the anatase - rutile phase transformation
The effect of 3-d-element oxides on the phase transformations of anatase into rutile has been studied. It has been shown that the oxide addition has a rutiling effect, regardless of the synthesis method of titanium dioxide in its anatase modification. Nickel and chromium oxides are rutiling additives and reduce the temperature of the anatase phase transition into rutile, with nickel oxide acting more efficiently than chromium oxide. The temperature of the polymorphic transformation depends on the prehistory of both nickel (II) oxide and titanium (IV) oxide.
Текст научной статьи Влияние оксидов 3d-элементов на фазовое превращение анатаз - рутил
Несмотря на многочисленные работы, посвященные фазовому переходу в диоксиде титана, интерес к этой системе не ослабевает до сих пор. Диоксид титана находит очень широкое применение, благодаря своим уникальным физико-химическим свойствам. Он используется в производстве пигментов, оптических материалов, фотокатализаторов, диэлектрической керамики и т. д. [1, 2].
Как правило, чаще используется рутильная модификация ТiO 2 , получаемая длительным прокаливанием анатаза. Хотя установлено, что при заданном соотношении анатазной и рутильной составляющей отмечается повышенная фотокаталитическая активность титаноксидного материала по сравнению с материалом, состоящим только из одной кристаллической фазы [3].
Известно, что фазовое превращение анатаз в рутил существенно зависит от условий синтеза, чистоты исходных компонентов и сопутствующих примесей, а также типа подложки в случае синтеза пленки TiO 2 [4, 5]. Однако различные примеси могут сыграть как отрицательную, так и положительную роль. Хорошо известно, что свойства фотокатализатора диоксида титана могут быть изменены путем введения небольших количеств примесей в его структуру [6, 7].
Все металлы или их оксиды по степени влияния на фазовый переход анатаз – рутил можно условно разделить на две группы: рутилирующие и, в противоположность им, ингибирующие фазовый переход анатаз-рутил . Так, трансформация анатаза в рутил ускорялась при содержании Nb, Cr, Si и Fe в TiO 2 . Установлено, что 1,0 мол. % NiO, CoO, MnO 2 , Fe 2 O 3 или CuO способствует превращению анатаза в рутил и росту зерен TiO 2 . Фазовая трансформация анатаза в рутил ускорялась также в зависимости от содержания хрома (> 10 ммоль %), железа, кремния и особенно смеси ниобия и хрома [8].
Оксид хрома один из хромофорных легирующих добавок к керамическому пигменту ТiO 2 , которые используются для улучшения его фотокаталитических характеристик [9, 10]. Поскольку ионный радиус Cr3+ (0,755 нм) немного больше, чем у Ti4+ (0,745 нм), ионы Cr3+ могут быть легко включены в решетку TiO2 и такое легирование не оказывает заметного влияния на кристаллические размеры анатаза и рутила [11]. Диоксид титана с оксидом хрома может образовывать твер-
Неорганическая химия дые растворы до 5 масс. % [12, 13], хотя в [6] сообщалось, что растворимость хрома в TiO2 возрастает с увеличением давления синтеза. TiO2 способен вмещать до 15,3 масс. % Cr2O3 при 3 GPa и 1300 ºC по сравнению с 5,7 масс. % при атмосферном давлении при той же температуре.
Легирование Cr3+ может эффективно способствовать образованию рутила и одновременно сдерживать образование анатаза, а также для регулирования отношения анатаза к рутилу [11].
Однако повышение соотношения титан – хром до 1:10 приводит к стабилизации анатазной модификации, как сообщают авторы, путем включения ионов Cr3+ в решетку ТiO2, что подтверждается уменьшением размеров кристаллитов. Такая стабилизация формы анатаза значима с точки зрения катализа, так как известно, что анатазная модификация каталитически более активна, чем рутильная [14].
Как и оксид хрома, оксид никеля усиливает кристаллографическую перегруппировку в TiO 2 и способствует понижению температуры фазового перехода анатаз – рутил [9 , 15, 16] .
Несмотря на большой объем информации, посвященной легированию диоксида титана различными металлами и их влиянию на фазовый переход, встречается много противоречий о влиянии тех или иных добавок. Чаще всего сравнивать данную информацию сложно из-за различных методов синтеза диоксида титана, в одних работах это керамический способ получения, в других золь-гель синтез и т. д. [8, 17–19].
Целью данной работы является исследование влияния ионов хрома и никеля на фазовый переход анатаз – рутил, а также изучение влияния предыстории получения исходных оксидов TiO 2 , NiO и Cr 2 O 3 на этот фазовый переход.
Экспериментальная часть
Для проведения исследования в качестве исходных препаратов брали диоксид титана анатазной и рутильной модификации, Cr 2 O 3 , NiCO 3 и NiNO 3 ⋅ 6H 2 O марки ч. д. а.
Оксид титана (IV), анатазной модификации получали двумя способами:
-
1. Синтез 1 : прокаливанием гидролизного оксида титана (ГДТ) при 600 °С в течение 2 часов. В свою очередь, ГДТ получали термическим гидролизом растворов сульфатных соединений Ti (IV). Гидролиз проводили в присутствии анатазных зародышей, которые являлись центрами образования первичных частиц ГДТ в процессе его гидролиза;
-
2. Синтез 2 : путем гидролиза TiCl 4 , детально описанным в [20];
Рутильную модификацию TiO2 получали путем прокаливания анатазной модификации при 1000 °С в течение 3 часов.
Химический анализ диоксида титана на примеси проводили на спектрометре PGS 2. Результаты анализа оксида титана представлены в табл. 1.
Таблица 1
Химический состав оксида титана, синтезированного из ГДТ и TiCl 4
|
Способ получения TiO2 (анатаз) |
Анализируемые элементы, масс. % |
||||||
|
As |
Bi |
Cu |
Pb |
Sb |
Sn |
Fe* |
|
|
ГДТ |
0,0057 |
0,0002 |
0,00023 |
0,0001 |
0,0005 |
0,0003 |
0,057 |
|
TiCl 4 |
0,0043 |
0,0002 |
0,00013 |
0,0001 |
0,0005 |
0,0002 |
0,011 |
* – данный показатель контролировался атомно-эмиссионным методом на ARL 3410.
Оксид никеля получали термолизом основного карбоната и 6-водного нитрата никеля. Выбор основного карбоната и нитрата в качестве прекурсора оксида никеля был основан на примерно одинаковой температуре разложения этих солей (t разл ~380 °C) и однородности распределения размеров частиц при термолизе соли. Синтез оксида никеля из нитрата и основного карбоната никеля проводили при 800 °С в течение 3 ч.
Чистоту веществ контролировали на спектрометре PGS 2 и рентгеноспектральном анализаторе СРМ 25. Результаты анализа оксида никеля представлены в табл. 2.
Исходные механические смеси соответствующих оксидов готовили тщательным перемешиванием предварительно синтезированного оксида титана (IV) и оксида хрома (III) или оксида ни- келя в агатовой ступке до получения порошков однородного цвета, которые затем исследовали различными физико-химическими методами.
Таблица 2
Химический состав оксида никеля, синтезированного из основного карбоната и нитрата никеля
|
Способ получения NiO |
Анализируемые элементы, масс. % |
|||||
|
As |
Bi |
Cd |
Co* |
Cu* |
P |
|
|
NiCO 3 |
0,000229 |
0,000165 |
0,000323 |
0,0167 |
0,00786 |
0,000765 |
|
NiNO 3 ⋅ 6H 2 O |
0,000300 |
0,000062 |
0,000474 |
0,0234 |
0,00451 |
0,000895 |
|
Анализируемые элементы, масс. % |
||||||
|
Sb |
Sn |
Zn |
Fe* |
Mg |
Si |
|
|
NiCO 3 |
0,00016 |
0,000085 |
0,000273 |
0,00062 |
0,00079 |
0,00752 |
|
NiNO 3 ⋅ 6H 2 O |
0,00018 |
0,000068 |
0,00161 |
0,00213 |
0,00203 |
0,01980 |
* – данные показатели контролировались на PGS-2 и СРМ-25.
Смеси оксидов системы TiO 2 – Cr 2 O 3 с содержанием 5 масс. % прокаливали в фарфоровых тиглях в интервале температур 600–1200 °С в течение 1–2 часов.
Для системы TiO2 – NiO было приготовлено 4 смеси:
Cмесь I : 95 масс. % TiO 2 (синтез 1) – NiO (5 масс. %), полученный из Ni(NO 3 ) 2 ,
Cмесь II : 95 масс. % TiO 2 (синтез 1) NiO (5 масс. %), синтезированный из основного карбоната.
Смесь III: 95 масс. % TiO 2 (синтез 2) –NiO (5 масс. %), полученный из Ni(NO 3 ) 2 ,
Cмесь IV : 95 масс. % TiO 2 (синтез 2) NiO (5 масс. %), синтезированный из основного карбоната.
Прокаливание вели аналогично смеси TiO 2 и Cr 2 O 3 .
Фазовый состав и средний размер кристалликов ( d ), рассчитанный из микроскопических данных и по ширине рентгеновских дифракционных максимумов, составлял для NiO d ≈ 20 нм; для α-Cr2О3 d ≈ 70 нм; для TiO2 анатазной и рутильной модификаций d ≈ 20 нм и d ≈ 60 нм соответственно.
Химический анализ исходных смесей проводили на атомно-эмиссионном спектрометре ARL 3410, рентгеноспектральном анализаторе СРМ 25 и спектрометре PGS 2 по стандартным методикам. Количественный и качественный фазовый анализ образцов проводили на дифрактро-метре ДРОН–3М с Kα-излучением меди. Спектры-ИК исследуемых образцов регистрировали на ИК-спектрометре TENSOR фирмы Bruker в области волновых чисел 400–4000 см–1. Термический анализ (ТГ-ДСК) проводили на термоанализаторе Netzch 449С Jupiter со скоростью нагрева 10 °C/мин до 1100 ºC в корундовых тиглях в токе аргона.
Обсуждение результатов
На рис. 1–3 представлены термоаналитические кривые анатаза, полученного из различных предшественников.
Как видно из рис. 1, относительное изменение массы ГДТ в интервале температур 20– 1100 °С составляет 21,0 %. На кривой ДСК фиксируются два широких эндоэффекта с максимумами при 150 и 625 °С, сопровождающиеся уменьшением массы, причем тепловым эффектам соответствует потеря массы с максимальной скоростью, согласно данным дифференциальной термогравиметрии, при 137 и 620 °С. На кривой ДСК также имеется экзоэффект при 950 °С.
Первый из эндоэффектов обусловлен процессом дегидратации, а второй – процессом разложения сульфат-ионов. Экзоэффект при 950 °С, обусловлен переходом анатаза в рутил.
Согласно данным термического анализа анатаза, полученного из ГДТ, в интервале температур 32–200 °С фиксируется небольшой эндоэффект, который обусловлен удалением воды (рис. 2). Изменение массы в указанном температурном интервале составляет 1,00 %.
Неорганическая химия
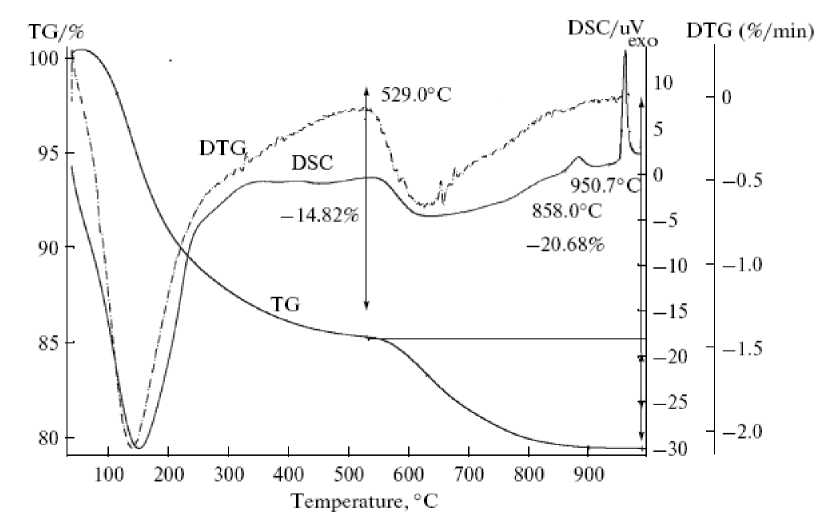
Рис. 1. Результаты термического анализа образца ГДТ
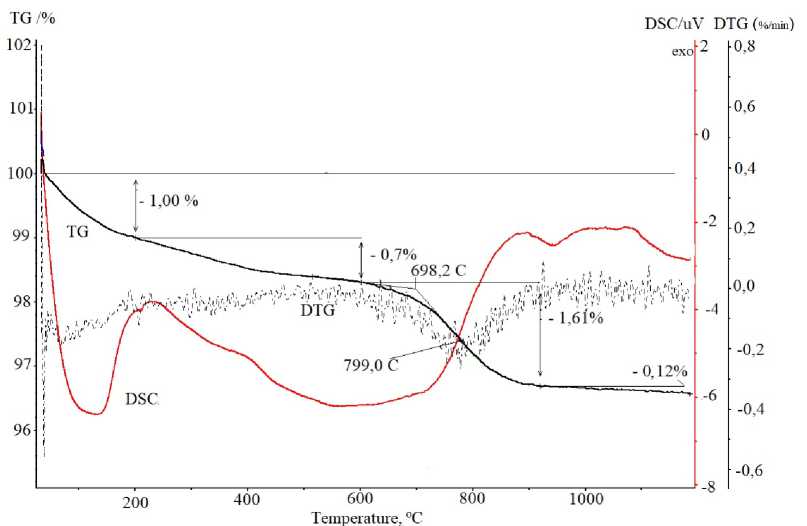
Рис. 2. Результаты термического анализа образца анатаза, полученного из ГДТ
В интервале температур 200–600 °C не наблюдаются каких-либо эндо- или экзоэффектов. Потеря массы в указанном температурном интервале составляет 0,70 %. Активная десульфатиза-ция образцов начинается при температуре порядка 700–710 °С и достигает максимальной скорости при 780 °С. Слабый экзоэффект при температуре ≈850 ºC может быть отнесен к началу полиморфного превращения анатаза в рутил.
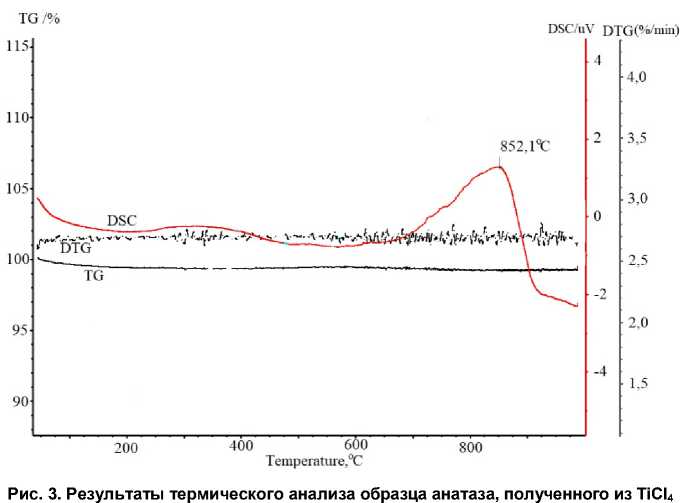
Для анатаза, полученного термолизом TiCl 4 (рис. 3), каких-либо экзоэффектов, связанных с десорбцией, не обнаружено. Экзоэффект в области 852 ºC, по-видимому, связан с началом фазового перехода анатаз – рутил.
Согласно данным рентгенофазового анализа, фазовый переход для чистых оксидов титана различен и зависит от предыстории их получения. Так, для TiO 2 (ГДТ) фазовый переход начинается при температуре 850 °C и заканчивается при 950 и 900 ºC в течение 1 часа и 3 часов, тогда как фазовый переход анатаз – рутил TiO 2 (TiCl 4 ) заканчивается при температуре на 100 °C выше (рис. 4).
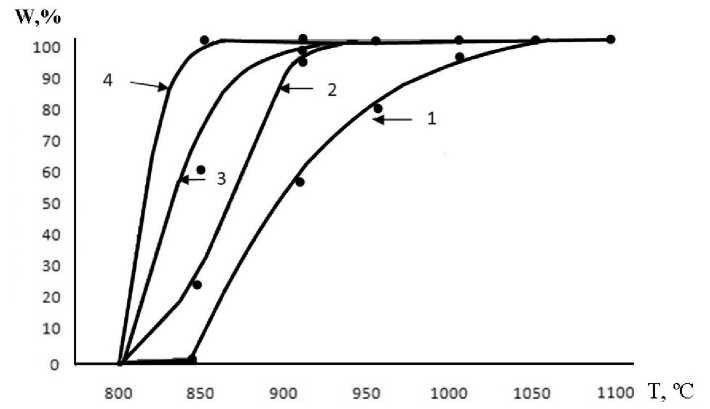
Рис. 4. Массовая доля рутила, образующегося при изотермической выдержке из исходных оксидов:
1 – TiO 2 (синтез 2) после 1 ч прокаливания; 2 – TiO 2 (синтез 1) после 1 ч прокаливания;
3 – TiO 2 (синтез 2) после 3 ч прокаливания; 4 – TiO 2 (синтез 1) после 3 ч прокаливания
Проведенные исследования полученных смесей показывают, что термоаналитические кривые смесей I–IV для системы TiO2 – NiO и соответствующего чистого анатаза практически идентичны. Разница заключается в эндоэффектах в температурном интервале 200 – 400 °C, связанных с разложением нитрата, либо основного карбоната никеля. На рис. 5 для примера приведены термоаналитические кривые для смеси II.
На термоаналитических кривых образца, содержащего 5 масс. % Cr 2 O 3 и 95 масс. % TiO 2 (рис. 6), экзоэффект, соответствующий фазовому переходу анатаз – рутил, осуществляется в широком температурном интервале, а зародыши рутила образуются при более низких температурах, чем в чистом анатазе.
Неорганическая химия
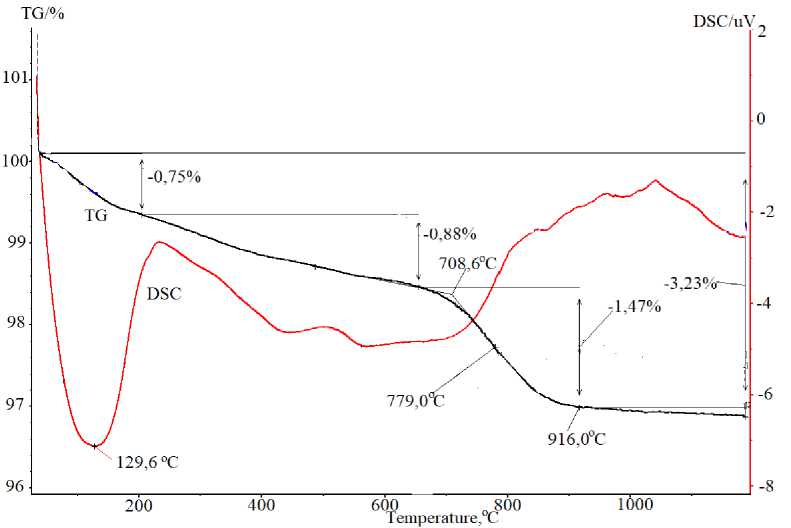
Рис. 5. Результаты термического анализа смеси 95 масс. % TiO 2 – 5 масс. % NiO (смесь II)
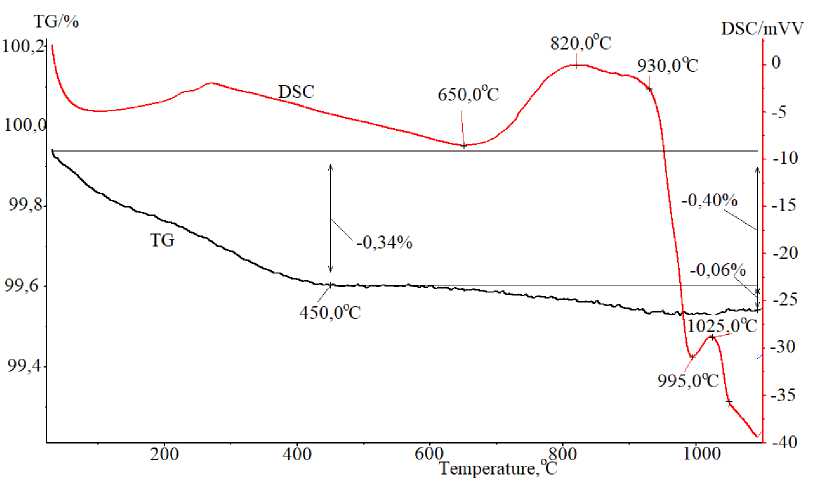
Рис. 6. Результаты термического анализа смеси 95 масс. % TiO 2 – 5 масс. % Cr 2 O 3
Исследование ИК-спект р о в исх о дны х и про кал енных обр аз цо в в интервале волновых чисел 400 – 4000 см–1 , п ред с т а в ле н н ы х н а рис. 7, показало, что в ИК-спектре исходного TiO2 присутствуют п ол ос ы п о гло щ е н и я с в о лн ов ыми чи с ла ми 5 50, 1 630 с м –1, которые соответствуют колебаниям связей Ti-O-Ti и Ti-OH-Ti.
Исследуя ИК- сп е к тры, м ожно сделать вывод, что после прокаливания м е х а н и че с к а я с месь TiO2–NiO име ют п одоб ные ИК -спектры, вид которых сохраняется вне зависимости от способа получения оксида никеля , и с п ол ьз ов а н н ого д л я и х п ри готов ле н и я.
В спектре Cr 2 O 3 ре гис трир уются полосы в области волновых чисел 65 0 (к о ле б а н и я Cr-O) и 2400 (колебания ОН–- г рупп ) с м–1 (рис. 8). Однако при совместном прокаливании оксидов почти п ол н ос тью и с че за е т п оло с а п ог лощ е н и я с волновым числом 2400 см–1, что указывает на участие связи Ме–ОН– в о в за и мод е й с тв и и .
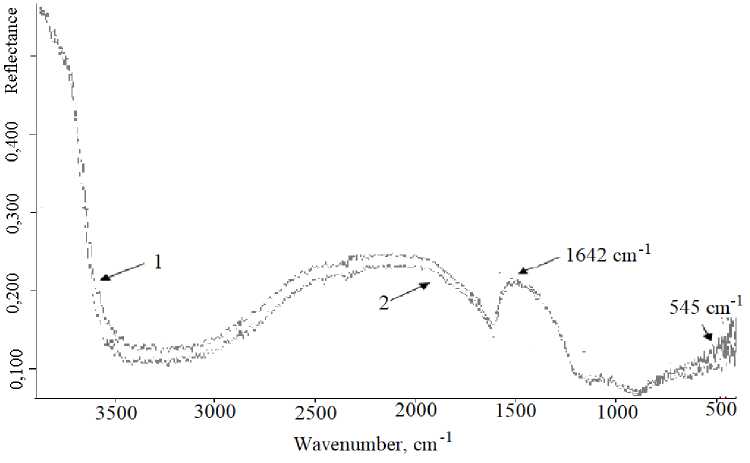
Рис. 7. ИК-спектры: 1 – исходного TiO 2 (синтез 1);
2 – механической смеси 95 масс. % TiO 2 (синтез 1) – 5 масс. % NiO
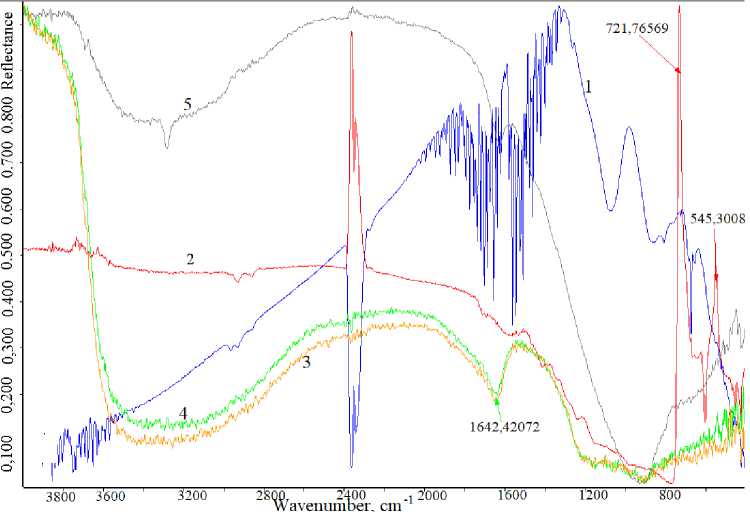
Рис. 8. ИК-спектры образцов TiO 2 и Cr 2 O 3 :
1 – фон; 2 – Cr 2 O 3 ,; 3 – TiO 2 (синтез 1); 4 – механическая смесь 95 масс. % TiO 2 (синтез 1) – 5 масс. % Cr 2 O 3 ,;
5 – смесь 95 масс. % TiO 2 (синтез 1) – 5 масс. % Cr 2 O 3 после прокаливания при 850 °С
Анатаз и механическая смесь TiO 2 –Cr 2 O 3 имеют подобные ИК-спектры, вид которых сохраняется до температуры 500 ºС. При прокаливании смеси TiO2–Cr2O3 в интервале температур от 600 до 850 ºС появляется линия с волновым числом 3568 см–, интенсивность которой с увеличением температуры прокаливания возрастает почти на два порядка. При дальнейшей термообработке интенсивность линии 3568 см–1 резко уменьшается и становится мало заметной для образца, прокаленного при 1000 ºС , спектр которого подобен ИК-спектру рутила.
В ходе экспериментов установили, что Cr 2 O 3 не образует твердые растворы с анатазом, независимо от способа его получения, до тех пор, пока не произойдет полиморфное превращение анатаза в рутил.
Неорганическая химия
Методом ренгенофазового анализа установили, что на начальных стадиях процесса с добавлением и без добавления NiO и Cr2O3 идут процессы формирования кристалликов анатаза и их рост. Интенсивное растворение оксида хрома и формирование титаната никеля начинается только при появлении рутильной фазы.
Следует отметить, что добавки оксида хрома и оксида никеля существенно влияют на временной и температурный интервал фазового перехода анатаза в рутил.
Для примера на рис. 9–10 приведены зависимости степени превращения анатаз–рутил для чистого оксида TiO2 (синтез 1) и для смесей диоксида титана с оксидом хрома или оксидами никеля.
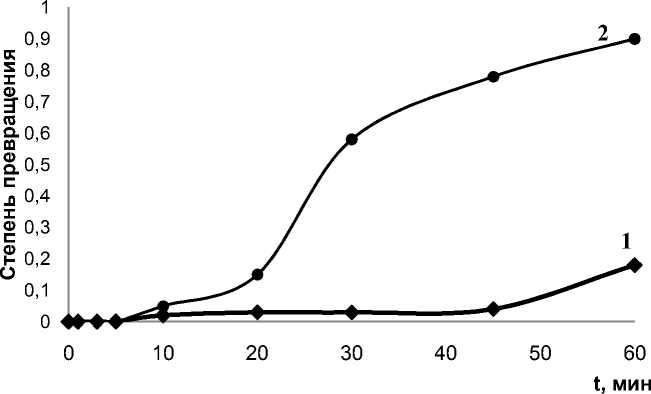
Рис. 9. Фазовый переход анатаза в рутил при изотермической выдержке 850 °C: 1 – TiO 2 (рутил) без добавки Cr 2 O 3 ; 2 – TiO 2 (рутил) c добавкой Cr 2 O 3
Появление рутильной фазы в чистом анатазе, полученном при синтезе 1, наблюдается на 40-й минуте прокаливания при температуре 850 °C, а с добавками Cr 2 O 3 формирование рутильной фазы наблюдали на 20 минут раньше при той же температуре (рис. 9) и на 10 мин раньше при 900 °С.
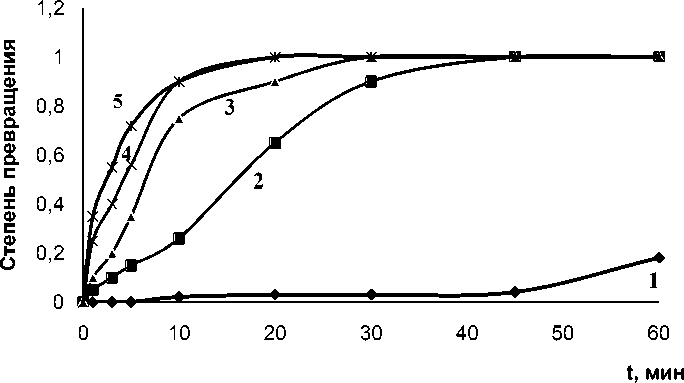
Рис. 10. Фазовый переход анатаза в рутил при изотермической выдержке 850 °C: 1 – TiO 2 (рутил) без добавки NiO; 2 – смесь II; 3 – смесь I; 4 – смесь IV; 5 – смесь III
При добавках оксида никеля рутилирующий эффект более заметен. Так при температуре 850 °С (рис. 10) формирование рутильной фазы наблюдали на 40 минут раньше. Кроме того, в случае добавок NiO температурный и временной сдвиг фазового превращения анатаз-рутил су- щественно зависит от предистории синтеза оксида никеля. Так для NiO, полученного из нитрата никеля, рутильная фаза появляется раньше, чем с NiO, синтезированного из основного карбоната. Самое эффективное снижение наблюдается для смеси III.
Таким образом, оксид никеля и оксид хрома являются добавками, стимулирующими образование рутильной фазы, причем ионы никеля понижают начальную температуру эффективнее и оказывают более сильный рутилирующий эффект, чем ионы хрома.
Заключение
Методами рентгенофазового и термического (ТГ–ДСК) анализов исследовано влияние NiO и Cr 2 O 3 на фазовый переход анатаза в рутил.
Оксиды никеля и хрома являются рутилирующими добавками и уменьшают температуру фазового перехода анатаза в рутил. Причем оксид никеля эффективнее снижает начальную температуру фазообразования и оказывает более сильный рутилирующий эффект, чем оксид хрома.
Температура полиморфного превращения зависит от предыстории получения как оксида никеля (II), так и оксида титана (IV). Титанат никеля NiTiO 3 в температурном интервале 700–850 °C образуется только из анатаза, при этом анатаз полностью переходит в рутил.
Твердый раствор Cr 2 O 3 в TiO 2 образуется только на основе рутильной модификации.
Список литературы Влияние оксидов 3d-элементов на фазовое превращение анатаз - рутил
- Викторов, В.В. Фазовые превращения в системе TiO2 -NiO/В.В. Викторов, Е.А. Белая, А.С. Сериков//Неорганические материалы. -2012.-Т. 48, № 5. -С. 570-575.
- Шабанова, Н.А. Химия и технология нанодисперсных оксидов/Н.А. Шабанова, В.В. Попов, П.Д. Саркисов. -М.: ИКЦ «Академкнига», 2006. -309 с.
- Артемьев, Ю.М. Введение в гетерогенный фотокатализ/Ю.М. Артемьев, В.К. Рябчук.-СПб.: Изд-во С.-Петерб. ун-та, 1999. -340 с.
- Термически стимулированные превращения дисперсного диоксида титана/А.С. Чернов, Ю.М. Коштял, А.А. Малков и др.//Изв. Санкт-Петербургского государственного технологического института. -2012. -№ 15. -С. 47-50.
- Miszczak, S. Anatase-rutile transformation of TiO2 sol-gel coat-ings deposited on different substrates/S. Miszczak, В. Pietrzyk//Ceram. International. -2015. -V. 41. -Р. 7461-7465.
- Escudero, А. Chromium incorporation into TiO2 at high pressure/А. Escudero, F. Langenhorst//Journal of Solid State Chemistry. -2012. -V. 190. -P. 61-67.
- Enhancement of photocatalytic properties of Cr2O3-TiO2 mixed oxides prepared by sol-gel method/J. Young-Soo, K. Kyung-Hwa, J. Tae-Young//Current Applied Physics. -2011. -V.11. -P. 358-361 DOI: 10.1016/j.cap.2010.08.001
- Karvinen, S. The effects of trace elements on the crystal properties of TiO2/S. Karvinen//Solid State Sciences. -2003. -V. 5 -P. 811-819.
- The role of counterions (Mo, Nb, Sb, W) in Cr-, Mn-, Ni-and V-doped rutile ceramic pigments. Part 1. Crystal structure and phase transformations/F. Matteucci, G. Cruciani, M. Dondi//Ceram. International. -2006. -V. 32. -P. 385-392 DOI: 10.1016/j.ceramint.2005.03.014
- An aqueous sol-gel synthesis of chromium (III) doped mesoporous titanium dioxide for visible light photocatalysis./B. Kanakkanmavudi, S. Ghosh, S. Sankar.//Material Research Bulletin. -2011. -V. 46. -P. 914-921 DOI: 10.1016/j.materresbull.2011.02.030
- Baozhu, T. One-step preparation, characterization and visible-light photocatalytic activity of Cr-doped TiO2 with anatase and rutile bicrystalline phases/T. Baozhu, L. Chunzhong, Z. Jinlong. Journal of Chemistry Engineering. -2012.-V. 191. -P. 402-409.
- Florke, O.W. Andersson Phasen, dichteste Packing und Wadsley Defekte im System Ti-Cr-О./O.W. Florke, C.W. Lee//Journal Solid State Chem. -1970. -V. l, № 3-4. -P. 445-453.
- Бережной, А.С. Многокомпонентные системы оксидов/А.С. Бережной. -Киев: Наукова думка, 1970. -544 c.
- Khaleel, A. Structural and textural characterization of sol-gel prepared nanoscale titanium-chromium mixed oxides/A. Khaleel, I. Shehadi, A. Mariam//Journal of Non-Crystalline Solids.-2010. -V. 356.-P. 1282-1287 DOI: 10.1016/j.jnoncrysol.2010.04.031
- Riyas, S. Rutilation in nickel oxide-doped titania prepared by different methods/S. Riyas, G. Krishnan, Das P.N. Mohan//Ceram. International. -2006. -V. 32. -P. 593-598 DOI: 10.1016/j.ceramint.2005.04.016
- Young, Ku. Characterization of coupled NiO/TiO2 photocatalyst for the photocatalytic reduction of Cr (VI) in aqueous solution/Ku Young, Lin Chia-Nan, Hou Wei-Ming//Journal of Molecular Catalysis A: Chemical. -2011. -V. 349. -Р. 20-27 DOI: 10.1016/j.molcata.2011.08.006
- Study of the TiO2-Cr2O3 system for photoelectrolytic decomposition of water/M. Radecka, K. Zakrzewska, M. Wierzbicka//Solid State Ionics. -2003. -V. 157. -P. 379-386 DOI: 10.1016/S0167-2738(02)00236-9
- Sol-gel route to synthesize titania-silica nano precursors for photoactive particulates and coatings/V.S. Smitha, K.A. Manjumol, K.V. Baiju//Journal of sol-gel Science and Technology. -2010. -V. 5. -P. 203-211 DOI: 10.1007/s10971-010-2178-9
- Control of micropore size in supermicroporous titania-chromia system TiO2-Cr2O3/W. Delouis, M. Sanchez, B. Shpeizer//Inorganic Chemistry Communications. -2006. -V. 9. -P. 1136-1140 DOI: 10.1016/j.inoche.2006.07.031
- Пат. 2049066 Российская Федерация, C01G23/04; С1. Способ получения гидроксида титана/Э.Е. Мовсесов, Л.П. Седова, Т.Н. Гришина и др.; заявитель и патентообладатель АО «Соликамский магниевый завод». -№ 92006375/26; заявл. 16.11.92; опубл. 27.11.95, Бюл. № 7. -4 с.


