Влияние октиламина на окислительно-восстановительные процессы при экстракции кобальта бис(2,4,4-триметилпентил) дитиофосфиновой кислотой
Автор: Григорьева Н.А., Флейтлих И.Ю., Пашков Г.Л., Никифорова Л.К.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 5 т.7, 2014 года.
Бесплатный доступ
Изучены окислительно-восстановительные процессы, протекающие в органической фазе при экстракции кобальта смесями бис(2,4,4-триметилпентил)дитиофосфиновой кислоты (HR) и октиламина (ОА). Показано, что восстановление дитиофосфината кобальта (III) до дитиофосфината кобальта (II) в присутствии ОА идёт очень быстро: за 10 мин кобальт восстанавливается на 94 %, тогда как в других изученных системах (СоR3 и СоR3+ триоктиламин) за этот период восстановления Со (III) практически не наблюдалось ( HR >> HR+ триалкиламин.
Жидкостная экстракция, кобальт, бис(2, 4-триметилпентил) дитиофосфиновая кислота, октиламин, окислительно-восстановительный процесс
Короткий адрес: https://sciup.org/146114872
IDR: 146114872 | УДК: 542.61:546.742
Octyl amine influence on redox processes during cobalt extraction with bis(2,4,4-trimethylpentyl)dithiophosphinic acid
The redox processes proceeding in the organic phase at cobalt extraction with mixtures bis(2,4,4trimethylpentyl)dithiophosphinic acid (HR, trade mark CYANEX 301) and octyl amine (ОА) are studied. It is shown, that reduction of Co (III) dithiophosphinate to Co (II) dithiophosphinate in the presence of ОА proceeds very quickly: for 10 minutes cobalt reduces on 94 %, whereas in other systems (СоR3 and СоR3 + trioctyl amine, ТОА) for this period cobalt reduction practically was not observed).
Текст научной статьи Влияние октиламина на окислительно-восстановительные процессы при экстракции кобальта бис(2,4,4-триметилпентил) дитиофосфиновой кислотой
В последнее время большой интерес для гидрометаллургии кобальта представляет экстрагент цианекс 301, активным компонентом которого является бис(2,4,4-триметилпентил) дитиофосфиновая кислота [1]. Кобальт совместно с никелем эффективно извлекается этим экстрагентом при переработке растворов выщелачивания окисленных никелевых руд [2], возможно разделение кобальта и никеля с цианексом 301, основанное на кинетических свойствах системы [3]. Сообщается о выделении кобальта из ацетатных [4] и сернокислых растворов и отделении его от марганца [5].
Ранее нами было показано [6], что в инертных растворителях Со(II) быстро (≤2 мин) извлекается цианексом 301 в органическую фазу с образованием комплекса CoR2 тетраэдрической конфигурации. В открытых системах кобальт медленно окисляется кислородом воздуха до Co(III) с образованием комплекса CoR3 октаэдрической конфигурации. Образующийся дитиофосфинат Co(III) в дальнейшем диспропорционирует на дитиофосфинат Co(II) и дисульфид дитиофосфиновой кислоты. В отличие от комплексов Со (II) комплексы Со (III) очень инертны, и реэкстрагировать кобальт из органической фазы растворами минеральных кислот без полного разложения экстрагента практически невозможно. Одним из способов предотвращения окисления кобальта в органической фазе с дитиофосфиновой кислотой мо
Дальнейшие исследования в этом направлении представляют значительный научный и практический интерес, так как введение электронно-донорных добавок в органическую фазу может привести к изменению состояния экстрагируемых соединений кобальта и, соответственно, экстракционных характеристик.
В настоящей статье приведены результаты исследований по изучению Red-Ox-процессов, протекающих при экстракции кобальта из сернокислых растворов бис(2,4,4-триметилпентил) дитиофосфиновой кислотой в присутствии первичного амина – октиламина, а также изучению экстракции кобальта в этой системе.
Экспериментальная часть
В работе использовали бис(2,4,4-триметилпентил)дитиофосфиновую кислоту, очищенную по методике [8]. Очищенный продукт содержал 98 % основного вещества. Дисульфид бис(2,4,4-триметилпентил)дитиофосфиновой кислоты, R2P(S)-S-S-(S)PR2, (R-R) получали по методике [9]. В качестве электронно-донорных добавок (ЭДД, L) использовали: триоктиламин (ТОА), триалкиламин фракции С7-С9 (ТАА) и октиламин (ОА).
Методика проведения экспериментов по экстракции кобальта и по изучению Red-Ox-процессов в органических растворах приведена в [10].
Определение кобальта проводили в водной фазе (рафинатах) атомно-абсорбционным методом, общее содержание кобальта в органической фазе определяли по разности между его исходным и конечным содержанием в водном растворе после экстракции. Кроме того, концентрацию Co (III) в экстрактах устанавливали спектрофотометрически, по величине оптической плотности (λ =455 нм; l = 1 см), в этом случае концентрацию Со(II) находили по разности между общей концентрацией кобальта и Co (III).
Результаты и обсуждение
Одним из самых труднопротекаемых Red-Ox-процессов при экстракции кобальта является процесс восстановления кобальта (III) до кобальта (II). Уравнение обратимой Red-Ox-реакции записывается следующем виде:
2СоR3 ^ 2СоR2 + R-R. (1)
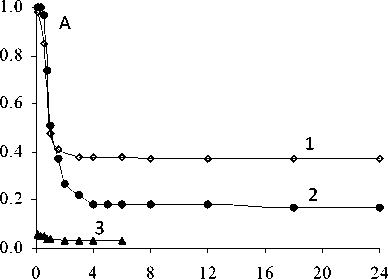
В нормальных условиях эта реакция характеризуется крайне низкой скоростью, однако при повышении температуры ее скорость значительно возрастает – содержание кобальта (III) в экстракте уменьшается (рис. 1, кр. 1). (По оси ординат отложены значения оптической плотности при λ = 455 нм, которые прямо пропорциональны концентрациям окисленного кобальта.)
Можно предположить, что восстановление кобальта в дитиофосфинате Со(III) происходит за счёт разрыва связи металл – сера в комплексе, с последующим образованием дисульфида. При этом лимитирующей стадией процесса является первая стадия.
Время, ч
Рис. 1. Влияние электронно-донорных добавок на восстановление СоR 3 в толуоле. Состав экстрактов: концентрация кобальта-СоR 3 (исх) = 0,0005 М; концентрация добавок – 0,1 М; 1.СоR 3 ; 2. СоR 3 + ТОА; 3.
СоR 3 + ОА Т0С: 1-60; 2,3 – 50
Введение в экстракт, содержащий дитиофосфинат Со(III), ТОА практически не влияет на начальную скорость реакции восстановления (рис. 1, кр. 2). Однако в системе с ТОА восстановление кобальта во времени проходит гораздо глубже, чем в отсутствие добавки (кр. 1 и 2). По-видимому, при восстановлении кобальта в системах СоR 3 с ТОА, как и с индивидуальным дитиофосфинатом Со(III), медленной стадией является разрыв связи между ионом металла и серой. В дальнейшем образовавшееся соединение Со (II), вероятно, быстро координирует дополнительные лиганды (ТОА) с образованием смешанного комплекса. Ранее образование смешанно-лигандных комплексов дитиофосфината кобальта (II) с ТОА показано в [7]. Суммарное уравнение обратимой Red-Ox-реакции в присутствии добавок можно записать в следующем виде:
2СоR 3 + nL ↔ 2 [СоR 2 • nL] + R-R, (2) где L – ТОА или ОА; n = 1,2.
В отличие от предыдущих систем введение в кобальтовые экстракты октиламина (рис. 1, кр. 3) приводит к очень быстрому восстановлению кобальта: за 10 мин кобальт восстанавливался на 94 %, тогда как в других изученных системах (СоR 3 и СоR 3 + ТОА) за этот период восстановления Со практически не наблюдалось (< 2 %). Причём окраска экстрактов в смеси с ОА заметно изменялась во времени – от коричневого (СоR 3 ) до голубого (по-видимому, смешаннолигандного комплекса [СоR2•nОА]). Более того, восстановление СоR3 в системе с ОА проходит достаточно интенсивно и практически необратимо уже при достаточно низких температурах, Т= 30 °С, т.е. в условиях, близких к нормальным. Выяснение точного механизма восстановления СоR 3 в присутствии электронно-донорных добавок, в том числе и с ОА, требует, очевидно, дополнительных исследований, выходящих за рамки настоящей работы.
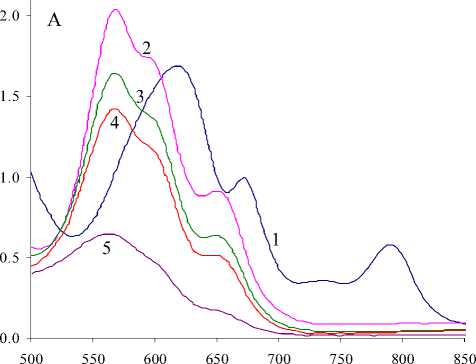
Подтверждением образования смешанных комплексов Со(II) с ОА является изменение электронных спектров поглощения экстрактов исходного комплекса CoR2 в присутствии октиламина (рис. 2).
Длина волны, нм
Рис. 2. Электронные спектры поглощения кобальтовых экстрактов с бис(2,4,4-триметилпентил) дитиофосфиновой кислотой в нонане в присутствии октиламина (ОА). Состав экстрактов: 1. СоR2 -0,02 М (I); 2. (I) + 0,1 М ОА; 3. (I) + 0,3 М ОА; 4. (I) + 0,5 М ОА; 5. (I) + 0,8 М ОА
В электронных спектрах поглощения экстрактов кобальта (II) в отсутствие добавок имеются полосы с максимумами в области 620, 675, 735 и 790 нм, относящиеся к тетраэдрической конфигурации CoR2 (рис. 2, кр. 1). Введение добавки во всех случаях приводит к появлению новых полос поглощения с максимумами в области 575, 600 и 650 нм в спектрах экстрактов и уменьшению интенсивности полос исходного тетраэдрического комплекса CoR2 (кр. 2-5). Невысокие интенсивности полос образовавшихся соединений в сравнении с исходным комплексом свидетельствуют о наличии в растворе комплексов с координационным числом (к.ч.) 5 или 6 [11]. На рисунке 2 видно, что с увеличением концентрации добавки интенсивность полос образовавщегося соединения падает, что свидетельствует о перестройке смешанного комплекса. По-видимому, в данном случае имеет место переход от тетрагонально-пирамидальной стереохимии типа СоR2•OA к комплексам октаэдрической конфигурации СоR2•2OA.
Стабилизация CoR2 октиламином препятствует окислению кобальта дисульфидом бис(2,4,4-триметилпентил)дитиофосфиновой кислоты, (R-R), присутствующем в техническом экстрагенте цианекс 301. Реакция (2) практически полностью смещена вправо в присутствии ОА. Это видно также на рис. 3. В отсутствие дисульфида заметного окисления кобальта не наблюдается (кр. 1), дисульфид заметно ускоряет окисление согласно реакции (1) (кр. 2). Октиламин существенно подавляет окисление кобальта (кривые 1 и 3 практически совпали).
Положительные результаты по стабилизации дитиофосфината кобальта ( II) октиламином позволили рассмотреть возможность использования этой добавки для экстрагента, содержащего в своём составе свободную дитиофосфиновую кислоту, поскольку, как показано было ранее [6, 10], одним из наиболее значимых факторов, влияющих на скорость окисления кобальта, является присутствие HR в органической фазе. Полученные данные оказались более чем разочаровывающими (рис. 4).
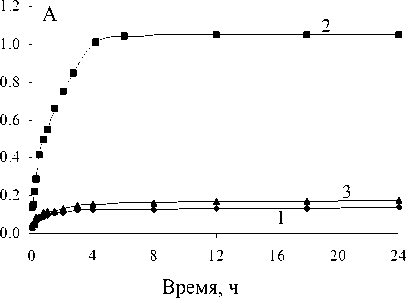
Рис. 3. Зависимость окисления CoR2 в толуоле дисульфидом в отсутствие и присутствии октиламина от времени выдержки экстрактов. Условия: 1 - 0,001 М CoR2 ; 2 - 0,0005 М CoR2 + 0,02 М R-R; 3 - 0,001 М
CoR2 + 0,02 М R-R + 0,01 М ОА
Время, ч
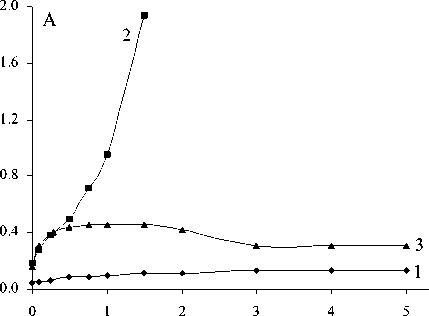
Рис. 4. Зависимость окисления CoR2 в присутствии HR и октиламина от времени выдержки экстрактов. 1. 0,001 М CoR2 в толуоле. 2. 0,001 М CoR2 + 0,2 М HR+ 0,2 М октиламина в толуоле. 3. 0,001 М CoR2 + 0,2
М HR+ 0,2 М октиламина в нонане; Т=22 °С
Из рисунка 4 видно, что как в ароматическом растворителе (толуоле, кр.2), так и в алифатическом (нонане, кр.3), наблюдалось заметное окисление кобальта. Хотя отметить, что в нонане окисление кобальта было существенно меньше, чем в толуоле. Эти данные достаточно неожиданные, поскольку ранее было показано, что в присутствии органических аминов (ТОА, ТАА) окисление кобальта в дитиофосфинате полностью предотвращается [7]. Этому можно дать следующее объяснение. Ингибирование процессов окисления Со(II) в присутствии добавок (L) обусловлено взаимодействием L с дитиофосфиновой кислотой и исходным экстрагируемым комплексом CoR2. Первое взаимодействие приводит к падению активности экстрагента и, соответственно, препятствует окислению кобальта, второе - препятствует координации кислорода воздуха (О2) к молекуле CoR2 за счёт образования смешанно-лигандных комплексов и тем самым также противодействует окислению кобальта.
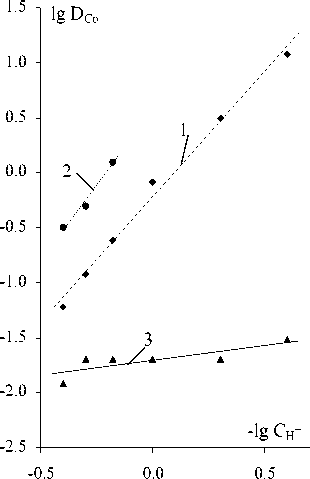
Рис.5. Зависимость экстракции кобальта 0,4 М раствором бис(2,4,4-триметилпентил)- дитиофосфиновой кислоты в нонане в присутствии добавок от кислотности водной фазы. 1 – HR без добавок; 2 – HR+ОА+15 % октанола; 3 – HR+ТАА. С L = 0,4 М; С Co в исходном растворе – 0,05 М; τ=5 мин
Судя по полученным данным, определяющим при подавлении окисления кобальта в системах HR с органическими аминами является взаимодействие этих компонентов с образованием Н-комплексов. С ОА оно менее сильное, чем с ТАА, в результате чего происходит окисление кобальта.
Это косвенно подтверждают результаты по экстракции кобальта бис(2,4,4-триметилпентил)дитиофосфиновой кислотой в присутствии ТАА и ОА (рис. 5). Из рисунка видно (кр. 2), что в присутствии ОА наблюдается улучшение экстракции кобальта (синергизм), тогда как с ТАА имеет место сильный антагонистический эффект (кр. 3). Очевидно, в смесях HR с октиламином преобладающим является взаимодействие экстрагируемого соединения (CoR2) с добавкой, тогда как в системах с ТАА определяющим при экстракции является уменьшение активности экстрагента из-за взаимодействия HR и ТАА (ТОА). Поскольку заметной экстракции кобальта из кислых растворов смесями HR и ТАА не наблюдается, его извлечение можно осуществить при повышении рН.
К сожалению, использование смесей цианекс 301 с октиламином не представляется возможным из-за образования труднорасслаивающихся эмульсий и осадков в органической фазе при содержании кобальта в экстракте ≥ 0,015 моль/л. Следует добавить, что кроме октиламина в качестве добавок рассматривались и другие первичные амины: цетиламин, Primene 81-JMT, а также п-толуидин. Эти экстрагенты в силу различных причин (окисление кобальта, образование осадков, затруднения на стадии реэкстракции) также технологически оказались малопригодны.
В настоящее время можно считать, что из рассмотренных экстракционных систем наибольший практический интерес представляют смеси HR и ТАА как с точки зрения эффектив-– 549 – ной экстракции кобальта и никеля, так и (особенно) их реэкстракции [12]. Остальные экстрагенты по разным причинам заметно уступают этой системе.


