Влияние парциального давления кислорода в брюшной полости на экспрессию фактора, индуцируемого гипоксией в эксперименте (HIF-1a)
Автор: Клюйко Д.А., Корик В.Е., Жидков С.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.16, 2021 года.
Бесплатный доступ
Обоснование: клинические проявления послеоперационных сращений брюшной полости в последнее время изучены достаточно хорошо, однако патофизиологические аспекты образования и механизмы развития адгезии до настоящего времени полностью не установлены. Целью исследования, проведенного на 35 морских свинках, явилось определение влияния газовой среды в брюшной полости и во вдыхаемом воздухе на экспрессию фактора, индуцируемого гипоксией, Результаты: на экспрессию фактора, индицируемого гипоксией (HIF-1 а), значимо влияют гипероксия, гипоксия в брюшной полости (уменьшение на 55% и увеличение на 187% от контрольной группы, соответственно), во вдыхаемом воздухе (уменьшение на 54% и увеличение на 194% от контрольной группы, соответственно), воздействие фибрина (на 245%), моделированная частичная (на 278%) и полная (на 248%) кишечная непроходимость, повышение внутрибрюшного давления (на 298%), (p
Спаечная болезнь, гипоксия, оксиметрия, иммуногистохимия
Короткий адрес: https://sciup.org/140290454
IDR: 140290454 | DOI: 10.25881/20728255_2021_16_4_51
Influence of parcial pressure of oxygen in the perychina on expression of the factor induced by hypoxia in experiment (HIF-1a)
Rationale: the clinical manifestations of postoperative abdominal fusion have recently been studied quite well, however, the pathophysiological aspects of the formation and the mechanisms of adhesion development have not yet been fully established. The aim of the study, carried out on 35 guinea pigs, was to determine the effect of the gas environment in the abdominal cavity and in the inhaled air on the expression of the factor induced by hypoxia, Results: the expression of the factor indicated by hypoxia (HIF-1 a) is significantly influenced by hyperoxia, hypoxia in the abdominal cavity (decrease by 55% and increase by 187% from the control group, respectively), in the inhaled air (decrease by 54% and increase by 194 % of the control group, respectively), the effect of fibrin (by 245%), simulated partial (by 278%) and complete (by 248%) intestinal obstruction, increased intra-abdominal pressure (by 298%), (p
Текст научной статьи Влияние парциального давления кислорода в брюшной полости на экспрессию фактора, индуцируемого гипоксией в эксперименте (HIF-1a)
Послеоперационная спаечная болезнь брюшной полости является наиболее частым отдаленным осложнением абдоминальной и тазовой хирургии. Независимо от вида или анатомической локализации в 50–95% случаях после оперативного вмешательства возникает адгезивный процесс в брюшной полости. В отличие от других послеоперационных осложнений, таких как инфицирование и несостоятельность анастомоза, последствия спайкообразования определяют пожизненный риск непроходимости кишечника и длительное, неуклонно прогрессирующее течение заболевания [1–3].
Зачастую пациенты со спаечной болезнью наблюдаются у специалистов разного профиля, в частности: гастроэнтерологов, проктологов, терапевтов, за исключением хирурга, который делал первую операцию. Поэтому абдоминальные хирурги нередко остаются в неведении о развитии данного осложнения у своих пациентов, что объясняет существенную недооценку сложившейся ситуации. Кроме того, имеет место мнение о безуспешно- сти попыток хирургического лечения спаечной болезни брюшной полости. Пациентов информируют о том, что каждое последующее вмешательство будет лишь усугублять состояние, а оперироваться нужно только в случае развития непроходимости кишечника. Вместе с тем, обратная связь и преемственность чрезвычайно важны для принятия верных хирургических решений, своевременного распознавания осложнений и надлежащего информирования пациентов [4–6].
Выраженная хроническая абдоминальная боль, дисфорические и диспепсические явления, дисфункция органов и систем значительно снижают качество жизни пациентов, повышают вероятность повторных операций и представляют собой серьезную клиническую и экономическую проблему. При наличии спаечного процесса в брюшной полости оперативные вмешательства чреваты увеличением их длительности, кровотечением и перфорацией [7–9].
Клинические проявления послеоперационных сращений брюшной полости в последнее время изучены достаточно хорошо, однако, патофизиологические аспекты

образования и механизмы развития адгезии до настоящего времени полностью не установлены [10; 11].
Исследования последних лет указывают на то, что спайкообразование — это нерегулируемый, динамический процесс репарации ткани брюшины, характеризующийся клеточным и иммунным ответом. При этом восстановление мезотелия всегда проходит стадию воспалительной реакции поврежденных тканей и гипоксии [7; 8; 11].
Некоторые доклинические и клинические исследования доказывают, что лапароскопический доступ снижает вероятность образования послеоперационных спаек, особенно в контексте адгезиолизиса. С другой стороны, кар-боксиперитонеум повышает внутрибрюшное давление, влияющее на функцию органов и систем и приводящее к химическому повреждению субклеточных структур, включая продукцию активных форм кислорода [3; 6].
Доказано, что гипоксия тканей играет ключевую роль в формировании адгезии применительно к любым локализациям. Вместе с тем, в данный момент нет количественной оценки гипоксических изменений в тканях при спаечной болезни брюшной полости. Исследование факторов роста и фактора, индуцированного гипоксией в экспериментальных условиях в зависимости от системной и местной гипоксии при спаечной болезни брюшной полости, является недостаточно изученной проблемой фундаментальной и клинической медицины.
Таким образом, идеальной стратегии профилактики и лечения спаечной болезни брюшной полости на данный момент нет.
Материал и методы
Исследование проведено на 35 животных, которым суммарно выполнено 128 измерений методом прямой оксиметрии. Всем животным выполнялось иммуногистохимическое исследование с целью определения экспрессии фактора, индуцируемого гипоксией (HIF-1а). Распределение по группам отражено в таблице 1.
Оперативные вмешательства проводили лапаротом-ным доступом в условиях операционной с соблюдением правил асептики и антисептики. Животных вводили в
Табл. 1. Распределение животных по группам
Методика изучения влияния концентрации кислорода в брюшной полости на экспрессию фактора, индуцируемого гипоксией (HIF-1a) и оксигенацию париетальной брюшины (группа — O). Лабораторному животному в условиях асептики и антисептики проводили лапароцентез по срединной линии, вводили и фиксировали одиночными швами гибкую прозрачную полихлорвиниловую трубку (внутренний диаметр 3 мм, наружный диаметр 5 мм) с коннектором. В группе O-1 лабораторным животным в брюшную полость инсуфлировали газовую смесь, содержащую 50% кислород. Газовая смесь представляла собой смесь кислорода с воздухом в соотношении 1:2. Во группе O-2 животных инсуфлировали 100% углекислый газ. В группе O-3 животным в брюшную полости инсуфлировали атмосферный воздух. Давление нагнетаемой газовой смеси в брюшной полости составляло 15 мм рт. ст. Длительность воздействия составляла 4 часа. Спустя указанный промежуток времени животные выводились из эксперимента с последующим проведением оксиметрии, иммуногистохимических и морфологических исследований тканей брюшины на расстоянии 2 см от края лапаротомной раны.
Методика изучения влияния концентрации кислорода во вдыхаемом воздухе на экспрессию фактора, индуцируемого гипоксией (HIF-1a) и оксигенацию париетальной брюшины (группа — G). В G-1 группу были включены лабораторные животные, которых помещали в гипербарическую камеру с газовой смесью содержащий 50% кислород. Газовая смесь представляла собой смесь кислорода с воздухом в соотношении 1:2. В группе G–2 животных помещали в гипербарическую камеру с газовой смесью содержащий 10% кислород. Длительность воздействия составила 8 часов со свободным доступом к воде и пище. Спустя указанный промежуток времени животные выводились из эксперимента с последующим морфологическим исследованием и оксиметрией брюшины на расстоянии 2 см от края лапаротомной раны.
Результаты и обсуждение
Анализ влияния концентрации кислорода в брюшной полости на оксигенацию париетальной брюшины и экспрессию факторов роста.
Показатели массопереноса кислорода, измеряемые в диапазонах 145–155, 30–35 мм рт. ст. и парциальное давление кислорода по результатам оксиметрии париетальной брюшины в исследуемых группах, распределились следующим образом (табл. 2).
Парциальное давление кислорода в группе (O-1) «Оксигенация брюшной полости 50% кислородной смесью» (Me = 43,79 мм рт. ст. (Ql = 37,13; Qu = 51,24), M = 44,35±2,8 мм рт. ст.). Данный показатель выше на 53%,
Табл. 2. Парциальное давление кислорода в брюшине
|
Название группы |
Ме, мм рт. ст. |
Ql, мм рт. ст. |
Qu, мм рт. ст. |
|
(O-1) Оксигенация брюшной полости 50% кислородной смесью, N = 17 |
43,79 |
37,13 |
51,24 |
|
(O-2) Оксигенация брюшной полости 5% кислородной смесью, N = 13 |
5,56 |
5,02 |
6,16 |
|
(O-3) Оксигенация брюшной полости 21% кислородной смесью, N = 30 |
27,15 |
16,40 |
32,70 |
|
(Cont) Контрольная группа, N = 30 |
28,70 |
19,90 |
34,65 |
Kruskal-Wallis test: H (3, N = 90) = 43,52469 p<0,0001
Табл. 3. Изменение индекса оксиметрии в брюшине
|
Название группы |
Ме, мм рт. ст. |
Ql, мм рт. ст. |
Qu, мм рт. ст. |
|
(O-1) Оксигенация брюшной полости 50% кислородной смесью, N = 17 |
6,75 |
6,29 |
7,71 |
|
(O-2) Оксигенация брюшной полости 5% кислородной смесью, N = 13 |
3,64 |
2,89 |
3,93 |
|
(O-3) Оксигенация брюшной полости 21% кислородной смесью, N = 30 |
5,62 |
5,30 |
6,22 |
|
(Cont) Контрольная группа, N = 30 |
6,24 |
5,09 |
6,54 |
Kruskal-Wallis test: H (3, N = 90) = 39,33136 p<0,0001

по сравнению с группой контроля (Me = 28,7 мм рт. ст. (Ql = 19,9; Qu = 34,65), M = 27,24±2,08 мм рт. ст.), Mann-Whitney U Test, U = 70,0, p = 0,00004. В группе (O-2) «Оксигенация брюшной полости 5% кислородной смесью» парциальное давление кислорода значимо изменятся до Me = 5,56 мм рт. ст. (Ql= 5,02; Qu = 6,16), M = 5,6±0,44 мм рт. ст., что ниже на 81%, чем в контрольной группе, Mann-Whitney U Test, U = 16,0, p = 0,0001. В группе (O-3) «Оксигенация брюшной полости 21% кислородной смесью» парциальное давление кислорода равно — Me = 27,15 мм рт. ст. (Ql = 16,4; Qu = 32,7), M = 25,82±2,32 мм рт. ст., что на 5% ниже, чем в контрольной группе, Mann-Whitney U Test, U = 406,0, p = 0,52.
Скорость массопереноса кислорода в интервале 145–155 мм рт. ст. у экспериментальных животных в группе (O-1) «Оксигенация брюшной полости 50% кислородной смесью» составила Me = 260,47 мм рт. ст./мин (Ql = 165,08; Qu = 276,59), M = 224,38±20,73 мм рт. ст./мин, что на 7% ниже, чем в контрольной группе Me = 243,01 мм рт. ст./мин (Ql= 210,25; Qu = 295,81), M = 252,98±9,79 мм рт. ст./мин, Mann-Whitney U Test, U = 70,0, p<0,0001. В группе (O-2) «Оксигенация брюшной полости 5% кислородной смесью» этот показатель значимо изменился до Me = 104,54 мм рт. ст./мин (Ql = 72,4; Qu = 176,64), M = 136,4±22,3 мм рт. ст./мин, увеличиваясь на 57%, по сравнению с контрольной группой, Mann-Whitney U Test, U = 51,5, p = 0,0001. В группе (O-3) «Оксигенация брюшной полости 21% кислородной смесью» скорость массопереноса равна Me = 273,67 мм рт. ст./мин (Ql = 218; Qu = 353,42), M = 285,84±14,78 мм рт. ст./мин, что ниже на 19% по сравнению с контрольной группой, Mann-Whitney U Test, U = 323, p = 0,09, таблица 3.
У экспериментальных животных в группе (O-1) «Оксигенация брюшной полости 50% кислородной смесью» индекс оксиметрии составил Me = 6,75 (Ql = 6,29; Qu = 7,71), M = 7,15±0,28, что выше на 8%, по сравнению с контрольной группой Me = 6,24 (Ql = 5,09; Qu = 6,54), M = 5,73±0,22, Mann-Whitney U Test, U = 108,5, p = 0,001. В группе (O-2) «Оксигенация брюшной полости 5% кислородной смесью» этот показатель значимо изменился до Me = 3,64 (Ql = 2,89; Qu = 3,93), M = 3,42±0,2 по сравнению с контрольной, при этом был ниже на 42%, Mann-Whitney U Test, U = 27,0, p<0,0001. В группе (O-3) «Оксигенация брюшной полости 21% кислородной смесью»
Табл. 4. Экспрессия фактора, индицируемого гипоксией (HIF-1 α ), при изменении концентрации кислорода внутри брюшной полости
Экспрессия фактора, индицируемого гипоксией (HIF-1 α ), при изменении концентрации кислорода внутри брюшной полости, значимо, p<0,001, изменялась в зависимости от концентрации кислорода, таблица 4.
Гипероксия — оксигенация брюшной полости 50% кислородной смесью, способствует уменьшению экспрессии фактора, индицируемого гипоксией (HIF-1 α ), на 55,5%. При оксигенации кислорода в концентрации 5% (гипоксия), экспрессия фактора, индицируемого гипоксией (HIF-1 α ), возрастает на 187,3%. При нормоксии — оксигенации брюшной полости 21% кислородной смесью, экспрессия HIF-1 α значимо не отличалась от таковой в контрольной группе, рисунок 1.
Выявленные изменения свидетельствует о существенной роли газовой среды для выполнения оперативного вмешательства. Применение гипоксических условий способствует развитию гипоксии мезотелия и стимулирует развитие спаечного процесса.
Анализ влияния концентрации кислорода в выдыхаемом воздухе на оксигенацию париетальной брюшины и экспрессию факторов роста.
Показатели массопереноса кислорода, измеряемые в диапазонах 145–155 мм рт. ст., 30–35 мм рт. ст. и парциальное давление кислорода по результатам оксиметрии париетальной брюшины в группах с различной концен-
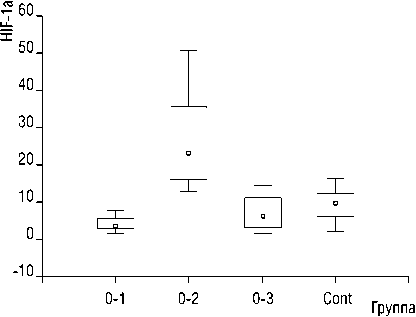
□ Median I 1 25-75% Min-Max
Рис. 1. Экспрессия фактора, индицируемого гипоксией (HIF-1 α ) в различных газовых средах.
Табл. 6. Индекс оксиметрии при различных дыхательных газовых смесях
|
Название группы |
Ме, ед |
Ql, ед |
Qu, ед |
|
(G-1) 50% кислородная смесью во вдыхаемом воздухе, N = 21 |
6,74 |
6,35 |
7,66 |
|
(G-2) 10% кислородная смесью во вдыхаемом воздухе, N = 17 |
2,58 |
0,96 |
3,69 |
|
(Cont) Контрольная группа, N = 30 |
6,24 |
5,09 |
6,54 |
Kruskal-Wallis test: H (2, N = 68) = 33,23271 p<0,0001
Табл. 5. Парциальное давление кислорода в брюшине
|
Название группы |
Ме, мм рт. ст. |
Ql, мм рт. ст. |
Qu, мм рт. ст. |
|
(G-1) 50% кислородная смесью во вдыхаемом воздухе, N = 21 |
39,83 |
34,59 |
52,70 |
|
(G-2) 10% кислородная смесью во вдыхаемом воздухе, N = 17 |
4,50 |
2,31 |
6,15 |
|
(Cont) Контрольная группа, N = 30 |
28,70 |
19,90 |
34,65 |
Kruskal-Wallis test: H (2, N = 62) = 36,83158 p<0,0001
” 50 ^45,
40,
35, 30.
25,
20, 15.
0_.
G-2
C°nt Группа
□ Median
I 1 25-75%
Min-Max
трацией кислорода во выдыхаемом воздухе, распределились следующим образом (табл. 5).
Скорость утилизации кислорода в интервале 145–155 мм рт. ст. в группе (G-1) «50% кислородная смесью во вдыхаемом воздухе» составила Me = 164,16 мм рт. ст./мин (Ql = 118,48; Qu = 257,5), M = 196,37±22,77 мм рт. ст./мин, что ниже на 32% по сравнению с контрольной группой (Me = 243,01 мм рт. ст./мин (Ql = 210,25; Qu = 295,81), M = 252,98±9,79 мм рт. ст./мин), Mann-Whitney U Test, U = 184,0, p = 0,01. В группе (G-2) «10% кислородная смесью во вдыхаемом воздухе» этот показатель значимо изменился до Me = 150,89 мм рт. ст./мин (Ql = 102,97; Qu = 167,7), M = 151,64±14,21 мм рт. ст./мин, при этом снижалась на 38%, по сравнению с контрольной группой, Mann-Whitney U Test, U = 53,0, p<0,0001. Парциальное давление кислорода в группе (G-1) «50% кислородная смесью во вдыхаемом воздухе» парциальное давление кислорода составила Me = 39,83 мм рт. ст. (Ql = 34,59; Qu = 52,7), M = 42,5±2,71 мм рт. ст, увеличиваясь на 39% по сравнению с контрольной группой Me = 28,7 мм рт. ст. (Ql = 19,9; Qu = 34,65), M = 27,24±2,08 мм рт. ст., Mann-Whitney U Test, U = 107,0, p = 0,0002 В группе (G-2) «10% кислородная смесью во вдыхаемом воздухе» этот показатель значимо изменился до Me = 4,5 мм рт. ст. (Ql = 2,31; Qu = 6,15), M = 4,76±0,66 мм рт. ст., при этом снизился на 84%, по сравнению с контрольной группой, Mann-Whitney U Test, U = 12,5 p = 0,0001, таблица 6.
Рис. 2. Экспрессия фактора, индицируемого гипоксией (HIF-1 α ) при изменении концентрации кислорода во вдыхаемом воздухе.
В группе (G-1) «50% кислородная смесью во вдыхаемом воздухе» индекс оксиметрии у экспериментальных животных составил Me = 6,74 (Ql = 6,35; Qu = 7,66), M = 6,53±0,53, что на 8% ниже по сравнению с контрольной группой Me = 6,24 (Ql = 5,09; Qu= 6,54), M = 5,73±0,22, Mann-Whitney U Test, U = 169,5, p = 0,005. В группе (G-2) «10% кислородная смесью во вдыхаемом воздухе» этот показатель значимо изменился до Me = 2,58 (Ql = 0,96; Qu = 3,69), снижаясь на 59%, M = 2,14±0,4, по сравнению с контрольной группой, Mann-Whitney U Test, U = 21,0, p<0,0001. При изменении концентрации кислорода во вдыхаемой смеси значимо изменялась экспрессия фактора, индицируемого гипоксией (HIF-1 α ), рисунок 2.
Нахождение лабораторного животного в газовой среде с 50% кислородной смесью способствует уменьшению экспрессии фактора, индицируемого гипоксией (HIF-1 α ) на 54,2%.
Иммуногистохимическая картина подтверждает представленные выводы, рисунок 3.
При гипоксии, нахождении в газовой смеси с 5% концентрацией кислорода, экспрессия фактора, индицируемого гипоксией (HIF-1 α ), возрастает на 194,2%. При нормоксии — экспрессия HIF-1 α значимо не отличалась от таковой в контрольной группе.
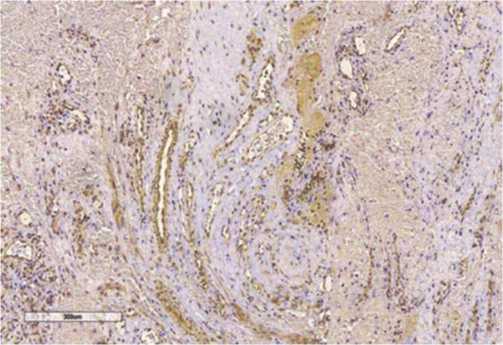
Рис. 3. Экспрессия фактора, индуцируемого гипоксией (HIF-1 α ) в группе Adhesion ileus.
Выводы
На экспрессию фактора, индицируемого гипоксией (HIF-1 α ), значимо влияют гипероксия, гипоксия в брюшной полости (уменьшение на 55% и увеличение на 187% от контрольной группы соответственно), во вдыхаемом воздухе (уменьшение на 54% и увеличение на 194% от контрольной группы соответственно), воздействие фибрина (на 245%), моделированная частичная (на 278%) и полная (на 248%) кишечная непроходимость, повышение внутрибрюшного давления (на 298%), (p<0,001), способствуя спаечному процессу.
Выявленные изменения свидетельствует о существенном влиянии гипоксии на оксигенацию органов брюшной полости. Развитие гипоксии в брюшине способствует продуцированию грубоволокнистой соединительной ткани и, как следствие, адгезивному процессу в брюшной полости. Поддержание нормоксии в послеоперационном периоде у пациентов с абдоминальной патологией важнейшая задача в лечении пациентов хирургического профиля.
Разобщение патологического каскада: ранняя активизация пациентов, купирование пареза кишечника, нормоксия или гипероксия тканей брюшины в послеоперационном периоде, является одним из приоритетных направлений лечения и профилактики спаечной болезни брюшной полости.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Влияние парциального давления кислорода в брюшной полости на экспрессию фактора, индуцируемого гипоксией в эксперименте (HIF-1a)
- Bayat Z, Guttman MP, Shiroky J, et al. Non-operative Management of Small Bowel Obstruction in Patients with No Previous Abdominal Surgery: A Systematic Review and Meta-analysis. World J Surg. 2021; 45(7): 2092-2099. doi: 10.1007/s00268-021 -06061 -z.
- Thornblade LW, Verdial FC, Bartek MA, et al. The Safety of Expectant Management for Adhesive Small Bowel Obstruction: A Systematic Review. J Gastrointest Surg. 2019; 23(4): 846-859. doi: 10.1007/s11605-018-4017-1.
- Zhao J, Samaan JS, Toubat O, et al. Laparoscopy as a Diagnostic and Therapeutic Modality for Chronic Abdominal Pain of Unknown Etiology: A Literature Review. J Surg Res. 2020; 252: 222-230. doi: 10.1016/ j.jss.2020.03.013.
- Pokharel P, Bista Y, Desar R, et al. Abdominal Cocoon Syndrome. J Nepal Health Res Counc. 2019; 17(2): 264-266. doi: 10.33314/jnhrc.v0i0.1934.
- Yang TWW, Prabhakaran S, Bell S, et al. Non-operative management for small bowel obstruction in a virgin abdomen: a systematic review. ANZ J Surg. 2020; 91(5): 802-80. doi: 10.1111/ans.16392.
- Moreno Roig E, Groot AJ, et al. HIF-1alpha and HIF-2alpha Differently Regulate the Radiation Sensitivity of NSCLC Cells. Cells. 2019; 8(1): 45. doi: 10.3390/cells8010045.
- Li Z, Zhang L, Liu X, et al. Diagnostic utility of CT for small bowel obstruction: Systematic review and meta-analysis. PLoS One. 2019; 14(12): 226740. doi: 10.1371/journal.pone.0226740.
- Carrica L, Li L, et al., Genetic inactivation of hypoxia inducible factor 1 -alpha (HIF-1 alpha) in adult hippocampal progenitors impairs neurogenesis and pattern discrimination learning. Neurobiol Learn Mem. 2019; 157: 79-85. doi: 10.1016/j.nlm.2018.12.002.
- Gerner-Rasmussen J, Donatsky AM, Bjerrum F, et al. The role of non-invasive imaging techniques in detecting intra-abdominal adhesions: a systematic review. Langenbecks Arch Surg. 2019. 404(6): 653-661. doi: 10.1007/s00423-018-1732-8.
- Ong AW, Early postoperative small bowel obstruction: A review. Am J Surg. 2020; 219(3): 535-539. doi: 10.1016/j.amjsurg.2019.11.008.
- Tong JWV, Lingam P, Shelat VG, et al. Adhesive small bowel obstruction — an update. Acute Med Surg. 2020; 7(1): 587. doi: 10.1002/ams2.587.


