Влияние патологического процесса в брюшной полости на экспрессию факторов роста
Автор: Клюйко Д.А., Корик В.Е., Жидков С.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.16, 2021 года.
Бесплатный доступ
Обоснование: спаечная болезнь брюшной полости является крайне актуальной проблемой современной хирургии по причине неуклонно возрастающей заболеваемости, высокой летальности и значительным снижением качества жизни пациентов. Целью исследования явилось изучение влияния патологического процесса в брюшной полости на экспрессию факторов роста и фактора, индуцируемого гипоксией. Результаты: Экспрессия факторов роста (GLUT-1, PDGF-AA, и -B, VEGF-C, TGF-α) и фактора, индуцируемого гипоксией (HIF-1 α), является биологическим ответом на воспаление, гипоксию, воздействие физико-химических факторов, деструкцию мезотелия брюшины и стимулирует образование кровеносных сосудов, внеклеточного матрикса, пролиферацию и деление мезенхимных клеток (фибробластов), являющихся основой спаек брюшной полости. Заключение: нивелирование гипоксии, воспаления и физико-химических факторов деструкции мезотелия брюшины позволит нормализовать экспрессию факторов роста (GLUT-1, PDGF-AA, и -B, VEGF-C, TGF-α) и фактора, индуцируемого гипоксией (HIF-1α), корректировать дифференцировку фибробластов и мезотелиоцитов, тем самым уменьшить вероятность развития и выраженность спаечного процесса у оперированных пациентов. Значимо на экспрессию фактора, индицируемого гипоксией (HIF-1 α), влияют гипероксия, гипоксия в брюшной полости (уменьшение на 55% и увеличение на 187% от контрольной группы соответственно), во вдыхаемом воздухе (уменьшение на 54% и увеличение на 194% от контрольной группы соответственно), воздействие фибрина (на 245%), моделированная частичная (на 278%) и полная (на 248%) кишечная непроходимость, повышение внутрибрюшного давления (на 298%), (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Спаечная болезнь, и -b
Короткий адрес: https://sciup.org/140261833
IDR: 140261833 | DOI: 10.25881/20728255_2021_16_4_56
Influence of the pathological process in the abdominal cavity on the expression of growth factors
Rationale: adhesive disease of the abdominal cavity is an extremely urgent problem of modern surgery, due to the steadily increasing morbidity, high mortality and a significant decrease in the quality of life of patients. The aim of the study was to study the influence of the pathological process in the abdominal cavity on the expression of growth factors and the factor induced by hypoxia. Results: expression of growth factors (GLUT-1, PDGF-AA, and -B, VEGF-C, TGF-α) and hypoxia-inducible factor (HIF-1α) is a biological response to inflammation, hypoxia, exposure to physicochemical factors , destruction of the peritoneal mesothelium and stimulates the formation of blood vessels, extracellular matrix, proliferation and division of mesenchymal cells (fibroblasts), which are the basis of abdominal adhesions. Conclusion: the leveling of hypoxia, inflammation and physicochemical factors of destruction of the peritoneal mesothelium will normalize the expression of growth factors (GLUT-1, PDGF-AA, and -B, VEGF-C, TGF-α) and hypoxia-inducible factor (HIF-1α), correct differentiation of fibroblasts and mesotheliocytes, thereby reducing the likelihood and severity of the adhesion process in operated patients. The expression of the factor indicated by hypoxia (HIF-1α) is significantly affected by hyperoxia, hypoxia in the abdominal cavity (a decrease by 55% and an increase by 187% from the control group, respectively), in the inhaled air (a decrease by 54% and an increase by 194% of the control group, respectively), the effect of fibrin (by 245%), simulated partial (by 278%) and complete (by 248%) intestinal obstruction, increased intra-abdominal pressure (by 298%), (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Влияние патологического процесса в брюшной полости на экспрессию факторов роста
Спаечная болезнь брюшной полости (СББП) является крайне актуальной проблемой современной хирургии по причине неуклонно возрастающей заболеваемости, высокой летальности и значительным снижением качества жизни пациентов [1–4].
Стремительное развитие медицинских наук, изучение заболеваний на генном и молекулярном уровнях, внедрение современных технологий в лечебно-диагностический процесс позволило значительно улучшить качество оказания хирургической помощи. Однако, достичь существенного снижения частоты заболеваемости СББП и количества ассоциированных с ней осложнений до настоящего времени так и не удалось [1; 3].
В научной литературе последних лет активно изучаются факторы роста и дифференцировки клеток и тканей различной локализации, внедряются методики стимуляции и ингибирования клеточного роста и диффе- ренцировки. Существенного развития достигли методы регулирования данных процессов в онкологии, кардиологии, нейрохирургии и других областях медицины. При этом до настоящего времени факторы роста, дифференцировки мезотелиоцитов, ингибирования фибробластов не рассматривались в контексте СББП [5–8]. Изучение влияния патологического процесса в брюшной полости на экспрессию факторов роста и фактора, индуцируемого гипоксией, явилось целью нашего исследования.
Материал и методы
Для решения поставленной цели проведен анализ медицинских карт 194 пациентов, находившихся на стационарном лечении в хирургических отделениях учреждения здравоохранения «2-я городская клиническая больница г. Минска» в период с марта 2019 по сентябрь 2020 гг. Все пациенты разделялись на группы по принципу наличия основного заболевания (Contr, Adhesion ileus, Adhesion и Vosp).

Группа контроля (Contr) сформирована для определения границ нормы исследуемых параметров и величин, разделена на 2 подгруппы «хирургические заболевания органов брюшной полости без признаков воспаления и острой кишечной непроходимости, лапаротомный доступ» (Contr Tomy, N = 24) и «хирургические заболевания органов брюшной полости без признаков воспаления и острой кишечной непроходимости, лапароскопический доступ» (Contr Scopy, N = 24). В группу включены пациенты, которым выполнялись оперативные вмешательства по поводу хронического холецистита вне обострения, грыжесечения и диагностические оперативные вмешательства.
В группу Adhesion ileus (N = 51) были включены пациенты, оперированные по поводу спаечной кишечной непроходимости. В группе Adhesion ileus оперативные вмешательства выполнялись в экстренном порядке. При наличии показаний применялась методика поэтапного лапароскопического адгезиолизиса с программируемыми релапароскопиями.
В группе Adhesion (N = 51), пациентам при наличии болевой формы СББП и безуспешности консервативного лечения выполняли лапароскопический адгезиолизис вне зависимости от длительности заболевания и предшествующих оперативных вмешательств.
С целью определения влияния на изучаемые явления воспалительного компонента сформирована группа (Vosp, N = 41). В группе анализировались результаты хирургического лечения пациентов с острыми воспалительными заболеваниями органов брюшной полости: острый холецистит, аппендицит, перитонит.
Группы были гомогенны по полу Kruskal-Wallis test: H (2, N = 194) = 0,95 p = 0,62 и возрасту Kruskal-Wallis test: H (2, N = 194) = 0,98 p = 0,61.
Влияние воспаления, гипоксии и повреждении брюшины на стимуляторы роста и дифференцировки эпителиальных (мезотелиальных) клеток и неоангиогенеза изучали на основании экспрессии следующих факторов: – облегченный глюкозный транспортер (GLUT-1
— glucose transporter), который, являясь маркером гипоксии, повышается при снижении уровня глюкозы и уменьшается при его повышении;
– тромбоцитарный фактор роста (PDGF-AA и PDGF-B — platelet-derived growth factor), регулирующий ангиогенез, клеточный рост, пролиферацию и деление мезенхимных клеток (фибробластов);
– фактор роста эндотелия сосудов (VEGF — vascular endothelial grown factor), который стимулирует образование кровеносных сосудов, восстанавливает подачу кислорода в ткани в гипоксических условиях;
– фактор, индуцированный гипоксией (HIF-1 α – hypoxia — inducible factor-1 α ), участвующий в процессах регуляции, доставки и утилизации кислорода, регенерации тканей и образования сосудов;
– трансформирующий фактор роста (TGF- α — ransf-orming growth factor), который отвечает за пролифе-
Табл. 1. Разведение антител для иммуногистохимического исследования
Иммуногистохимическое исследование проводили по стандартной методике с разведением антител, как представлено в таблице 1.
Подсчет результатов проводили в программе Aperio Image Scope с вычислением процентного отношения изучаемых факторов к 1.
Результаты и обсуждение
Экспрессия факторов роста и факторов, индуцируемых гипоксией, при невоспалительных заболеваниях органов брюшной полости без непроходимости (Contr)
Характеристика иммуногистохимических показателей экспрессии в исследуемой группе представлена в таблице 2.
Данные, полученные в группе контроля (Contr), были приняты за условную норму. Величина экспрессии в исследуемых группах сравнивалась с таковой в группе контроля.
Табл. 2. Экспрессия факторов в группе Contr
|
Фактор |
Кол-во, N |
Среднее арифметическое, М±SD |
Медиана, Me [Ql; Qu] |
|
GLUT-1 |
25 |
15,54±3,98 |
9,96 [5,24; 16,18] |
|
PDGF-AA |
10 |
55,74±3,2 |
40,67 [31,29; 52,96] |
|
PDGF-B |
16 |
41,32±4,34 |
40,2 [31,69; 47,86] |
|
VEGF-C |
15 |
17,61±6,46 |
5,13 [5,38; 14,51] |
|
HIF-1 α |
19 |
9,68±1,25 |
7,56 [5,56; 14,2] |
|
TGF- α |
16 |
8,68±1,59 |
9,57 [4,05; 10,1] |
Экспрессия факторов роста и факторов, индуцируемых гипоксией, при острой кишечной непроходимости (Adhesion ileus)
Характеристика иммуногистохимических показателей экспрессии в исследуемой группе представлена в таблице 3.
Табл. 3. Экспрессия факторов в группе Adhesion ileus
|
Фактор |
Кол-во, N |
Среднее арифметическое, М±SD |
Медиана, Me [Ql; Qu] |
|
GLUT-1 |
20 |
30,79±5,09 |
29,92 [13,7; 42,76] |
|
PDGF-AA |
10 |
76,1±1,61 |
76,43 [72,27; 80,52] |
|
PDGF-B |
13 |
43,02±2,86 |
39,15 [36,37; 53,65] |
|
VEGF-C |
10 |
19,2±3,93 |
18,78 [9,75; 27,47] |
|
HIF-1 α |
18 |
20,81±2,56 |
17,18 [11,69; 29,47] |
|
TGF- α |
9 |
13,34±1,9 |
12,6 [10; 16,81] |
В ходе проведенного исследования выявлено увеличение образования факторов роста на поверхности исследуемой спайки брюшной полости при острой кишечной непроходимости, а также выявлены следующие закономерности:
Экспрессия GLUT-1 в группе Adhesion ileus: N = 20; M = 30,79±5,09, Me = 29,92 (Ql = 13,7; Qu = 42,76), увеличилась на 98,2% по отношению к группе Contr: GLUT-1: N = 25; M = 15,54±3,98, Me = 9,96 (Ql = 5,24; Qu = 16,18). GLUT-1: (Mann-Whitney U Test, Z = 3,03, p<0,001), что свидетельствует о снижении транспорта глюкозы и возникновении гипоксии в изучаемой ткани. GLUT-1, способствует облегченному переносу глюкозы через плазматическую мембрану клеток, отвечает за усвоение базальной глюкозы, необходимое для обеспечения процесса дыхания всех клеток. Уровень GLUT-1 в клеточной мембране повышается при снижении уровня глюкозы и уменьшается при его повышении, являясь маркером гипоксии.
Экспрессия PDGF-AA в группе Adhesion ileus: N = 10; M = 76,1±1,61, Me = 76,43 (Ql = 72,27; Qu = 80,52), увеличилась на 389,8% по отношению к группе Contr: PDGF-AA: N = 10; M = 55,74±3,2, Me = 40,67 (Ql = 31,29; Qu = 52,96). PDGF-AA: Mann-Whitney U Test, Z = 0,14, p = 0,27). Экспрессия PDGF-B в группе Adhesion ileus: N = 13; M = 43,02±2,86, Me = 39,15 (Ql= 36,37; Qu = 53,65) увеличилась на 176,9% по отношению к группе Contr: PDGF-B: N = 16; M = 41,32±4,34, Me = 40,2 (Ql = 31,69; Qu = 47,86). PDGF-B: Mann-Whitney U Test, Z = 0,42, p = 0,68), свидетельствует о стимуляции клеточного роста, пролиферации мезенхимных клеток (фибробластов). PDGF регулирует клеточный рост и деление, является потенциальным митогеном клеток мезенхимного происхождения, включая гладкомышечные и глиальные клетки, играет значительную роль в ангиогенезе, митогенезе, т.е. пролиферации мезенхимных клеток, таких как фибробласты и мезенхимальные стволовые клетки.
Экспрессия VEGF-C в группе Adhesion ileus: N = 10; M = 19,2±3,93, Me = 18,78 (Ql = 9,75; Qu = 27,47) увеличилась на 23,6% по отношению к группе Contr: VEGF-C: N = 15; M = 17,61±6,46, Me = 5,13 (Ql = 5,38; Qu = 14,51), VEGF-C: N = 15; M = 17,61±6,46, Me = 5,13 (Ql = 5,38; Qu = 14,51). VEGF-C: Mann-Whitney U Test, Z = 1,38, p = 0,68), что указывает на стимуляцию неоангиогенеза в гипоксических условиях. Во вновь образуемых тканях имеется значительный дефицит кислорода, что вызывает потребность в образовании кровеносных сосудов. Гипоксия, вызванная увеличением потребления кислорода, запускает ангионеогенез через экспрессию сосудистого эндотелиального фактора роста. Ангионеогенез необходим для репарации, заживления ран, регенерации тканей или органов.
Экспрессия HIF-1 α в группе Adhesion ileus: N = 18; M = 20,81±2,56, Me = 17,18 (Ql = 11,69; Qu = 29,47) увеличилась на 34% по отношению к группе Contr: HIF-1 α : N = 19; M = 9,68±1,25, Me = 7,56 (Ql = 5,56; Qu = 14,2). HIF-1a:
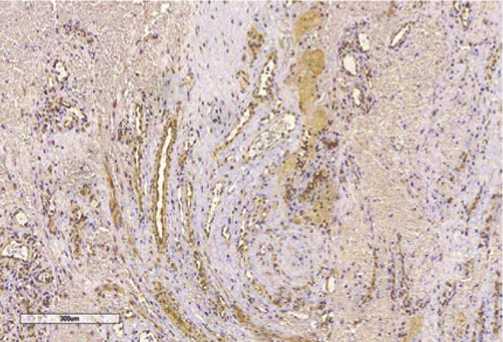
Рис. 1. Экспрессия фактора, индуцируемого гипоксией (HIF-1 α ) в группе Adhesion ileus.
Mann-Whitney U Test, Z = 3,39, p<0,001), что свидетельствует о гипоксии и, как следствие, запуске регенерации тканей и образования сосудов. Фактор, индуцированный гипоксией (HIF-1 α ), участвует в процессах регуляции, доставки и утилизации кислорода, регенерации тканей и образования сосудов. Стабильность HIF-1 α , субклеточная локализация, а также активность транскрипции особенно зависят от уровня кислорода.
Иммуногистохимическая картина подтверждает представленные выводы (Рис. 1).
Экспрессия TGF- α в группе Adhesion ileus: N = 9; M = 13,34±1,9, Me = 12,6 (Ql = 10; Qu = 16,81), уменьшилась на 14,1% по отношению к группе Contr: TGF- α : N = 16; M = 8,68±1,59, Me = 9,57 (Ql = 4,05; Qu = 10,1). TGF- α : Mann-Whitney U Test, Z = 3,03, p = 0,68), что указывает на снижение пролиферации в производстве зрелого внеклеточного матрикса фибробластами. TGF- α , являясь митогенным полипептидом, активирует сигнальный путь для пролиферации, дифференциации и развития клеток. Участвует в регулировании воспалительной реакции и производстве внеклеточного матрикса фибробластами. Эти два процесса связаны с образованием фиброзных спаек после абдоминальной хирургии. Когда мезотелий поврежден, образуются нить фибрина, пространство между которыми сначала заполняется воспалительными клетками, а затем фибробластами, формируя внеклеточный матрикс и образуя постоянную адгезию.
Снижение парциального давления кислорода на поверхности спайки усиливает экспрессию HIF-1 α , тем самым, способствует низкой дифференцировке фибробластов в грубую соединительную ткань. Увеличенная экспрессия факторов роста и созревания соединительной ткани (GLUT-1, TGF) указывает на усиление пролиферативных процессов на поверхности брюшины, что также способствует развитию соединительной ткани на поверхности кишечных петель. При этом факторы, отвечающие за дифференцировку фибробластов (PDGF-AA, PDGF-В), статистически значимого изменения не продемонстрировали, что указывает на отсутствие образования мягких
рубцов, способных с самостоятельной редукции, на поверхности брюшины.
Экспрессия факторов роста и факторов, индуцируемых гипоксией, при спаечной болезни брюшной полости без непроходимости (Adhesion)
Характеристика иммуногистохимических показателей экспрессии в исследуемой группе представлена в таблице 4.
Табл. 4. Экспрессия факторов в группе Adhesion
|
Фактор |
Кол-во, N |
Среднее арифметическое, М±SD |
Медиана, Me [Ql; Qu] |
|
GLUT-1 |
19 |
22,89±3,09 |
16,66 [12,77; 36,31] |
|
PDGF-AA |
5 |
85,32±2,35 |
83,68 [83,5; 89,85] |
|
PDGF-B |
17 |
38,52±4,33 |
34,32 [30,17; 45,18] |
|
VEGF-C |
7 |
12,48±5,79 |
8,4 [3,36; 10,73] |
|
HIF-1 α |
8 |
21,67±4,86 |
19,32 [9,49; 32,54] |
|
TGF- α |
13 |
12,5±1 |
12,01 [11,07; 14,4] |
В ходе проведенного исследования выявлено изменение экспрессии факторов роста и пролиферации клеток на поверхности исследуемой спайки брюшной полости при СББП без кишечной непроходимости, а также доказаны следующие закономерности:
Экспрессия GLUT-1 в группе Adhesion: N = 19; M = 22,89±3,09, Me = 16,66 (Ql = 12,77; Qu = 36,31), увеличилась на 47,3% по отношению к группе Contr GLUT-1: N = 25; M = 15,54±3,98, Me = 9,96 (Ql = 5,24; Qu = 16,18), GLUT-1: (Mann-Whitney U Test, Z = 2,8, p = 0,01). Данное наблюдение указывает на меньшую, чем в группе пациентов с кишечной непроходимостью спаечной этиологии, гипоксию и снижении уровня глюкозы. Экспрессия PDGF-AA в группе Adhesion: N = 5; M = 85,32±2,35, Me = 83,68 (Ql = 83,5; Qu = 89,85), увеличилась на 53,1% по отношению к группе Contr PDGF-AA: N = 10; M = 55,74±3,2, Me = 40,67 (Ql = 31,29; Qu = 52,96), PDGF-AA: Mann-Whitney U Test, Z = 1,38, p = 0,42). Экспрессия PDGF-B в группе Adhesion: N = 17; M = 38,52±4,33, Me = 34,32 (Ql = 30,17; Qu = 45,18), уменьшилась на 6,7% по отношению к группе Contr PDGF-B: N = 16; M = 41,32±4,34, Me = 40,2 (Ql = 31,69; Qu = 47,86), PDGF-B: Mann-Whitney U Test, Z = -0,67, p = 0,51), это свидетельствует о снижении скорости ангиогенеза и клеточного роста мезенхимных клеток (фибробластов).
Экспрессия VEGF-C в группе Adhesion: N = 7; M = 12,48±5,79, Me = 8,4 (Ql = 3,36; Qu = 10,73), уменьшилась на 29,1% по отношению к группе Contr VEGF-C: N = 15; M = 17,61±6,46, Me = 5,13 (Ql = 5,38; Qu = 14,51), VEGF-C: Mann-Whitney U Test, Z = 0,42, p = 0,68), это указывает на снижение ангиогенеза в поврежденной брюшине. Экспрессия HIF-1α в группе Adhesion: N = 8; M = 21,67±4,86, Me = 19,32 (Ql = 9,49; Qu = 32,54), увеличилась на 123,9% по отношению к группе Contr HIF-1α: N = 19; M = 9,68±1,25, Me = 7,56 (Ql = 5,56; Qu = 14,2), HIF-1a: Mann-Whitney U Test, Z = 2,63, p = 0,01), что указы- вает на возрастание гипоксии в ткани брюшины. Экспрессия TGF-α в группе Adhesion: N = 3; M = 12,5±1, Me = 12,01 (Ql = 11,07; Qu = 14,4), увеличилась на 44,1% по отношению к группе Contr TGF-α: N = 16; M = 8,68±1,59, Me = 9,57 (Ql = 4,05; Qu = 10,1), TGF-α: Mann-Whitney U Test, Z = 2,8, p = 0,27), что указывает на инициацию пролиферации, дифференциации и развития клеток, производство внеклеточного матрикса фибробластами.
По аналогии с группой Adhesion ileus, в данной группе также происходит усиление экспрессии HIF-1 α , фактора роста и созревания сосудов (VEGF), что указывает на усиление неоангиогенеза на поверхности брюшины, что также способствует развитию грубой соединительной ткани на поверхности кишечных петель. При этом экспрессия факторов (PDGF-AA, PDGF-В), статистически значимо не изменялась.
Экспрессия факторов роста и факторов, индуцируемых гипоксией, при воспалительных заболеваниях органов брюшной полости без непроходимости (Vosp)
Характеристика иммуногистохимических показателей экспрессии в исследуемой группе представлена в таблице 5.
Табл. 5. Экспрессия факторов в группе Vosp
|
Фактор |
Кол-во, N |
Среднее арифметическое, М±SD |
Медиана, Me [Ql; Qu] |
|
GLUT-1 |
19 |
19,2±3,61 |
13,12 [7,32; 28,25] |
|
PDGF-AA |
5 |
70,92±5,19 |
68,81 [62,64; 71,95] |
|
PDGF-B |
14 |
39,3±3,87 |
34,13 [29,39; 42,87] |
|
VEGF-C |
6 |
13,97±8,84 |
5,78 [2,28; 10,14] |
|
HIF-1 α |
11 |
21,56±4,02 |
15,9 [12,42; 32,94] |
|
TGF- α |
2 |
6,61±2,32 |
6,61 [4,29; 8,92] |
В ходе проведенного исследования выявлена зависимость экспрессии и парциального давления кислорода на поверхности исследуемой спайки брюшной полости при воспалительных заболеваниях брюшной полости.
Экспрессия GLUT- 1 в группе Vosp: N = 19; M = 19,2±3,61, Me = 13,12 (Ql = 7,32; Qu = 28,25), увеличилась на 23,6% по отношению к группе Contr, GLUT-1: N = 25; M = 15,54±3,98, Me = 9,96 (Ql = 5,24; Qu = 16,18), GLUT-1: (Mann-Whitney U Test, Z = -1,4, p = 0,16), что свидетельствует о гипоксии, снижении уровня глюкозы, однако изменения по отношению к контрольной группе статистически не значимы. Экспрессия PDGF-AA в группе Vosp: N = 5; M = 70,92±5,19, Me = 68,81 (Ql= 62,64; Qu = 71,95), увеличилась на 27,3% по отношению к группе Contr, PDGF-AA: N = 10; M = 55,74±3,2, Me = 40,67 (Ql = 31,29; Qu = 52,96), PDGF-AA: Mann-Whitney U Test, Z = 0,42, p = 0,68). Экспрессия PDGF-B в группе Vosp: PDGF-B: N = 14; M = 39,3±3,87, Me = 34,13 (Ql = 29,39; Qu = 42,87), уменьшилась на 4,8% по отношению к группе Contr, PDGF-B: N = 16; M = 41,32±4,34, Me = 40,2 (Ql = 31,69; Qu = 47,86): PDGF-B: Mann-Whitney U Test, Z = 0,6, p = 0,55). Экспрессия VEGF-C в группе Vosp: N = 6;

M = 13,97±8,84, Me = 5,78 (Ql = 2,28; Qu = 10,14), уменьшилась на 20,6% по отношению к группе Contr, VEGF-C: N = 15; M = 17,61±6,46, Me = 5,13 (Ql = 5,38; Qu = 14,51), VEGF-C: Mann-Whitney U Test, Z = 1,38, p = 0,09).
Экспрессия HIF- 1 α в группе Vosp: N = 1 1 ; M = 21,56±4,02, Me = 15,9 (Ql = 12,42; Qu = 47,46), увеличилась на 122,8% по отношению к группе Contr, HIF-1 α : N = 19; M = 9,68±1,25, Me = 7,56 (Ql = 5,56; Qu = 14,2), HIF-1a: Mann-Whitney U Test, Z = 2,63, p = 0,01), что указывает на гипоксию в ткани брюшины. Экспрессия TGF- α в группе Vosp: N = 2; M = 6,61±2,32, Me = 4,29 (Ql = 4,29; Qu = 32,94), уменьшилась на 23,8% по отношению к группе Contr, TGF- α : N = 16; M = 8,68±1,59, Me = 9,57 (Ql = 4,05; Qu = 10,1), TGF- α : Mann-Whitney U Test, Z = 3,03, p = 0,68), что указывает на рост, пролиферацию, дифференциацию и развитие клеток, образование внеклеточного матрикса фибробластами.
Воспалительный процесс, характеризуется статистически достоверным увеличением экспрессии HIF-1 α , что указывает на гипоксию, усиление развития, деления и пролиферации фибробластов на поверхности поврежденной брюшины.
Межгрупповые Adhesion ileus, Adhesion и Vosp сравнения выявили следящие закономерности: достоверные статистические отличия выявлены только между группами Adhesion ileus и Adhesion по показателю экспрессии: PDGF-AA: Mann-Whitney U Test, Z = -2,51, p = 0,01); GLUT-1: (Mann-Whitney U Test, Z = 1,11, p = 0,27); PDGF-B: Mann-Whitney U Test, Z = 1,38, p = 0,17); VEGF-C: Mann-Whitney U Test, Z = 1,71, p = 0,09); HIF-1a: Mann-Whitney U Test, Z = 0,14, p = 0,89); TGF- α : Mann-Whitney U Test, Z = 0,42, p = 0,27). Таким образом, непроходимость кишечника способствует развитию спаечной болезни в брюшной полости, поэтому плановый адгезиолизис является лечебно-профилактическим оперативным вмешательством.
Отсутствуют отличия между группами Adhesion ileus и Vosp: GLUT-1: (Mann-Whitney U Test, Z = 1,67, p = 0,09); PDGF-AA: Mann-Whitney U Test, Z = 1,41, p = 0,16); PDGF-B: Mann-Whitney U Test, Z = 1,29, p = 0,2); VEGF-C: Mann-Whitney U Test, Z = 1,46, p = 0,14); HIF-1a: Mann-Whitney U Test, Z = -0,02, p = 0,98); TGF- α : Mann-Whitney U Test, Z = 1,53, p = 0,13), а также между Adhesion и Vosp: GLUT-1: (Mann-Whitney U Test, Z = 0,99, p = 0,32); PDGF-AA: Mann-Whitney U Test, Z = 1,67, p = 0,09); PDGF-B: Mann-Whitney U Test, Z = -0,1, p = 0,92); VEGF-C: Mann-Whitney U Test, Z = 0,36, p = 0,72); HIF-1a: Mann-Whitney U Test, Z = -0,12, p = 0,9); TGF- α : Mann-Whitney U Test, Z = 1,44, p = 0,15). Данное наблюдение указывает на увеличение гипоксических явлений при воспалительной реакции в обеих группах. Иммуногистохимическая картина подтверждает представленные выводы, (Рис. 2).
Таким образом, гипоксия, влияя на факторы роста, является стимулятором фибробластов и, как следствие, соединительной ткани, коррелирует с выраженностью
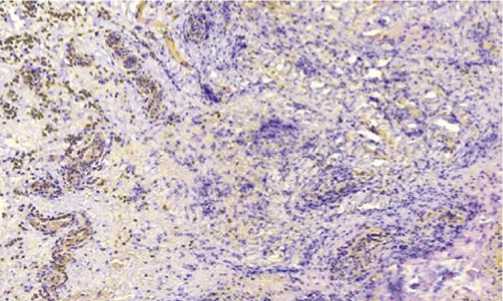
Рис. 2. Экспрессия фактора, индуцируемого гипоксией (HIF-1 α ).
воспаления в брюшной полости. Оказывая влияние на HIF-1 α через регуляцию уровня парциального давления кислорода в брюшной полости, возможна коррекция дифференцировки фибробластов, увеличение количества зрелых мезотелиоцитов, уменьшение выраженности спаечного процесса в брюшной полости у оперированных пациентов.
Заключение
Экспрессия факторов роста (GLUT-1, PDGF-AA, и -B, VEGF-C, TGF- α ) и фактора, индуцируемого гипоксией (HIF-1 α ), является биологическим ответом на воспаление, гипоксию, воздействие физико-химических факторов, деструкцию мезотелия брюшины, и стимулирует образование кровеносных сосудов, внеклеточного матрикса, пролиферацию и деление мезенхимных клеток (фибробластов), являющихся основой спаек брюшной полости.
При острой спаечной кишечной непроходимости экспрессия GLUT-1 увеличилась на 98,2% по отношению к контрольной группе, p<0,001, а экспрессия HIF-1 α увеличилась на 34%, p<0,001, указывая на запуск регенерации тканей с низкой дифференцировкой фибробластов, неоангиогенез, снижении транспорта глюкозы и гипоксии. При этом факторы, отвечающие за дифференцировку фибробластов (PDGF-AA, PDGF-В), статистически значимого изменения не продемонстрировали. Данное соотношение в реакции факторов роста свидетельствует об образовании грубых рубцов (спаек) на поверхности брюшины не способных с самостоятельной редукции.
При СББП без непроходимости экспрессия GLUT-1 увеличилась на 47,3% по отношению к группе контроля, p = 0,01. Экспрессия HIF-1 α , увеличилась на 123,9% по отношению к группе контроля, p = 0,01, что указывает на меньшую, чем в группе пациентов с кишечной непроходимостью спаечной этиологии, гипоксию, неоангиогенез, однако на равнонаправленное влияние. При этом экспрессия факторов (PDGF-AA, PDGF-В), статистически значимо не изменялась.
Воспалительный процесс в брюшной полости усиливает экспрессию VEGF-C на 20,6%, p = 0,09 и HIF-1 α – на

122,8% по отношению к группе контроля, указывая на неоангиогенез и гипоксию тканей, способствуя развитию грубой соединительной ткани на поверхности кишечных петель, снабженной капиллярной сетью.
Нивелирование гипоксии, воспаления и физикохимических факторов деструкции мезотелия брюшины позволит нормализовать экспрессию факторов роста (GLUT-1, PDGF-AA, и -B, VEGF-C, TGF- α ) и фактора, индуцируемого гипоксией (HIF-1 α ), корректировать дифференцировку фибробластов и мезотелиоцитов, тем самым уменьшить вероятность развития и выраженность спаечного процесса у оперированных пациентов.
Значимо на экспрессию фактора, индицируемого гипоксией (HIF-1 α ), влияют гипероксия, гипоксия в брюшной полости (уменьшение на 55% и увеличение на 187% от контрольной группы соответственно), во вдыхаемом воздухе (уменьшение на 54% и увеличение на 194% от контрольной группы соответственно), воздействие фибрина (на 245%), моделированная частичная (на 278%) и полная (на 248%) кишечная непроходимость, повышение внутрибрюшного давления (на 298%), (p<0,001), способствуя спаечному процессу.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Влияние патологического процесса в брюшной полости на экспрессию факторов роста
- Ong AW, Early postoperative small bowel obstruction: A review. Am J Surg. 2020; 219(3): 535-539. DOI: 10.1016/j.amjsurg.2019.11.008
- Apte RS, Chen DS, Chen DS, et al. VEGF in Signaling and Disease: Beyond Discovery and Development. Cell. 2019; 176(6): 1248-1264. 10.1016/ j.cell.2019.01.021. DOI: 10.1016/j.cell.2019.01.021
- Moreno Roig E, Groot AJ, et al. HIF-1 alpha and HIF-2alpha Differently Regulate the Radiation Sensitivity of NSCLC Cells. Cells. 2019; 8(1):45. DOI: 10.3390/cells8010045
- Thornblade LW, Verdial FC, Bartek MA, et al. The Safety of Expectant Management for Adhesive Small Bowel Obstruction: A Systematic Review. J Gastrointest Surg. 2019; 23(4): 846-859. DOI: 10.1007/s11605-018-4017-1
- Bayat Z, Guttman MP, Shiroky J, et al. Non-operative Management of Small Bowel Obstruction in Patients with No Previous Abdominal Surgery: A Systematic Review and Meta-analysis. World J Surg. 2021; 45(7): 2092-2099. 10.1007/s00268-021 -06061 -z. DOI: 10.1007/s00268-021-06061-z
- Tong JWV, Lingam P, Shelat VG, et al. Adhesive small bowel obstruction - an update. Acute Med Surg. 2020; 7(1): 587. DOI: 10.1002/ams2.587
- Yang TWW, Prabhakaran S, Bell S, et al. Non-operative management for small bowel obstruction in a virgin abdomen: a systematic review. ANZ J Surg. 2020; 91(5): 802-80. DOI: 10.1111/ans.16392
- Carrica L, Li L, et al. Genetic inactivation of hypoxia inducible factor 1 -alpha (HIF-1 alpha) in adult hippocampal progenitors impairs neurogenesis and pattern discrimination learning. Neurobiol Learn Mem. 2019; 157: 79-85. DOI: 10.1016/j.nlm.2018.12.002


