Влияние перекиси водорода на содержание запретов Phb3 и Phb4 в листьях Arabidopsis thaliana
Автор: Коротаева Н.Е., Боровский Г.Б.
Журнал: Журнал стресс-физиологии и биохимии @jspb
Статья в выпуске: 3 т.15, 2019 года.
Бесплатный доступ
Согласно современным представлениям, митохондрии растений регулируют экспрессию ядерных генов и сигнальных органелл, действующих на акты, обеспечивая устойчивость растений к внешним стрессорам. Высококонсервативные мембранные белки запрещают (Phb), ответственные за мембрано-пептидные взаимодействия в органеллах животных, растений и микроорганизмов, накапливаются в митохондриях и модулируют состояние их мембран, участвуя в регуляции митохондриально-опосредованной передачи сигналов. Настройка содержания Phb плохо изучена на сегодняшний день. Большинство биотических и абиотических стрессов связаны с продукцией активных форм кислорода (АФК), которые могут играть как сигнальную роль, так и наносить ущерб. Перекись водорода является одной из форм АФК. Целью данного исследования было изучение влияния различных доз перекиси водорода на содержание Phb3 и Phb4 в растениях Arabidopsis. В листьях Arabidopsis thaliana тепловой шок (HS, 42 ° C, 3 ч) вызывал увеличение содержания Phba через 24 ч после прекращения воздействия и увеличение содержания супероксидного радикала сразу после HS. Таким образом, увеличение содержания Phb и ROS в результате ГС происходит одновременно. Далее мы исследовали влияние окислительного стресса на содержание Phb. Сначала было показано, что H2O2 снижает содержание Phb дозозависимым образом в начальные часы действия (использовалось от 2 до 40 мМ H2O2 в течение 1-2 часов). При продолжении воздействия до 24 ч содержание Phb возвращается к контрольному значению. При этом подавляющий эффект демонстрируется не стрессовыми дозами H2O2 (от 2 до 10 мМ). Стрессовая доза H2O2 (40 мМ в сутки) не влияет на содержание Phb, но вызывает увеличение содержания Hsp 17,7 и увядание листьев, что указывает на напряженное состояние растений. Полученные результаты говорят в пользу того, что на уровне белка увеличение содержания Phb3 и Phb4 не активируется ROS-опосредованной системой даже во время развития окислительного стресса.
Короткий адрес: https://sciup.org/143168581
IDR: 143168581
The influence of hydrogen peroxide on the content of prohibitines Phb3 and Phb4 in the leaves of Arabidopsis thaliana
According to modern ideas, plant mitochondria regulate the expression of nuclear genes and actas signaling organelles providing the tolerance of plants to external stressors. Highlyconservative membrane proteins prohibitines (Phb) responsible for membrane-peptideinteractions in organelles of animals, plants and microorganisms accumulate in mitochondriaand modulate the state of their membranes, participating in the regulation of mitochondrial-mediated signaling. The tuning of the content of the Phb is poorly investigated for today day.Most of biotic and abiotic stresses are associated with production of reactive oxygen species(ROS) which can play as signaling role as well as cause damage. Hydrogen peroxide is one ofthe forms of ROS. The goal of this research was to study the effect of different doses ofhydrogen peroxide on the Phb3 and Phb4 content in Arabidopsis plants. In the leaves ofArabidopsis thaliana heat shock (HS, 42°C, 3 h) caused the increasing of the content of Phbafter 24 h from the stop of the influence and the increasing of superoxide radical contentimmediately after HS. So the increasing of the content of Phb and ROS as a result of HS occurssimultaneously. Next we investigated the influence of oxidative stress on Phb content. It wasshown at first that H2O2 decreases the content of Phb in dose-depend manner at the startinghours of the action (2 to 40 mM H2O2 during 1 to 2 h were used). At the continuation of theinfluence till 24 h the content of Phb returns to the control value. Herewith the suppressing effectis demonstrated by non-stress doses of H2O2 (2 to 10 mM). The stress dose of H2O2 (40 mM at24 h) doesn’t effect on the content of Phb, but causes the increasing of the content of Hsp 17.7and wilting of the leaves which indicates the stressed condition of the plants. The resultsreceived speak in favor that at the protein level the increasing of Phb3 and Phb4 content is notactivated by ROS-mediated system even during the development of the oxidative stress.
Текст научной статьи Влияние перекиси водорода на содержание запретов Phb3 и Phb4 в листьях Arabidopsis thaliana
Прохибитины (Phb) - небольшие (Mr около 30 кД) высококонсервативные структурные и фолдинг-белки, относящиеся к семейству мембранных белков "band-7" (Gehl and Sweetlove 2014) и обнаруженные на сегодняшний день в клетках всех изученных эукариот (Artal-Sanz and Tavernarakis 2009, Van Aken et al., 2010). В клетках растений, животных и микроорганизмов Phb локализованы, в первую очередь, во внутренней митохондриальной мембране, и в составе мембраны клеточного ядра (Artal-Sanz and Tavernarakis 2009, Gehl and Sweetlove 2014). О Phb растений к настоящему времени пока накоплено немного информации. Помимо митохондрий, Phb растений также обнаружены в составе вакуолярной мембраны (Carter et al., 2004) и в плазмалемме (Marmagne et al., 2004). В мультимерный белковый комплекс Phb растений, помимо Phb1 и Phb2, включены белки Phb3, Phb4 и Phb6 (Van Aken et al., 2010). Для растений, в отличие от животных, показано участие Phb в процессах роста (Artal-Sanz and Tavernarakis 2009) и в специфической для растений реакции сверхчувствительности (Nadimpalli et al., 2000).
Активная экспрессия генов Phb растений происходит в интенсивно растущих тканях под действием ауксина (Van Aken et al., 2010; Van Aken et al., 2007). На этом этапе роль Phb, скорее всего, тесно связана с накоплением митохондрий в пролиферирующих молодых клетках и сводится к формированию структуры внутренней митохондриальной мембраны; таким образом, в период активного роста Phb участвуют в обеспечении клеток энергетическими молекулами для дальнейшего развития растения. Как негативные регуляторы активности mAAA-протеазы, Phb растений, вероятно, участвуют в контроле качества белков в матриксе митохондрий по типу механизма действия Phb животных (Piechota et al., 2010; Artal-Sanz and Tavernarakis 2009). Phb накапливаются в митохондриях трансгенных растений табака с недостатком альтернативной оксидазы, что говорит в пользу их участия в защите от окислительного стресса (Sieger et al., 2005) и в регуляции реакции сверхчувствительности и\или апоптоза (Takahashi et al., 2003).
На экспрессию генов Phb оказывает влияние как изменение содержания альтернативной оксидазы (Van Aken et al ., 2010), так и прямое стрессовое воздействие, например, высокая освещенность (Vandenabeele et al ., 2003), температура (Ahn et al ., 2006) или УФ (AtGenExpress Visualization Tool). Таким образом, Phb являются частью программ регуляции протеома растительных митохондрий как в нормальных, так и в стрессовых условиях, в том числе, в условиях окислительного стресса. Поскольку в настоящее время принято, что митохондрии играют важную роль в формировании устойчивости, с одной стороны, и в осуществлении программируемой гибели в условиях стресса, с другой, изменение содержания Phb, в частности белков Phb3 и Phb4, может модулировать состояние мембран митохондрий и быть одним из факторов развития стрессового ответа (Van Aken et al., 2010). Таким образом, Phb могут участвовать в системе митохондриально-ядерной (ретроградной) регуляции в ответ на стрессовые условия (Pucciariello et al. , 2012).
Активные формы кислорода (АФК) выполняют функцию универсальных сигнальных молекул в живой клетке, поскольку служат модуляторами и передатчиками сигналов мобилизации восстановительных программ, а также являются маркерами стрессового воздействия (Mittler et al., 2011). В стрессовых условиях основными источниками АФК в клетке являются ЭТЦ митохондрий и хлоропластов, пероксисомы и мембранная NADPH оксидаза (Pucciariello et al., 2012). H2O2 является одной из форм АФК, в нестрессовых условиях он регулирует многие физиологические процессы: старение (Gill and Tuteja 2010), фотосинтез и фотодыхание (Peng et al., 2005), движение устьиц (Bright et al., 2006), клеточный цикл (Mittler et al., 2004), рост и развитие (Foreman et al., 2003). H2O2 имеет среднюю активность и более длительный срок жизни по сравнению с остальными формами АФК (Bhattachrjee 2005). Благодаря продолжительному периоду жизни и высокой способности проникать через мембраны, H2O2 играет роль вторичного мессенджера в развитии и передаче внутриклеточных сигналов с помощью АФК (Quan et al., 2008). В период окислительного стресса H2O2 в низких концентрациях участвует в сигналинге, активирующем программы устойчивости и адаптации к биотическим и абиотическим воздействиям (Quan et al., 2008). Так, предобработка небольшой концентрацией H2O2 вызывает активацию генов антиоксидантных белков, снижает количество окисленного глутатиона и предотвращает стресс-индуцированное окисление белков (Gill and Tuteja 2010). Накопление в растительных клетках большого количества H2O2 приводит к развитию окислительного стресса (Gill and Tuteja 2010). В высоких дозах H2O2 способствует развитию ПКС (Quan et al., 2008).
Накопление Phb в митохондриях также может активироваться при развитии внутриклеточного окисления (Sieger et al ., 2005). Однако может ли рост содержания прохибитинов напрямую активироваться с помощью АФК, т.е. тем же путем, что и накопление других стресс-индуцированных факторов защиты и адаптации, остается неизвестным. Целью данной работы стало выявление влияния H 2 O 2 на накопление Phb в листьях Arabidopsis thaliana .
MATERIALS AND METHODS
В работе использовали 25-суточные растения Arabidopsis thaliana (L.) Heynh (экотип Columbia), выращенные на грунте в климатической камере МКТ-240 (“Binder”, Германия; 22–24°C, 16/8 ч день/ночь, влажность воздуха 50%, освещенность 9 клк). Температурную обработку проводили у несрезанных растений в термостате MIR-154 (“Sanyo”, Япония) при температурах 35 и 45°С в течение 3 ч, после чего надземную часть срезали, немедленно замораживали в жидком азоте и хранили в криостате при -80°С. Пробы использовали для выделения общего белка. Часть растений по окончании термической обработки выдерживали 24 ч в климатической камере в условиях выращивания, после чего замораживали.
Для определения содержания супероксидного аниона использовали метод окрашивания образовавшегося в присутствии супероксидного аниона формазана с помощью NBT (AppliChem, Германия) (Meyer et al., 2009). Экстракцию формазана проводили в листьях растений арабидопсиса по методу Myouga et al. (2008). Содержание формазана определяли колориметрически (SmartSpec Plus, BioRad) при 700 нм. Получившееся значение оптической плотности относили к сырому весу пробы (Myouga et al., 2008).
Для создания окислительного стресса надземную часть растений срезали, помещали в чашки Петри на растворы в объеме 50 мл, содержащие H 2 O 2 (ЗАО “Реактив”, Россия) в концентрациях 2, 4, 10 или 40 мМ, либо бидистиллированную воду, и оставляли при комнатной температуре (22-24°С) под бумажным колпаком на 1 ч, 2 ч или 24 ч. Затем растения промывали бидистиллированной водой, немедленно замораживали в жидком азоте, помещали для хранения в криостат при -80°С, после чего использовали для выделения общего белка.
Общий белок экстрагировали из 0.5 г листьев. Листья замораживали в жидком азоте и растирали с кварцевым песком в 2.5 мл буфера, содержащего 100 мМ Трис-HCl (pH 7.4–7.6), 0.1% ДДС-Na, 12 мМ β-меркаптоэтанола, 0.5–1 мМ фенилметилсульфонилфлюорида и нерастворимый поливинилпирролидон (10% от веса пробы). После центрифугирования (18 000 g, 10 мин) белок из полученного супернатанта осаждали пятикратным объемом охлажденного до –20 °C ацетона (8500 g, 10 мин). Осадок общего клеточного белка растворяли в буфере для образца (0.125 M Трис-HCl (pH 6.8), 10% ДДС-Na, 10 мМ β-меркаптоэтанол, 1 мМ ЭДТА, 20% глицерин) с последующим нагреванием при 97°C в течение 3 мин на водяной бане и центрифугированием при 12000 g в течение 10 мин. Содержание белка в полученных белковых пробах определяли с помощью реактива Брэдфорда (BioRad). Определение содержания Phb, Hsp 101 и Hsp 17.7 проводили денситометрически после электрофоретического фракционирования и Western Blot в системе Mini-Protean III (“BioRad”, США) в соответствии с прилагаемой инструкцией. На гель наносили по 10 мкг белка. Количество наносимого белка нормализовали по окрашиванию геля Кумасси. Для детекции использовали первичные антитела против Hsp101 (AS07 253, “Agrisera”, Швеция), Hsp17.7 (AS07 255, “Agrisera”, Швеция) и прохибитинов PHB3 и PHB4 (антитела любезно предоставлены док. Hillel Fromm, Weizmann Institute of Science, Rehovot, Israel (Van Aken et al., 2007, Snedden and Fromm 1997)). Интенсивность окрашивания пятна, соответствующего анализируемому белку, определяли с помощью программы Gel Analysis (Россия) в условных единицах и выражали для каждого белка как долю от интенсивности окрашивания в контроле, которую принимали равной 1. В качестве контроля использовали белок из несрезанных растений, растущих в контрольных условиях. Каждый опыт проводился не менее чем в 3 биологических повторностях. Статистическую обработку проводили в программе Sigma plot.
RESULTS AND DISCUSSION
Действие ТШ вызывало небольшое увеличение содержания Phb сразу после воздействия и более отчетливый рост их содержания через сутки после него (рис. 1А, Б). Дозозависимое накопление Hsp 101, которое происходило через 3 ч и через сутки после ТШ (рис. 1А), говорило об активации защитных программ, реализующихся посредством АФК (Pucciariello et al ., 2012). Сразу после воздействия в листьях арабидопсиса происходил достоверный дозозависимый рост содержания супероксидного аниона (рис. 1В), что соответствует современным представлениям о развитии стрессовой реакции (Pucciariello et al ., 2012). Таким образом, рост содержания Phb и супероксидного аниона происходят одновременно в ответ на обработку ТШ. Однако, по сравнению с накоплением Hsp101, накопление Phb происходит гораздо медленнее.
Для обработки H2O2 были выбраны такие значения его концентрации, в которой он накапливается в клетке в стрессовых условиях при развитии окислительного стресса: 2-40 мМ (Rao et al., 2000, Kotchoni et al., 2006, Sweetlove et al., 2002). 24часовое воздействие H2O2 в концентрации 40 мМ приводило к съеживанию и завяданию мелких молодых листьев, что может указывать на создание стрессовых условий при обработке этой концентрацией (рис. 2А). Эта же концентрация вызывала накопление стрессового белка Hsp 17.7, хотя оно было не очень значительным по сравнению с накоплением после теплового воздействия (рис. 2Б). Накопление стрессового белка также говорит в пользу развития стрессового состояния и является результатом активации сигнальных систем, задействованных в развитии стрессового ответа. Более низкие концентрации H2O2 и более короткое инкубирование не вызывали накопления Hsp 17.7. Сходным образом, на листьях арабидопсиса было показано, что 2-х часовое инкубирование с 10 мМ H2O2 может увеличить акклиматизацию PSII к избыточному свету, т.е. оказать закаливающее действие, тогда как инкубирование с 1 мМ H2O2 и ниже не приводит к такому эффекту (Hou et al., 2018); концентрации H2O2 до 5 мМ не приводили к снижению жизнеспособности клеток суспензионной культуры табака (Houot et al., 2001) и арабидопсиса (Desican et al., 1998) даже после суток инкубирования, тогда как концентрация 88 мМ в течение 16 ч в результате развития окислительного стресса приводила к подавлению скорости роста и появлению продуктов ПОЛ (Sweetlove et al., 2002). Таким образом, концентрации H2O2 2-10 мМ по силе воздействия можно считать “фоновыми”, не приводящими к стрессированию, тогда как длительное инкубирование (24 ч) с 40 мМ H2O2 приводит к неблагоприятным последствиям, симптомами которых может быть накопление стрессового белка и завядание самых молодых листьев.
Наибольшее влияние на содержание Phb оказывали дозы H2O2 10 и 40 мМ (рис. 2В, Г, Д). Наиболее яркий дозозависимый эффект наблюдался в первый час после начала воздействия (рис. 2Д). Использование 40 мМ H2O2 в первый час инкубации приводило к отчетливому снижению содержания Phb (рис. 2Г). Через 24 ч содержание Phb восстанавливалось и почти достигало контрольных значений. Таким образом, результаты говорят в пользу того, что H2O2 в исследованных дозах не стимулирует рост содержания Phb. H2O2 оказал подавляющее действие на содержание Phb уже через 1 ч, при этом не произошло накопления стрессового белка Hsp 17.7 и не было выявлено видимых изменений во внешнем виде растений. Перечисленные факты говорят в пользу того, что в “фоновых” дозах H2O2 снижает содержание Phb. В “стрессовых” дозах роста содержания Phb также не происходит. Таким образом, рост содержания Phb через сутки после действия ТШ (рис. 1) скорее может быть обусловлен функционированием сигнальных систем, не связанных с АФК. В пользу большей роли таких систем сигналинга говорит слабая активация, либо отсутствие активации экспрессии генов Phb в ответ на многие стрессы, сопряженные с окислением (например, холодовой и раневой) (AtGenExpress Visualization Tool).
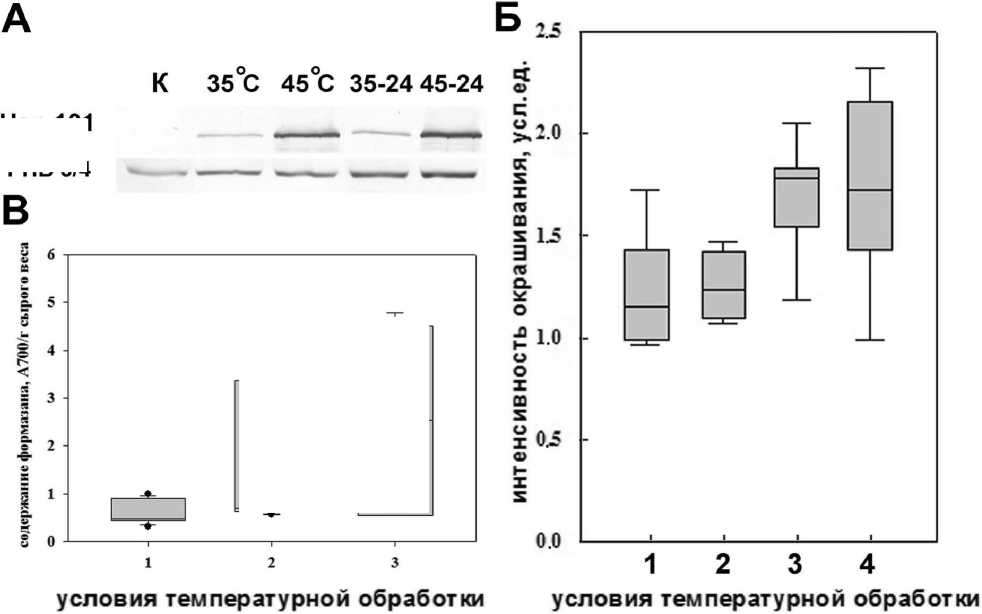
Figure 1. Влияние ТШ на содержание Phb и супероксидного аниона в листьях арабидопсиса. А - результат Western Blot с антителами против Phb (Phb3 и Phb4) и Hsp 101. Сверху указаны условия температурной обработки. 35 и 45°C – обработка в течение 3 ч; 35-24 и 45-24 - 3-часовая обработка при 35 и 45°С и 24часовой “отдых” в условиях выращивания; к – растения без обработки. Представлена типичная мембрана. Б – денситометрическая оценка содержания Phb. 1 – 35°С, 3 ч; 2 - 45°С, 3 ч; 3, 4 - 3-часовая обработка при 35°С (3) или 45°С (4) и 24-часовой “отдых” в условиях выращивания. Интенсивность окрашивания для каждого образца пересчитывали в условных единицах относительно принятого за 1 контрольного образца. Ме [25%; 75%], бары показывают минимальное и максимальное значения. n =4– 9. Приведен результат анализа не менее чем четырех биологических повторностей. В – результат измерения количества образовавшегося формазана в листьях арабидопсиса. 1 – контроль (22-24°С); 2 – ТШ (35°С, 3 ч); 3 – ТШ (45°С, 3 ч). Ме [25%; 75%], бары показывают минимальное и максимальное значения. Приведен результат анализа трех биологических повторностей.* - значения достоверно отличаются от контроля (критерий Манна-Уитни, p <0.05; n =6-10).
Hsp 101
PHB 3/4
2 мМ
4 мМ
10 мМ
40 мМ

К
10 мМ
40 мМ
вода
2 мМ
4 мМ
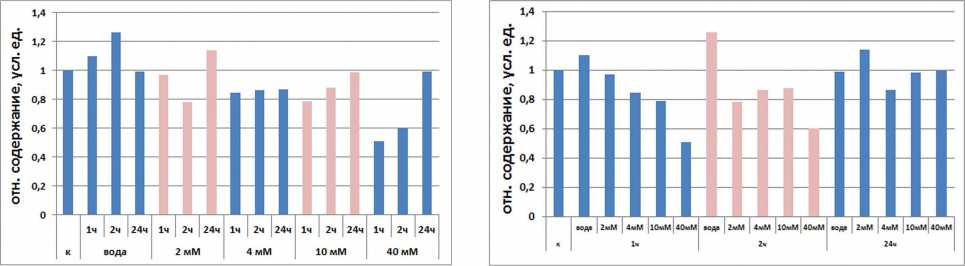
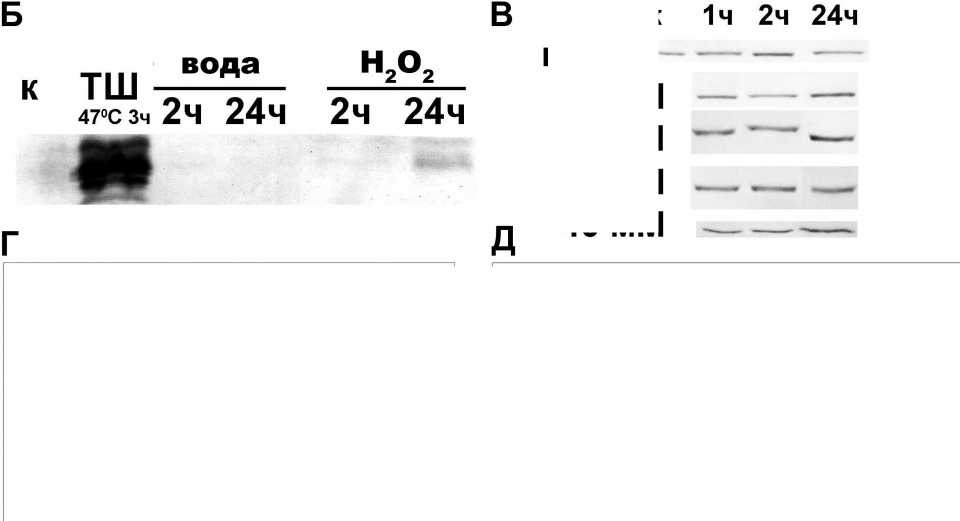
Figure 2. Влияние H 2 O 2 на растения арабидопсиса. А - влияние H 2 O 2 на внешний вид растений арабидопсиса. Сверху указаны использованные концентрации H 2 O 2 . к – инкубирование с бидистиллированной водой. Продолжительность ингибирования – 24 ч. Завядшие листья обведены маркером. Б - влияние 40 мМ H 2 O 2 на содержание Hsp 17.7 в листьях арабидопсиса. к – растения арабидопсиса того же возраста, произрастающие на грунте. ТШ – для термической обработки использовались растения, произрастающие на грунте. В, Г, Д - влияние H 2 O 2 на содержание Phb в листьях арабиопсиса. В – вестерн блот (типичная мембрана), сверху указана продолжительность обработок; Г, Д – диаграммы по результатам денситометрического подсчета содержания Phb после вестерн блот. Г – данные сгруппированы относительно концентрации H 2 O 2 ; Д – данные сгруппированы относительно продолжительности воздействия. Приведены средние арифметические ( n =3). Данные представлены в условных единицах и вычислены относительно контроля, принятого за 1. к – растения того же возраста, произрастающие на грунте.
Ранее было показано, что уровень мРНК Phb2 в листьях табака повышался через 6 ч после нагревания при 55°С, которое приводило к развитию ПКС в растениях (Ahn et al., 1999). Причем развитие ПКС происходило через 12 ч после воздействия (Balk et al., 1999). К сожалению, в данном исследовании мы не оценивали дальнейшую жизнеспособность растений после обработки ТШ и через сутки после нее (рис. 1). Возможно, рост содержания Рhb через 24 ч после ТШ может быть обусловлен развитием ПКС. В таком случае использованные нами “фоновая” и “стрессовая” дозы H2O2 не активируют рост содержания Phb, поскольку также не приводят к развитию ПКС. Дальнейшее исследование выживаемости растений после воздействия H2O2 и ТШ могло бы дать ответ на этот вопрос.
В целом, в первые часы обработки пероксид водорода в исследованных концентрациях дозозависимо подавляет содержание Phb3 и Phb4. Таким образом, маловероятно, что в данных дозах он может быть сигнальной молекулой, вызывающей накопление Phb в условиях ТШ.
ACKNOWLEDGEMENT
Список литературы Влияние перекиси водорода на содержание запретов Phb3 и Phb4 в листьях Arabidopsis thaliana
- Ahn C.S., Lee J.H., Reum Hwang A., Kim W.T., Pai H.S. (2006) Prohibitin is involved in mitochondrial biogenesis in plants. Plant J., 46, 658-667
- Artal-Sanz M., Tavernarakis N. (2009) Prohibitin and mitochondrial biology. Trends Endocrinol. Metab., 20, 394-401
- AtGenExpress Visualization Tool (AVT), http://jsp.weigelworld.org/expviz/expviz.jsp
- Balk J., Leaver C.J., McCabe P.F. (1999) Translocation of cytochrome c from the mitochondria to the cytosol occurs during heat-induced programmed cell death in cucumber plants. FEBS Lett., 463, 151-154
- Bhattachrjee S. (2005) Reactive oxygen species and oxidative burst: roles in stress, senescence and signal transduction in plant. Curr. Sci., 89, 1113-1121
- Bright J., Desikan R., Hancock J.T., Weir I.S., Neill S.J. (2006) ABA-induced NO generation and stomatal closure in Arabidopsis are dependent on H2O2 synthesis. The Plant J., 45, 113-122
- Carter C., Pan S., Zouhar J., Avila E.L., Girke T., Raikhel N.V. (2004) The vegetative vacuole proteome of Arabidopsis thaliana reveals predicted and unexpected proteins. Plant Cell., 16, 3285-3303
- Desikan R., Reynolds A., Hancock J.T., Neill S.J. (1998) Harpin and hydrogen peroxide both initiate programmed cell death but have differential effects on defence gene expression in Arabidopsis suspension cultures. Biochem. J., 330, 115-120
- Foreman J., Demidchik V., Bothwell J.H., Mylona P., Miedema H., Torres M.A., Linstead P., Costa S., Brownlee C., Jones J.D., Davies J.M., Dolan L. (2003) Reactive oxygen species produced by NADPH oxidase regulate plant cell growth. Nature, 422, 442-446
- Gehl B., Sweetlove L.J. (2014) Mitochondrial Band-7 family proteins: scaffolds for respiratory chain assembly? Front. Plant Sci., 5, 141-147
- Gill S.S., Tuteja N. (2010) Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants. Plant Physiol Biochem., 48, 909-30
- Hou Q.Z., Wang Y.P., Liang J.Y., Jia L.Y., Feng H.Q., Wen J., Ehmet N., Bai J.Y. (2018) H2O2-induced acclimation of photosystem II to excess light is mediated by alternative respiratory pathway and salicylic acid. Photosynthetica, 56, 1154-1160
- Houot V., Etienne P., Petitot A.-S., Barbier S., Blein J.-P. (2001) Hydrogen peroxide induces programmed cell death features in cultured tobacco BY-2 cells in a dose-dependent manner. J. Exp. Bot., 52, 1721-1730
- Kotchoni S.O., Kuhns C., Ditzer A., Kirch H.-H., Bartels D. (2006) Over-expression of different aldehyde dehydrogenase genes in Arabidopsis thaliana confers tolerance to abiotic stress and protects plants against lipid peroxidation and oxidative stress. Plant, Cell and Environ., 29, 1033-1048
- Marmagne A., Rouet M.A., Ferro M., Rolland N., Alcon C., Joyard J., Garin J., Barbier-Brygoo H., Ephritikhine G. (2004) Identification of new intrinsic proteins in Arabidopsis plasma membrane proteome. Mol. Cell Proteomics, 3, 675-691
- Meyer E.H., Tomaz T., Carroll A.J., Estavillo G., Delannoy E., Tanz S.K., Small I.D., Pogson B.J., Millar A.H. (2009) Remodeled respiration in ndufs4 with low phosphorylation efficiency suppresses Arabidopsis germination and growth and alters control of metabolism at night. Plant Physiol., 151, 603-619
- Mittler R., Vanderauwera S., Gollery M., Van Breusegem F. (2004) Reactive oxygen gene network of plants. Trends Plant Sci., 9, 490-498
- Mittler R., Vanderauwera S., Suzuki N., Miller G., Tognetti V.B., Vandepoele K., Gollery M., Shulaev V., Van Breusegem F. (2011) ROS signaling: the new wave? Trends Plant Sci., 16, 300-309
- Myouga F., Hosoda C., Umezawa T., Iizumi H., Kuromori T., Motohashi R., Shono Y., Nagata N., Ikeuchi M., Shinozaki K. (2008) A heterocomplex of iron superoxide dismutases defends chloroplast nucleoids against oxidative stress and is essential for chloroplast development in Arabidopsis. Plant Cell, 20, 3148-3162
- Nadimpalli R., Yalpani N., Johal G.S., Simmons C.R. (2000) Prohibitins, stomatins, and plant disease response genes compose a protein superfamily that controls cell proliferation, ion channel regulation, and death. J. Biol. Chem., 275, 29579-29586
- Peng C.L., Ou Z.Y., Liu N., Lin G.Z. (2005) Response to high temperature in flag leaves of super high-yielding rice Pei'ai 64S/E32 and Liangyoupeijiu. Rice Sci. 12, 179-186
- Piechota J., Kolodziejczak M., Juszczak I., Sakamoto W., Janska H. (2010) Identification and characterization of high molecular weight complexes formed by matrix AAA proteases and prohibitins in mitochondria of Arabidopsis thaliana. J. Biol. Chem., 285, 12512-12521
- Pucciariello C., Banti V., Perata P. (2012) ROS signaling as common element in low oxygen and heat stresses. Plant Physiol. and Biochem., 59, 3-10
- Rao M.V., Lee H., Creelman R.A., Mullet J.E., Davis K.R. (2000) Jasmonic acid signaling modulates ozone-induced hypersensitive cell death. The Plant Cell, 12, 1633-1646
- Quan L.-J., Zhang B., Shi W.-W., Li H.-Y. (2008) Hydrogen peroxide in plants: a versatile molecule of the reactive oxygen species network, J. Integrat. Plant Biol., 50, 2-18
- Sieger S.M., Kristensen B.K., Robson C.A., Amirsadeghi S., Eng E.W., Abdel-Mesih A., Møller I.M., Vanlerberghe G.C. (2005) The role of alternative oxidase in modulating carbon use efficiency and growth during macronutrient stress in tobacco cells. J. Exp. Bot., 56, 1499-1515
- Snedden W.A., Fromm H. (1997) Characterization of the plant homologue of prohibitin, a gene associated with antiproliferative activity in mammalian cells. Plant Mol. Biol., 33, 753-756
- Sweetlove L.J., Heazlewood J.L., Herald V., Holtzapffel R., Day D.A., Leaver C.J., Milla A.H. (2002) The impact of oxidative stress on Arabidopsis mitochondria. The Plant J., 32, 891-904
- Takahashi A., Kawasaki T., Wong H.L., Suharsono U., Hirano H., Shimamoto K. (2003) Hyperphosphorylation of a mitochondrial protein, prohibitin, is induced by calyculin A in a rice lesion-mimic mutant cdr1. Plant Physiol., 132, 1861-1869
- Van Aken O., Pecenková T., van de Cotte B., De Rycke R., Eeckhout D., Fromm H., De Jaeger G., Witters E., Beemster G.T., Inzé D., Van Breusegem F. (2007) Mitochondrial type-I prohibitins of Arabidopsis thaliana are required for supporting proficient meristem development. Plant J., 52, 850-864
- Van Aken O., Whelan J., Van Breusegem F. (2010) Prohibitins: mitochondrial partners in development and stress response. Trends Plant Sci., 15, 275-282
- Vandenabeele S. Van Der Kelen K., Dat J., Gadjev I., Boonefaes T., Morsa S., Rottiers P., Slooten L., Van Montagu M., Zabeau M., Inzé D., Van Breusegem F. (2003) A comprehensive analysis of hydrogen peroxide-induced gene expression in tobacco. Proc. Natl. Acad. Sci. U. S. A., 100, 16113-16118


