Влияние прерывистой гипобарической гипоксии на экспрессию HIF-1 и морфофункциональные изменения в миокарде
Автор: Балыкин Михаил Васильевич, Сагидова Светлана Александровна, Жарков Александр Владимирович, Айзятулова Екатерина Дмитриевна, Павлов Денис Анатольевич, Антипов Игорь Викторович
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 2, 2017 года.
Бесплатный доступ
Цель - оценить экспрессию Hif-1α, активность свободнорадикального окисления и морфофункциональные изменения в миокарде на разных этапах адаптации к прерывистой гипобарической гипоксии. Материалы и методы. Исследование проводилось на 96 крысах-самцах линии «Вистар». Прерывистую гипоксию (ПГГ) воспроизводили в барокамере (Рв - 330 мм рт. ст.) по схеме: 5 мин - снижение Рв, 10 мин - пребывание в гипобарии, 5 мин - повышение Рв, 5 мин - пребывание в условиях нормоксии (3 гипобарических цикла ежедневно, 6 раз в неделю на протяжении 30 сут). Во время ПГГ в миокарде определяли экспрессию Hif-1α (ПЦР), активность малонового диальдегида, супероксиддисмутазы, каталазы и глутатион-S-трансферазы (спектрофотометрия). Морфометрию капилляров и волокон миокарда проводили на гистологических препаратах после посмертной инъекции кровеносного русла контрастом (световая микроскопия). Результаты. Установлено, что во время ПГГ возникает артериальная гипоксемия (PaO2 - 52,0-57,5 мм рт. ст.) на фоне смешанного метаболического и респираторного ацидоза (1-е сут) и компенсированного респираторного алкалоза (15-30-е сут). Во время сеансов ПГГ аккумуляция Hif-1α в миокарде возрастает в 11,6; 6,4 и 2,7 раза на 1, 15, 30-е сут адаптации. На 1-15-е сут ПГГ активируются процессы ПОЛ (увеличение МДА), повышается активность каталазы и глутатион-S-трансферазы. В последующий период (30-е сут) активность ПОЛ снижается, а ферментов антиоксидантной защиты (СОД, МДА, глутатион-S-трансферазы) повышается. Адаптация к ПГГ приводит к повышению общего числа капилляров на единицу поверхности миокарда (14,0 и 19,8 %) на 15-е и 30-е сут эксперимента. Заключение. ПГГ сопровождается экспрессией Hif-1α, активацией процессов ПОЛ, возникновением реактивных морфофункциональных изменений в миокарде во время первого гипоксического сеанса; на 15-30-е сут экспрессия Hif-1α и активность ПОЛ снижаются при повышении активности системы антиоксидантной защиты, увеличении васкуляризации сердца.
Гипоксия, крысы, адаптация, миокард, перекисное окисление липидов, капилляры
Короткий адрес: https://sciup.org/14113268
IDR: 14113268 | УДК: 612.273.2:612.172 | DOI: 10.23648/UMBJ.2017.26.6227
Effect of intermittent hypobaric hypoxia on HIF-1 expression and morphofunctional changes in the myocardium
The main study objective is to evaluate the expression of Hif-1α, free radical oxidation activity and morphofunctional changes in the myocardium at different adaptation stages to intermittent hypobaric hypoxia. Materials and Methods. The study was conducted on 96 male Wistar rats. Intermittent hypoxia (IH) was reproduced in an altitude chamber (330 mm Hg) according to the following scheme: 5 min - decrease in Pb, 10 min - hypobaria, 5 min - increase in Pb, 5 min - normoxia. Rats underwent 3 hypobaric cycles daily, 6 days a week, for 30 days. IH was associated with the expression of Hif-1α in the myocardium (PCR), activity of malondialdehyde, superoxide dismutase, catalase and glutathione-S-transferase (spectrophotometry). Morphometry of capillaries and myocardial fibers was conducted on histologic specimen after injecting a postmortem contrast material into the bloodstream (light microscopy). Results. It was established that arterial hypoxemia arises during IH (PaO2 - 52.0-57.5 mm/Hg). It appeared in association with mixed metabolic and respiratory acidosis (1st day) and compensated respiratory alkalosis (15-30 day). During IH the accumulation of Hif-1α in the myocardium increases by 11.6, 6.4 and 2.7 times on the 1st, 15th and 30th day of adaptation. During 1-15 days of IH lipid peroxidation (LPO) is activated (MDA increases). The activity of catalase and glutathione-S-transferase is also increased. During the next 30 days LPO activity decreases, while the activity of antioxidant defense enzymes (SOD, MDA, glutathione-S-transferase) increase. Adaptation to IH leads to an increase in the total number of capillaries per unit of the myocardium surface (14.0 and 19.8 %) on the 15th and 30th day of the study.
Текст научной статьи Влияние прерывистой гипобарической гипоксии на экспрессию HIF-1 и морфофункциональные изменения в миокарде
Введение. В настоящее время достаточно хорошо известны пато- и саногенные эффекты гипоксии, ее пре- и посткондициони-рующие воздействия на организм [1–4]. Широкое применение в медицинской практике получили методы прерывистой (интервальной) нормо- и гипобарической гипоксии, которые показали свою эффективность в профилактике, терапии и реабилитации нарушений сердечно-сосудистой системы [5–8], дыхания [9], крови [10], метаболизма [11] и т.д.
В последние годы широко обсуждается прекондиционирующий эффект гипоксии – повышение толерантности органов и тканей к ишемии после однократного или серии гипоксических воздействий и реоксигенации [12, 13].
Установлено, что предварительное гипоксическое воздействие приводит к повышению устойчивости структур миокарда к экспериментальной ишемии (окклюзия венечных артерий) и реоксигенации [2, 12], уменьшению зоны некроза и сохранению высокой сократительной способности миокарда в этих условиях [12, 13]. Показано, что в основе прекондиционирующего действия гипоксии лежит совокупность тканевых и молекулярно-клеточных изменений [12], однако вопрос об их реализации на уровне отдельных органов и тканей остается открытым.
Триггером, запускающим совокупность системных и тканевых механизмов адаптации, является гипоксией индуцированный фактор (hypoxia inducible factor) Hif-1 [14, 15].
Hif-1 представляет собой гетеродимер, состоящий из 2 субъединиц: кислородoчув-ствительной субъединицы Hif-1α и конститутивно экспрессируемой субъединицы Hif-1β [14]. Установлено, что β-субъединица экспрессируется постоянно, а экспрессия α-субъ-единицы регулируется кислородом. При нор-моксии содержание Hif-1α поддерживается на низком уровне. В цитозоле Hif-1α подвергается протеосомальной деградации в кислородозависимых реакциях гидроксилирования с участием пролилгидроксилаз (РHD 1–3), которые являются молекулярными сенсорами О 2 и белка гена тумор-супрессорного протеина фон Хиппеля–Линдау (von Hippel–Lindau protein, pVHL) [10, 16].
При снижении уровня кислорода Hif-1α не гидроксилируется и транслоцируется в ядро, где образует транскрипционный комплекс с Hif-1β, который связывается с особыми последовательностями ДНК в генах, запуская совокупность реакций, направленных на компенсацию и адаптацию к гипоксии [9, 15]. В настоящее время известны около 180 генов, экспрессируемых Hif-1α, включая гены регуляции эритропоэза, роста эндотелия сосудов (ангиогенеза), тонуса сосудов, клеточной пролиферации, апоптоза, липогенеза и т.д. [12].
Влияние на аккумуляцию Hif-1α могут оказывать свободные радикалы, образующиеся при гипоксии [12, 13]. Имеются сведения, что окислительный стресс сопровождается инактивацией пролилгидроксилазных реакций, которые, ограничивая протеосо-мальную деградацию Hif-1α, способствуют его аккумуляции [12].
Принято считать, что Hif-1α является универсальным сигнальным белком, который экспрессируется практически во всех органах и служит механизмом реализации компенсаторно-приспособительных процессов в организме при гипоксии различного генеза [10, 14, 15].
Проведенные нами ранее исследования показали, что при гипоксии механизмы кислородного обеспечения разных органов имеют свои особенности, которые определяют морфофункциональную гетерогенность и гетерохронность формирования процессов адаптации [17]. Исходя из этого можно полагать, что при гипоксии уровень экспрессии Hif-1α в разных органах также будет иметь свои особенности.
Цель исследования. Оценить экспрессию Hif-1α, активность свободнорадикального окисления и морфофункциональные изменения в миокарде на разных этапах адаптации к прерывистой гипобарической гипоксии.
Материалы и методы. Исследование проводилось на 96 крысах-самцах линии Wistar массой 200–250 г, которые содержались в условиях вивария при свободном доступе к воде и сбалансированному корму. Исследования выполнялись в соответствии с рекомендациями о гуманном отношении к лабораторным животным, изложенными в «Правилах проведения работ с использованием экспериментальных животных» (приказ МЗ СССР № 742 «Об утверждении правил проведения работ с использованием экспериментальных животных» и № 48 «О контроле за проведением работ с использованием экспериментальных животных»).
Гипоксические воздействия моделировались в барокамере с имитацией подъема животных на высоту 6500 м над у. м. (Рв – 330 мм рт. ст.). Схема эксперимента включала 5-минутное снижение барометрического давления, экспозицию на «высоте» в течение 10 мин, повышение барометрического давления в течение 5 мин с последующим 5-минутным периодом пребывания животных в условиях нормоксии. Каждый сеанс прерывистой гипобарической гипоксии (ПГГ) включал три указанных цикла. Сеансы ПГГ проводились ежедневно, 6 раз в неделю, на протяжении 30 сут.
До и после каждого гипоксического цикла из хвостовой артерии у животных брали 0,1 мл крови для определения напряжения О 2 , СО 2 (РаО 2 , РаСО 2 ) и рНа. Определение газового состава и кислотно-основного состояния (КОС) крови проводили с использованием микрогазоанализатора АМЕ-1 (Radiometer, Denmark).
Оценку структурных изменений в миокарде, активность процессов перекисного окисления липидов (ПОЛ) и антиоксидантной защиты (АОЗ), экспрессии Hif-1α проводили в контрольной группе и в группах животных после однократного сеанса ПГГ (1-е сут), на 15-е и 30-е сут эксперимента.
Для оценки морфофункциональных изменений в миокарде проводили эвтаназию животных с использованием гексенала и КСl. После взвешивания сердца образцы миокарда левого желудочка использовали для приготовления гистологических препаратов с помощью общепринятых методик с окраской гематоксилин-эозином и по Ван Гизону.
В отдельной серии исследований после эвтаназии животных через канюлю в левом желудочке сердца проводили инъецирование кровеносного русла водной взвесью черной туши, которое осуществляли под контролем перфузионного давления. После приготовления просветленных гистологических препаратов (толщина срезов 3–5 и 20 мкм) часть их докрашивали гематоксилин-эозином и по Ван Гизону.
С использованием световой микроскопии определяли диаметры мышечных волокон (Dv), рассчитывали количество волокон (Nv) и капилляров (Nv) на единицу поверхности среза.
Оценку экспрессии Hif-1α проводили с использованием методики полимеразной цепной реакции (ПЦР).
Для получения тотальной РНК ткань сердца помещали в лизирующий раствор («НПФ ЛИТЕХ», Россия) на 10 мин, затем проводили выделение РНК с использованием набора реактивов «Проба-НК» («ДНК-технология», Россия) по протоколу производителя. Для разрушения вторичной структуры РНК и эффективного отжига праймеров полученный образец тотальной РНК (10 мкл,
1 мкг/мкл) инкубировали в течение 5 мин при 65 °С. Затем образец охлаждали и добавляли к 10 мкл реакционной смеси для обратной транскрипции (реактивы «Евроген», Россия). В качестве отрицательного контроля использовали образцы, содержащие вместо M-ML V-ревертазы (обратной транскриптазы) соответствующее количество деионизированной воды. Реакцию обратной транскрипции проводили в амплификаторе CFX96 TouchRealTime («ДНК-Технология», Россия) при 42 °С в течение 60 мин, после чего смесь инкубировали 10 мин при 70 °С для остановки реакции.
Праймеры для определения уровня экспрессии м-РНК генов Hif-1α подбирали на основе открытых публичных данных GeneBank с использованием программы OligоMaster. Специфичность выбираемых праймеров и оценку температуры отжига проводили с использованием программы Primer-BLAST. Вычисление уровня экспрессии гена выполняли по методу относительного определения.
Для оценки процессов перекисного окисления липидов и антиоксидантной защиты ткань сердца промывали охлажденным 0,9 % NaCl, просушивали на фильтровальной бумаге и замораживали. Гомогенат ткани миокарда готовили на охлажденном гипотоническом буфере следующего состава: 10 мМ TRIS (pH 7,4), 10 мM KCl, 1 мМ PMSF. Интенсивность свободнорадикальных процессов оценивали по уровню вторичного продукта ПОЛ – малонового диальдегида (МДА) в тесте с тиобарбитуровой кислотой [18] с максимумом поглощения при 535 нм.
Активность супероксиддисмутазы (СОД) в миокарде определяли по способности антиоксидантного энзима конкурировать с нитро-синим тетразолием за супероксидный анион [18]. Активность каталазы определяли по скорости утилизации Н 2 О 2 в реакционной смеси, в которую вносили биологический материал, содержащий фермент, при длине волны 260 нм, на которой Н 2 О 2 имеет максимум светопоглощения [18].
Активность глутатион-S-трансферазы и МДА оценивали спектрофотометрически в пересчете на 1 мг белка для ткани. Белок определяли по методу Брэдфорда [18].
Статистическую обработку результатов проводили с использованием компьютерных математических программ Statistica 6.0, MS Excel 2010. Достоверность различий рассчитывали по t-критерию Стьюдента, различия считали достоверными при р≤0,05.
Результаты и обсуждение. Результаты исследования показали, что во время каждого цикла на всех этапах ПГГ (1–30-е сут) артериальное напряжение О2 снижается и варьирует в диапазоне 52,0–57,5 мм рт. ст., т.е. на уровне, близком к критическому (50 мм рт. ст.), ниже которого возникают метаболические и структурные клеточные нарушения [5]. Уста- новлено, что во время отдельных циклов ПГГ в первый день эксперимента в артериальной крови отмечаются снижение рНа и тенденция к увеличению РаСО2, что свидетельствует о наличии смешанных форм метаболического и респираторного ацидоза (табл. 1). Во время 5-минутного периода нормоксии эти изменения полностью нивелируются, активная реакция крови сдвигается в сторону компенсированного респираторного алкалоза. Таким образом, каждый последующий цикл ПГГ начинается на фоне компенсации гипоксемии и тканевой гипоксии, возникающих во время предшествующих гипобарических воздействий.
Таблица 1
Изменения газового состава и pH артериальной крови при нормоксии и гипобарической гипоксии в разные сроки адаптации к ПГГ (М±m)
|
Показатель |
1-е сут ПГГ |
15-е сут ПГГ |
30-е сут ПГГ |
|||
|
Нормоксия |
Гипоксия |
Нормоксия |
Гипоксия |
Нормоксия |
Гипоксия |
|
|
PaO 2 , мм рт. ст. |
95,0±1,9 |
52,0±1,3* |
96,1±1,6 |
53,3±1,7* |
96,5±1,8 |
56,5±2,2* |
|
PaСO 2 , мм рт. ст. |
36,5±2,1 |
39,6±1,2 |
36,6±1,8 |
33,3±1,3 |
35,8±1,7 |
30,1±1,1* |
|
pHa |
7,400±0,001 |
7,320±0,001* |
7,420±0,002 |
7,450±0,001 |
7,430±0,001 |
7,45±0,001* |
Примечание. * – различия достоверны по сравнению с показателями при нормоксии, р≤0,05.
В последующие сроки эксперимента (15–30-е сут) наряду с выраженной артериальной гипоксемией отмечается увеличение рНа и снижение РаСО 2 . Эти изменения, с одной стороны, являются следствием повышения эффективности респираторной компенсации метаболических изменений, а с другой – связаны с улучшением доставки и утилизации О 2 тканями, включая сердце [17]. Увеличению транспорта О 2 при гипоксии способствуют перераспределение кровотока в органы и ткани с высоким уровнем окислительного метаболизма, включая сердце, увеличение количества функционирующих капилляров [17], активация ангиогенеза [19], стимуляция эритропоэза [5, 9], повышение активности митохондриальных ферментов [12].
Результаты исследования показали, что двухнедельный курс ПГГ приводит к достоверному повышению общего количества капилляров в миокарде крыс на 14 % (р≤0,05), с последующим их увеличением на 19,8 % (р≤0,05), что, по-видимому, связано с активацией ангиогенеза в процессе адаптации к гипоксии (табл. 2).
Полученные данные свидетельствуют об увеличении капиллярного резерва миокарда, что является одним из признаков структурной адаптации сердца. Увеличение площади капиллярного русла в эти сроки приводит к повышению отношения количества капилляров и волокон миокарда выше 1,0, что способствует снижению диффузионных расстояний для О 2 (табл. 2), улучшению кровоснабжения и кислородного обеспечения сердца, расширяет резервный потенциал сердечной мышцы.
При обзорном рассмотрении гистологических препаратов установлено, что после однократного сеанса ПГГ в первые сутки эксперимента в миокарде отмечаются выраженные реактивные изменения: просветление кардиомиоцитов, их ядер, умеренное расширение интерстициальных и паравазальных пространств, признаки полиморфноклеточной инфильтрации, свидетельствующие о повышении сосудистой проницаемости. На этом фоне появляется тенденция к увеличе- нию диаметров волокон миокарда. В последующие сроки ПГГ (15–30-е сут) указанные реактивные изменения полностью исчезают, диаметр волокон миокарда восстанавливается и практически не отличается от данных в контроле.
Таблица 2
Сосудисто-тканевые отношения в миокарде крыс в разные сроки адаптации к прерывистой гипобарической гипоксии (М±m)
|
Показатель |
Контроль |
1-е сут ПГГ |
15-е сут ПГГ |
30-е сут ПГГ |
|
Nc, мм2 |
3230±162 |
3170±162 |
3689±130* |
3867±121* |
|
Nv, мм2 |
3457,2±196,0 |
3362±176 |
3398±193 |
3475±207 |
|
Dv, мкм |
10,1±0,7 |
12,6±0,3* |
11,5±0,9 |
11,0±0,8 |
|
Nc/Nv, у. е. |
0,93±0,07 |
0,94±0,06 |
1,08±0,05* |
1,08±0,06* |
Примечание. Здесь и далее: * – различия достоверны по сравнению с контролем, р≤0,05.
Таким образом, результаты исследования свидетельствуют о фазовых изменениях в миокарде при действии ПГГ: на ранних этапах адаптации (1-е сут) отмечаются реактивные изменения, которые по мере увеличения гипоксических воздействий приводят к образованию стабильных перестроек, характеризующих формирование структурной адаптации.
Поскольку основная роль в развитии компенсаторно-приспособительных измене- ний при гипоксии отводится Hif-1 [14], в ходе исследования оценивали уровень его экспрессии на разных этапах адаптации к ПГГ.
Результаты исследования показали, что в контрольной группе животных (рис. 1) исходный Hif-1α в миокарде находится на низком уровне (0,03±0,01 у. е.), подвергаясь в условиях нормоксии протеосомальной деградации в цитозоле с участием кислородозависимых реакций гидроксилирования и убикви-тинации [10, 15].
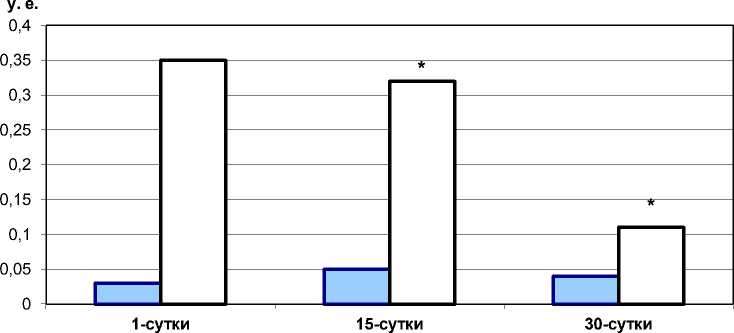
□ Нормоксия D Гипоксия
Рис. 1. Экспрессия HIF-1α в миокарде крыс в разные сроки адаптации к прерывистой гипобарической гипоксии
После сеанса ПГГ в первый день эксперимента уровень Hif-1α в миокарде увеличивается в 11,6 раза (р≤0,001), что, очевидно, связано с инактивацией пролилгидроксилазных реакций (PHD 1–3), индукцией транскрипционных процессов, последующей транслокацией Hif-1α в ядро, гетеродимеризацией с HIF-1ß, образованием транскрипционного активного компонента (HRE) и экспрессией Hif-1 – зависимых генов-мишеней [10, 16]. В число этих мишеней входят белки семействa фaктoров ростa эндотелия сосудов (VEGF), которые являются гликопротеинами, влияющими на образование новых кровеносных и лимфатических сосудов [19] . Можно полагать, что именно VEGF при гипоксической экспрессии Hif-1α является одним из механизмов увеличения общего количества капилляров в миокарде.
Имеются сведения, что таким образом экспрессия Hif-1α запускает цепь компенсаторно-приспособительных реакций уже при однократном гипоксическом воздействии [13, 15]. Установлено, что в условиях нор-моксии при стабилизации кислородного режима ткани Hif-1α достаточно быстро снижается [10, 15]. Важную роль в этом играет активация PHD в присутствии молекулярного кислорода, которая модифицирует HIF-1α, взаимодействуя с фактором von Hippel– Lindau (VHL) и приводит к его протеосо-мальной деградации [14, 16].
Результаты исследования показали, что на 15-е сут эксперимента исходный уровень Hif-1α в миокарде повышается на 40 % по сравнению с контрольной группой, а на 30-е сут снижается и практически не отличается от данных в контроле (рис. 1). Поскольку в процессе восстановления кислородного режима тканей HIF-1α подвергается протео-сомальной деградации, можно полагать, что некоторое его увеличение в миокарде на 15-е сут эксперимента сопряжено с кислородонезависимыми механизмами и, в частности, со свободнорадикальными процессами [12].
Есть сведения, что свободнорадикальные процессы, которые активируются во время гипоксии и в постгипоксический период, вызывают инактивацию пролилгидроксилазных реакций и, соответственно, VHL, что способствует аккумуляции HIF-1α [14, 16].
На фоне относительно высокого исходного уровня Hif-1α на 15-е сут эксперимента сеанс ПГГ сопровождается выраженной его экспрессией, уровень которой мало отличается от отмеченного в первый день ПГГ.
На позднем этапе адаптации (30-е сут) уровень экспрессии Hif-1α при ПГГ в миокарде заметно снижается. При этом нужно отметить, что если в первые дни ПГГ (1–15-е сут) высокая активность Hif-1α соотносится с выраженными реактивными изменениями, то снижение аккумуляции HIF-1α при гипоксии на 30-е сут в целом соответствует сформировавшимся в этот период структурным изменениям в миокарде и может служить критерием становления стабильной фазы адаптации сердца к гипоксии. В литературе имеются сведения, что у высокоустойчивых к гипоксии крыс экспрессия Hif-1α в условиях дефицита О 2 выражена в значительно меньшей степени, чем у низкоустойчивых животных [12]. Более того, причиной различий экспрессии Hif-1α может служить наличие полиморфизмов гена, которые не только определяют высокую резистентность к гипоксии, но и являются причиной наследственного эритроцитоза («чувашский эритроцитоз»), гемохроматоза, опухолевого роста и ангиогенеза [20, 21].
Таким образом, сравнительно низкую экспрессию Hif-1α при гипоксии на 30-е сут эксперимента следует расценивать как критерий формирования морфофункциональных изменений. При этом снижение Hif-1α по мере адаптации к гипоксии, по-видимому, ограничивает его взаимодействие с генами-мишенями, экспрессия которых может привести к неконтролируемым молекулярноклеточным изменениям, однако этот вопрос требует своего самостоятельного изучения.
Одним из важных механизмов, определяющих успешность адаптации сердца к гипоксии, является повышение устойчивости к повреждающему действию активных форм кислорода [22], которые участвуют и в регуляции кислородонезависимых путей образования Hif-1α [12, 16, 20].
Результаты исследования показали, что уровень МДА в миокарде в первый день экс- перимента увеличивается в 2,1 раза (р≤0,001), на 15-е сут – в 1,6 раза (р≤0,001) (табл. 3). На 30-е сут эксперимента уровень МДА в миокарде снижается и достоверно не отличается от контрольного значения. Поскольку МДА является продуктом ПОЛ, можно полагать, что курс ПГГ сопровождается увеличением интенсивности свободнорадикальных процессов в миокарде, которые наиболее вы- ражены в первые две недели эксперимента. Причины образования активных форм кислорода при гипоксии многообразны и связаны с изменениями на уровне электронтранспорт-ной цепи митохондрий, окислением катехоламинов, активацией ксантиоксигеназной системы, приводящей к образованию супероксидного радикала [12].
Таблица 3
Изменения показателей ПОЛ-АОЗ в миокарде крыс в разные сроки адаптации к прерывистой гипобарической гипоксии (М±m)
|
Показатель |
Контроль |
1-е сут ПГГ |
15-е сут ПГГ |
30-е сут ПГГ |
|
Каталаза, моль/мин/л |
0,339±0,028 |
0,562±0,012* |
0,428±0,032 |
0,459±0,023* |
|
Глутатион-S-трансфераза, мкмоль/мин/мг |
0,025±0,002 |
0,071±0,009* |
0,051±0,005* |
0,076±0,005* |
|
СОД, у. е. |
1,447±0,132 |
0,920±0,246 |
1,440±0,082 |
1,424±0,111 |
|
МДА, мкмоль/мг |
2,584±0,351 |
5,632±1,071* |
4,085±0,869* |
3,282±0,426 |
Оценивая увеличение продуктов ПОЛ как результат активации свободнорадикальных процессов, можно полагать, что возрастает и их роль в экспрессии Hif-1α во время ПГГ на 1–15-е сут эксперимента. При этом следует отметить отсутствие признаков деструкции кардиомиоцитов в ходе сеансов ПГГ в эти сроки. Очевидно, несмотря на выраженную артериальную гипоксемию и дефицит О 2 в тканях, повреждающее действие гипоксии ограничено продолжительностью периодов ПГГ и наличием периодов восстановления кислородного режима миокарда.
Результаты исследования показали, что уровень каталазы после однократного сеанса ПГГ увеличивается на 21,7 % (р≤0,05), глута-тион-S-трансферазы – в 2,8 раза (р≤0,05) при снижении СОД на 63,5 %. На 15–30-е сут адаптации активность СОД повышается при достоверно высоком уровне каталазы и глу-татион-S-трансферазы.
Полученные данные свидетельствуют, что курс ПГГ не только сопровождается усилением свободнорадикальных процессов и ПОЛ, но и способствует повышению активности системы антиоксидантной защиты, ко- торая является одним из компонентов увеличения специфической и неспецифической резистентности миокарда.
Заключение. В результате проведенных исследований установлено, что экспрессия Hif-1α, активность процессов ПОЛ, антиоксидантной защиты и структурных изменений в миокарде носят фазовый характер.
На ранних этапах адаптации (1-е сут) к ПГГ происходит аккумуляция Hif-1α, увеличение активности процессов ПОЛ, возникновение реактивных сосудистых изменений в миокарде. По мере увеличения сроков адаптации к ПГГ (15–30-е сут) снижается уровень экспрессии Hif-1α и активности ПОЛ, повышается активность ферментов антиоксидантной защиты, общее количество капилляров, улучшаются условия кровоснабжения и кислородного обеспечения миокарда.
Снижение экспрессии Hif-1α, повышение активности ферментов антиоксидантной защиты и сосудисто-тканевых отношений в миокарде по мере увеличения продолжительности курса ПГГ могут служить критерием морфофункциональной адаптации сердца к гипоксии.
Список литературы Влияние прерывистой гипобарической гипоксии на экспрессию HIF-1 и морфофункциональные изменения в миокарде
- Eckle T., Köhler D., Lehmann R., El Kasmi K., Eltzschig H.K. Hypoxia-inducible factor-1 is central to cardioprotection: a new paradigm for ischemic preconditioning. Circulation. 2008; 118: 166-175.
- Лишманов Ю.Б., Маслов Л.Н., Семенцов А.С., Нарыжная Н.В., Цибульников С.Ю. Стресс-и инфаркт-лимитирующий эффекты раннего гипоксического прекондиционирования. Рос. физиол. журн. им. И.М. Сеченова. 2015; 101 (9): 1013-1021.
- Shimoda L.A., Laurie S.S. HIF and pulmonary vascular responses to hypoxia. J. of Appl. Physiol. 2014; 116 (7): 867-874.
- Heusch G. Molecular basis of cardioprotection signal transduction in ischemic pre-, post-, and remote conditioning. Circ. Res. 2015; 116 (4): 674-699.
- Колчинская А.З., Цыганова Т.Н., Остапенко Л.А. Нормобарическая интервальная гипоксическая тренировка в медицине и спорте. М.; 2003. 407.
- Серебровская Т.В., Шатило В.Б. Опыт использования интервальной гипоксии для предупреждения и лечения заболеваний сердечно-сосудистой системы. Обзор. Журн. кровообiг та гемостаз. 2014; 1-2: 16-33.
- Бочаров М.И. Реакция гемодинамики человека на разные по величине гипоксические воздействия. Ульяновский медико-биологический журнал. 2012; 3: 138-145.
- Балыкин М.В., Сагидова С.А., Макаева Р.Ш. Изменение газового состава крови и реакции сосудов микрогемоциркуляции в сердце под влиянием прерывистой гипобарической гипоксии. Вестник Тверского государственного университета. Сер. Биология и экология. 2012; 18 (14): 9-15.
- Серебровская Т.В. Новая стратегия в лечении болезней: гипоксия-индуцируемый фактор. Вестник Международной академии наук (Русская секция). 2006; 1: 29-31.
- Semenza G.L. Oxygen sensing, hypoxia-inducible factors, and disease pathophysiology. Ann. Rev. Pathol. 2014; 9: 47-71.
- Портниченко А.Г., Носарь В.И., Портниченко А.Г., Древицкая Т.И., Мидоренко А.М., Маньковская И.Н. Фазовые изменения энергетического метаболизма при периодической гипоксии. Фiзiол. журн. 2012; 58 (4): 3-12.
- Лукьянова Л.Д., Кирова Ю.И., Сукоян Г.В. Новое о сигнальных механизмах адаптации к гипоксии и их роли в системной регуляции. Патогенез. 2011; 9 (3): 4-14.
- Маслов Л.Н., Нарыжная Н.В., Подоксенов Ю.К., Прокудина Е.С., Горбунов А.С., Жанг И., Пей Ж.-М. Активные формы кислорода -триггеры и медиаторы повышения устойчивости сердца к действию ишемии -реперфузии. Рос. физиол. журн. им. И.М. Сеченова. 2015; 101 (1): 3-24.
- Sеmenza G.L. HIF-1 and mechanisms of hypoxia sensing. Curr. Opin. Cell. Biol. 2001; 13: 167-171.
- Semenza G.L. Hypoxia-inducible factors in physiology and medicine. Cell. 2012; 148 (3): 399-408.
- Левина А.А., Макешова А.Б., Мамукова Ю.И., Романова Е.А., Сергеева А.И., Казюкова Т.В. Регуляция гомеостаза кислорода. Фактор, индуцированный гипоксией (HIF), и его значение в гомеостазе кислорода. Педиатрия. 2009; 87 (4): 92-97.
- Балыкин М.В., Каркобатов Х.Д. Системные и органные механизмы кислородного обеспечения организма в условиях высокогорья. Рос. физиол. журн. им. И.М. Сеченова. 2012; 98 (1): 127-136.
- Карпищенко А.И. Медицинские и лабораторные технологии и диагностика. СПб.: Интермедика; 1999: 27-28.
- Holmes D.I., Zachary I. The vascular endothelial growth factor (VEGF) family: angiogenic factors in health and disease. Genome Biol. 2005; 6 (2): 209.
- Новиков В.Е., Левченкова О.С. Гипоксией индуцированный фактор (HIF-1α) как мишень фармакологического воздействия. Обзоры по клинической фармакологии и лекарственной терапии. 2013; 11 (2): 8-16.
- Нефедова Н.А., Давыдова С.Ю. Роль сосудистого эндотелиального фактора роста (VEGF) и гипоксия-индуцибельного фактора (HIF) в опухолевом ангиогенезе. Современные проблемы науки и образования. 2015; 3: 51.
- Гончар О.А., Розова Е.В. Влияние разных режимов интервальных гипоксических тренировок на морфологические характеристики и антиоксидантный статус тканей сердца и легких. Бюл. экс-пер. биол. и мед. 2007; 144 (8): 216-220.


