Влияние продолжительности ферментолиза на свойства белковых гидролизатов
Автор: Зотова Кира Вениаминовна, Кучина Юлия Анатольевна, Широнина Анастасия Юрьевна, Новиков Виталий Юрьевич, Деркач Светлана Ростиславовна
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Статья в выпуске: 1 т.15, 2012 года.
Бесплатный доступ
Изучены физико-химические свойства ферментативных белковых гидролизатов. Показано, что с увеличением продолжительности процесса гидролиза вязкость гидролизатов уменьшается. Ферментативный гидролиз в течение 60 мин приводит к накоплению в гидролизате белковых фрагментов с молекулярной массой не более 100 кД.
Ферментативный гидролиз, белковый гидролизат, степень гидролиза, вязкостные свойства, электрофорез, молекулярная масса
Короткий адрес: https://sciup.org/14294410
IDR: 14294410
Текст научной статьи Влияние продолжительности ферментолиза на свойства белковых гидролизатов
Одним из перспективных направлений мирового научно-технического прогресса в области изыскания новых материалов биологического происхождения за последние десятилетия является изучение свойств хитина и хитозана, а также способов их получения и переработки – с целью создания на их основе биологически активных и медицинских препаратов различного назначения.
Потенциальные источники хитина многообразны и широко распространены в природе. Хитин, входящий в состав панцирей ракообразных, рассеян в мировом океане, и его сбор в промышленных масштабах связан с утилизацией отходов переработки промысловых ракообразных. В России массовым источником хитинсодержащего сырья являются промысловые крабы на Дальнем Востоке, а также северная розовая креветка и акклиматизированный в Баренцевом море камчатский краб ( Немцев , 2006).
Хитин является одним из основных источников промышленного получения ценного для медицинских целей вещества – D(+)-глюкозамина гидрохлорида (ГлАXHCl). Многие лекарственные препараты и биологически активные добавки содержат в своем составе этот моносахарид в качестве основы. До недавнего времени в России единственным лицензированным производителем субстанции ГлА XHCl была фирма ООО "НТЦ Экобиотек-Мурманск". После проведения клинических испытаний на эту субстанцию были получены фармакопейная статья (ВФС 42-3512-99) и разрешение для применения в России.
Одним из основных методов получения D(+)-глюкозамина гидрохлорида является химический кислотный гидролиз хитина. При полном гидролизе хитина в концентрированной хлороводородной кислоте образуется деацетилированный мономер ГлАXHCl, что обычно используют для его промышленного получения.
Целью данной работы является совершенствование технологии получения D(+)-глюкозамина гидрохлорида. Для повышения выхода D(+)-глюкозамина гидрохлорида было изучено влияние степени деацетилирования хитина на скорость и глубину кислотной деструкции этого полисахарида.
условиях (в 50 % NaOH, при температуре 98-99 C, 1 ч). В работе (Чеботок и др., 2006) было установлено, что в условиях стандартного деацетилирования степень полимеризации хитина и хитозана практически не изменяется.
Содержание D(+)-глюкозамина гидрохлорида в гидролизатах определяли по методике Эльсона и Моргана ( Rondle, Morgan , 1955).
Деацетилирование хитина и хитозана проводили в 50%-ном растворе NaOH при 100 C. Образцы с разными степенями деацетилирования получали из хитина и хитозана повторными обработками 50%-ной NaOH при температуре 100 C.
Хитин ацетилировали уксусным ангидридом. Для этого одну часть (100 г) хитина заливали десятью частями (1 л) 20 % раствора уксусного ангидрида в этаноле, тщательно перемешивали в течение 2-3 ч и оставляли при 4 С в течение 24 ч при периодическом перемешивании. По окончании реакции в раствор добавляли 2 л воды, доводили раствор до рН 7 при помощи 1 н NaOH, фильтровали и несколько раз промывали ацетилированный хитин дистиллированной водой. Затем образцы сразу подвергали кислотному гидролизу или предварительно высушивали при температуре не выше 60 C.
Степень ацетилирования определяли методом ИК-спектрофотометрии ( Чеботок и др. , 2007).
Идентификацию и характеристику качества препарата D(+)-глюкозамина проводили в соответствии с фармакопейной статьей ВФС 42-3512-99 (Глюкозамина гидрохлорид. Glucosamini hydrochloridum (2-дезокси-2-амино-р-D-глюкозы гидрохлорид).
В научной литературе обсуждается, что гликозидные связи у второго углеродного атома деацетилированного мономерного звена частично деацетилированного хитина (или хитозана) подвергаются кислотной деструкции с меньшей скоростью, чем такие же связи у ацетилированного звена (рис. 1) ( Varum , 2001).
Данное явление объясняется тем, что аминогруппа у второго атома углерода, заряженная положительно в условиях кислотно-катализируемого гидролиза понижает электронную плотность на гликозидном центре, тем самым дестабилизирует образующиеся по механизму реакции промежуточные интермедиаты – кaрбокатионы и сдвигает равновесие в сторону негидролизованного продукта. С другой стороны, ацетилирование амингруппы у второго углеродного атома ускоряет гидролиз гликозидов за счет повышения электронной плотности на реакционном центре и за счет анхимерного содействия N-ацетильной группы (Varum, 2001).
В случае ацетамидной группы на кислородном атоме есть свободная пара электронов, которая может участвовать во взаимодействии с положительно заряженным гликозидным углеродным атомом, приводя к стабилизации карбокатиона, снижению вероятности смещения реакции в сторону исходных продуктов и, следовательно, к увеличению скорости прямой реакции гидролиза (Ганстон и др., 1986).
Следует отметить, что количественная характеристика этих процессов в рамках химической кинетики в литературе не обсуждается.
Из литературных данных известно, что скорость кислотной деструкции резко уменьшается с увеличением начальной степени деацетилирования хитина ( Новиков , 2004). Это приводит к снижению выхода мономера D(+)-глюкозамина и увеличению выхода побочных продуктов.
С целью математического моделирования процесса деструкции был изучен гидролиз хитина при 50 C в хлороводородной кислоте различной концентрации.
Механизм процесса деструкции хитина может быть описан следующими параллельно протекающими элементарными реакциями первого порядка с константами скоростей ( k ): 1 – гидролиз гликозидных связей у ацетилированного звена (константа реакции k 1); 2 – гидролиз гликозидных связей у деацетилированного звена (константа
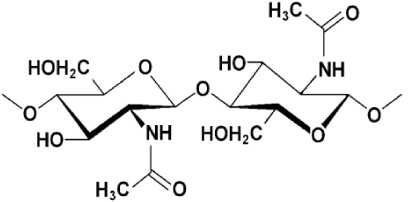
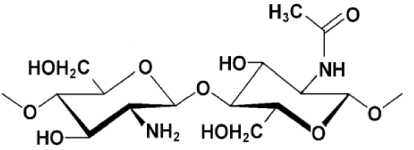
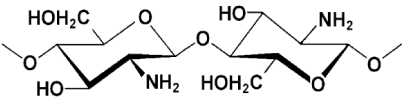
в)
Рис. 1. Структурная формула хитина (а), частично деацетилированного хитина (б) и хитозана (в)
реакции k 2); 3 – реакция деацетилирования (константа реакции k 3).
Решение системы дифференциальных уравнений, описывающих предложенный механизм, позволило с помощью программы Maple 13 (Waterloo Maple Inc.) получить аналитическое выражение для кинетики деструкции, из которого мы оценили константы скоростей реакций ( k 1, k 2 и k 3) (табл. 1).
Таблица 1. Константы скорости реакций расщепления гликозидных связей и амидной связи в молекуле хитина, рассчитанные по модели
|
С (HCl), моль/л |
k 1 |
k 2 |
k 3 |
|
0.5 |
0.0272 |
0.00077 |
0.0601 |
|
1 |
0.0829 |
0.00205 |
0.0160 |
|
2 |
0.1300 |
0.00214 |
0.0720 |
Используя полученные константы скорости элементарных реакций, были построены кинетические кривые деструкции хитина/хитозана с различной начальной степенью деацетилирования. В качестве примера на рис. 2 приведены кинетические кривые деструкции хитина в хлороводородной кислоте с концентрацией 1.0 моль/дм3 (для концентраций кислоты 0.5 моль/дм3 и 2.0 моль/дм3 получены аналогичные зависимости).
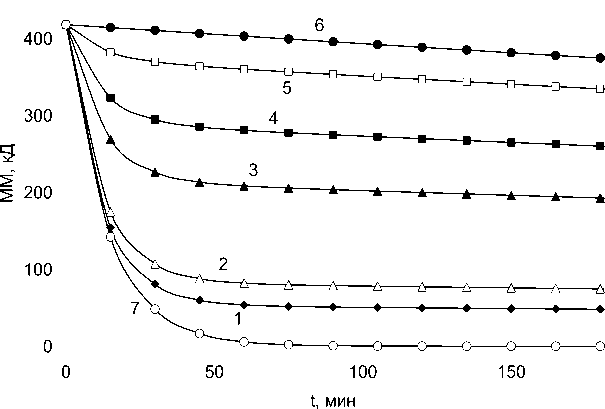
Рис. 2. Кинетические кривые деструкции хитина в 1 н. HCl при 50 C, рассчитанные по математической модели. Начальная степень деацетилирования хитина:
0 % (1), 10 % (2), 50 % (3), 70 % (4), 90 % (5) и 100 % (6). Кинетическая кривая 7 описывает деструкцию хитина без учета реакции деацетилирования
Из данных, приведенных на рис. 2, следует, что деацетилирование хитина в процессе кислотного гидролиза ведет к заметному уменьшению скорости деструкции. Как показывают расчеты, даже при степени деацетилирования 10 % после гидролиза остаются фрагменты олигосахаридов с молекулярной массой около 50 кДа.
Известные технологии получения D(+)-глюкозамина гидрохлорида заключаются в полной кислотной деполимеризации хитина, выделении полученного продукта из гидролизата и его очистки ( Новиков, 1997; 1999).
В качестве сырья обычно используется хитин, полученный по технологии, включающей депротеинизацию горячим раствором щелочи (обычно 4%-ным раствором NaOH) и раствором минеральной кислоты (обычно 3.5-7%-ным раствором HCl) при комнатной температуре ( No, Meyers , 1995).
Анализ образцов хитина и данные, приведенные в научной литературе, показали, что хитин, полученный известным в литературе способом, имеет исходную степень деацетилирования около 15 %. Это объясняется тем, что в процессе получения хитина как при щелочной обработке, так и при кислотной, происходит гидролиз ацетамидных связей, вызывающий повышение степени деацетилирования полисахарида. Следует отметить, что в зависимости от свойств хитинсодержащего сырья и режимов технологической обработки степень деацетилирования промышленных образцов хитина может достигать 30 %.
Различными способами ( Новиков, Иванов , 1995; Казаков и др. , 1995) был получен D(+)-глюкозамина гидрохлорид из исходного и предварительно ацетилированного хитина и рассчитан его выход.
Получение D(+)-глюкозамина гидрохлорида состояло из следующих основных операций:
-
- способ 1: гидролиз хитина в концентрированной хлороводородной кислоте, добавление активированного угля, фильтрование гидролизата, упаривание, промывка кристаллов D(+)-глюкозамина и сушка;
-
- способ 2: гидролиз хитина в HCl, охлаждение гидролизата и кристаллизация D(+)-глюкозамина гидрохлорида, фильтрование, растворение осадка в воде, добавление активированного угля, фильтрование, упаривание, промывка кристаллов, сушка;
-
- способ 3: гидролиз хитина в концентрированной HCl, охлаждение гидролизата и кристаллизация D(+)-глюкозамина гидрохлорида, фильтрование, промывка осадка этанолом, растворение в воде, фильтрование, упаривание, промывка, сушка;
-
- способ 4: влажный хитин гидролизовали раствором хлороводородной кислоты, насыщенной газообразным хлороводородом.
Выход D(+)-глюкозамина гидрохлорида, полученного различными способами из исходного и предварительно ацетилированного хитина, приведен в табл. 2.
Таблица 2. Влияние способа получения на выход D(+)-глюкозамина гидрохлорида
|
№ способа |
Выход D(+)-глюкозамина гидрохлорида, % |
|
|
из исходного хитина |
из предварительно ацетилированного хитина |
|
|
1 |
69 |
81 |
|
2 |
74 |
86 |
|
3 |
76 |
87 |
|
4 |
72 |
82 |
Из табл. 2 следует, что при предварительном ацетилировании исходного хитина перед кислотным гидролизом выход D(+)-глюкозамина гидрохлорида увеличивается по сравнению с неацетилированным хитином на 10-12 %. Это позволяет сделать вывод о том, что ацетилирование можно использовать для предварительной подготовки хитина перед кислотным гидролизом. Особенно это важно в том случае, если используется хитин различного происхождения, который может содержать партии полисахарида с различной исходной степенью деацетилирования.
Использование влажного ацетилированного хитина для получения глюкозамина гидрохлорида по способу 4, затруднено наличием в нем после фильтрования около 70 % воды, что ведет к уменьшению выхода готового продукта почти на 10 %. В этом способе практически теряется выигрыш в выходе продукта за счет ацетилирования исходного хитина.
Усовершенствованная технология получения ГлАхHCl из предварительно ацетилированного хитина заключается в следующем. В реактор загружали 20%-й раствор ацетилирующего агента в этаноле. Раствор охлаждали до температуры 4± 1OC, затем в раствор загружали при перемешивании исходный хитин, соответствующий ТУ 9228-001-04703997-93 "Хитин из панциря крабов". Соотношение масс хитина и ацетилирующего агента - 1:10. Смесь тщательно перемешивали в течение 2-3 ч и оставляли при температуре 4±1 °С в течение 24 ч при периодическом перемешивании.
По окончании процесса ацетилирования в реакционную смесь добавляли дистиллированную воду (соотношение масс хитина и воды 1:20) и нейтрализовали раствор 4%-ным раствором гидроксида натрия до рН реакционной среды 7±0.5. Смесь фильтровали на закрытом нутч-фильтре через 2-3 слоя фильтровальной бумаги. Далее ацетилированный хитин обрабатывали в соответствии с известной технологией.
D(+)-глюкозамина гидрохлорид, полученный из предварительно ацетилированного хитина, представляет собой белый кристаллический порошок без запаха, не гигроскопичный, остаточная влажность 0.5 % зольный остаток менее 0.1 %. Температура разложения (почернения пробы) 195-200 ОС, рН 3.5-4.5 водного 20%-ного раствора при 20 ОС. Массовая доля D(+)-глюкозамина гидрохлорида в продукте, полученном из предварительно ацетилированного хитина, составляет 99.5-99.9 %.
Для характеристики D(+)-глюкозамина гидрохлорида в качестве стандарта использовали препарат по ТУ 6-09-05-936-78 (D(+)-глюкозамина гидрохлорид квалификации "чистый") и препарат, полученный по фармокопейной статье ВФС 42-3512-99 (Глюкозамина гидрохлорид. Glucosamini hydrochloridum (2-дезокси-2-амино-р-D-глюкозы гидрохлорид)).
Определение оптимальных технологических параметров процесса получения глюкозамина из предварительно ацетилированного хитина было проведено с использованием метода планирования эксперимента. В качестве функции отклика V был выбран выход D(+)-глюкозамина гидрохлорида, в качестве влияющих факторов – концентрация кислоты (С) и степень деацетилирования хитина (DD). Математическая модель, описывающая процесс гидролиза D(+)-глюкозамина гидрохлорида, была получена с помощью компьютерной программы STATISTICA Ver. 8.0 (StatSoft., Inc.), позволяющей получить уравнение регрессии, связывающее функцию отклика с выбранным количеством влияющих факторов.
В результате расчетов получено следующее уравнение регрессии процесса кислотного гидролиза хитина с целью получения D(+)-глюкозамина гидрохлорида:
V = 11,85 – 1,89 × DD – 0,37 × DD2+ 5,29 X C – 0,09 × C2.
Поверхность функции отклика V в зависимости от влияющих факторов представлена на рис. 3.
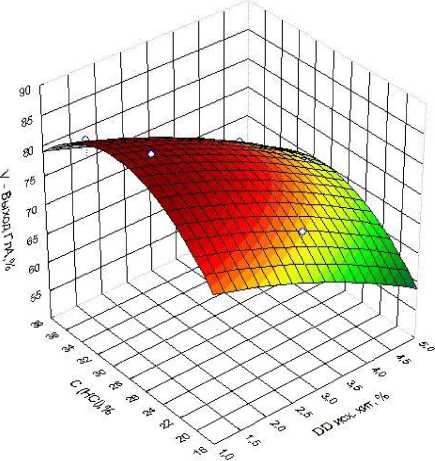
Рис. 3. Поверхность функции отклика в зависимости от влияющих факторов. V – выход D (+)-глюкозамина гидрохлорида, С – концентрация кислоты, DD – степень диацетилирования хитина
Анализ поверхности функции отклика показал, что оптимальное значение степени деацетилирования исходного хитина (DD) – менее 3 %, концентрации HCl (C) – 28-29 %.
Были получены значения влияющих факторов, соответствующие максимальному выходу D(+)-глюкозамина гидрохлорида. В точке оптимума был поставлен контрольный опыт, который подтвердил хорошую сходимость расчетного значения функции отклика с экспериментальным значением. Расчетное значение функции отклика, соответствующее найденным оптимальным значениям влияющих факторов, составляет 85.74 %. Экспериментальное значение – 86 %, что хорошо совпадает с расчетным, подтверждая адекватность модели.
-
3. Выводы
-
1. Показано, что предварительное ацетилирование хитина до 96-97 % увеличивает скорость его кислотного гидролиза, скорость образования и выход мономера ГлАXHCl на 10-12 %. Экспериментально подтверждено, что скорость деструкции и полной деполимеризации хитина и хитозана возрастает с уменьшением степени деацетилирования.
-
2. Разработана математическая модель, адекватно описывающая процесс гидролиза предварительно ацетилированного хитина. Определены близкие к оптимальным условия производства ГлА XHCl из предварительно ацетилированного хитина.
Научно-исследовательская работа выполнена в рамках реализации ФПЦ "Научные и научнопедагогические кадры инновационной России на 2009-2013 годы".


