Влияние производителя противотуберкулёзных препаратов на частоту развития нежелательных явлений
Автор: Токтоналиева Н.У., Токтоналиев И.У.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 3 т.12, 2026 года.
Бесплатный доступ
Проведён анализ частоты нежелательных явлений (НЯ), ассоциированных с противотуберкулёзными препаратами (ПТП), поступивших в национальную систему фармаконадзора в период с 2023 по 2024 год. Основное внимание уделено распределению НЯ в зависимости от производителя препарата. Полученные данные свидетельствуют о значительной вариабельности частоты НЯ в зависимости от страны и компании-производителя. Преобладание сообщений о НЯ, связанных с определёнными производителями, требует дальнейшего изучения профиля безопасности, биоэквивалентности и производственных характеристик препаратов. Оценка причинно-следственной связи между применением препарата и развитием НЯ проводилась в соответствии с классификацией ВОЗ (WHO-UMC), и в большинстве случаев отнесена к категории «возможная» или «условная».
Туберкулёз, фармаконадзор, нежелательные явления, производитель, противотуберкулёзные препараты
Короткий адрес: https://sciup.org/14134715
IDR: 14134715 | УДК: 615.065:616-002.5 | DOI: 10.33619/2414-2948/124/33
Influence of Anti-Tuberculosis Medicines Manufacturer on the Incidence of Adverse Events
An analysis of the frequency of adverse events (AEs) associated with anti-tuberculosis drugs (ATDs) reported to the national pharmacovigilance system between 2023 and 2024 was conducted. The focus was on the distribution of AEs by drug manufacturer. The data obtained indicate significant variability in the frequency of AEs depending on the country and manufacturer. The predominance of AE reports associated with certain manufacturers requires further study of the safety profile, bioequivalence, and manufacturing characteristics of these drugs. The causal relationship between drug use and the development of AEs was assessed in accordance with the WHO-UMC classification and was categorized, in most cases, as "possible" or "conditional".
Текст научной статьи Влияние производителя противотуберкулёзных препаратов на частоту развития нежелательных явлений
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 615.065:616-002.5
Туберкулёз (ТБ) по-прежнему остаётся одной из ведущих причин смертности от инфекционных заболеваний в мире. По данным Всемирной организации здравоохранения
(ВОЗ), в 2023 году туберкулёз был диагностирован у более чем 10,6 млн человек, при этом около 1,3 млн случаев завершились летально [1, 2].
Важным аспектом в лечении туберкулёза является безопасность и переносимость противотуберкулёзной терапии, особенно на фоне увеличения доли лекарственно-устойчивых форм заболевания [3].
Противотуберкулёзные препараты (ПТП), особенно при длительном и комбинированном применении, часто вызывают широкий спектр НЯ, которые могут стать причиной снижения приверженности лечению, временной или полной отмены терапии, а также ухудшения прогноза заболевания [4].
Кроме того, значительную роль в профиле безопасности лекарственных средств играет производитель, что связано с различиями в качестве сырья, технологиях производства, контроле качества, а также биоэквивалентности дженериков по сравнению с оригинальными препаратами [5-8].
В последние годы на фармацевтическом рынке наблюдается активное использование дженериков, выпускаемые различными производителями с развивающейся экономикой, которые, могут обладать различным профилем безопасности. Это обусловлено их доступностью и включением в государственные программы лечения туберкулёза. Однако, как показывают данные фармаконадзора, препараты разных производителей могут демонстрировать различную частоту и тяжесть побочных эффектов [9-12].
Таким образом, систематический мониторинг сообщений о НЯ, связанных с применением ПТП разных производителей, является актуальной задачей для оптимизации схем лечения, повышения безопасности терапии и рационального выбора препаратов.
Цель настоящего исследования — проанализировать частоту и структуру НЯ, зарегистрированных при применении ПТП различных производителей, с учётом возможной причинно-следственной связи в соответствии с классификацией ВОЗ.
Материалы и методы исследования
В ходе ретроспективного анализа изучены карт-извещений о НЯ, поступившие в отдел фармаконадзора и рекламы департамента лекарственных средств и медицинских изделий министерства здравоохранения Кыргызской Республики ( ДЛС и МИ МЗКР) в период с января 2023 года по декабрь 2024 года. Всего было принято в обработку 1152 карты, касающиеся применения ПТП. Для оценки причинно-следственной связи между применением лекарственного средства и развитием НЯ использована классификация ВОЗ (WHO-UMC). В условиях отсутствия полной клинической информации и результатов лабораторной верификации сообщения были отнесены преимущественно к категориям возможной (Possible) и условной (Conditional/Unclassified) связи.
Статистическая обработка данных осуществлялась с использованием программного обеспечения Excel 365 и SPSS Statistics 26.0.
Критерии включения: сообщения о НЯ, связанных с применением ПТП у пациентов, получающих лечение в рамках государственной программы противотуберкулёзной помощи; указание производителя препарата в извещении.
Критерии исключения: карты-извещения с неполными данными.
Результаты исследования
В исследовании представлены данные о частоте НЯ, ассоциированных с препаратами различных производителей. Лидирующее место занимает российская компания АО «Фармасинтез», на препараты которой приходится 48% всех зарегистрированных НЯ. Это возможно связано как объёмами поставок и широким применением в рамках государственной программы лечения туберкулёза, так и характеристиками производственного процесса.
На втором месте находится индийская компания Hetero Labs Limited (15,3%), далее следуют Rhydburg Pharmaceuticals Ltd (12,7%) и Macleods Pharmaceuticals LTD (7,5%), что свидетельствует о значительной поставке ПТП индийских производителей в фармацевтический рынок. Общий вклад производителей из Индии составляет более 40%, что подчёркивает необходимость особого внимания к качеству и биоэквивалентности индийских дженериков. Компании из Европы и других стран (Novartis — Швейцария, Catalent — Германия, Janssen — Бельгия, DONG-A ST — Китай) демонстрируют существенно более низкие показатели побочных реакций. Однако низкий процент может отражать не только лучшую переносимость, но и меньшие объёмы применения этих препаратов в выборке (Рисунок).
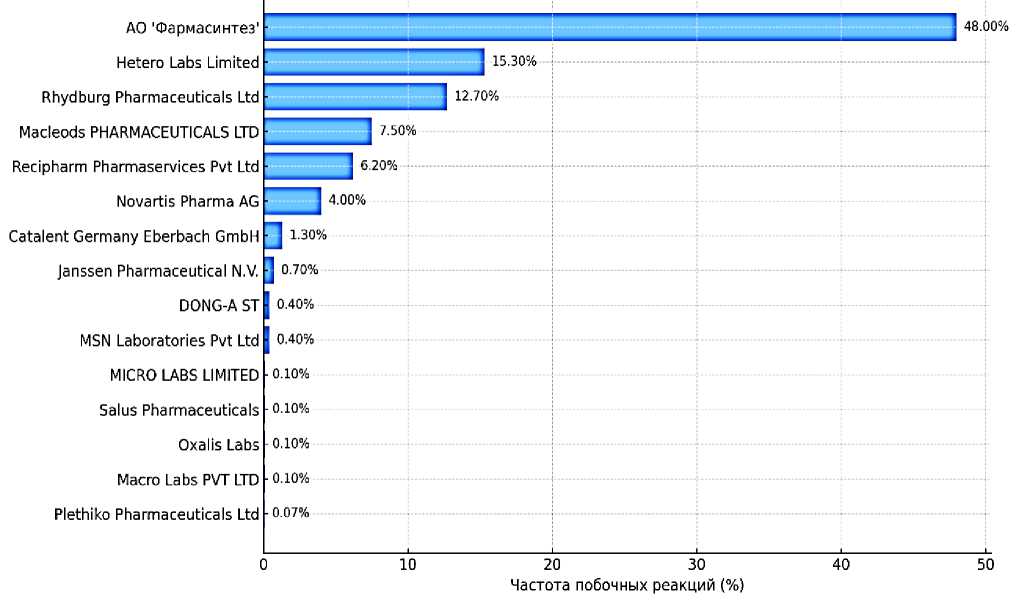
Рисунок. Распределение побочных реакций по производителям ПТП
Согласно полученным данным, общее количество зарегистрированных случаев НЯ при применении бедаквилина (Sirturo) составило 93 случая. Наибольшее количество осложнений зафиксировано у пациентов, получавших препарат, произведённый компанией Recipharm Pharmaservices Private Limited (Индия). На долю данного производителя приходится 83 случаев НЯ, что составляет 89,2% от общего числа зарегистрированных НЯ на данный препарат, что может свидетельствовать о более высокой общей частоте нежелательных явлений по сравнению с другими производителями. После применения Бедаквилина (Sirturo), произведенного Janssen Pharmaceutical N.V. (Бельгия), было зафиксировано 10 случаев НЯ, что составляет 10,8%. Установление достоверной причинной связи невозможно из-за отсутствия полной информации, поэтому сообщения классифицируются как возможные (Possible) .
В результате проведённого анализа частоты НЯ при применении циклосерина (Кансамин) свидетельствуют о наличии существенных различий в зависимости от производителя препарата. Препарат производства Macleods Pharmaceuticals Ltd. (Индия) оказался ассоциирован с наибольшим числом неблагоприятных реакций — 76,1% (n=51) от общего числа зарегистрированных случаев. Это может указывать на менее благоприятный профиль безопасности по сравнению с препаратами других производителей.
В то же время препараты, произведённые АО «Фармасинтез» (Россия) и DONG-A ST (Китай), демонстрировали значительно меньшую частоту НЯ — 15% (n=10) и 8,9% (n=6) соответственно. Учитывая разницу в частоте, возможно наличие вариабельности профиля безопасности, однако без фармакокинетической и лабораторной информации связь оценивается как условная (Conditional).
Общее число зарегистрированных случаев НЯ при применении клофазимина (Лапреме) составило 76. Наибольшее количество осложнений было связано с применением оригинального препарата, произведённого компанией Novartis Pharma AG (Швейцария) — 54 случаев (71%). Несмотря на высокий процент, это возможно обусловлено большей распространённостью клинического применения данного препарата. Второе место по частоте НЯ занял препарат производства Catalent Germany Eberbach GmbH (Германия), с 18 зарегистрированными случаями (23,7%). Наименьшее количество НЯ отмечено при применении Клофазимина, произведённого Macleods Pharmaceuticals Ltd. (Индия) — 4 случая (5,3%). Несмотря на высокую частоту НЯ у оригинального препарата, это может отражать масштаб его применения. Связь оценивается как возможная .
С применением линезолида было зарегистрировано 214 случаев НЯ, поступивших от различных производителей. Существенное большинство осложнений — 205 случаев (95,8%) — зарегистрировано у пациентов, получавших препарат, произведённый компанией Hetero Labs Limited (Индия). Продукция других производителей была представлена меньшим количеством зарегистрированных побочных эффектов. Так, препарат Macleods pharmaceuticals LTD (Индия) ассоциировался с 4 случаями (1,9%), АО «Фармасинтез» (Россия) — с 3 случаями (1,4%), а препарат производства Macro Labs PVT LTD (Индия) — с 2 случаями (0,9%). Преобладание сообщений по Hetero Labs требует дополнительной оценки профиля безопасности, однако причинная связь классифицируется как возможная.
В ходе анализа было зарегистрировано 65 случаев НЯ, связанных с применением пиразинамида, различного производства. Препарат, произведённый АО «Фармасинтез» (Россия), составил подавляющее большинство зарегистрированных реакций — 57 случаев (87,7%).
Препараты других производителей встречались значительно реже. В частности, на продукцию Macleods pharmaceuticals LTD (Индия) приходилось 5 случаев (7,7%), на Oxalis Labs (Индия) — 2 случая (3,1%), и только 1 случай (1,5%) был зарегистрирован при применении препарата Plethiko Pharmaceuticals Limited (Индия, Montozin 500). Связь между препаратом и НЯ может быть возможной, требует фармаконадзорной верификации.
По результатам анализа было зарегистрировано 193 случая НЯ, связанных с применением левофлоксацина. Наибольшее число реакций — 171 случай (88,6%) — связано с приёмом препарата, произведённого Rhydburg Pharmaceuticals Ltd (Индия). Препарат от Macleods Pharmaceuticals LTD (Индия) ассоциировался с 15 случаями (7,8%), продукция АО «Фармасинтез» (Россия, Иркутск) — с 5 случаями (2,5%), а MICRO LABS LIMITED (Индия) — с 2 случаями (1,1%). Высокий процент сообщений по одному производителю требует внимания, но причинная связь остаётся неподтверждённой (Conditional) .
В отношении моксифлоксацина общее число зафиксированных НЯ составило 30 случаев. Препарат Macleods Pharmaceuticals LTD (Индия) показал наибольшую долю зарегистрированных реакций — 22 случая (73%), препарат MSN Laboratories Private Limited

(Индия, торговое наименование «Стаксом») — 6 случаев (20%), и Salus Pharmaceuticals (Индия, «Аквамокс») — 2 случая (7%). Сообщения носят характер возможных, с необходимостью дальнейшего фармаконадзора.
Эти данные подчёркивают необходимость систематического мониторинга переносимости фторхинолонов разных производителей, особенно с учётом их широкого применения в схемах лечения туберкулёза с множественной лекарственной устойчивостью.
Среди зарегистрированных НЯ, связанных с препаратами российского производства (АО «Фармасинтез»), наибольшее число случаев было связано с комбинированным противотуберкулёзным препаратом протуб 4 — 440 зарегистрированных НЯ. Применение протуб 2 сопровождалось 22 случаями НЯ. Кроме того, НЯ были зафиксированы при использовании монопрепаратов: рифампицина — 72 случая, изониазида — 27 случаев, и этамбутола — 48 случаев. Эти данные позволяют предположить возможное накопление токсичности при комбинированной терапии, а также подчёркивают значимость оценки безопасности как фиксированных комбинаций, так и отдельных действующих веществ при их назначении в рамках схем стандартного лечения туберкулёза. Однако без клинической экспертизы причинная связь с компонентами схемы остаётся возможной .
Выводы
-
1. Выраженные различия в частоте НЯ установлены между ПТП различных производителей — как оригинальных, так и дженериковых.
-
2. Наибольшее количество сообщений о НЯ зарегистрировано на препараты компании АО «Фармасинтез» (Россия), что требует дальнейшего анализа в контексте как объёмов применения, так и производственного контроля.
-
3. Индийские производители (Hetero, Macleods, Rhydburg и др.) составляют значительную долю зарегистрированных НЯ, что подчёркивает необходимость строгого контроля качества при импорте и применении их продукции.
-
4. Наименьшая частота НЯ зафиксирована при применении бедаквилина Sirturo (Janssen, Бельгия), что может свидетельствовать о более высоком профиле безопасности оригинального препарата по сравнению с дженериками.
-
5. Различия в частоте НЯ между производителями могут быть обусловлены: особенностями технологических процессов, качеством субстанций, соответствием стандартам GMP, составом вспомогательных веществ и биодоступностью лекарственных форм.
-
6. Эти данные могут быть полезны при оптимизации схем лечения, выборе препаратов и разработке национальных клинических рекомендаций.
Заключение
Анализ представленных данных подчёркивает значительное влияние производителя на частоту и профиль НЯ при применении ПТП, особенно в условиях масштабного использования дженериков в государственных программах. Полученные результаты указывают на необходимость пересмотра подходов к фармаконадзору и лекарственному обеспечению: от усиления пострегистрационного контроля до внедрения требований по обязательному указанию производителя в системе регистрации побочных реакций. Выявленная вариабельность в переносимости препаратов от различных производителей требует более глубокого клинико-фармакологического изучения, включая оценку биоэквивалентности, качества сырья и соблюдения стандартов GMP. Особенно актуальным становится проведение независимых многоцентровых наблюдательных и контролируемых исследований для подтверждения безопасности и эффективности дженериков, используемых в лечении туберкулёза, в том числе форм с множественной лекарственной устойчивостью. Таким образом, для повышения качества лечения и снижения риска развития НЯ необходим системный подход к обеспечению лекарственной безопасности: чёткие критерии отбора поставщиков, приоритет оригинальных и доказано эквивалентных дженериков, а также развитие культуры ответственного фармаконадзора, ориентированного на пациента.


