Влияние психротолерантных метилотрофных бактерий на рост, пигментный состав и накопление белка и углеводов у микроводоросли chlorella vulgaris
Автор: Шаравин Д.Ю., Беляева П.Г., Цещинская Е.М., Галямина В.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2024 года.
Бесплатный доступ
Изучено влияние шести психротолерантных метилотрофных бактерий, выделенных из образцов мохово-лишайниковой растительности и водных объектов на территории Антарктических оазисов и горных районов республики Алтай на рост, пигментный состав и накопление белка и углеводов в культуре зелёной микроводоросли Chlorella vulgaris при температурах +10 и +20°С. Стандартные графики роста хлореллы без бактериальной суспензии при +20 и +10°С выходили на плато на 5-6 и 9 сутки соответственно, достигая 30 и 16^106 кл/мл. Установлено, что пять из шести психротолерантных штаммов при совместном культивировании с хлореллой при температуре +10°С на численность хлореллы, содержание пигментов и концентрацию белка влияния не оказывали. Положительное воздействие выявлено только для хПргЗ, в частности на содержание углеводов. Также обнаружен негативный эффект Бел19 на численность хлореллы и содержание пигментов при +10°С. При культивировании хлореллы со штаммами бактерий при температуре +20°С выявлено увеличение численности водорослей с хПргЗ, концентрации хлорофилла а с Бел19 (119% от контроля), углеводов с изолятом хПрг17 и содержания внутриклеточного белка хлореллы с Ал5, Бел19, Бел62 и хПрг17.
Chlorella vulgaris, метилотрофы, пигменты, белки, углеводы, холодовой стресс
Короткий адрес: https://sciup.org/147247246
IDR: 147247246 | УДК: 579.68 | DOI: 10.17072/1994-9952-2024-4-412-420
The effect of psychrotolerant methylotrophic bacteria on the growth, pigment content and accumulation of protein and carbohydrates in the microalgae chlorella vulgaris
The study is devoted to the effect of six psychrotolerant methylotrophic bacteria isolated from samples of moss-lichen community and water bodies, collected at the territory of Antarctic oases and mountainous region of the Altai republic on the growth, pigment content and accumulation of protein and carbohydrates by the green microalgae Chlorella vulgaris at temperatures of +10°C and +20°C. Standard growth curves of chlorella without bacterial suspension at +20°C and +10°C reached the stationary growth phase on days 5-6 and 9, respectively, reaching 30 and 16*106 cells/ml. It was found that five of the six psychrotolerant strains had no effect on the number of chlorella cells, pigment content and protein concentration when co-cultured with microalgae at the temperature of +10°C. A positive effect was found only for xPrg3, in particularly on the carbohydrate concentration. A negative effect of Bel19 on the cell number and pigment content at +10°C was also found. Inoculation of chlorella under the temperature of +20°C with same bacterial strains lead to increase in: cell number with the strain xPrg3, chlorophyll a with Bel19 (119% of the control), carbohydrates with the isolate xPrg17 and intracellular protein content with Al5, Bel19, Bel62 and xPrg17.
Текст научной статьи Влияние психротолерантных метилотрофных бактерий на рост, пигментный состав и накопление белка и углеводов у микроводоросли chlorella vulgaris
Криосфера представляет интерес как долгосрочное хранилище микробного разнообразия планеты, где доминируют различные виды холодоустойчивых микроорганизмов [Priscu, Christner, 2004; Miteva, 2008; Sajjad et al., 2020]. Психрофильные и психротолерантные бактерии способны синтезировать широкий спектр пигментов, экзополисахаридов, уникальные ферменты холодового шока и другие полимеры для защиты от воздействий окружающей среды [Hoover, Pikuta, 2010; Sajjad et al., 2020]. Предполагается, что психротолерантные и психрофильные микроорганизмы как составная часть растительно-микробных ассоциаций могут эффективно стимулировать рост и продуктивность сельскохозяйственных растений в условиях холодного климата [Balcazar et al., 2015].
Растения являются глобальным продуцентом C 1 -соединений, а аэробные метилотрофные бактерии часто ассоциированы с ними и могут заселять поверхность листьев, присутствуя в семенах и ризосфере многих растений, поставляя растению-симбионту фитогормоны (ауксины, цитокинины), витамины и другие биологически активные вещества [Kutschera, 2007; Madhaiyan et al., 2007; Delmotte et al., 2009]. Ввиду того, что источником метанола могут служить не только наземные растения, но и водоросли, можно сделать вывод о глобальном распространении фитосимбиоза метилотрофных бактерий на поверхности планеты [Mincer, Aicher, 2016].
Зелёная микроводоросль Chlorella vulgaris наиболее интенсивно используется для биологической очистки сточных вод, получения зелёной биомассы, в качестве кормовой и пищевой добавки, в медицинской и парфюмерной промышленности. Биомасса хлореллы может служить источником разнообразных высокомолекулярных соединений: белков, жиров, углеводов, органических кислот, витаминов и т.д. Бактериальное микроокружение хлореллы (фикосфера) играет существенную роль в продуктивности экосистем и совместно с ассоциированными бактериями может использоваться в целях биоремедиации и производстве зелёной водорослевой биомассы [Wirth et al., 2020].
Несмотря на интерес со стороны исследователей к бактериям, ассоциированным с представителями рода Chlorella , есть единичные работы, где метилотрофные бактерии рассматривались как симбионты хлореллы и микроводорослей в целом. Поэтому, особенно актуально в этой связи использование экстре-мофильных, в частности психрофильных метилотрофов для снижения негативного воздействия низких температур на хлореллу.
Цель работы – изучить возможность использования холодоустойчивых метилотрофов, выделенных из Антарктики и горных районов, для стимулирования роста и увеличения содержания пигментов и метаболитов Chlorella vulgaris при пониженных температурах.
Материалы и методы
Объектом исследований служил штамм Chlorella vulgaris IMBR-19 (получен из Института морских биологических исследований им. А.О. Ковалевского РАН) без бактериального загрязнения, поддерживаемый в стерильных условиях при оптимальной для данного штамма температуре +28°C (точность поддержания температуры ±0.1°С) на жидкой среде BG-11, с освещённостью около 6500 Лк и чередованием световых и темновых фаз 12ч/12ч [Rogers et al., 2020]. Колбы, содержащие микроводоросли, встряхивали вручную два раза в день.
Для выделения холодоустойчивых культур метилотрофов использовали образцы воды из водотоков, альгобактериальных матов и биообрастаний, почв, мха и лишайников, отобранные в ходе полевых работ 65-й Российской антарктической экспедиции и в горных районах республики Алтай. Для получения изо- лятов метилотрофных бактерий использовали модифицированную среду «К» [Sharavin, Belyaeva, 2024]. Для выделения и культивирования метилобактерий, обладающих альтернативной метанолдегидрогеназой, вместо CaCl2×2H2O добавляли смесь LaCl3×7H2O и Ce2(SO4)3×4H2O до концентрации 30 μM каждого. Культивирование метилотрофов осуществляли при +10°С. Оптическую плотность культур измеряли при длине волны 590 нм на спектрофотометре (Cary 100, Agilent Technologies). Бактериальные клетки осаждали центрифугированием при 6 000 об/мин, осадок ресуспендировали в физрастворе. Влияние 6 штаммов метилобактерий (список штаммов представлен в таблице) на рост зелёной водоросли Chlorella оценивали в процессе их совместного культивирования в стеклянных ёмкостях объёмом 25 мл при температурах +10°С и +20°С. Засевная доза хлореллы содержала 1.5–1.6 ×106 кл./мл. Начальная pH культуральной среды составляла 7.0. Оптимальная температура роста для большинства из используемых в данной работе культур бактерий составляла +20°С.
Список использованных в работе культур бактерий [List of bacterial cultures]
|
Штамм |
Источник выделения |
Координаты точки отбора |
Оптимальная температура роста культуры, °С |
|
Ал1 |
Вода с эпилитоном из горного озера (Алтай) |
49°52.6649' СШ 86°34.3694' ВД |
20 |
|
Ал5 |
Обрастания на камнях, р. Кучерла (Алтай) |
49°54.1298' СШ 86°24.9902' ВД |
20 |
|
Бел19 |
Вода из руч. Станционный, вытекающего из оз. Китеж |
62° 11,869' ЮШ 58° 57,777' ЗД |
20 |
|
Бел62 |
Накипной лишайник (р-н ст. Беллинсгаузен, о. Кинг-Джордж) |
62° 12.713' ЮШ 59° 00.374' ЗД |
20 |
|
хПрг3 |
Мхи и водоросли на солнечной стороне скал (р-н ст. Прогресс, Холмы Ларсе-манн) |
69° 22.975' ЮШ 76° 23.252' ВД |
20 |
|
хПрг17 |
Отложения чёрного цвета на дне озера (р-н ст. Прогресс, Холмы Ларсеманн) |
69° 23.200' ЮШ 76° 22.538' ВД |
12 |
Соотношение стартовых концентраций клеток бактерий и водорослей (при засеве) составляло 1:1. Подсчёт численности клеток хлореллы проводили в камере Горяева на микроскопе ZEISS Axiostar Plus (Германия) [Dvoretsky et al., 2017]. Эксперименты проведены в трёх биологических повторностях.
Определение пигментов микроводорослей производили в карбиноловых экстрактах на 14-е сутки культивирования. Аликвоты культур осаждали центрифугированием и отмывали от культуральной жидкости дистиллированной водой. Осаждённые клетки хлореллы разрушали при помощи ручного гомогенизатора. Затем в гомогенат добавляли холодный ацетон «хч» (80%), содержимое встряхивали и помещали в темноту на 12 часов при 4°C. После этого центрифугировали при 6 000 об/мин 10 мин. Надосадочную жидкость, которая представляла собой вытяжку пигментов, переносили в кварцевую кювету и спектрофотометрировали на Cary 100 (Agilent Technologies, США) при длинах волн, соответствующих максимуму абсорбции пигментов (663 нм – хлорофилл а , 645 нм – хлорофилл b , 470 нм – каротиноиды и 750 нм – поправка на неспецифическую абсорбцию и рассеяние света экстрактом). Концентрацию (мкг/мл) исследуемых пигментов – хлорофиллов a , b и каротиноидов – в клетках хлореллы определяли по формулам H.K. Lichtenthaler [1987].
Количественную оценку внутриклеточного белка в разрушенных при помощи ручного гомогенизатора клетках осуществляли методом Бредфорда с использованием красителя Кумасси бриллиантовый синий G-250 (100 мг) при длине волны 595 нм [Bradford, 1976].
Общее содержание углеводов определяли по методу Герберт с антроновым реактивом при длине волны 625 нм. Концентрацию углеводов в пробах высчитывали по калибровочной кривой стандартных растворов глюкозы [Herbert, Phipps, Strange, 1971].
Полученные результаты обработаны статистически с использованием программы Statistica 6.0 по t–критерию Стьюдента.
Результаты и обсуждение
Согласно графику роста хлореллы (рис. 1), полученному опытным путём, через 2 дня культивирования количество клеток при +20°С достигало 11×106 кл/мл, в то время как при +10°С – не превышало 5×106 кл/мл. К пятым суткам плотность культур составляла 30 и 7 ×106 кл/мл при +20 и +10°С соответственно. Кривые роста выходили на плато на 5–6 сутки при +20°С и на 9 сутки при +10°С (до 16×106 кл/мл).
+20℃ ■ +10℃
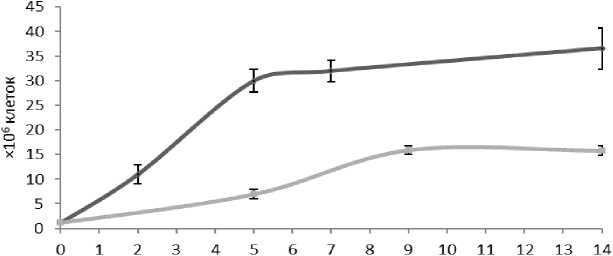
Сутки
Рис. 1. Стандартный график роста хлореллы при +10°С и +20°С
[Standard chlorella growth curve at +10°C and +20°C]
При совместном культивировании хлореллы с тестируемыми штаммами метилотрофных бактерий стимулирующего влияния бактерий на численность микроводорослей при температуре +10°С на 7 и 14 сутки не выявлено (рис. 2). Более того, эффект штамма Бел19 был негативный. При температуре инкубации +20°С заметный положительный эффект на рост хлореллы оказал хПрг3 на 14е сутки (126% от контроля) (рис. 3). Остальные варианты опыта при +20°С не имели существенных отличий от контроля.

ШПІ
□ 7 сут.
圆 14 сут.
Алі Ал5 Бел 19 Бел62 хПргЗ хПрг17
Рис. 2. Численность хлореллы на 7 и 14 сутки при инокулировании с культурами бактерий при +10°С [The number of chlorella cells inoculated with bacterial cultures at +10°C on day 7 and 14]
35 -1
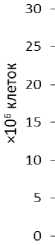
ІІ11ІІ1
□ 7 сут.
圖 14 сут.
К Алі Ал5 Бел 19 Бел62 хПргЗ хПрг17
Рис. 3. Численность хлореллы на 7 и 14 сутки при инокулировании с культурами бактерий при +20°С [The number of chlorella cells inoculated with bacterial cultures at +20°C on day 7 and 14]
На содержание пигментов микроводоросли при +10°С метилотрофные бактерии значимого положительного воздействия также не оказали. За исключением хлорофилла а у хПрг3 (3.13 мкг/мл), опытные варианты либо находились на уровне контрольных значений (К – 3.00 мкг/мл; хПрг17 – 2.98 мкг/мл), либо имели более низкую концентрацию (рис. 4). Ранее, при +10°С, нами было выявлено стимулирующее влияние штамма хПрг3 как на численность, так и на содержание пигментов хлореллы [Шаравин и др., 2023].
В текущем эксперименте обнаружено негативное воздействие Бел19 как на содержание пигментов при +10°С, так и на численность клеток хлореллы. Однако при +20°С данный штамм оказал стимулирующее влияние на содержание хлорофилла а , превысив контроль на 19% (рис. 5), при этом численность соответствовала контрольным значениям (рис. 3). Количество каротиноидов при +20°С в эксперименте со штаммами Ал1, хПрг3 и хПрг17 на 14 сутки выше контрольных в среднем в 1.7 раза, что может быть связано со старением культуры водоросли.
§^-v=>-
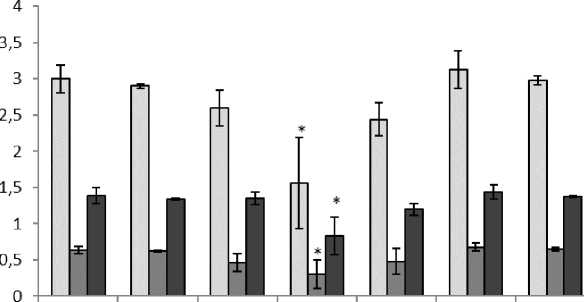
К Ал1 Ал5 Бел 19 Бел62 хПргЗ хПрг17
Рис. 4. Содержание пигментов, на 14 сутки (+10°С) [Pigment content, within 14 days (+10°C)]]
-
□ Хл а ОХл Ь ИКэр
3 5 2 5 15 0 2.1.0,

3,5
HAI/JHIAI
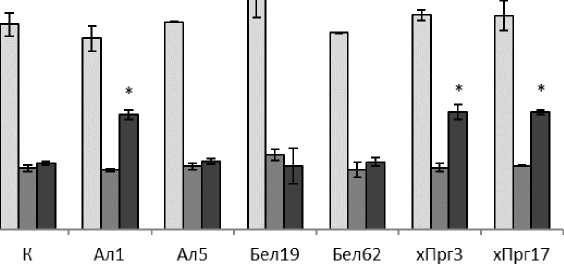
Рис. 5. Содержание пигментов, на 14 сутки (+20°С) [Pigment content, within 14 days (+20°C)]]
Эксперимент по совместному культивированию психротолерантных метилотрофов с хлореллой при +10 и +20°С выявил положительное влияние двух штаммов (хПрг3 на 16% при +10°С и хПрг17 на 37% при +20°С относительно контролей) на содержание углеводов в хлорелле (рис. 6). Концентрация углеводов в хлорелле в опытах при +10°С с Ал5, Бел19 и Бел62 не могла быть достоверно измерена из-за сильного развития бактериальных культур и невозможности полного разделения компонентов.
Данные по синтезу углеводов при воздействии низких температур, исходя из ряда источников – весьма противоречивы. Согласно [Lindberg et al., 2022], концентрация некоторых сахаров в Ch. vulgaris может существенно увеличиваться при пониженной (+5°С) температуре, по сравнению со значениями при +22°С. Однако показано, что при увеличении температуры роста относительно оптимальной (на 7–12°С), также может воз- растать содержание углеводов [Dai et al., 2022]. Некоторые представители рода Chlorella склонны выделять растворимые сахара в культуральную среду с увеличением температуры, в то время как содержание внутриклеточных растворимых сахаров не изменялось с колебаниями температуры [Cao et al., 2016].
На содержание внутриклеточного белка хлореллы в опытах при температуре +20°С выявлено положительное воздействие Ал5, Бел19, Бел62 и хПрг17 (120, 144, 111 и 136% относительно контроля соответственно). При инокулировании хлореллы штаммами Ал1 и хПрг3 при температуре +10°С на 14-е сутки зафиксировано снижение количества белка в культуре микроводоросли относительно контроля (рис. 7). Как и в случае с углеводами, данные по внутриклеточным белкам хлореллы при +10°С с Ал5, Бел19 и Бел62 получить не удалось по вышеуказанной причине. В литературе показано, что Chlorella sp.-Arc накапливает белки, а также липиды при низких температурах (менее +15°С) [Cao et al., 2016]. Также отмечено, что разные штаммы хлореллы могут синтезировать большее количество белка как при повышенных, так и при пониженных (5–10°С) температурах [Cao et al., 2016; Idenyi et al., 2021]. В нашем случае используется относительно теплолюбивый штамм хлореллы и для него температура +10°С, исходя из графика роста (см. рис. 1), является существенным фактором, замедляющим рост культуры. При этом метилотрофные бактерии, продолжая своё развитие, вероятно, начинали подавлять микроводоросли, находясь в ограниченном объёме.
-
□ 20℃ 01О℃
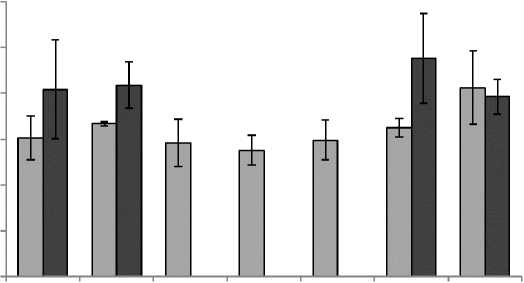
К Дл1 Ал5 Бел 19 Бел62 хПргЗ хПрг17
Рис. 6. Концентрация углеводов в культуре Chlorella с бактериями на 14 сутки при +20°С и +10°С [Carbohydrate concentration in Chlorella culture with bacteria on day 14 at +20°C and +10°C]]
-
□ 20℃ Е10℃
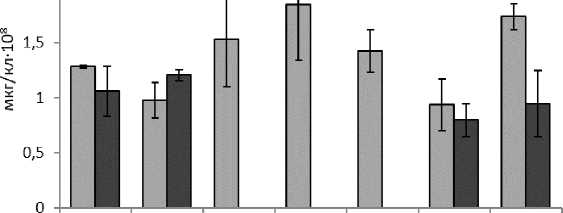
К Ал1 Ал5 Бел 19 Бел62 хПргЗ хПрг17
Рис. 7. Концентрация белка в культуре Chlorella с бактериями на 14 сутки при +20°С и +10°С [Protein concentration in Chlorella culture with bacteria on day 14 at +20°C and +10°C]]
В литературе можно встретить работы по изучению влияния психрофильного бактериального микроокружения холодоустойчивых микроводорослей, но не используемых в биотехнологии штаммов хлореллы. Упоминания метилотрофных компонент таких сообществ единичны, а данные о положительном влиянии психрофилов на морфологические и биохимические показатели представителей рода Chlorella не отличаются стабильностью.
Заключение
В результате проведённого исследования явного стимулирующего влияния психротолерантных мети-лотрофных бактерий на численность, содержание пигментов и концентрацию белка хлореллы при температуре +10°С не выявлено, но при этом обнаружено положительное влияние на содержание углеводов в хлорелле при культивировании с хПрг3 (116% от контроля).
Более значимое воздействие оказали используемые штаммы бактерий при сокультивировании с хлореллой при температуре +20°С. Заметный положительный эффект на численность культуры водоросли оказал только штамм хПрг3 (126% от контроля), на содержание пигментов, в частности хлорофилла а – Бел19 (119% от контроля), на содержание углеводов относительно контроля хПрг17 (137% от контроля). На содержание внутриклеточного белка хлореллы выявлено положительное воздействие с Ал5, Бел19, Бел62 и хПрг17 (120, 144, 111 и 136% от контроля соответственно).
Для использования психротолерантных метилотрофов стимуляции роста Chlorella vulgaris при пониженных температурах необходимы дальнейшие исследования по подбору оптимальных соотношений численности бактерий и водорослей для достижения устойчивого положительного эффекта.
Список литературы Влияние психротолерантных метилотрофных бактерий на рост, пигментный состав и накопление белка и углеводов у микроводоросли chlorella vulgaris
- Шаравин Д.Ю. и др. Влияние психротолерантных метилотрофных бактерий на рост и концентрацию пигментов микроводоросли Chlorella vulgaris // Развитие современных систем земледелия и животноводства, обеспечивающих экологическую безопасность окружающей среды: материалы Всерос. науч. конф. Пермь, 2023. С. 398-404.
- Balcazar W. et al. Bioprospecting glacial ice for plant growth promoting bacteria // Microbiol. Res. 2015. Vol. 177. P. 1-7. DOI: 10.1016/j.micres.2015.05.001.
- Bradford M.M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding // Analytical Biochemistry. 1976. Vol. 72. P. 248-254. DOI: 10.1006/abio.1976.9999.
- Cao K. et al. The eurythermal adaptivity and temperature tolerance of a newly isolated psychrotolerant Arctic Chlorella sp. // J. Appl. Phycol. 2016. Vol. 28. P. 877-888. DOI: 10.1007/s10811-015-0627-0.
- Dai Y.R. et al. Thermal-tolerant potential of ordinary Chlorella pyrenoidosa and the promotion of cell harvesting by heterotrophic cultivation at high temperature // Front. Bioeng. Biotechnol. 2022. Vol. 10. Art. 1072942. DOI: 10.3389/fbioe.2022.1072942.
- Delmotte N. et al. Community proteogenomics reveals insights into physiology of phyllosphere bacteria // PNAS. 2009. Vol. 106, № 38. P. 16428-16433. DOI: 10.1073/pnas.0905240106.
- Dvoretsky D. et al. The effect of the complex processing of microalgae Chlorella vulgaris on the intensification of the lipid extraction process // Chem. Eng. Trans. 2017. Vol. 57. P. 721-726. DOI: 10.3303/CET1757121.
- Herbert D., Phipps P.J., Strange R.E. Chapter III. Chemical analysis of microbial cells // Methods in microbiology / eds. J.R. Norris, D.W. Ribbons. 1971. Vol. 5. P. 209-344.
- Hoover R.B., Pikuta E.V. Psychrophilic and psychrotolerant microbial extremophiles in polar environments. CRS Press, 2010. P. 1-42. URL: https://ntrs.nasa.gov/api/citations/20100002095/downloads/20100002095.pdf.
- Idenyi J.N. et al. Characterization of strains of Chlorella from Abakaliki, Nigeria, for the production of high-value products under variable temperatures // J. Appl. Phycol. 2021. Vol. 33. P. 275-285. DOI: 10.1007/s10811-020-02313-y.
- Kutschera U. Plant-associated methylobacteria as co-evolved phytosymbionts // Plant Signaling & Behavior. 2007. Vol. 2, № 2. P. 74-78. DOI: 10.4161/psb.2.2.4073.
- Lichtenthaler H.K. Chlorophylls and carotenoids: pigments of photosynthetic biomembranes // Methods Enzymol. 1987. Vol. 148. P. 350-382. doi: 10.1016/0076-6879(87)48036-1.
- Lindberg A. et al. Cold stress stimulates algae to produce value-added compounds // Biores. Technol. Rep. 2022. Vol. 19. Art. 101145. DOI: 10.1016/j.biteb.2022.101145.
- Madhaiyan M. et al. Methylobacterium oryzae sp. nov., an aerobic pinc-pigmented, facultatively methylotrophic, 1-aminocyclopropane-1-carboxylate deaminase-producing bacterium isolated from rice // IJSEM. 2007. Vol. 57. P. 326-331. DOI: 10.1099/ijs.0.64603-0.
- Mincer T.J., Aicher A.C. Methanol production by a broad phylogenetic array of marine phytoplankton // PLoS ONE. 2016. Vol. 11, № 3. Art. e0150820. DOI: 10.1371/journal.pone.0150820.
- Miteva V.R. Bacteria in Snow and Glacier Ice // Margesin R. et al. Psychrophiles: from biodiversity to biotechnology. 2008. P. 31-50. DOI: 10.1007/978-3-540-74335-4_3.
- Priscu J.C., Christner B.C. Earth's icy biosphere // Microbial diversity and bioprospecting. ASM Press, 2004. P. 130-145.
- Rogers T.L. et al. Trophic control changes with season and nutrient loading in lakes // Ecol. Lett. 2020. Vol. 23, № 8. P. 1287-1297. DOI: 10.1111/ele. 13532.
- Sajjad W. et al. Pigment production by cold-adapted bacteria and fungi: colorful tale of cryosphere with wide range applications // Extremophiles. 2020. Vol. 24. P. 447-473. DOI: 10.1007/s00792-020-01180-2.
- Sharavin D.Y., Belyaeva P.G. Biotechnological potential of psychrotolerant methylobacteria isolated from biotopes of Antarctic oases // Arch. Microbiol. 2024. Vol. 206, № 323. P. 1-16. DOI: 10.1007/s00203-024-04056-7.
- Wirth R. et al. Chlorella vulgaris and its phycosphere in wastewater: Microalgae-bacteria interactions during nutrient removal // Front. Bioeng. Biotechnol. 2020. Vol. 8. Art. 557572. DOI: 10.3389/fbioe.2020.557572.


