Влияние растительного средства на течение экспериментального гепаторенального синдрома, вызванного комплексом противотуберкулезных средств
Автор: Усов Лев Акимович, Мондодоев Александр Гаврилович, Разуваева Янина Геннадьевна, Бартанова Елена Алексеевна, Бутуханова Ирина Сергеевна, Юндунова Оюна Владимировна
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Медицина
Статья в выпуске: SC, 2012 года.
Бесплатный доступ
Комплекс противотуберкулезных препаратов вызывает развитие гепаторенального синдрома у белых крыс. Курсовое введение животным растительного средства «нефрофит» в экспериментально-терапевтической дозе на фоне туберкулостатической терапии оказывает позитивное влияние на течение гепаторенального синдрома.
Туберкулостатики, гепаторенальный синдром, "нефрофит"
Короткий адрес: https://sciup.org/148181398
IDR: 148181398 | УДК: 615.244-322
The effect of plant remedy on the course of experimental hepatorenal syndrome induced by the complex of antituberculosis remedies
The complex of antituberculosis preparations induces the development of hepatorenal syndrome in white rats. The course introduction of the «nephrophyt» plant remedy to animals in experimental-therapeutic dose on the background of tuberculostatic therapy positively influences on the development of hepatorenal syndrome.
Текст научной статьи Влияние растительного средства на течение экспериментального гепаторенального синдрома, вызванного комплексом противотуберкулезных средств
Успешность лечения туберкулеза во многом зависит от возможности проведения полного курса терапии туберкулостатиками в адекватных ситуации дозах и режимах. Тем не менее наблюдаемая частота лекарственных осложнений приводит к необходимости смены препаратов, изменения доз, перерывам в лечении, что в итоге может привести к снижению эффективности терапии. Одним из частых осложнений, лимитирующих назначение противотуберкулезных препаратов, является нарушение функций почек и печени на фоне приема указанных средств или уже имеющиеся сниженные функциональные возможности этих органов в результате их отягощенных состояний. По данным литературы, нарушения функций почек разной степени выраженности наблюдаются в 68,3% случаев при назначении туберкулостатиков, а среди больных туберкулезом легких в 16,3% случаев развивается токсический гепатит лекарственной этиологии [4]. Нарушения функционального состояния почек и печени связывают с нефро-и гепатотоксическими свойствами туберкулостатиков [4,5].
В сложившейся ситуации представляется оправданным и логичным предупреждать или максимально снижать токсическое действие противотуберкулезных препаратов. Одним из вариантов решения указанной проблемы, на наш взгляд, является использование растительных средств, которые способны оказывать не только нефро- и гепатопротекторное действие, но и повышать адаптивные возможности организма в целом. Ранее нами были установлены выраженные нефропротекторные свойства комплексного растительного средства, условно названного «нефрофит» при поражениях почек токсической и ишемической этиологии [6].
Целью настоящего исследования явилось определение влияния «нефрофита» на функциональную активность почек и печени при назначении комплекса туберкулостатиков.
Материалы и методы
Исследования проведены на крысах линии Wistar обоего пола массой 160-180 г. Повреждение почек и печени туберкулостатиками моделировали по методике Н.П. Скакуна, О.Е. Табачука (1992). Лабораторным животным внутрижелудочно с 2-часовым интервалом вводили противотуберкулезные препараты (ПТП): изониазид (50 мг/кг), рифампицин (50 мг/кг), пиразинамид (1,5 мг/кг) 1 раз в сутки в течение 14 дней.
Животные опытной группы на фоне введения туберкулостатиков получали комплексный фитоэкстракт «нефрофит», в состав которого входят сухие экстракты: толокнянки обыкновенной – 2 части, ортосифона тычиночного - 4 части, горца птичьего – 3,5 части, десмодиума канадского – 0,5 части, в экспериментально-терапевтической дозе 150 мг/кг массы 1 раз в сутки, внутрижелудочно, в течение эксперимента. Препарат сравнения «канефрон» вводили другой группе животных на фоне введения ПТП в объеме 1,5 мл/кг 1 раз в сутки внутрижелудочно по аналогичной схеме. Животные контрольной группы получали дистиллированную воду в эквиобъемных количествах в аналогичных условиях. На 3-и и 15-е сутки после введения ПТП оценивали функциональное состояние почек и печени общепринятыми методами, а также определяли содержание продуктов перекисного окисления липидов (ПОЛ) и активность ферментов антиоксидантной защиты организма (АОЗ). Концентрацию диеновых конъюгатов (ДК) в плазме крови определяли по Гаврилову, Мишкорудной (1983). Концентрацию малонового диальдегида (МДА) определяли в сыворотке крови и в гомогенате почек белых крыс (Osakawa, Matshushita, 1980). Активность каталазы сыворотки крови определяли по Королюк и соавт., (1988). Активность супероксиддисмутазы (СОД) определяли по Чевари и соавт., (1985). Статистическая обработка результатов проводилась с использованием t-критерия Стьюдента. Полученные данные представлены в таблицах 1 - 5.
Результаты и обсуждение
Как следует из данных табл. 1, введение комплекса ПТП у белых крыс на 3-и сутки наблюдения не оказывает заметного влияния на функциональное состояние почек, тем не менее, отмечалась выраженная индукция процессов свободнорадикального окисления биомакромолекул и компенсаторное увеличение каталитической активности. Так, концентрация ДК и МДА в крови почках белых крыс возрастала по сравнению с показателями у интактных животных соответственно в 1,9, 1,5 и 1,6 раза.
Курсовое введение «нефрофита» оказывало антиоксидантное действие, об этом свидетельствовало достоверное снижение уровня накопления ДК и МДА в крови и гомогенате почек животных на 24, 34 и 20 %, также отмечалось выраженное повышение активности каталазы на 70% соответственно по сравнению с показателями у крыс контрольной группы. При этом антиоксидантная активность препарата сравнения «канефрона» значительно уступала действию «нефрофита».
Таблица 1
Влияние «нефрофита» на показатели азотистого обмена, перекисного окисления липидов и активность ферментов АОЗ в сыворотке крови белых крыс при комплексном введении противотуберкулезных препаратов (3-и сутки)
|
Показатели |
Группы |
|||
|
Интактная |
Контрольная (ПТП) |
Опытная 1 (ПТП + «Нефрофит» |
Опытная 2 (ПТП + «Канефрон» |
|
|
Креатинин, мкмоль/л |
62,00±0,77 |
64,50±2,35 |
62,25±1,18 |
63,78±0,76 |
|
Мочевина, ммоль/л |
5,37±0,46 |
5,62±0,41 |
5,39±0,59 |
5,45±0,76 |
|
ДК, усл. ед. |
6,11±0,39 |
11,45±0,87* |
8,73±0,52** |
10,63±1,09 |
|
МДА в сыворотке, мкмоль/мл |
11,45±0,83 |
17,59±1,56* |
11,53±0,94** |
15,74±1,26 |
|
МДА, нмоль/г ткани |
10,30±0,56 |
16,47±1,52* |
13,24±1,28 |
16,82±1,56 |
|
Каталаза, млкат/л |
4,01±0,37 |
4,20±0,45 |
7,25±0,66** |
4,72±0,36 |
Примечание: здесь и далее * - различия достоверны между группами интакт – контроль, ** - различия достоверны между группами контроль – опыт при Р ≤ 0,05
Как следует из таблицы 2, курсовое введение ПТП вызывает у лабораторных животных умеренное поражение почек, сопровождающееся гиперазотемией, протеинурией, повышением диуреза, снижением скорости клубочковой фильтрации (СКФ) и относительной плотности мочи. Так, на 15-е сутки исследования в сыворотке крови животных контрольной группы наблюдали возрастание концентрации креатинина и мочевины в 1,2 и 1,3 раза соответственно; уровень протеинурии – на 50 %; диурез увеличивается в 1,5 раза, а СКФ снижалась на 26 % по сравнению с данными у интактных крыс. Снижение СКФ, удельного веса мочи и увеличение диуреза у крыс контрольной группы следует рассматривать как проявление угнетения концентрационной функции почек под влиянием комплекса туберкулостатических средств.
Таблица 2
Влияние «нефрофита» на функциональное состояние почек белых крыс при экспериментальной лекарственной нефропатии, вызванной комплексным введением противотуберкулезных препаратов (ПТП) (15-е сутки)
|
Показатели |
Группы животных |
|||
|
Интактная |
Контрольная (ПТП) |
Опытная 1 (ПТП + «Нефрофит») |
Опытная 2 (ПТП + «канефрон») |
|
|
Креатинин, мкмоль/л |
52,10±3,16 |
63,02±3,98* |
54,42±3,02 |
56,83±5,11 |
|
Мочевина, ммоль/мл |
5,56±0,32 |
7,19±0,38* |
5,78±0,42 |
6,45±0,58 |
|
Белок в моче, г/л |
0,70±0,05 |
1,05±0,07* |
0,65±0,04** |
0,78±0,06 |
|
СКФ, мкл/мин |
173,41±10,34 |
127,68±9,37* |
152,90±8,76 |
134,82±12,03 |
|
Объем мочи за 2 часа, мл/100 г. |
80,66±5,02 |
120,50±6,56* |
86,21±4,85** |
89,36±7,93 |
|
Удельный вес мочи |
1030,21±65,47 |
1021,14±78,01 |
1029,45±76,31 |
1024,01±91,22 |
Курсовое введение «нефрофита» в указанной дозе сопровождалось сохранением функционального состояния почек. В частности, не наблюдали увеличения уровня креатинина и мочевины в сыворотке крови животных опытных групп, роста протеинурии. СКФ повышалась в 1,2 раза; диурез снижался на 28 % по сравнению с контролем. Основные регистрируемые показатели у животных опытной группы к данному сроку наблюдения статистически не отличались от аналогичных данных у интактных крыс.
Данные, приведенные в таблице 3, свидетельствуют, что введение ПТП сопровождается выраженной индукцией процессов ПОЛ и снижением активности эндогенной антиокислительной системы организма. Так, на 15-е сутки эксперимента наблюдали повышение содержания ДК и МДА в сыворотке крови и почках белых крыс соответственно в 2,3; 1,4 и 1,5 раза; одновременно с этим происходило снижение активности каталазы и СОД на 29 и 45 % соответственно по сравнению с показателями у крыс интактной группы.
Таблица 3
Влияние «нефрофита» на показатели перекисного окисления липидов и активность ферментов АОЗ в сыворотке крови белых крыс при комплексном введении противотуберкулезных препаратов (15-е сутки)
|
Группы животных |
ДК, усл. ед. |
МДА, в сыворотке крови, мкмоль/л |
МДА, мкмоль/г ткани почки |
Каталаза, млкат/л |
СОД, в эритроцитах, мкмоль/л |
|
Интактная |
5,81±0,42 |
13,28±0,65 |
14,01±1,27 |
8,60±0,61 |
14,06±1,26 |
|
Контрольная (ПТП) |
10,34±0,72* |
19,17±1,70* |
21,59±1,76* |
6,10±0,36* |
7,69±1,04* |
|
Опытная 1 (ПТП + «Нефрофит» |
7,18±0,56** |
13,94±0,76** |
16,01±0,96** |
8,61±0,77** |
12,32±0,86** |
|
Опытная 2 (ПТП + «Канефрон» |
8,26±1,01 |
15,92±1,49 |
17,36±1,52 |
7,92±0,49 |
11,41±0,91 |
Курсовое введение «нефрофита» животным, получавшим ПТП, сопровождалось достоверным снижением накопления продуктов пероксидации липидов в крови и почках белых крыс. Так, под влиянием испытуемого средства происходило снижение концентрации ДК в сыворотке крови на 30 %; концентрации МДА в крови и почках белых крыс - на 27 и 26 % соответственно по сравнению с показателями у крыс контрольной группы. Наряду с этим, у животных, получавших фитоэкстракт, повышалась активность каталазы и СОД в сыворотке крови в 1,4 и 1,6 раза по сравнению с показателями у крыс контрольной группы. Антиоксидантная активность препарата сравнения в этих условиях уступала таковой у «нефрофита».
Как следует из таблицы 4, при сочетанном введении белым крысам изониазида, рифампицина и пирази-намида в указанных дозах в сыворотке крови повышается активность мембраносвязанных ферментов : аланинаминотрансферазы (АлТ) и аспартатаминотрансферазы (АсТ) в 2,2 и 1,5 раза соответственно по сравнению с показателями у крыс интактной группы. Наряду с этим, отмечали повышение в сыворотке крови: тимоловой пробы в 2,1 раза, концентрации общего билирубина в 7 раз, активности щелочной фосфатазы на 30% соответственно с аналогичными показателями у интактных крыс.
Влияние «нефрофита» на функциональное состояние печени белых крыс при комплексном введении противотуберкулезных препаратов (15-е сутки)
Таблица 4
|
Показатели |
Группы животных |
||
|
Интактная |
Контрольная (ПТП) |
Опытная (ПТП + «Нефрофит» |
|
|
АсТ, ЕД/л |
38,41±2,68 |
86,01±5,17* |
66,34±3,79** |
|
АлТ, ЕД/л |
58,09±4,17 |
87,59±7,01* |
69,18±4,39** |
|
Тимоловая проба, ЕД |
0,81±0,05 |
1,70±0,08* |
1,06±0,05** |
|
Общий билирубин, мкм/л |
3,36±0,16 |
23,59±1,87* |
19,56±1,23 |
|
Щелочная фосфатаза, ЕД/л |
4,52±0,31 |
5,87±0,31 |
5,56±0,29 |
Под влиянием «нефрофита» на фоне введения туберкулостатиков наблюдали менее выраженные проявления цитолиза, холестаза, улучшалась белковообразующая функция печени. Так, уровни активности АсТ и АлТ и концентрация билирубина в сыворотке крови были ниже на 23, 21 и 17 % соответственно, показатель тимоловой пробы ─ на 38 % ниже по сравнению с аналогичными данными у животных контрольной группы.
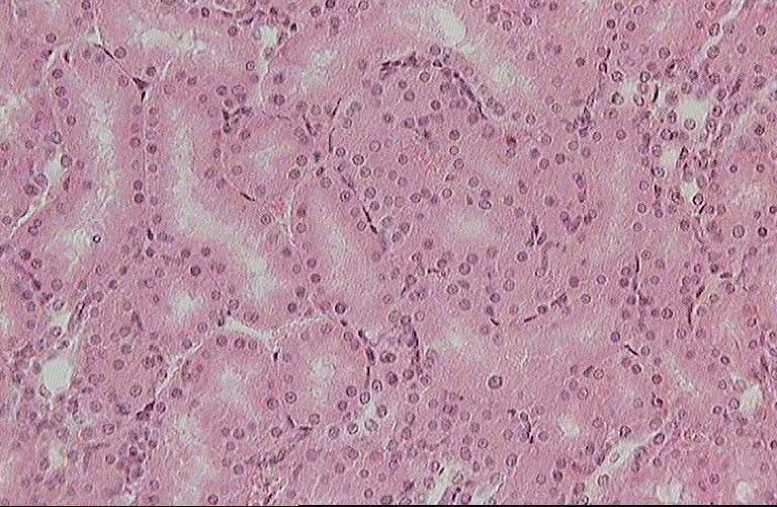
При патоморфологическом исследовании было установлено, что сочетанное введение ПТП оказывает повреждающее действие на канальцы коркового слоя почек, в частности, на проксимальные канальцы. Просветы канальцев представлялись расширенными, многие из них были заполнены белковыми и гиалиноподобными массами. Эпителий канальцев был подвержен разной степени дистрофии (рис.1): некоторые эпителиальные клетки были увеличены в объеме и представляли собой рыхлые образования с небольшими компактными ядрами; другие клетки, наоборот, представлялись уплощенными и не содержали ядер или ядра имели бледную окраску. Также встречались канальцы в состоянии деструкции с разрушенными эпителием и базальной мембраной. На фоне курсового введения «нефрофита» отмечено его защитное действие на структуры канальцев. На рис. 2 просматриваются канальцы с сохраненными эпителием и базальной мембраной. Просветы канальцев свободны от возможных включений. При морфометрической оценке подтверждено нефрозащитное влияние данного средства (табл. 5).
Таблица 5
Влияние «нефрофита» на площадь и периметр канальцев при нефропатии, вызванной комплексным введением противотуберкулезных препаратов (ПТП) (15-е сутки)
|
Показатели |
Группы животных |
|
|
Контрольная (ПТП) |
Опытная (ПТП +«нефрофит») |
|
|
Площадь канальцев, мкм² |
959,81±38,79 |
412,57±12,53** |
|
Периметр канальцев, мкм |
150,31±7,54 |
83,04±4,72** |
Выводы и заключение . Таким образом, комплексное введение лабораторным животным рифампицина, изониазида, пиразинамида в указанных дозах сопровождается развитием полиорганной патологии, характеризующейся как гепаторенальный синдром и способствует развитию синдромов: цитолиза (повышение активности ферментов АсТ и АлТ), холестаза (возрастание активности щелочной фосфатазы, гипербилирубинемия) и мезинхимального воспаления (повышение показателя тимоловой пробы), а также вызывает снижение белково-синтетической функции печени, на что указывало повышение осадочной тимоловой пробы. Эти данные согласуются с положением о биотрансформации указанных препаратов, происходящих в основном в печени, вызывая ее токсические изменения [5]. Поражение почек при назначении ПТП характеризовалось незначительной азотемией, протеинурией, снижением скорости клубочковой фильтрации, умеренным повышением диуреза и гипостенурией. На фоне медикаментозного гепаторенального синдрома у белых крыс развивался оксидативный стресс с понижением возможностей эндогенной антиокислительной защиты. Также комплексное введение ПТП сопровождалось дистрофическими изменениями эпителия проксимальных канальцев и реакцией интерстициальной ткани.
Курсовое введение «нефрофита» животным на фоне ПТП сопровождалось нефропротекторным и умеренным гепатозащитным влиянием, благодаря способности данного полиэкстракта экранировать отрицательное действие противотуберкулезных препаратов. Этот эффект обусловлен комплексом биологически активных веществ, прежде всего фенольной природы, оказывающих антиоксидантное, мембраностабилизирующее действие [7]. Кроме того, в дополнительных сериях экспериментов было установлено стимулирующее влияние «нефрофита» на макрофагальное звено иммунитета при азати-оприновой иммуносупрессии у мышей линии СВА х F1 [1]. Также было показано, что данный полиэкстракт подавляет активность каспазы-3 в гомогенате почек белых крыс при их ишемии/реперфузии [8], что характеризует его как средство, ингибирующее индуцированный апоптоз. Эти наблюдения имеют определенное значение, поскольку есть данные, свидетельствующие о важной роли ускорения процессов ПОЛ при назначении ПТП как фактора, способствующего развитию указанных нарушений, а также роли индуцированного апоптоза в генезе лекарственных повреждений почек [9]. Очевидно, благодаря указанным свойствам «нефрофита», обеспечивается его положительное влияние на течение гепаторенального синдрома при использовании комплекса противотуберкулезных средств.
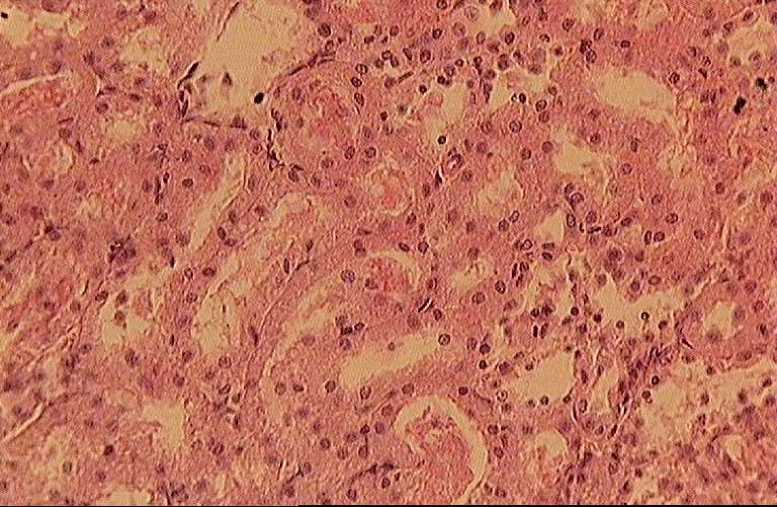
Рис. 1. Почка крысы. Контроль. 15-е сутки исследования. Расширение канальцев. Наличие в просвете канальцев белково-гиалиновоподобных цилиндров. Окраска гемотоксилин-эозином. Увел. 10х40
V С<
О о
«♦о
1 .. »'L 0
У О ;*•* "Л
“оу о
0ф 1ft ^ ^^
• V^" 0 Г1^
-0 $, .@ “ •
° '\- V ■■' и v**^ \. ч и |1Р‘ ‘*к
Рис. 2. Почка. Курсовое введение «Нефрофита». 15 сутки исследования. В проксимальных канальцах почки отсутствуют белково-гиалиновые цилиндры. Окраска гематоксилин-эозином. Увел. 10х40


