Влияние растворимых соединений марганца на высшие растения и оценка фитоэкстракционной способности растений
Автор: Рогачева Светлана Михайловна, Каменец Алексей Федорович, Шилова Наталья Александровна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Общая биология
Статья в выпуске: 5-3 т.18, 2016 года.
Бесплатный доступ
Изучено влияние ионов марганца в концентрациях 1, 10, 30 ПДК на рост высших растений Tagetes patula L. и Phragmites australis. Показано, что оба вида растений проявляют устойчивость к высоким концентрациям водорастворимых соединений марганца в почве. Оценена способность растений аккумулировать ионы марганца (II), отмечена возможность их применения в фиторемедиационных мероприятиях.
Ионы марганца, почва, фитоэкстракция, фиторемедиация
Короткий адрес: https://sciup.org/148204947
IDR: 148204947 | УДК: 504.53.062.4:
The effect of soluble manganese compounds at higher plants and assessment of plants's phytoextraction ability
The effect of manganese ions at concentrations of 1, 10, 30 MPC at the growth of higher plants Tagetes patula L. and Phragmites australis was investigated. It was shown that the both types of plants exhibit resistance to high concentrations of soluble manganese compounds in the soil. The ability of plants to accumulate manganese was assessed, which indicates the possibility of their application in phytoremediation events.
Текст научной статьи Влияние растворимых соединений марганца на высшие растения и оценка фитоэкстракционной способности растений
Марганец поступает в почву и водоемы в результате природных процессов - выщелачивания железомарганцевых руд, горизонтов почвогрунтов и разложения растительных остатков; из техногенных источников - с выбросами предприятий черной и цветной металлургии, при нефтедобыче и нефтепереработке, добыче железной руды, при использовании минеральных удобрений в сельском хозяйстве [1,2].
В почве под воздействием различных процессов соединения марганца распределяются по ее компонентам: металл входит в состав кристаллической решетки минералов, адсорбируется на поверхности почвенной биоты, соединяется с оксидами и гидроксидами железа, находится в растворенном состоянии в почвенном растворе.
Из водорастворимых соединений в почве встречаются соли Мn2+: Mn(NO3)2 . 6H2O; MnSO4 . (NH4)2 . 6H2O; MnSO4 . nH2O; MnCl2; MnCl2 . 4H2O и комплексные соединения, их содержание возрастает в условиях кислой реакции среды [3]. В водоемах 98% марганца, как правило, находится во взвешенной форме, концентрация водорастворимых соединений увеличивается при низких окислительно-восстановительных потенциалах и значениях pH [4].
Ионы марганца, подобно катионам других металлов, проникают в растения через корни, лишь незначительное количество Mn может поступать через листья из атмосферных осадков [3, 4]. Марганец является эссенциальным микро
Каменец Алексей Федорович, аспирант кафедры «Природная и техносферная безопасность».
Шилова Наталья Александровна, кандидат биологических наук, доцент кафедры «Природная и техносферная безопасность».
элементом для растений. Известно более 35 ферментов, активируемых марганцем, большинство из них являются катализаторами реакций окисления-восстановления, декарбоксилирования, гидролиза. Марганцевозависимые ферменты участвуют в биосинтезе ароматических аминокислот, лигнина, флавоноидов, каротиноидов и стеролов, в процессе фотосинтеза. Ионы марганца активно влияют на структуру и функции хроматина, они необходимы для репликации и функционирования ДНК и РНК-полимераз, т.е. участвуют в процессах деления клеток и размножении [4].
С другой стороны, повышение содержания марганца приводит к угнетению и гибели растений. Токсичность элемента проявляется на кислых дерново-подзолистых почвах, особенно при повышенной влажности, образовании корки и внесении физиологически кислых удобрений без их нейтрализации, т.е. в условиях образования водорастворимых соединений марганца.
Известны растения, устойчивые к высоким концентрациям металлов и накапливающие их повышенное количество. Способность растений извлекать из окружающей среды тяжёлые металлы используют в фиторемедиации – комплексе методов очистки сточных вод, грунтов и атмосферного воздуха [5].
Высокой экстрагирующей активностью по отношению к тяжёлым металлам обладают тростник обыкновенный ( Phragmites australis ) и бархатцы мелкоцветные ( Tagetes patula L . ) [6]. P. australis – укореняющийся макрофит, способный аккумулировать химические вещества, в том числе тяжёлые металлы, очищать воду от взвешенных частиц. T. patula L . – декоративное однолетнее растение, также проявляет способность экстрагировать тяжёлые металлы из почвы, например, цинк, медь, мышьяк при содержании выше ПДК.
Вопросы толерантности и экстракционной способности растений по отношению к соедине- ниям марганца изучены недостаточно, поэтому целью данной работы явилось исследование эффектов воздействия ионов марганца на рост высших растений T. patula L. и P. australis и оценка способности растений аккумулировать марганец.
МАТЕРИАЛЫ И МЕТОДЫ
В работе использовали высшие растения: 1) бархатцы мелкоцветные ( T. patula L.), 2) тростник обыкновенный ( P. australis). Культивирование проводили в чернозёме с внесенным в него MnSO4 . H2O, pH=7.
Для создания модельных почв, загрязнённых ионами Mn2+, в образцы природного чернозёма (m=0,45 кг) вносили в виде водного раствора (V=0,1 л) соль MnSO4 . H2O в определенных концентрациях и тщательно перемешивали. В экспериментах использовали образцы почвы: К – контрольный образец, без добавления ионов Mn2+; 1 – концентрация ионов Mn2+ 140 мг/кг (1 ПДК); 2 – концентрация ионов Mn2+ 1400 мг/кг (10 ПДК); 3 – концентрация ионов Mn2+4200 мг/кг (30 ПДК) [7].
В модельные почвы высаживали 10-дневную рассаду T. рatula и P. australis по одному растению в контейнер (450 г почвы), опыт осуществляли в пяти повторностях. На протяжении 24 дней наблюдали за ростом растений, особенностями их развития и поддерживали почву в увлажненном состоянии. Эксперимент проводили в сентябре месяце, в застекленной теплице, в условиях естественного освещения при температуре 22-25°С, растения поливали не менее 1 раза в 3 дня в объеме 75-100 мл/кг почвы.
Через 24 дня производили отбор и подготовку анализируемых образцов почв и растений, согласно нормативным документам [8,9]. Анализ содержания марганца в подготовленных пробах почвы и фитомассы проводили рентгенофлуоресцентным способом на Спектроскане Макс-G.
Математическую обработку результатов эксперимента проводили с использованием ком- пьютерной программы Microsoft Excel. Рассчитывали среднее арифметическое, доверительный интервал, стандартное отклонение. Статистическая достоверность всех представленных результатов оценивалась с использованием t-критерия Стьюдента и составляла 95%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
Растительные культуры T. patula L. и P. australis культивировали в течение 24 суток на почвах, загрязнённых Mn2+, наблюдали за их ростом и развитием: измеряли высоту стебля, длину листьев, количество листьев, фиксировали у бархатцев появление бутонов. Результаты измерений приведены в табл. 1, из которой видно, что при концентрации Mn2+ 1 и 10 ПДК у бархатцев наблюдалось увеличение высоты стебля, при концентрации 30 ПДК - замедление роста стебля, нарушение развития листовых пластин, ускорение бутонообразования. У тростника при загрязнении почвы ионами марганца фиксировали увеличение длины листьев, отрицательного воздействия марганца на его рост и развитие не обнаружено.
Далее была проведена оценка фитореме-диационной способности растений. Для этого до и после их культивирования образцы почвы анализировали на валовое содержание марганца. Из данных, приведенных в табл. 2, видно, что в процессе культивирования бархатцев и тростника содержание марганца в почве уменьшается, это может свидетельствовать о накоплении металла в биомассе растений.
На рис. 1 приведены значения изменения концентрации марганца в почве в результате культивирования T. patula и P. аustralis, из которых видно, что, чем выше исходная масса марганца в почве, тем больше металла переходит из почвы в растение.
Рассчитана степень поглощения марганца T. patula и P. australis (рис. 2) по формуле (1):
Таблица 1. Изменение показателей роста растений при выращивании в почвах, содержащих ионы Mn2+, в течение 24 суток
|
Растение |
T. patula L |
P. australis |
|||||
|
Образцы почвы |
Изменение высоты стебля, см |
Изменение длины листьев, см |
Изменение кол-ва пар листьев |
Кол-во бутонов |
Изменение высоты стебля, см |
Изменение длины листьев, см |
Изменение кол-ва листьев |
|
К |
3,5±0,5 |
1,8±0,3 |
3±0,4 |
0 |
3,1±1,1 |
0,7±1,1 |
1±0,8 |
|
1 |
4,2±0,4 |
1,5±0,5 |
4±1,1 |
1зачаточный |
4,0±1,2 |
3,1±1,2 |
2±0,1 |
|
2 |
4,1±0,1 |
1,6±0,3 |
3±0,6 |
1зачаточный |
4,2±0,3 |
4,3±2,5 |
1±0,5 |
|
3 |
2,5±0,1 |
0,7±0,3 |
3±0,4 |
1бутон |
4,5±0,4 |
3,9±2,0 |
1±0,1 |
Таблица 2. Среднее содержание марганца в образцах почвы до и после культивирования T. patula L . и P. australis
|
Образцы почвы |
Масса марганца в почве (450 г) до начала эксперимента, мг |
Масса марганца в почве после культивирования T. patula L в мг |
Масса марганца в почве после культивирования P. australis в мг |
|
К |
3,1±0,1 |
1,8±0,3 |
1,8±0,9 |
|
1 |
66,1±1,2 |
64,3±1,4 |
61,4±2,0 |
|
2 |
633,1±5,1 |
617,5±6,5 |
601,9±11,5 |
|
3 |
1893,2±10,1 |
1826,8±11,5 |
1788,7±30,4 |
Э=(m1–m2)/m1•100%, (1)
где m1 – масса металла в почве до культивирования растений;
m2 – масса металла в почве после культивирования растений.
Из диаграммы (рис. 2) видно, что наибольшая степень поглощения марганца обоими видами растений зафиксирована в контрольных образцах с концентрацией 6,9 мг/кг, т.е. уже на начальной стадии вегетации на незагрязненных марганцем
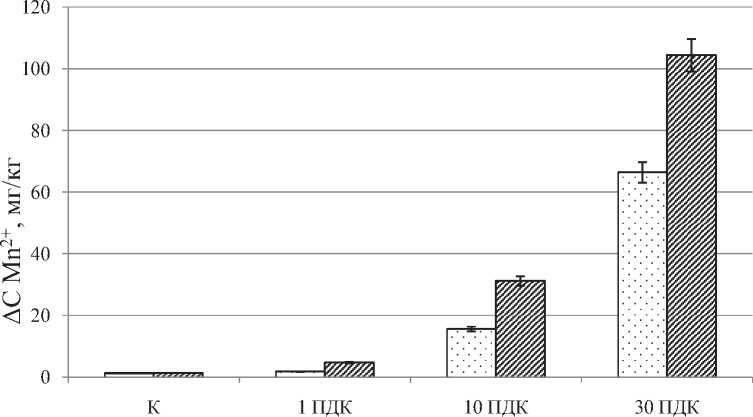
□ эксперимент с Т. patula L . И эксперимент с Р. australis
Рис. 1. Изменение концентрации марганца в почве (мг/кг) в результате культивирования T. patula L. и P. australis в зависимости от исходной концентрации Mn2+
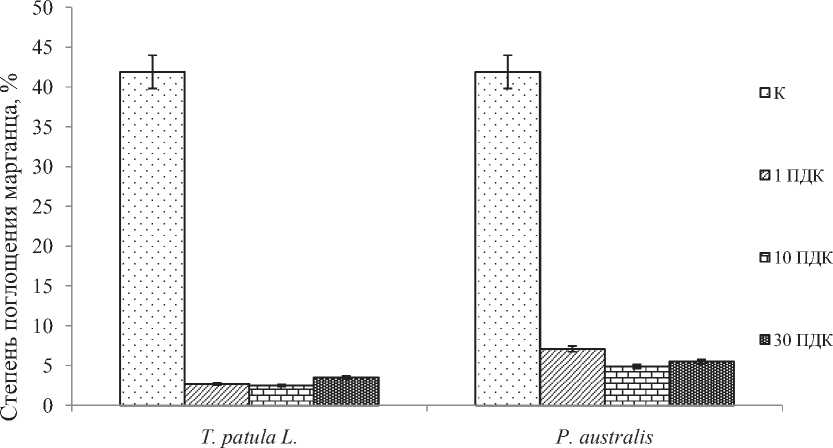
Рис. 2. Степень поглощения марганца T. patula и P. australis почвах растения используют более 40 % общего Mn для своего роста и развития. В случае загрязнения почв металлом на уровне 1, 10, 30 ПДК степень поглощения марганца бархатцами составляет 2,7, 2,5, 3,5%, тростником – 7,1, 4,9, 5,5%, поглощенный марганец растения используют в биохимических процессах.
Если принять, что изменение концентрации марганца в почве обусловлено его аккумуляцией в растительной культуре, можно рассчитать концентрацию (табл. 4) металла в сухой фитомассе (СMn., мг/г сух.веса) по формуле (2):
СMn.=(m1-m2)/ mраст, (2)
где m1 – масса марганца в почве до культивирования растений, мг;
m2 – масса марганца в почве после культивирования растений, мг;
mраст – масса растения, г.
Рассчитанные величины мы сравнили с результатами измерения концентрации марганца в фитомассе рентгенофлуоресцентным методом (табл. 3). Видно, что результаты
ВЫВОДЫ
При культивировании растений T. patula L. и P. australis в почвах, загрязненных сульфатом марганца (II) на уровне 1, 10 и 30 ПДК, в течение 24 суток нами установлено, что Mn2+ проявляет токсичность по отношению к бархатцам при концентрации 30 ПДК и не оказывает токсического действия на ростки тростника. Растения обладают способностью аккумулировать марганец в фитомассе, эффективность поглощения металла составляет 2,5-3,5% – у бархатцев и 4,9-7,1% – у тростника и мало зависит от степени загрязнения почвы. На незагрязненных почвах (C = 6,9 мг/кг) степень поглощения марганца составляет более 40%, что свидетельствует о быстром истощении микроэлемента в почве при выращивании рас- тительных культур.
Устойчивость бархатцев и тростника к высоким концентрациям марганца в почве, способность растений экстрагировать металл свидетельствует о возможности применения данных
Таблица 2. Среднее содержание марганца в образцах почвы до и после культивирования T. patula L . и P. australis
|
Образцы почвы |
Масса марганца в почве (450 г) до начала эксперимента, мг |
Масса марганца в почве после культивирования T. patula L в мг |
Масса марганца в почве после культивирования P. australis в мг |
|
К |
3,1±0,1 |
1,8±0,3 |
1,8±0,9 |
|
1 |
66,1±1,2 |
64,3±1,4 |
61,4±2,0 |
|
2 |
633,1±5,1 |
617,5±6,5 |
601,9±11,5 |
|
3 |
1893,2±10,1 |
1826,8±11,5 |
1788,7±30,4 |
Таблица 3. Расчетные и измеренные значения концентрации марганца в фитомассе T. patula L. и P. australis
Таким образом, установлено, что оба вида растений проявляют устойчивость к высоким концентрациям водорастворимых соединений марганца в почве. Токсический эффект марганца зафиксирован только при содержании его в почве на уровне 30 ПДК в отношении T. patula . Обнаружена способность растений аккумулировать ионы марганца (II), что определяет возможность их применения в фиторемедиационных мероприятиях.
культур в фиторемедиационных мероприятиях, например, T. patula L. – для очистки почв и индикации их загрязнения вблизи марганцевых обогатительных заводов, P. australis – на гидро-ботанических площадках очистных сооружений сточных вод металлургических предприятий.
Список литературы Влияние растворимых соединений марганца на высшие растения и оценка фитоэкстракционной способности растений
- Алексеев Ю.В. Тяжелые металлы в агроландшафте. СПб.: Изд-во ПИЯФ РАН, 2008. 2016 с.
- Васильев А.В., Дегтерева М.С. Источники загрязнения почвы и пути снижения их воздействия//Экология и безопасность жизнедеятельности промышленно-транспортных комплексов: Сбор. труд. мол. уч. I Международного экол. конгресса. 2007. С. 164-165
- Кабата-Пендиас А., Пендиас Х. Микроэлементы в почвах и растениях: Пер. с англ. М.: Мир, 1989. -439 с.
- Битюцкий, Н.П. Микроэлементы и растение: Учебное пособие. СПб.: Издательство Санкт-Петербургского университета. 1999. 232 с.
- Ковалевкий А.Л. Биогеохимия растений/отв. ред. В.М. Корсунов. Новосибирск: Наука. Сиб. отделение, 1991. 288 с.
- Фиторемедиация городских почв, загрязненных тяжелыми металлами, декоративными цветочными культурами/Гальченко С.В. и др.//Вестник Рязанского государственного университета им. С.А. Есенина. 2015. №4(49). С.144-153.
- ГН 2.1.7.2041-06. Предельно допустимые концентрации (ПДК) химических веществ в почве: Гигиенические нормативы. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2006. 15 с.
- ГОСТ Р ИСО 11464-2011 Качество почвы. Предварительная подготовка проб для физико-химического анализа, 2011. 16 с.
- Методика измерений массовой доли металлов в порошковых пробах растительных материалов рентгенофлуоресцентным методом с применением аппаратов рентгеновских для спектрального анализа СПЕКТРОСКАН МАКС (М-049-РМ/12). СПб., 2012. 12 с.


