Влияние различных групп синтетических пестицидов на развитие, выживаемость и антагонистическую активность некоторых видов аэробных спорообразующих бактерий
Автор: Тимофеева Марина Габдулгазизовна, Актуганов Глеб Эдуардович, Крутьков Владимир Михайлович, Галимзянова Наиля Фауатовна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Проблемы прикладной экологии
Статья в выпуске: 5-2 т.13, 2011 года.
Бесплатный доступ
Изучена устойчивость представителей различных таксономических групп бацилл-антагонистов к действию ряда синтетических гербицидов и фунгицидов in vitro. Выявлены различия во влиянии пестицидов на рост видов Bacillus subtilis, Paenibacillus ehimensis и P. polymyxa. Показана более высокая резистентность споровой культуры бактерий к химическим препаратам по сравнению с их вегетативными клетками. Выявлена зависимость между влиянием пестицидов на рост бактерий и продукцию ими антигрибных соединений.
Гербициды, фунгициды, микробный антагонизм, фитопатогенные грибы
Короткий адрес: https://sciup.org/148200396
IDR: 148200396 | УДК: 579.64:632.952:632.954
The influence of several groups of synthetic pesticides on growth, survival and antagonistic activity of some species of aerobic spore-forming bacteria
The resistance of strains from various taxonomic groups of antagonistic bacilli toward the number of synthetic herbicides and fungicides was studied in vitro. The specific differences were revealed in the influence of pesticides on growth of Bacillus subtilis, Paenibacillus ehimensis и P. polymyxa species. The higher tolerance of spore bacterial cultures was indicated in comparison with its vegetative cells. The dependence was found between the influence of pesticides on bacterial growth and its production of antifungal compounds.
Текст научной статьи Влияние различных групп синтетических пестицидов на развитие, выживаемость и антагонистическую активность некоторых видов аэробных спорообразующих бактерий
темы защиты в современном растениеводстве, призванный существенно снизить дозы применения химических препаратов [7-8]. Эффективность комбинированного применения биопрепаратов совместно с пестицидами во многом зависит от устойчивости их биологической составляющей к действующим веществам химических препаратов.
В связи с этим, при разработке биопрепаратов на основе новых штаммов бактерий-антагонистов оценка их резистентности к синтетическим пестицидам должна стать существенным критерием их отбора. Важным является и мониторинг индивидуальной чувствительности и совместимости компонентов уже существующих биопрепаратов с различными классами пестицидов, что позволит разработать скоординированный подход при совместном применении известных биологических и химических препаратов в интегрированной системе защиты растений.
Бактерии-антагонисты, относящиеся к родам Bacillus и Paenibacillus , широко используются в качестве основы многих биопрепаратов для защиты растений [9], однако сведения об их устойчивости к пестицидам остаются достаточно фрагментарными и малоизученными, равно как и оценка специфики влияния различных классов химических средств на таксономически близкие и удаленные виды этих бактерий [10].
Целью настоящей работы являлось изучение влияния ряда широко используемых в растениеводстве синтетических пестицидов, в т.ч. гербицидов и фунгицидов, на рост и выживаемость некоторых видов бацилл-антагонистов и продукцию ими анти-грибных соединений in vitro .
Практическая задача работы состояла в оценке перспектив и эффективности типовых представителей бактерий-антагонистов и препаратов на их основе в условиях комбинированного применения с различными химическими препаратами.
МАТЕРИАЛ И МЕТОДЫ
В качестве тест-объектов исследований использовали различные штаммы бацилл-антагонистов из коллекции ИБ УНЦ РАН, в том числе Bacillus subtilis ИБ-54, Paenibacillus ehimensis ИБ-739 и P. polymyxa ИБ-37, депонированные во Всероссийских коллекциях микроорганизмов и показывающие различную степень антагонистической активности к фитопатогенным грибам и отличающиеся по механизму защитного действия на растения. Бактериальные штаммы поддерживали на картофельном агаре (КА) при 37оС в течение 2-4 сут после засева, после чего хранили при комнатной температуре. Оценку антагонистической активности исследуемых штаммов проводили в отношении гриба – возбудителя корневой гнили злаковых Bipolaris sorokiniana Sacc. Shoemaker из коллекции ИБ УНЦ РАН. Степень подавления гриба оценивали методом диффузии в агар.
В качестве тестируемых гербицидов использовали растворимые в воде и полярных органических растворителях известные препаративные формы и действующие вещества, включая гранстар – коммерческий препарат на основе трибенуронметила (75% д.в.), глифосат, 2,4-Д (2,4-дихлорбензойная кислота), дикамба, клопиралид. В работе тестировали также препаративные формы и комбинированные препараты фунгицидов, применяемых в сельском хозяйстве, в том числе соединения триазолового ряда, включая пенконазол, тебуконазол (раксил), дифеноконазол (скор) и азарол (триади-мефон). Из комбинированных препаратов использовали коммерческий «Профит Голд», содержащий по 25% д.в. цимоксанила (1-(2-метоксимино-2-цианацетил)-3-этилмочевина) и фамаксадона, соответственно. Влияние пестицидов на рост бактерий изучали по изменения оптической плотности и титра бактериальной популяции после 1-2 сут культивирования в жидкой питательной среде в присутствии тестируемых препаратов. Бактерии предварительно культивировали в течение 18-24 ч в жидкой питательной среде следующего состава (г/л):
KH 2 PO 4 , 1,0; K 2 HPO 4 *3H 2 0, 0,5; (NH 4 ) 2 HPO 4 , 0,5; MgSO 4 *7H 2 O, 0,2; пептон ферментативный, 3,0; дрожжевой экстракт, 3,0; кукурузный экстракт, 3,0; глицерин, 5,0. Культивирование проводили в конических колбах объемом 250 мл на качалке УВМТ-12-250 при 36,5±0,5◦С и 165 об/мин. Ночную культуру вносили по 1 мл на 50 мл жидкой питательной среды того же состава. В опытные варианты вносили растворы пестицидов в стерильной дистиллированной воде для выявления степени роста бактерий в интервале концентраций, рекомендуемых для обработки растений в полевых условиях: гранстар – 0,008-0,024%; 2,4 – Д – 0,3-0,6%; глифосат – 0,51,0%; дикамба –0,024-0,037%; клопиралид – 0,10,2%; тебуконазол –0,24-0,3%; профит голд – 0,040,12%. Интенсивность развития бактерий в культуральной среде регистрировали на 1-е и 2-е сут культивирования по светорассеянию на спектрофотометре СФ-46 при 630 нм. В тестах на выживаемость для споровых культур использовали верхние пределы концентраций пестицидов: гранстар -0,024%; 2,4 – Д – 0,6%; глифосат – 2%; дикамба – 0,037%; клопиралид – 0,1%; тебуконазол – 0,3%; профит голд – 0,12%; азарол – 0,1%; дифеноконазол – 0,25%; пенконазол – 0,2%. В образцы добавляли по 1 мл 24-ч КЖ, 1 мл раствора пестицида и 8 мл 0,85% физиологического раствора. В контрольный образец вносили 1 мл 24-ч КЖ бактерий и 9 мл физиологического раствора. Образцы инкубировали 24 ч при комнатной температуре, затем высевали на титр на КА.
Эксперименты проводили в 3-кратной повторности. Статистическую обработку результатов проводили с помощью программы Origin 7.0 Pro и Excel-2007.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При испытании in vitro препаративных форм гербицидов и фунгицидов штаммы B. subtilis ИБ-54 и P. ehimensis ИБ-739 проявляли более высокую стабильность по сравнению со штаммом P. po-lymyxa ИБ-37, что, возможно, отчасти связано с их более высокой скоростью роста (рис. 1).
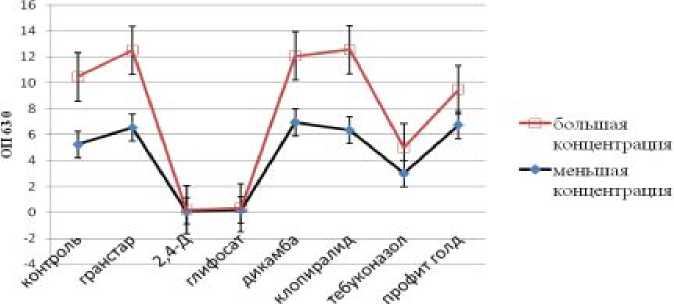
Рис. 1. Кривые устойчивости B. subtilis ИБ-54 к рекомендуемым верхним и нижним пороговым концентрациям некоторых синтетических пестицидов, используемым для обработки в полевых условиях.
Рост двух первых штаммов резко снижался в присутствии 2,4-Д, глифосата и, отчасти, тебукона- зола, тогда как развитие P. polymyxa не испытывало влияния только со стороны препаратов Гранстар (трибенуронметил) и Профит Голд. Следует отме тить, что среди гербицидов дикамба, а среди фунгицидов Профит Голд при своей нижней пороговой концентрации даже активировали рост B. subtilis на
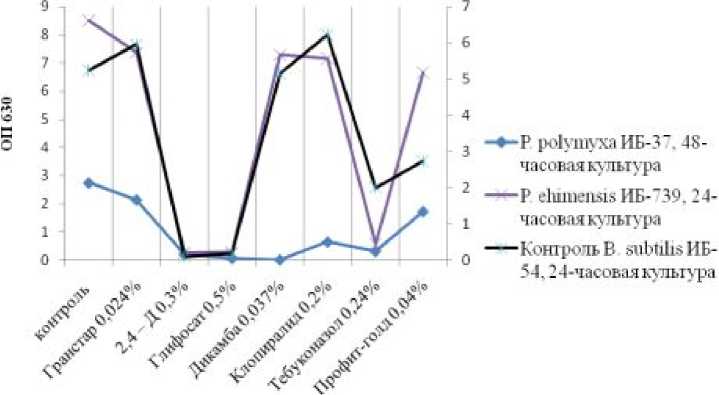
33% и 28%, соответственно, тогда как при верхней пороговой концентрации их действие носило угне- тающий характер (снижение роста на 4,4% и 48%, соответственно) (рис. 2). Стимулирующее влияние на B. subtilis было отмечено также для препарата
Гранстар и клопиралида (24% и 19% соответственно).
* ti> / 4? 01»
X X Z
-♦“Р polymyxaИБ-37,48-часовая культура
---Р elmneiuis ИБ-739, 24часовая культура
---Контроль В subtilis ИБ-
54,24-часовая культура
Рис. 2. Сравнительная устойчивость антагонистических штаммов различных таксономических групп бацилл к верхней пороговой концентрации некоторых коммерческих препаратов гербицидов и фунгицидов.
Известна способность некоторых гербицидов стимулировать рост бактерий. В частности такая активность была выявлена у нитралина в опыте с Pseudomonas fluorescens [11]. Среди тестируемых гербицидов в наибольшей степени рост B. subtilis подавляли 2,4-Д и глифосат, при этом снижение титра бактерий составляло 98 и 96%. Штамм P. polymyxa ИБ-37 проявлял наибольшую чувствительность к действию большинства гербицидов, интенсивность роста этой культуры в присутствии всех препаратов снижалась в среднем на 80-95% (рис. 2). Таким образом, в плане пестицидной устойчивости бактерии B. subtilis в данных условиях были более резистентными. При этом рост всех групп бактерий резко подавлялся в присутствии 2,4-Д и глифосата. В целом кривые влияния гербицидов на штаммы различных таксономических групп бацилл имели сходный характер.
При оценке влияния пестицидов на антигриб-ную активность (уровень продукции антигрибных соединений) бацилл-антагонистов in vitro в качестве основного тест-объекта использовали наиболее устойчивый штамм B. subtilis ИБ-54. Для этого надосадочную жидкость, полученную из культуральной среды штамма после 24 ч культивирования в присутствии различных химических препаратов оценивали на степень подавления фитопатогенного гриба B. sorokiniana (рис. 3). Как видно из рис. 3, синтез активных соединений изучаемым штаммом резко снижался в присутствии 2,4-Д и глифосата вследствие подавления его роста и гибели большей части клеток. Значительное повышение антигриб-ной активности вторичных метаболитов B. subtilis ИБ-54 в присутствии нижней пороговой концентрации таких гербицидов, как клопиралид и дикам-ба, и верхней пороговой концентрации препарата Гранстар могло объясняться более интенсивным ростом штамма в этих условиях, как было обнаружено ранее. Микроскопия 24-ч культуры B. subtilis ИБ-54 подтвердила низкую чувствительность его клеток к клопиралиду. В присутствии 0,04% препарата Профит Голд (по 25% д.в. фамаксадона и ци-моксанида) наблюдалось почти 2-кратное повышение антигрибной активности B. subtilis ИБ-54, которое может быть связано как с увеличением интенсивности роста бактерий в этих условиях, так и дополнительным фунгицидным эффектом самого препарата, присутствующего в культуральной среде. С другой стороны, при верхней пороговой концентрации Профит Голд (0,08%) наблюдалось заметное снижение роста и активности штамма, что ставит под сомнение аддитивный эффект этого препарата (рис. 3). Это подтверждалось и при оценке влияния другого синтетического фунгицида - тебуконазола, который сильно снижал рост и ан-тигрибную активность B. subtilis ИБ-54, не оказывая дополнительного собственного эффекта на B. sorokiniana.
i i +клопиралид, 0,02%
।* +клопиралид, 0,01% i—|—। +Фамаксадон и цимоксанид, 0,08%
+Фамаксадон и цимоксанид, 0,04% нф
+роксацин, 0,5 мл/л КЖ ф +тебуконазол, 0,30% нф +тебуконазол, 0,24%
-ф —। +дикамба, 0,037%
1----1----1 +дикамба, 0,024% ф +глифосат, 1,0%
1—Я —1 +глифосат, 0,5%
।—| —। +2,4-Д, 0,060%
---1 +2,4-Д, 0,030%
Ф +Трибенуронметил (Гранстар), 0,024%
।----1 ----1 +Трибенуронметил (Гранстар), 0,008%
। |-----1 Контроль B. subtilis ИБ-54
—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I—I 0 200 400 600 800 1000
Средняя площадь зоны подавления развития Bipolaris sorokiniana вокруг лунки с 0,1 мл супернанта КЖ
Рис. 3. Влияние внесения синтетических гербицидов и фунгицидов на антигрибную активность внеклеточных метаболитов 24-часой культуры B. subtilis ИБ-54.
Как показали полученные результаты оценки выживания споровой культуры бацилл-антагонистов при инкубации в присутствии синтетических гербицидов/фунгицидов и в условиях отсутствия активного роста, эндоспоры большинства штаммов показывали существенно более высокую устойчивость в сравнении с вегетативными клетками. Однако, следует отметить, что как и в случае активного роста бактерий, наибольшее влияние на выживаемость споровых культур оказывали 2,4-Д и глифосат. Инкубация в течение суток при комнатной температуре в присутствии этих препаратов приводила к снижению титра споровых культур различных штаммов в среднем на один порядок (рис. 4). Наименьшую индивидуальную чувствительность к этим препаратам проявлял штамм P. ehimensis ИБ-739.
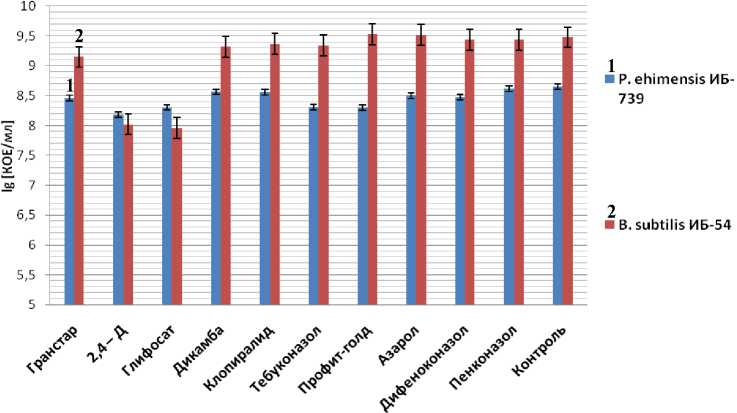
Рис. 4. Влияние синтетических гербицидов и фунгицидов на споровую культуру бацилл-антагонистов
Наименьшим бактерицидным действием на эндоспоры всех тестируемых штаммов характеризовались фунгцидные препараты - Профит Голд, Азарол (триадимефон), дифеноконазол и пенкона- зол (рис. 4). Полученные результаты свидетельствуют об относительной устойчивости споровых культур бацилл к большинству испытанных пестицидов, за частичным исключением 2,4-Д и глифо- сата, что демонстрирует возможность эффективного применения биопрепаратов на основе споровой культуры наиболее активных штаммов совместно с протравителями и гербицидами в комплексной защите растительных культур. Однако для оценки эффективности комбинированного применения синтетических фунгицидов с биопрепаратами была необходима дальнейшая проверка их совместного действия на фитопатогенные грибы in vitro.
Список литературы Влияние различных групп синтетических пестицидов на развитие, выживаемость и антагонистическую активность некоторых видов аэробных спорообразующих бактерий
- Журавлева Н.В., Лукьянов П.А. Хитинолитические ферменты: источники, характеристика и применение в биотехнологии//Вестник ДВО РАН. 2004. № 3. С. 76-86.
- Желдакова Р. А., Мямин В. Е. Фитопатогенные микроорганизмы. Минск: Изд. БГУ, 2006. 116 с.
- Волкова Д.А. и др. Изменение биологической активности почвы под влиянием пестицидов. Кишинев: Штиинца, 1984. С. 79-90.
- Migamoto Ed. J., Kearney P.С. Pesticides chemistry: Human Welfare and the Environment. Oxford: Pergamon Press, 1983. 429 p.
- Федоров Л.А., Яблоков А.В. Пестициды: токсический удар по биосфере и человеку. М.: Наука, 1999. 462 с.
- Злотников А.К., Злотников К.М. Борьба с пестицидным стрессом -важный резерв повышения продуктивности пшеницы//Земледелие. 2009. № 4. С. 30-31.
- Гончаров Н.Р. Развитие инновационных процессов в защите растений//Защита и карантин растений. 2010. № 4. С. 4-8.
- Самойлов Ю.К. Перспективы развития микробиометода//Защита и карантин растений. 2008. № 9. С. 47-48.
- McSpadden Gardener B. Ecology of Bacillus and Paenibacillus spp. in agricultural systems//Phytopathology. 2004. V. 94. № 11. P. 1253-1258.
- Singh A.K., Ghodke I. and Chhatpar H.S. Pesticide tolerance of Paenibacillus sp. and its chitinase//J. Environ. Management. 2009. V. 91. №. 2. P. 358-362.
- Breazeale F. W., Сamper N. D. Effect of Selected Herbicides on Bacterial Growth Rates//Appl. Microbiology. 1972. V. 23. № 2. Р. 431-432.


