Влияние совместного применения медного хлорофиллина, глутатиона и гидролизата плаценты на физиологические параметры и выживаемость мышей при остром облучении
Автор: Ромодин Л.А., Никитенко О.В., Бычкова Т.М., Московский А.А., Тюкалова О.М., Ильязов Р.Г.
Рубрика: Научные статьи
Статья в выпуске: 2 т.34, 2025 года.
Бесплатный доступ
Поиск эффективных и безопасных способов коррекции лучевого синдрома остаётся актуальным направлением исследований. В ходе многочисленных работ, проведённых ранее, не удалось обнаружить одновременно эффективный и безопасный противолучевой препарат. Поэтому перспективным представляется разработка терапевтических схем лечения лучевой болезни, предполагающих совместное использование нескольких препаратов. В настоящей работе на самцах мышей ICR (CD-1), подвергнутых разовому воздействию рентгеновским излучением в дозе 6,5 Гр, мы оценили эффективность терапевтической схемы, предполагающей применение медного хлорофиллина в дозировке 100 мкг/г массы тела за 20-30 мин до облучения, глутатиона в дозировке 200 мкг/г через 30 мин после облучения и препарата «Лаеннек» (гидролизат плаценты человека) в дозировке 560 мкг/г через 1, 2, 3 и 4 сут после облучения и в дозировке 112 мкг/г через 8, 9, 10 и 11 сут после облучения. Эффективность применения данной схемы оценивали на основании 30-суточной выживаемости и следующих показателей через 4 и 7 сут после облучения: массы тимуса и селезёнки, гематологических показателей (лейкоциты, эритроциты, тромбоциты, гемоглобин, гематокрит, тромбокрит), количества ядросодержащих клеток в костном мозге. Применение данной схемы не способствовало облегчению течения лучевой болезни. Хотя в литературе и в наших более ранних исследованиях данные препараты по отдельности проявляли радиозащитные свойства. Полученный результат мы объясняем несовместимостью фармакологических эффектов исследуемых препаратов. По нашему мнению, это связано с токсическими свойствами медного хлорофиллина. Таким образом, настоящая работа актуализирует дальнейшие исследования возможности совместного применения различных веществ для коррекции лучевого синдрома с изучением вклада каждого вещества в складывающуюся в итоге общую клиническую картину.
Ионизирующее излучение, рентгеновское излучение, хлорофиллин, глутатион, гидролизат плаценты, лаеннек, мыши, гематология, выживаемость, радиобиология
Короткий адрес: https://sciup.org/170209564
IDR: 170209564 | УДК: 539.1.047:599.323.4 | DOI: 10.21870/0131-3878-2025-34-2-50-62
The effect of the combined use of copper chlorophyllin, glutathione and placenta hydrolysate on the physiological parameters and survival of mice under acute irradiation
The search for effective and safe ways to correct radiation syndrome remains a relevant area of research. In the course of numerous studies carried out previously, it was not possible to discover both an effective and safe anti-radiation drug. Therefore, it seems promising to develop therapeutic regimens for the treatment of radiation sickness that involve the combined use of several drugs. In this study, using male ICR (CD-1) mice exposed to a single exposure to X-ray radiation at a dose of 6.5 Gy, we assessed the effectiveness of a therapeutic regimen involving the use of copper chlorophyllin at a dosage of 100 μg/g body weight 20-30 minutes before irradiation , glutathione at a dosage of 200 μg/g 30 minutes after irradiation and the drug “Laennec” (hydrolyzed human placenta) at a dosage of 560 μg/g 1, 2, 3 and 4 days after irradiation and at a dosage of 112 μg/g after 8, 9, 10 and 11 days after irradiation. We assessed the effectiveness of this scheme on the basis of 30-day survival and on the basis of the following indicators 4 days and 7 days after irradiation: weight of the thymus and spleen, hematological parameters (leukocytes, erythrocytes, platelets, hemoglobin, hematocrit, thrombocrit), the number of nucleated cells in the bone marrow. The use of this regimen did not help alleviate the course of radiation sickness. Although in the literature and in our earlier studies, these drugs individually showed radioprotective properties. We explain the obtained result by the incompatibility of the pharmacological effects of the studied drugs. In our opinion, this is due to the toxic properties of copper chlorophyllin. Thus, this work actualizes further research into the possibility of joint use of various substances for the correction of radiation syndrome with the study of the contribution of each substance to the resulting overall clinical picture.
Текст научной статьи Влияние совместного применения медного хлорофиллина, глутатиона и гидролизата плаценты на физиологические параметры и выживаемость мышей при остром облучении
Поиск эффективных и безопасных способов коррекции лучевого синдрома продолжает оставаться актуальным направлением исследований. В ходе многочисленных работ в этой области, проведённых ранее и посвящённых изучению радиозащитных свойств различных препаратов по отдельности, не удалось обнаружить безопасный препарат, который бы эффективно защищал от воздействия радиации и не проявлял при этом токсического действия [1-3]. Поэтому перспективным представляется разработка терапевтических схем лечения лучевой болезни, предполагающих совместное использование нескольких препаратов с различными свойствами и механизмом действия.
В последнее время в литературе всё больше сообщений о том, что при разработке противолучевых средств целесообразно использовать малотоксичные, так называемые природные,
соединения, многие из которых являются естественными метаболитами [1-3]. По причине высокой роли естественной антиоксидантной системы клеток в защите клеточных структур от различных свободнорадикальных реакций [4, 5], играющих ключевую роль в реализации биологического действия ионизирующего излучения [5, 6], перспективным представляется использование антиоксидантов для облегчения течения лучевой болезни.
В естественной системе антиоксидантной защиты клетки большую роль играет глутатион. Данное соединение обеспечивает восстановление биомолекул, подвергшихся атаке свободных радикалов [7, 8]. В норме его концентрация в цитоплазме настолько высока, что позволяет восстанавливать любую окисленную HS-группу [8]. Однако при действии ионизирующего излучения наблюдается резкий спад антиоксидантного потенциала клеток за счёт снижения концентрации антиоксидантов [5]. И в этой связи введение глутатиона для коррекции лучевого синдрома выглядит оправданным. Тем более, что в литературе имеются сведения о радиозащитном эффекте экзогенного глутатиона [9].
В литературе достаточно много информации о радиозащитных свойствах водорастворимого производного зелёного пигмента растений хлорофилла – хлорофиллина [10, 11]. В нашей недавней работе [12] для медного хлорофиллина мы определили значение фактора изменения дозы (ФИД) – отношения дозы ионизирующего излучения для получивших данный радиозащит-ный препарат животных к равноэффективной дозе для животных, не получавших препарат, – при профилактическом внутрибрюшинном (в/б) введении мышам в дозировке 100 мкг/г массы тела. Оно составило 1,1. Данное значение нельзя считать высоким. Однако полагаем, что радиозащит-ный эффект хлорофиллина можно усилить за счёт применения других соединений, обладающих радиозащитными свойствами. И в первую очередь мы решили изучить возможность совместного использования глутатиона и хлорофиллина.
Данная терапевтическая схема предполагает введение хлорофиллина в дозировке 100 мкг/г массы тела до облучения, аналогично тому, как это было работе [12], и введение глутатиона в дозировке 200 мкг/г после облучения. При составлении данной схемы руководствовались тем, что введение восстановленного глутатиона после облучения приведёт к росту его концентрации в пострадавших от облучения клетках с пониженной его концентрацией. А это, в свою очередь, должно привести к более эффективной работе антиоксидантной системы защиты клеток. Дозировка глутатиона, равная 200 мкг/г, составляет примерно двадцатую часть от ЛД 50 глутатиона при в/б введении мышам, поэтому указанную дозировку можно считать безопасной с точки зрения химической токсичности данного вещества [13].
В информационном поле, правда, в большей степени в рекламной и публицистической его части, много информации о целебных свойствах плаценты и различных произведённых из неё препаратов. В описании терапии препаратом «Лаеннек» производства Japan Bio Products на сайтах ряда клиник прямо указывается, что он был разработан как средство лечения лучевой болезни. По данной причине мы включили указанный препарат в тестируемую в настоящем исследовании схему терапии лучевого синдрома.
В научной литературе также есть сообщения о радиозащитных свойствах гидролизата плаценты. Так, авторы исследования [14] изучали защитные свойства гидролизата плаценты при применении против энтеропатий, вызванных облучением в дозе 10 Гр. Указанный эксперимент проводился на мышах C57BL/6, которым один раз в день в течение 5 дней в/б вводили гидролизат плаценты, облучая их через 1 ч после последней инъекции. И в описываемом исследовании гидролизат плаценты дозозависимо снижал число апоптотических клеток, смягчая действие радиации на крипты Либеркюна в тощей кишке мышей. Данный эффект авторы [14] связывают со способностью гидролизата плаценты стимулировать регенерацию тканей, ссылаясь на работу авторов [15], показавших интенсификацию регенерации повреждённых аксонов седалищного нерва за счёт усиления синтеза белковых факторов: GAP-43, обеспечивающего развитие нейронов и синапсов, и циклин-зависимой киназы 2 (Cdc2). Последняя играет ключевой роль при переходе от G2-фазы клеточного цикла к делению [15].
Авторы работы [16] сообщают о выраженных гепатопротекторных свойствах препарата гидролизата плаценты при неалкогольном поражении печени: концентрации аспартатаминотрансферазы, аланинаминотрансферазы и гамма-глутамилтрансферазы возвратились к нормальным значениям. Пациенты, получавшие гидролизат плаценты, свидетельствовали об улучшении общего самочувствия. В случае алкогольного или лекарственного поражения печени гепато-протекторные свойства гидролизата плаценты сохраняются [17]. О снижении выраженности жировой дистрофии печени на фоне применения препарата Лаеннек сообщают авторы работы [18]. Нефропротекторные свойства данного препарата проявляются в снижении воспаления, анти-стрессорных эффектах и предотвращении фибротических изменений ткани почек за счёт наличия в его составе фрагментов нефропротекторных адреномедуллинов, пептидов-ингибиторов ряда киназ (FYN, SHH, WNK1/4, SGK1, IRAK4, ROCK1/2) и фиброгенных рецепторов (PDGFR, TGFB1I1) [19]. Описанные эффекты препарата гидролизата плаценты могут обуславливать его способность смягчать постковидный синдром [20], а также синдром хронической усталости, что сопровождается снижением ситуативных депрессии и тревоги, улучшением субъективных оценок качества жизни, а также достоверным повышением значений индикаторов физической работоспособности: максимального потребления кислорода, анаэробного порога, времени нагрузки до отказа [21].
Анализируя эти данные, мы больше склоняемся к определению гидролизата плаценты не как классического радиопротектора, применяемого непосредственно разово перед облучением, а радиомодулятора-адаптогена, повышающего регенеративный потенциал организма, а потому способного проявить защитный эффект и после облучения [22]. А, так как особенностью адапто-генов является «накопительный эффект», обуславливающий рекомендацию применять данные препараты многократно, курсом [22, 23], мы вводили гидролизат плаценты на протяжении нескольких дней.
Целью настоящего исследования была оценка радиозащитного эффекта совместного применения медного хлорофиллина, глутатиона и гидролизата плаценты (коммерческий препарат Лаеннек) при разовом воздействии на самцов мышей рентгеновского излучения в дозе 6,5 Гр. Применяемая схема предполагала введение медного хлорофиллина перед облучением для возможности проявления им показанных нами ранее радиопротекторных свойств [12], глутатиона - после облучения, что может способствовать исправлению выведенного радиацией из равновесия баланса прооксидантов и антиоксидантов в пользу последних [7, 8], гидролизата плаценты - на протяжении нескольких дней после облучения (табл. 1), это должно было способствовать общему укреплению организма и ускорению его восстановления после облучения, в соответствии с представленными в литературе данными [14, 15, 18, 20].
Материалы и методы
Эксперименты были выполнены на аутбредных самцах мышей линии ICR (CD-1) SPF-категории (массой 34,6 ± 0,2 г), полученных из питомника лабораторных животных Российской академии наук (Пущино). Однократное кратковременное одностороннее тотальное облучение мышей осуществляли на рентгеновской биологической установке РУБ РУСТ-М1 (Россия), мощность дозы в контейнере с мышами составляла 0,85 Гр/мин ± 10%, анодное напряжение – 200 кВ, алюминиевый фильтр – 1,5 мм, доза излучения – 6,5 Гр.
В качестве изучаемых препаратов в составе терапевтической схемы использовали: медный хлорофиллин (Macklin, Китай) при в/б введении в объёме 0,32 мл, глутатион (препарат Гла-тион производства Шаньдун Луи Фармасьютикал, Китай) при в/б введении в объёме 0,32 мл, гидролизат плаценты человека (препарат Лаеннек, Japan Bio Products, Япония, приобретён у поставщика ООО «ТД-Фарм») при в/б введении в объёме 0,32 мл. Мышам из группы облучённого контроля вводили 0,2% раствор уротропина, который выступал в роли среды для растворения всех используемых препаратов, в объёме 0,32 мл.
В табл. 1 приведены сведения о дозировках и сроках введения используемых препаратов, а также о времени эвтаназии животных для проведения гематологического исследования. На основании информации о низкой токсичности препарата гидролизата плаценты во всех источниках [14-20] применяли его в относительно высоких дозировках, указанных в табл. 1.
Таблица 1
Схема введения препаратов с указанием дней эвтаназии некоторых мышей из экспериментальных групп для проведения гематологического исследования
|
Дни после облучения |
Группа I Виварный контроль |
Группа II Облучённый контроль |
Группа III Экспериментальная группа |
|
0 |
- |
Раствор уротропина за 15-20 мин до облучения; облучение в дозе 6,5 Гр |
Медный хлорофиллин, 100 мкг/г, за 20-30 мин до облучения; облучение в дозе 6,5 Гр; глутатион, 200 мкг/г, 30 мин после облучения |
|
1 |
- |
- |
Лаеннек, 560 мкг/г |
|
2 |
- |
- |
Лаеннек, 560 мкг/г |
|
3 |
- |
- |
Лаеннек, 560 мкг/г |
|
4 |
Эвтаназия 5 мышей |
Эвтаназия 5 мышей |
Эвтаназия 5 мышей; Лаеннек, 560 мкг/г |
|
5 и 6 |
- |
- |
- |
|
7 |
Эвтаназия 5 мышей |
Эвтаназия 5 мышей |
Эвтаназия 5 мышей |
|
8-11 |
- |
- |
Лаеннек, 112 мкг/г |
Выживаемость мышей оценивали в течение 30 сут после облучения. Кумулятивную долю выживших животных рассчитывали по Каплану-Майеру [24]. Кривые выживаемости были проанализированы log-rank тестом – сравнение выживаемости групп с учётом всего периода наблюдения. Статистически значимыми считали различия при p(log-rank test)<0,05.
В эксперименте было задействовано 90 мышей: 60 – для оценки 30-суточной выживаемости, 30 – для оценки изучаемых физиологических показателей. Последнее проводилось посредством эвтаназии 5 мышей из каждой экспериментальной группы с использованием следующих показателей: массы тимуса и селезёнки, параметров крови (содержания лейкоцитов, эритроцитов, тромбоцитов, уровня гемоглобина, процента гематокрита, тромбокрита), количества ядросодержащих клеток в костном мозге – через 4 и 7 дней после облучения.
Определение массы тимуса и селезёнки производили взвешиванием на электронных весах OHAUS Adventurer AR3130 (OHAUS Corporation, Швейцария) с ценой деления 1 мг. Определение форменных элементов крови производилось с помощью ветеринарного гематологического анализатора Mindray BC-2800 Vet (Китай).
Определение количества кариоцитов в костном мозге (п х 10 6 ядросодержащих клеток на бедро) проводили следующим образом. Очищенную от мышцы бедренную кость животного промывали 5% раствором уксусной кислоты объёмом 4 мл, вымывая содержимое кости шприцем, а затем подсчитывали число ядросодержащих клеток в камере Горяева. Считали клетки костного мозга при малом увеличении (объектив х 8 или х 9, окуляр х 10 или х 15). Подсчёт производился в 5 больших квадратах, разделённых на 16 маленьких. Полученное число умножали на 0,2. Так получали число клеток костного мозга в бедренной кости мыши [25].
Статистический анализ полученных результатов проводили общепринятыми методами вариационной статистики (U-критерий Манна-Уитни). Данные представлены в виде среднего зна-чения ± ошибка среднего (M ± m). Различия считали значимыми при p<0,01.
Результаты и их обсуждение
Изучаемая нами схема коррекции лучевого синдрома не дала положительных результатов. Её применение не смогло повысить количество ядросодержащих клеток костного мозга, лейкоцитов и тромбоцитов в крови, по сравнению с группой облучённого контроля.
Рис. 1 иллюстрирует данные по количеству ядросодержащих клеток в костном мозге бедренной кости, числу лейкоцитов и тромбоцитов в крови через 4 и 7 дней после облучения в дозе 6,5 Гр. В табл. 2 представлены сведения о массе селезёнки и тимуса, гематокрите, тромбокрите и концентрации гемоглобина в крови мышей в указанные сроки после радиационного воздействия.
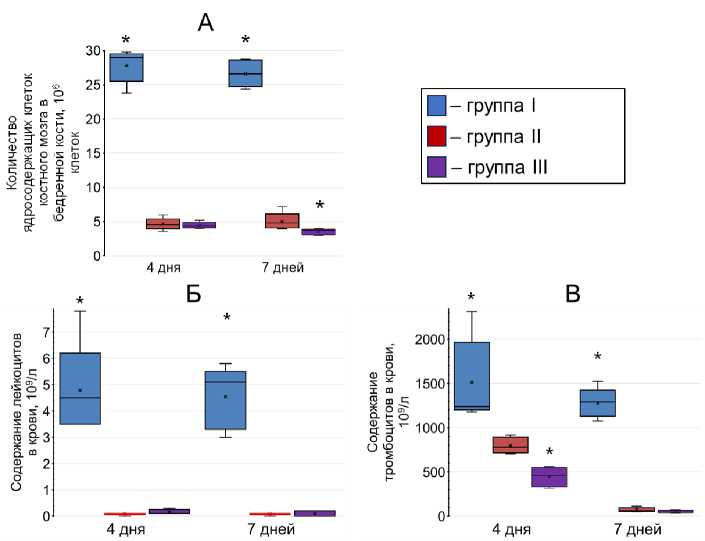
Рис. 1. Сравнение различающихся изучаемых физиологических параметров через 4 и 7 дней после воздействия рентгеновским излучением в дозе 6,5 Гр на мышей из групп виварного (синие прямоугольники) и облучённого (красные прямоугольники) контролей и облучённых мышей, которым вводили хлорофиллин перед облучением, глутатион через 30 мин после облучения с последующими суточными интервалами четырьмя введениями гидролизата плаценты в дозировке 560 мкг/г (фиолетовые прямоугольники).
* – статистически значимое (U-критерий Манна-Уитни, p<0,01) отличие от группы облучённого контроля.
Таблица 2
Сведения о массе тимуса и селезёнки, гематокрите, тромбокрите и уровне гемоглобина у экспериментальных животных через 4 и 7 дней после воздействия рентгеновским излучением в дозе 6,5 Гр
|
Группа |
Число дней, прошедших с момента облучения |
Масса селезёнки, мг |
Масса тимуса, мг |
Гематокрит, % |
Тромбокрит, % |
Концентрация гемоглобина, г/л |
|
1 |
4 |
191,8±37,4 |
49,8±9,8 |
43,3±1,5 |
0,5±0,006 |
135±4,6 |
|
7 |
136,2±15,9 |
65,8±10,1 |
43±0,4 |
0,5±0,03 |
145,4±1,8 |
|
|
II |
4 |
32,2±3,0 |
13,6±2,7 |
41,2±0,7 |
0,3±0,02 |
130,4±2,4 |
|
7 |
29,4±1,6 |
23±2,3 |
39,6±1,6 |
0,04±0,01 |
132,6±5,4 |
|
|
III |
4 |
40,8±3,1 |
9,6±1,7 |
40,4±2,6 |
0,2±0,03 |
126,8±8,6 |
|
7 |
31,2±3,2 |
15±1,9* |
34,2±0,8 |
0,03±0,004 |
111±3,3** |
Примечание: * – статистически значимая разница с группой II (в соответствующие сутки), p≤0,05;
** – статистически значимая разница по сравнению с группой II (в соответствующие сутки), p≤0,01.
На основании представленных в табл. 2 и на рис. 1 данных можно говорить, что острое воздействие рентгеновским излучением в дозе 6,5 Гр привело к статистически значимому снижению массы тимуса и селезёнки, числа ядросодержащих клеток костного мозга в бедренной кости, количества лейкоцитов и тромбоцитов, а также уровня гематокрита, тромбокрита и гемоглобина в периферической крови по сравнению с группой виварного контроля. По показателю уровня тромбоцитов на 4-е сут после облучения отмечено статистически значимое снижение в группе III по сравнению с группой II (U-критерий Манна-Уитни, p ≤ 0,01). На 7-е сут после облучения в дозе 6,5 Гр было отмечено статистически значимое снижение в группе III по сравнению с группой II по количеству ядросодержащих клеток костного мозга в бедренной кости (U-критерий Манна-Уитни, p ≤ 0,01). Отмечено статистически значимое снижение по концентрации гемоглобина в крови в группе III по сравнению с группой облучённого контроля (II, U-критерий Манна-Уитни, p ≤ 0,01) на 7-е сут после облучения. В остальных случаях статистически значимой разницы отмечено не было.
В рамках настоящей работы было проведено исследование влияния изучаемой терапевтической схемы на выживаемость мышей, подвергнутых воздействию рентгеновского излучения в дозе 6,5 Гр в течение 30 сут после облучения. Полученные сведения о доле выживших животных и средней продолжительности жизни погибших облучённых мышей можно считать адекватными, т.к. к концу периода наблюдения выжили все животные из группы виварного контроля, а на протяжении всего этого времени не было зафиксировано каких-либо признаков ухудшения их самочувствия.
Изучаемая в настоящей работе терапевтическая схема коррекции лучевого синдрома, вызванного облучением мышей в летальной (6,5 Гр) дозе, не обеспечила повышения выживаемости мышей по сравнению с группой облучённого контроля (рис. 2, log-rank test, p=0,86).
При этом, ранее мы установили, что медный хлорофиллин при аналогичном для настоящего исследования способе применения обладает хоть и незначительными, но достоверными радиопротекторными свойствами: ФИД для данного вещества равен 1,1 [12]. Т.е. на основании полученных в настоящей работе данных можно говорить о том, что применение глутатиона или гидролизата плаценты после использования медного хлорофиллина убирает радиозащитный эффект последнего.
Как уже указывалось выше, применение гидролизата плаценты [14] и экзогенного глутатиона [9] по отдельности также характеризуется радиозащитным эффектом. Но данный эффект исчезает при введении медного хлорофиллина перед облучением, т.е. при совместном применении данных веществ их фармакологическое взаимодействие приводит к потере тех радиоза-щитных свойств, которые проявляют данные препараты по отдельности. Под фармакологическим взаимодействием мы понимаем не столько непосредственные химические реакции между веществами, введёнными в организм (хотя этот аспект тоже входит в это понятие), сколько результат от совокупности реакций организма на введённые препараты.
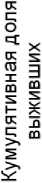
Время после облучения, сутки
Рис. 2. Динамика выживаемости самцов мышей ICR (CD-1) по Каплану-Майеру после воздействия рентгеновского излучения в дозе 6,5 Гр.
В препарате гидролизата плаценты содержится большое число различных веществ, среди которых много олигопептидов, витаминов и антиоксидантов, сигнальных ростовых факторов [15]. Глутатион является одним из главных, если не основным, антиоксидантом клетки [7, 8]. По логике в препарате гидролизата плаценты также должно содержаться относительно много глутатиона. Поэтому весьма маловероятно, что сочетание гидролизата плаценты и чистого препарата глутатиона могло снижать до нуля радиозащитные свойства обоих препаратов.
Отсутствие радиозащитного эффекта изучаемой терапевтической схемы, скорее всего, обусловлено фармакологическим взаимодействием медного хлорофиллина и глутатиона или хлорофиллина и суммарно глутатиона и гидролизата плаценты. Однако не исключено, что при ином способе применения, например, в случае существенно более длительного курса, гидролизат плаценты может оказать некоторый защитный эффект. Но, тем не менее, уже на основании нашего исследования понятно, что величина данного эффекта будет незначительной и существенно более низкой, чем у табельных радиопротекторов.
Согласно паспорту безопасности медного хлорофиллина данное вещество при пероральном применении является практически нетоксичным: ЛД 50 при в/б введении мышам составляет 7000 мкг/г массы тела. На основании данной информации можно сделать вывод о полной безопасности применения медного хлорофиллина с точки зрения химической токсичности. Однако результаты нашего недавнего исследования [26] токсичности данного вещества при в/б введении мышам показали, что ЛД 50 медного хлорофиллина при данном способе применения составляет всего лишь 633 ± 37,2 мкг/г. Скорее всего, данный относительно высокий показатель химической токсичности обусловлен наличием в составе молекулы данного вещества атома меди. Однако конкретные механизмы реализации токсического действия медного хлорофиллина не изучались. Поэтому говорить о возможных путях его фармакологического взаимодействия с другими препаратами невозможно. В то же время, именно данное взаимодействие, скорее всего, приводит к потере радиозащитных свойств и медного хлорофиллина, и других изучаемых в настоящей работе препаратов.
Совместное влияние данных препаратов на фоне облучения усугубляет тромбоцитопению через 4 дня после него (рис. 1В), а через 7 дней после облучения наблюдается снижение числа ядросодержащих клеток в костном мозге бедренной кости по сравнению с группой облучённого контроля (рис. 1А). Это можно объяснить негативными эффектами фармакологического взаимодействия изучаемых препаратов.
Тем не менее, поиск эффективных комбинаций различных веществ для терапии лучевой болезни, в том числе вызванной внешним облучением, является перспективным направлением исследований. Например, авторы работы [27] смогли добиться повышения радиозащитного эффекта солей кальция в рационе за счёт дополнительного включения в него рыбьего жира. В обзоре [28] обобщены сведения относительно перспективности совместного использования мелатонина и витамина D для облегчения побочных эффектов лучевой терапии онкологических заболеваний. В качестве ещё одного примера можно привести нашу недавнюю работу [29], в которой была разработана схема совместного применения веществ с различным механизмом радиоза-щитного действия. Данная схема обеспечила полную выживаемость мышей, облучённых в дозе 6,5 Гр, т.е. в условиях, аналогичных таковым в настоящей работе. К слову, в той же работе можно найти примеры фармакологической несовместимости некоторых веществ. Так, например, добавление рибоксина в схему, подразумевающую применение хлорофиллина и тролокса, способствовало бо́льшей смертности мышей даже по сравнению с группой облучённого контроля. Хотя сам рибоксин может проявлять некоторые радиозащитные свойства [22].
Подводя итог вышеизложенного, считаем необходимым указать на актуальность проведения работ по изучению эффекта совместного применения нескольких препаратов для лечения лучевой болезни. Как показала настоящая работа, не всегда совместное использование препаратов с радиозащитными свойствами способно облегчить течение острого лучевого синдрома. Именно поэтому необходимо в дальнейших исследованиях детально изучать эффекты, имеющие место при поступлении в организм различных веществ на фоне воздействия ионизирующего излучения. При этом, необходимо иметь в виду, что при различных режимах воздействия излучения (острое, хроническое, фракционированное, различные дозы и мощности дозы и т.п.) эффект от совместного применения различных веществ может быть различным, не исключено, что даже противоположным.
Заключение
Таким образом, схема комбинированного применения медного хлорофиллина до облучения, глутатиона после облучения в день облучения и препарата гидролизата плаценты через 1, 2, 3, 4, 8, 9, 10 и 11 дней после облучения не обеспечила смягчения течения лучевой болезни. При этом, показанные нами ранее радиопротекторные свойства медного хлорофиллина в случае применения его в составе указанной терапевтической схемы терялись. Полученные нами данные не свидетельствуют в пользу целесообразности применения гидролизата плаценты против облучения. По крайней мере, применение данного препарата после облучения и профилактического введения медного хлорофиллина в используемых нами условиях абсолютно бессмысленно.
Исследование выполнено за счёт гранта Российского научного фонда № 23-24-00383,


