Влияние света разной интенсивности на рост и развитие артемии (Artemia salina) в искусственной экосистеме
Автор: Шленкина Т.М., Романова Е.М., Романов В.В., Фазилов Э.Б.У., Любомирова В.Н., Свешникова Е.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 2, 2023 года.
Бесплатный доступ
Науплии артемии являются лучшим стартовым кормом для большинства объектов современной аквакультуры. Живые стартовые корма - науплии артемии - содержат ингредиенты, необходимые для выживаемости гидробионтов в критические периоды раннего постэмбрионального онтогенеза. В связи с этим актуальным является совершенствование биотехнологии культивирования артемии в искусственной экосистеме. Цель работы - исследование влияния режимов освещенности на морфологические особенности артемии на разных стадиях ее жизненного цикла. Материалы и методы. В ходе исследования были использованы различные режимы освещенности: 1,5; 2,5 и 4 клк, чтобы определить наиболее эффективный. Результаты. Использованные режимы освещенности по-разному влияют на развитие артемии. Наиболее эффективной на этапе эмбрионального развития и начальных стадиях постэмбрионального онтогенеза была освещенность, равная 4 клк
Искусственно созданная экосистема, аквакультура, артемия, условия культивирования, режимы освещенности
Короткий адрес: https://sciup.org/14128725
IDR: 14128725 | УДК: 639.51 | DOI: 10.34014/2227-1848-2023-2-166-180
Effect of different light intensities on growth and development of artemia (Artemia salina) in an artificial ecosystem
Artemia nauplii are the best initital food for most fish larvae. Feeder fish, Artemia nauplii, contain the ingredients necessary for the survival of aquatic organisms during critical periods of early postembryonic ontogenesis. Thus, it is important to improve the biotechnology of Artemia cultivation in artificial ecosystems. Materials and Methods. In the course of the study, various illumination modes were used, namely, 1.5; 2.5 and 4 klx to determine the most effective one. Results. Various illumination modes affect Artemia development in different ways. The most effective illumination mode at the stage of embryonic development and the initial stages of postembryonic ontogenesis was 4 klx.
Текст научной статьи Влияние света разной интенсивности на рост и развитие артемии (Artemia salina) в искусственной экосистеме
Введение. Артемии – жаброногие ракообразные, населяющие морские мелководья и гипергалинные озера. Это планктонные организмы, которые питаются фитопланктоном, фильтруя воду с помощью грудных конечностей. Наиболее известный вид – Artemia salina .
Артемия имеет большое значение для развития мировой аквакультуры. Представители этого рода являются общепризнанным кормовым объектом, который используется в качестве живых стартовых кормов для рыб, ракообразных, моллюсков и других гидробионтов в аквакультуре [1].
Науплии жаброногого рачка рода Artemia содержат уникальные биологически активные вещества, обеспечивающие выживаемость, рост и развитие рыб и других гидробионтов на критических стадиях развития, когда предли-чинки переходят на экзогенное питание после истощения запасов желтка.
Однако мировая добыча цист артемии в естественных природных экосистемах удовле- творяет мировой спрос всего на 40 %. Спрос настолько высок, что 95 % добываемой в России артемии экспортируется в Европу и страны Азии, прежде всего в Китай. Цены на цисты артемии в России находятся на уровне мировых, и этот природный продукт мало доступен для отечественных рыбоводных предприятий, в первую очередь для фермерских хозяйств [2]. Поэтому, учитывая высокий спрос на жаброногих рачков, культивирование артемии в искусственной экосистеме актуально для развития аквакультуры в целом, имеет большую практическую значимость и является важным звеном в системе искусственного воспроизводства и выращивания гидробионтов.
На цикл развития артемии и ее морфологические параметры в естественной и искусственной экосистеме оказывает влияние комплекс абиотических факторов среды.
Рачки рода Artemia проявляют высокую адаптационную пластичность, имеют широ- кую экологическую валентность. Они обладают способностью противостоять неблагоприятным факторам среды, однако это противостояние не проходит бесследно. В неблагоприятных условиях артемии снижают свою плодовитость, количество циклов воспроизводства и продолжительность жизни [3, 4].
При культивировании артемии есть все возможности создать максимально благоприятную среду для наиболее полной реализации ее генетического потенциала продуктивности.
В России ареал артемии ограничен гипер-галинными водоемами Алтая, Сибири, Крыма, заливами и лиманами Каспийского, Азовского и Черного морей. Все эти районы – места промысла цист артемии.
Однако видовой состав артемии на территории России до сих пор не изучен, принято условно выделять Artemia salina и ее расы (экоморфы) в зависимости от особенностей абиотических факторов места их обитания [5].
К числу основных абиотических факторов, оказывающих влияние на цикл развития и репродуктивный потенциал артемии, можно отнести температуру, рН, соленость и освещенность среды обитания.
В природных экосистемах артемии обладают высокой устойчивостью к химическому загрязнению, в частности к высоким концентрациям сероводорода. Известно, что сероводород для остальных гидробионтов смертелен даже в незначительных количествах. Поэтому артемии являются единственными обитателями (кроме микроорганизмов) богатых сероводородными илами озер [6].
В каждом из мест обитания артемии существует единый устоявшийся комплекс абиотических факторов, обусловленных климатическими условиями и сезонностью, вызывающей их циклические колебания.
В искусственной экосистеме имеются необходимые условия, чтобы избежать колебаний абиотических факторов среды и оптимизировать их, устранить сезонность, повысить возможность наиболее полной реализации генетического потенциала организма артемии. Это позволяет получать науплии и цисты артемии круглогодично, а не только в летний период.
Артемии теплолюбивы, оптимальная для разных рас температура лежит в пределах 20–30 °С [7], но рачки могут существовать и при температуре от 2 до 35–37 °С. Однако некоторые таиландские и вьетнамские расы артемий адаптированы и к более высокой температуре, близкой к 40 °С [8]. При температуре ниже 5 °С движение рачков замедляется и прекращается их рост.
Артемия считается достаточно хорошо изученным природным объектом. Но это касается артемии из естественных природных ги-пергалинных водных экосистем. По отношению к артемии, выращиваемой в искусственной экосистеме, этого утверждать нельзя. Культивируемая артемия используется преимущественно в качестве живых стартовых кормов на личиночных стадиях онтогенеза рыб и других гидробионтов. При этом и, как правило, in situ используется методология культивирования, максимально приближенная к усредненным условиям внешней среды естественных экосистем без учета сезонных особенностей. На практике условия искусственного круглогодичного разведения артемии в аквакультуре, как показали исследования, по большинству абиотических факторов не оптимизированы [9]. Особенно отчетливо это проявляется при разведении артемии по замкнутому циклу [10]. Как оказалось, факторы среды, обеспечивающие размножение артемии по типу живорождения в аквакультуре, отличаются от условий, необходимых и достаточных для продуцирования цист [11]. Поэтому процесс культивирования артемии нуждается в оптимизации абиотических факторов, что сделало бы его максимально эффективным. Световой фактор в этом процессе играет ведущую роль.
Анализ современных литературных источников показывает, что искусственное воспроизводство артемии по замкнутому циклу находится на недостаточно высоком уровне [12]. Пока продуктивность артемии в условиях аквакультуры остается низкой.
Культивирование и воспроизводство артемии по замкнутому циклу, по сравнению с традиционным получением науплий артемии, – не до конца изученный процесс. По- этому оптимизация абиотических факторов среды в условиях искусственного разведения артемии относится к числу актуальных проблем, требующих решения [13, 14].
Наша работа посвящена исследованию влияния одного из абиотических факторов среды – света разной интенсивности – на этапы метаморфоза определенной расы (экоморфы) артемии – А. var. Principalis – в искусственно созданной экосистеме.
Цель исследования. Оценить влияние режимов освещенности на особенности метаморфоза А. var. Principalis в искусственной экосистеме.
Материалы и методы. Для исследования использовалась артемия расы А. var. Principalis из Алтайских гипергалинных озер, поставщиком цист являлось предприятие «Барром». Цвет цист был бежево-коричневым с преобладанием коричневого.
Для получения науплий цисты артемии культивировались в аппарате Вейса в искусственно созданной экосистеме со следующими параметрами: соленость воды – 30 г/л (NaCl), температура воды – 26–28 °С, рН – 8,2, плотность посадки цист – 2,5 г/л, насыщение воды кислородом – 80–90 %. Применялись разные режимы освещенности.
Для изучения влияния света на онтогенез и продуктивность артемии в аквакультуре были заложены три серии опытов. Освещение в 1-м и 2-м опытах обеспечивалось блоками с лампами дневного света OSRAM L 18w/765, световой поток и цветовая температура каждой из которых составляли 1050 Лм и 5000 К соответственно. Для освещения в третьем опыте использовался светодиодный источник света IEK CDO 06-100 6500K со световым потоком 8000 Лм. Измерение освещенности выполнялось фотометром/люксометром MASTECH MS6610 с выносным датчиком измерения освещенности.
В первом опыте, который служил контролем, освещенность (E) культивируемой артемии составляла 1,5 клк, во втором опыте – 2,5 клк, в третьем – 4 клк.
Морфометрические показатели изучались по стандартным методикам. Для исследования рачки фиксировались в 4 % растворе форма- лина. Измерение проводилось с помощью микроскопа МБС-10, оборудованного окулярным микрометром.
При работе использовались также микроскоп «Микромед 2» (вар. 3-20), аналитические весы ViBRA HT-224RCE с точностью до 0,0001 г, чашки Петри, бинокуляр Levenhuk 3ST, компрессор Resum AIR-3000, препаровальные иглы.
Достоверность различий выборок оценивалась по критерию Стьюдента. Проводилась традиционная биометрическая обработка данных.
Результаты и обсуждение. На первом этапе работы исследовалось влияние разных режимов освещенности на развитие эмбриона и ранних личинок артемии – науплий; изучались морфометрические параметры артемии в раннем онтогенезе.
Перед загрузкой цист (рис. 1) артемии в аппарат Вейса определялось их качество. При микроскопии было установлено, что доля цист с вмятинами в исследованных образцах достигала 20–30 %.
Исследование размеров сухих цист артемии показало, что средний диаметр цист составил 0,227±0,016 мм. Полученные результаты достаточно хорошо согласуются с данными других исследований, по результатам которых диаметр сухих цист колеблется от 230 до 400 мкм [15–17]. Разброс размеров цист был достаточно высоким. Неоднородность цист артемии обусловлена колебаниями факторов среды естественных экосистем в местах их добычи.
Artemia salina в зависимости от факторов среды обитания формирует определенные расы (экоморфы), характеризующиеся морфологическими различиями.
Известно, что эмбрион в цисте находится в стадии недифференцированной гаструлы и полностью неметаболичен при влажности ниже 10 %.
Если же влажность превышает 10 % и кислород присутствует в достаточном количестве, то к эмбриону возвращается жизнеспособность [18]. Вылупившиеся эмбрионы артемии и их метаморфоз в науплии изображены на рис. 2.
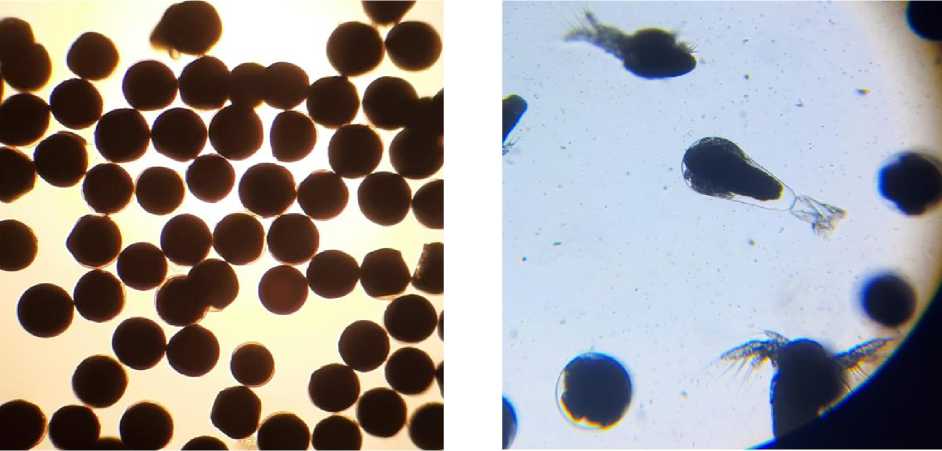
Рис. 2. Свободные эмбрионы и появление науплий
Fig. 2. Free embryos and nauplii formation
Рис. 1. Сухие цисты артемии
Fig. 1. Dry artemia cysts
Морфометрия вылупившихся эмбрионов показала, что абсолютные значения их размеров в контрольной (освещенность 1,5 клк) и экспериментальных группах (2-я группа – ос- вещенность 2,5 клк; 3-я группа – освещенность 4 клк) находились в пределах 236– 288 мкм (рис. 3).
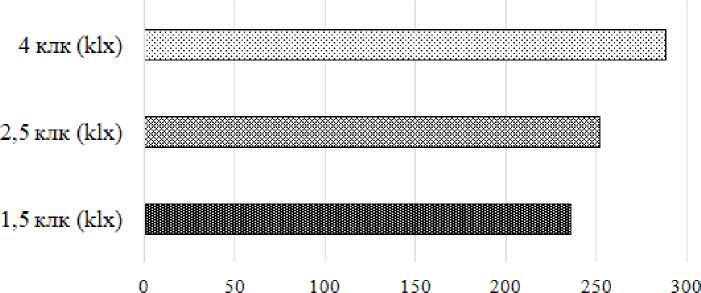
Рис. 3. Усредненный размер свободного эмбриона, мкм
Fig. 3. Average size of a free embryo, microns
При сравнительном анализе размеров эмбриона было установлено, что во второй экспериментальной группе они на 6,3 %, а в третьей на 11,03 % превышали показатели контроля.
Таким образом, увеличение уровня освещенности оказало положительное влияние на размер эмбриона.
На начальных этапах развития, на стадии ортонауплий, артемии быстро растут за счет резервов желтка. Науплии I личиночной стадии находятся на эндогенном питании и не способны потреблять корма, их пищеварительная система не функционирует, так как рот и анус еще закрыты.
Спустя 8–12 ч после первой линьки завершается науплиальный период и личинки артемий переходят в метанауплиальную стадию. У личинок I метанауплиальной стадии начинает функционировать пищеварительный тракт и появляется возможность отфильтровывать частицы размером 1–40 мкм.
В течение последующих 8–10 дней рачки проходят три следующие метанауплиальные стадии, характеризующиеся различной степенью сегментации тела. После пятой линьки ме-танауплиальный период заканчивается и начинается ювенальный с семью стадиями развития, сопровождающийся преобразованием антенн и развитием торакопод (грудных ножек).
После тринадцатой линьки начинается предвзрослый период, состоящий из пяти стадий развития. Этот период характеризуется формированием генитальных структур: вторая пара антенн претерпевает половую диффе- ренциацию. У самцов развиваются крючковатые хвататели, в то время как у самок антенны редуцируются в сенсорные придатки.
При длине рачка 6 мм и более уже можно различить будущих самцов и самок. После семнадцатой линьки завершается постэмбриональное развитие, рачки имеют все половые признаки.
Наблюдения за динамикой выклева науп-лий в искусственной среде в зависимости от освещенности приведены в табл. 1.
Из культивируемой артемии из групп с разным освещением через 8, 12, 18, 25, 30, 34, 38, 42, 48 ч отбирались образцы, которые фиксировались формалином и исследовались под микроскопом.
Индивидуальная масса только что вылупившихся науплий колебалась в пределах 0,01–0,023 мг (рис. 4), что согласуется с литературными данными [19].
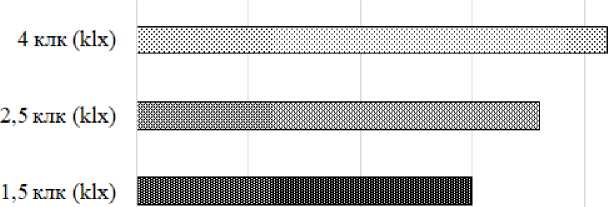
О О.ОО5 0.01 0.015 0.02 0.025 мг (mg)
Рис. 4. Индивидуальная масса только что вылупившихся науплий в зависимости от освещенности
Fig. 4. Individual weight of newly hatched nauplii depending on illumination
Динамика выклева науплиусов в зависимости от уровня освещенности
Таблица 1
Table 1
Dynamics of nauplii hatching, depending on illumination level
|
Период наблюдения Observation period |
I группа (контрольная) (освещенность 1,5 клк) Group I (control) Illumination 1,5 klx |
II группа (экспериментальная) (освещенность 2,5 клк) Group II (experimental) Illumination 2,5 klx |
III группа (экспериментальная) (освещенность 4 клк) Group III (experimental) Illumination 4 klx |
|
Через 8 ч 8 hours later |
Изменений не происходит No changes |
Циста начинает трескаться. Доля таких цист 0,18–0,24 % The cyst begins cracking. The proportion of such cysts is 0.18–0.24 % |
Цисты напитываются водой и раздуваются, активируется развитие эмбриона. Хорион у 0,24–0,28 % цист начинает трескаться |
|
Период наблюдения Observation period |
I группа (контрольная) (освещенность 1,5 клк) Group I (control) Illumination 1,5 klx |
II группа (экспериментальная) (освещенность 2,5 клк) Group II (experimental) Illumination 2,5 klx |
III группа (экспериментальная) (освещенность 4 клк) Group III (experimental) Illumination 4 klx |
|
Cysts are saturated with water and inflate; embryo development is activated. Chorion in 0.24–0.28 % of cysts begins to crack. |
|||
|
Через 12 ч 12 hours later |
Изменений не происходит No changes |
Хорион разрывается, появляются эмбрионы, которые все еще завернуты в инкубационную мембрану. В течение нескольких часов эмбрионы остаются сцепленными с оболочкой цисты. Доля таких форм составляет 12,7 % The chorion ruptures, leaving the embryos still wrapped in the incubation membrane. For several hours, the embryos remain linked to the cyst membrane. The proportion of such forms is 12.7 % |
Оболочки цист продолжают растрескиваться, и эмбрион выходит из хориона. В течение определенного времени эмбрионы остаются сцепленными с оболочкой. Доля таких форм достигает 16,6 % Cysts continue to crack; the embryo leaves the chorion. For some time, the embryos are still linked to the shell. The proportion of such forms is 16.6 % |
|
Через 18 ч 18 hours later |
Хорион лопается Chorion ruptures |
Часть особей (21,9 %) находятся на стадии «парашютика» Hatchling (21.9 %) is at a “parachute” stage |
Часть особей (28,7 %) находятся на стадии «парашютика» Hatchling (28.7 %) is at a “parachute” stage |
|
Через 25 ч 25 hours later |
Хорионы лопаются, эмбрионы выходят из цисты, их доля составляет 1,8 % Chorions rupture, embryos leave the cyst. The proportion of such cysts is 1.8 % |
Выклюнувшиеся из хориона личинки I стадии развития (прозрачные ортонауплии) составляют 33,1 %, в длину достигают 0,5 мм. Доля более развитых, свободно плавающих науплий составляет 7,6 % The larvae hatched from the chorion, 1st stage of development (transparent orthonauplii), make up 33.1 %. Their length is up to 0.5 mm. The proportion of more developed, free-swimming nauplii is 7.6 % |
Вылупившиеся из хориона личинки, завершившие эмбриональную стадию, составляют 38,1 %. Они прозрачные, их длина 0,5 мм. Более развитые, свободно плавающие науплии составляют 9,1 % The larvae hatched from the chorion, which completed the embryonic stage, account for 38.1 %. They are transparent, their length is 0.5 mm. More developed, free-swimming nau-plii account for 9.1 % |
|
Период наблюдения Observation period |
I группа (контрольная) (освещенность 1,5 клк) Group I (control) Illumination 1,5 klx |
II группа (экспериментальная) (освещенность 2,5 клк) Group II (experimental) Illumination 2,5 klx |
III группа (экспериментальная) (освещенность 4 клк) Group III (experimental) Illumination 4 klx |
|
Через 30 ч 30 hours later |
Появились выклюнувшиеся науплии. На их долю приходится 24,8 % The proportion of hatched nauplii is 24.8 % |
Доля выклюнувшихся науплий возросла до 52,7 %. Науплии имеют прозрачное тело, две антенны, усики по бокам головы. На голове расположен примитивный глаз, различающий свет от тени. Проявляется положительный фототаксис The proportion of hatched nauplii is 52.7 %. Their bodies are transparent; they have two antennae and antennules. On the head there is a primitive eye that distinguishes light from shadow. Positive phototaxis is observed |
Доля вылупившихся науплий составляет 59,3 %. Они имеют небольшое продолговатое тело и две антенны, на голове расположен примитивный глаз. Проявляют положительный фототаксис The proportion of hatched nau-plii is 59.3 %. They have a small elongated body and two antennae, there is a primitive eye on the head. Positive phototaxis is observed |
|
Через 34 ч 34 hours later |
Доля выклюнувшихся науплий составляет 36,2 % The proportion of hatched nauplii is 36.2 % |
Доля выклюнувшихся науплий составляет 61,1 % The proportion of hatched nauplii is 61.1 % |
Доля выклюнувшихся науплий составляет 69,4 % The proportion of hatched nauplii is 69.4 % |
|
Через 38 ч 38 hours later |
Доля выклюнувшихся науплий составляет 53,7 % The proportion of hatched nauplii is 53.7 % |
Доля выклюнувшихся науплий составляет 68,5 % The proportion of hatched nauplii is 68.5 % |
Доля выклюнувшихся науплий составляет 77,8 % The proportion of hatched nauplii is 77.8 % |
|
Через 42 ч 42 hours later |
Доля выклюнувшихся науплий составляет 68,2 % The proportion of hatched nauplii is 68.2 % |
Доля выклюнувшихся науплий составляет 79,6 % The proportion of hatched nauplii is 79.6 % |
Доля выклюнувшихся науплий составляет 82,4 % The proportion of hatched nauplii is 82.4 % |
|
Через 48 ч 48 hours later |
Итоговый выклев – 70,3 % Final hatch is 70.3 % |
Итоговый выклев – 81,9 % Final hatch is 81.9 % |
Итоговый выклев – 84,5 % Final hatch is 84.5 % |
Необходимо отметить, что спустя 8 ч после начала инкубации в контрольной группе изменений не произошло. Во второй группе на яйцах начали появляться трещины. Количество треснувших яиц в пробах составило от 0,18 % до 0,24 %. В третьей группе отмечены первые цисты с треснувшим хорионом (рис. 5). Их количество составило 0,24–0,28 %. Раз- ница между экспериментальными группами по количеству цист с треснувшим хорионом составила 33,3 %. Это говорит о том, что в небольшом количестве цист эмбриогенез завершился и начался процесс выхода науплий из хориона.
Через 12 ч после начала инкубации в контрольной группе изменений также не произо- шло. В экспериментальных группах количество цист с треснувшим хорионом увеличилось и составило во второй группе 12,7 %, в третьей – 16,6 %.
Через 18 ч в контрольной группе цисты начинали лопаться. В экспериментальных группах процесс усилил свою интенсивность: доля особей на стадии «парашютика» во второй группе составила 21,7 %, в третьей – 28,7 % (рис. 6). Таким образом, количество цист с треснувшим хорионом в третьей группе было больше, чем во второй, на 32,3 %.
Через 25 ч после начала инкубации в кон- трольной группе наблюдался процесс растрескивания хорионов (рис. 7), эмбрион появлялся из скорлупы в 1,8 % случаев. Во второй группе на долю выклюнувшихся науплий приходилось 33,1 %. Отмечены первые свободно плавающие науплии (7,6 %) (рис. 7, 8). В третьей группе эти показатели составили соответственно 38,1 % и 9,1 %. Таким образом, в обеих экспериментальных группах встречались вылупившиеся науплии, однако их количество было разным, что свидетельствует о влиянии интенсивности освещенности на скорость выклева науплий.
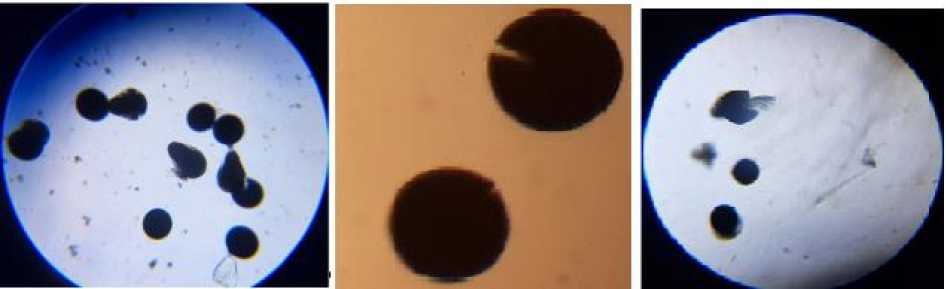
Рис. 5. Цисты с треснувшим хорионом и свободные эмбрионы
Fig. 5. Cysts with a cracked chorion and free embryos
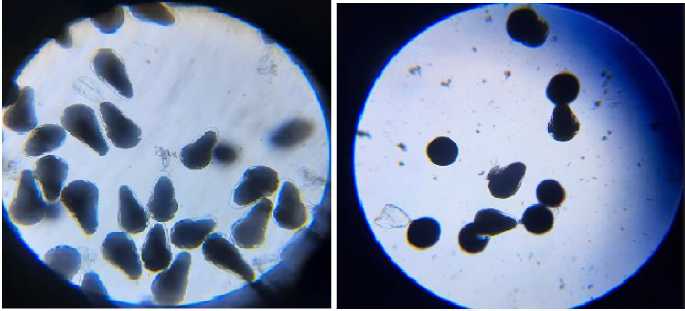
Рис. 6. Интактные и треснувшие цисты, стадия «парашютика»
Fig. 6. Intact and cracked cysts, “parachute” stage
Спустя 30 ч количество выклюнувшихся науплий в контрольной группе достигло 24,8 %, во второй группе – 52,7 % (в 2,7 раза больше, чем в контроле), в третьей – 59,3 % (почти в 3 раза больше, чем в контроле). Таким образом, через 30 ч после начала инкуба- ции в экспериментальных группах отмечался массовый выход эмбрионов (рис. 7), при этом разница между второй и третьей группами составила 12,5 %.
Итоговый выклев науплий в зависимости от освещенности представлен на рис. 9.

Рис. 7. Треснувшие хорионы и свободно плавающие науплии, массовый выклев науплий
Fig. 7. Cracked chorions and free-floating nauplii, mass nauplii hatch

Рис. 8. Науплии
Fig. 8. Nauplii
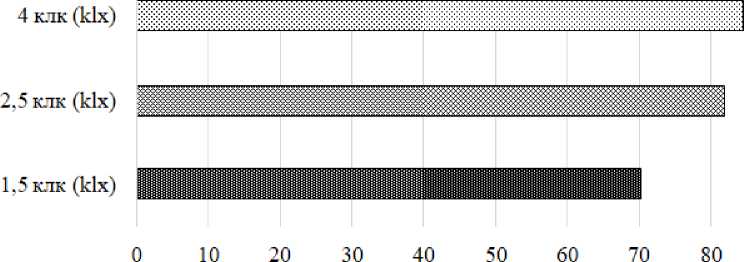
Рис. 9. Итоговый выклев науплий в зависимости от освещенности
Fig. 9. Final nauplii hatch depending on the illumination
Полученные в результате исследования данные свидетельствуют об активирующем влиянии освещенности на динамику и интенсивность выклева, а также развитие артемии на начальных этапах. Наиболее выраженный эффект отмечался при освещенности 4 клк.
Наблюдение за артемиями в процессе их метаморфоза показало, что варьирование условий культивирования цист позволяет добиться различных результатов: от ускорения вылупления науплий до получения более развитых и крепких рачков.
Как показали результаты исследований, высокая интенсивность освещения не только повышает скорость выклева, но и достоверно увеличивает выход личинок, а также влияет на скорость метаморфоза в личиночном периоде.
Таким образом, полученные данные свидетельствуют о том, что освещение является активирующим фактором для инкубации цист артемии и ее последующего культивирования. Установлено, что уровень освещенности приобретает наибольшее значение на заключительных стадиях эмбриогенеза и начальных этапах постэмбрионального развития. В эти периоды артемия наиболее чувствительна к световому воздействию.
Для получения максимального выхода науплий повышенную освещенность необходимо поддерживать на протяжении всего периода инкубации.
Заключение. В перечне стратегических направлений развития РФ отдельно отмечен переход к развитию экологически чистой аквакультуры. Развитие и совершенствование биотехнологий культивирования гидробионтов в искусственно созданной экосистеме – это основное направление развития современной аквакультуры.
Важность выбранного нами направления исследований обусловлена тем, что артемия, в частности живые науплии, является признанным лидером в числе стартовых кормов для рыб и других гидробионтов в мировом рыбоводстве. Живые науплии – короткоживущий объект, поэтому их необходимо получать in situ в каждом из предприятий аквакультуры, занимающихся разведением и выращиванием рыбы, ракообразных или моллюсков. Поэтому технология культивирования артемии должна быть оптимизирована по всему спектру абиотических факторов, необходимых и достаточных для ее выращивания в искусственно созданной среде.
Наше внимание было сосредоточено на таком абиотическом факторе, как интенсивность освещения, который мы варьировали, стабилизировав при этом соленость, рН и температуру среды.
Результаты наших исследований показали, что интенсивность освещения оказывала влияние на эмбриогенез, стадии метаморфоза личинок и рост науплий артемии. В частности, было установлено, что для максимального проявления генетического потенциала продуктивности, реализующегося в количестве выклюнувшихся науплий, при культивировании артемии в аквакультуре важно на начальных этапах ее онтогенеза использовать режим освещенности 4 клк.
Исследование выполнено при поддержке программы развития Саратовского государственного университета генетики, биотехнологии и инженерии им. Н.И. Вавилова «Приоритет – 2030».
Список литературы Влияние света разной интенсивности на рост и развитие артемии (Artemia salina) в искусственной экосистеме
- Мухитова М.Э., Романова Е.М., Любомирова В.Н., Романов В.В., Шленкина Т.М., Шадыева Л.А. Проблемы культивирования стартовых живых кормов для аквакультуры. Международный научно-исследовательский журнал. 2017; 1 (55): 13-15.
- Костромин Е.А. Влияние факторов среды (соленость, температура, освещение) на инкубацию Artemia salina в эксперименте. Известия Санкт-Петербургского государственного аграрного университета. Санкт-Петербург; 2016: 164-168.
- Litvinenko L.I., Litvinenko A.I., Boyko E. G. Brine shrimp Artemia in Western Siberia lakes. Novosibirsk; 2016. 295.
- Рожков А.Г. Артемия салина (Artemia salina), особенности и применение. Современные технологии в деятельности особо охраняемых природных территорий: материалы II Международной молодежной научно-практической конференции. Омск; 2020: 44-45.
- Старовойтова Д.А., Бурмистрова О.С. Размеры цист популяций артемии разнотипных озер Ку-лундинской низменности. Известия АО РГО. 2017; 4 (47): 84-92.
- Литвиненко Л.И. Жаброногие рачки рода Artemia Leach, 1819 в гипергалинных водоемах Западной Сибири (география, биоразнообразие, экология, биология и практическое использование): ав-тореф. дис. ... д-ра биол. наук. Пермь; 2009. 46.
- Asem A., Rastegar-Pouyani N. Sexual dimorphism in Artemia urmiana Günther, 1899 (Anostraca: Arte-miidae) from the Urmia Lake (West Azerbaijan, Iran). Journal of Animal and Veterinary Advances. 2007; 6 (12): 1409-1415.
- Разова Л.Ф. Оценка биологических и репродуктивных особенностей артемии сибирских популяций: дис. ... канд. биол. наук. Тюмень; 2022. 172.
- Романова Е.М., Романов В.В., Любомирова В.Н., Фазилов Э.Б. Факторы, регулирующие онтогенез A. salina и ее продуктивность при культивировании IN VITRO. Вестник Ульяновской государственной сельскохозяйственной академии. 2022; 3 (59): 148-153.
- Романова Е.М., Романов В.В., Любомирова В.Н., Фазилов Э.Б. У. Технология обогащения ранних науплий Артемии и результативность их использования в качестве стартовых кормов. Вестник Ульяновской государственной сельскохозяйственной академии. 2022; 4 (60): 150-155.
- Макаров А.В., Мишвелов А.В. Сведения о перспективах хозяйственного применение Artemia salina и продуктов ее жизнедеятельности. 2021; 19-2 (195): 85-86.
- Mazhibaeva Zh.O., Barakbayev T.T., Shalgimbaeva G.M., Isbekov K.B., Asylbekova S.Zh., Fefelov V.V. Populations of Artemia crustaceans of Karabassky floods of Pribalkhashye. Vestnik of Astrakhan State Technical University. Series: Fishing Industry. 2021; 3: 47-54.
- Садчиков А.П. Культивирование водных и наземных беспозвоночных (принципы и методы). Москва: Изд-во Московского государственного университета им. М.В. Ломоносова: МАКС Пресс; 2009. 272.
- Жигин А.В. Артемия - объект аквакультуры. Доклады ТСХА. 03-05 декабря 2019. Выпуск 292, часть IV. Москва: Российский государственный аграрный университет - МСХА им. К. А. Тимирязева; 2020: 277-281.
- Руднева И.И., Залевская И.Н., Шайда В.Г., Щерба А.В., Завьялов А.В. Экологические особенности Артемии соленых озер Евпаторийской группы (Республика Крым). Экология водных беспозвоночных: тезисы Международной конференции, посвященной 110-летию со дня рождения Ф.Д. Мордухай-Болтовского. 09-13 ноября 2020. Борок; Ярославль; 2020: 70.
- Тимошенко Ю.А. Характеристика морфологических показателей артемии из некоторых озер Крыма. Международный академический вестник. 2019; 5 (37): 5-8.
- Мухитова М.Э., Романова Е.М., Любомирова В.Н., Шленкина Т.М. Оценка синхронности метаморфоза Artemia salina в лабораторных условиях. Аграрная наука и образование на современном этапе развития: опыт, проблемы и пути их решения: материалы VIII Международной научно-практической конференции. Ульяновск; 2017: 155-158.
- Мухитова М.Э., Романова Е.М. Технологические особенности выращивания живых кормов для аквакультуры. Современные научные исследования и разработки. 2017; 2 (10): 363-364.
- Белых О.А., Розанов С.Е. Особенности выращивания живого корма Artemia salina в аквакультуре. Известия Байкальского государственного университета. 2021; 31 (3): 400-406.


