Влияние температурного стресса на спектр жирных кислот штаммов Vibrio cholerae
Автор: Шипко Елена Сергеевна, Дуванова Ольга Викторовна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2022 года.
Бесплатный доступ
В условиях смоделированного температурного стресса методом газовой хроматографии в сочетании с масс-спектрометрией был изучен спектр жирных кислот штаммов Vibrio cholerae O1, О139, non O1/non O139 серогрупп с различным набором детерминант патогенности, выделенных от больных и из проб воды поверхностных водоемов. Выявлены достоверные отличия в составе жирных кислот при холодовом и тепловом стрессах в клетках возбудителя холеры относительно контрольных образцов. Штаммы, выделенные из воды поверхностных водоемов, отличались по спектру жирных кислот при холодовом стрессе от штаммов, выделенных от больных. У штаммов, выделенных из воды, снижение температуры культивирования до 23°С сопровождалось синтезом докозановой, тетракозановой и гексакозановой кислот, а до 4°С - увеличением количества тетрадекановой и гексадекановой кислот. Тогда как у штаммов, выделенных от больных, снижение температуры культивирования вызывало закономерное увеличение гексадеценовой и октадеценовой кислот. Реакция на тепловой стресс у большинства изученных штаммов, независимо от набора детерминант патогенности и источника выделения, имела общую тенденцию: увеличение суммарного количества насыщенных жирных кислот, синтез trans-изомеров ненасыщенных жирных кислот, появление ω-алициклических и iso-разветвленных жирных кислот. Помимо ремоделирования жирно-кислотного состава мембраны под действием температурного стресса отмечен синтез оксилипинов, фенилпропаноидов, терпеноидов, возможно, играющих роль адаптогенов.
Vibrio cholerae, жирные кислоты, холодовой стресс, тепловой стресс
Короткий адрес: https://sciup.org/147238653
IDR: 147238653 | УДК: 579.843.1:577.115.3:577.1 | DOI: 10.17072/1994-9952-2022-2-143-154
Influence of temperature stress on the spectrum of fatty acids of Vibrio cholerae strains
Under conditions of simulated temperature stress gas chromatography combined with mass spectrometry was used to study the spectrum of fatty acids of strains of Vibrio cholerae O1, O139, non O1/non O139 serogroups with a different set of pathogenicity determinants isolated from patients and from water samples of surface water bodies. Significant differences in the composition of fatty acids under cold and heat stress in the cells of the causative agent of cholera relative to control samples were revealed. The strains isolated from the water of surface reservoirs differed in the spectrum of fatty acids under cold stress from the strains isolated from patients. In strains isolated from water, a decrease in cultivation temperature to 23 °C was accompanied by the synthesis of docosanoic, tetracosanoic and hexacosanoic acids and to 4 °C - an increase in the amount of tetra-decanoic and hexadecanoic acids. While in strains isolated from patients, a decrease in cultivation temperature caused a regular increase in hexadecenoic acids. and octadecenoic acids. The reaction to heat stress in most of the studied strains regardless of the set of pathogenicity determinants and the source of isolation had a general trend: an increase in the total amount of saturated fatty acids, the synthesis of trans-isomers of unsaturated fatty acids and the appearance of ω-alicyclic and iso-branched fatty acids. In addition to the remodeling of the fatty acid composition of the membrane under the influence of temperature stress, the synthesis of oxylipins, phenylpropanoids and terpenoids, possibly playing the role of adaptogens, was noted.
Текст научной статьи Влияние температурного стресса на спектр жирных кислот штаммов Vibrio cholerae
Глобальное распространение Vibrio cholerae за пределами эндемичных территорий, постоянное эволюционирование и совершенствование внутри- и межвидовых стратегий сохранения возбудителя в разных биоценозах с широким диапазоном экологических факторов, диктуют необходимость изучения механизмов, формирующих адаптационный/персистентный потенциал возбудителя и пути его реализации – на генетическом, протеомном, метаболомном уровнях.
Одним из наиболее значимых экологических факторов, с которым сталкиваются бактерии в процессе своей жизнедеятельности, является воздействие температуры. Учитывая два стиля жизни холерного виб-риона– водное окружение и кишечник человека, ему необходимо адаптироваться к широкому диапазону температур.
Температурная адаптация на клеточном уровне осуществляется за счет общих стрессовых реакций, которые включают адаптацию механизмов трансляции и транскрипции, структурную перестройку энзимов, экспрессию специфических белков, а также изменение текучести мембран.
Клеточные мембраны играют ключевую роль в устойчивости бактерий к действию абиотических и биотических факторов среды, осуществляя динамическое взаимодействие клетки и окружающей среды: обеспечивают избирательную проницаемость для ионов, метаболитов, генерацию трансмембранного потенциала, восприятие, обработку и передачу информации в виде химических и электрических сигналов.
Модулирование текучести мембраны – один из центральных процессов, лежащих в основе формирования адаптационного ответа бактериальной клетки на термический стресс. Известно, что при изменении температуры липиды могут претерпевать несколько фазовых переходов. Наиболее важными из них являются переходы кристалл (гель) – жидкий кристалл и жидкий кристалл – изотропное состояние. Поддержание жидкокристаллического состояния мембраны осуществляется за счет гомеовязкостной адаптации, в которую вовлечены следующие липидные модуляции – температурные вариации липида А молекулы липополисахарида, изменение типа этерификации фосфолипидов [Vigh, Landry, Nakamoto, 2007; Watson, 2015].
Изменение жирнокислотного состава липидов, как наиболее лабильной их части, может быть достигнуто несколькими путями: в результате синтеза жирных кислот (ЖК) de novo либо ремоделированием – удлинением, разветвлением, циклизацией, десатурацией цепей. Недавние исследования выявили способность патогенных вибрионов извлекать жирные кислоты из источников окружающей среды и ассимилировать их в собственные клеточные мембраны. Включение экзогенных длинноцепочечных полиненасы-щенных жирных кислот в фосфолипиды оказывало влияние на проницаемость мембран, повышая стрес-соустойчивость микроорганизмов [Moravec et al., 2017; Smith et al., 2021].
Резкая смена температур (при попадании патогена в организм теплокровного хозяина или его выход в окружающую среду) требует срочной ответной/адаптивной реакции клеток возбудителя на стресс. Основные механизмы, обеспечивающие данный процесс – это cis-trans -изомеризация ННЖК, циклопропанирование ЖК, а также iso - и anteiso -метилирование ацильных цепей.
Циклопропановые ЖК обладают уникальными физическими и химическими характеристиками – проявляют высокую окислительную стабильность, способны к самополимеризации и т.д. Они формируют первую линию защиты клетки от термического стресса и действия агрессивных сред, оказывая влияние на структуру и динамику липидного бислоя. Показано, что включение циклопропановых ЖК способствует возникновению гош-эффекта в ацильных цепях (углеродная цепь изгибается под углом 120º), что приводит к увеличению латеральной диффузии липидов и повышению текучести мембран при холодовом стрессе [Poger, Mark, 2015]. В то же время ω-алициклические ЖК с крупными циклогексильными, циклогептильными кольцами способствуют большей упорядоченности ацильных цепей, снижению диффузии липидов и увеличению вязкости мембран при действии высоких температур [Poger, Caron, Mark, 2015].
Механизм cis-trans-изомеризации ННЖК, запускаемый при экстремальной смене температурного режима, обусловливает быструю ригидизацию клеточной мембраны, препятствуя избыточному ее разжижению при высоких температурах либо проникновению внутрь клеток токсичных веществ [Heipieperm, Hachicho, 2014]. Данный механизм присущ лишь тем представителям грамотрицательных бактерий, ко- торые способны существовать в широком диапазоне экосистем, как например, представители родов Pseudomonas и Vibrio [Heipieper, Meinhard, Segura, 2003]. В trans-ННЖК, по сравнению с cis-изомерами, ацильные цепи более тесно взаимодействуют, подобно остаткам насыщенных жирных кислот, что позволяет эффективно снижать текучесть мембраны, когда это необходимо [Eberlein et al., 2018]. Было предложено считать увеличение соотношения trans- к cis-изомерам ЖК более 0.1 биомаркером стресса, переживаемого бактериальной клеткой [Heipieper, Hachicho, 2014].
Одной из реакций на холодовой стресс у многих микроорганизмов, помимо увеличения доли ННЖК и короткоцепочечных вариантов, является синтез anteiso -разветвленных ЖК, повышающих текучесть мембраны и снижающих температуру фазового перехода. Аnteiso -метильное разветвление имеет тенденцию уменьшать толщину липидного бислоя при одновременном снижении упорядоченности ацильных цепей с эффектом повышения текучести мембран за счет образования перегибов в точке ветвления [Poger, Caron, Mark, 2014]. Напротив, в ответ на действие теплового шока, помимо увеличения средней длины цепи ЖК и доли cis -изомеров ЖК, отмечено увеличение соотношения iso - к anteiso -разветвленным ЖК. Iso -разветвленные цепи имеют точки плавления существенно выше, чем anteiso -разветвленные, как, например, точки плавления туберкулостеариновой кислоты (13.2°С) и стеариновой кислоты (69.6°C) [Janse, 1997].
Важно отметить, что термические модификации липидного состава мембран тесно связаны с синтезом и секрецией ключевых факторов патогенности и для ряда патогенов могут являться инструментом модулирования степени их вирулентности [Бахолдина, Соловьева, 2009; Rowe, Hantley, 2015; Seydlova et al., 2017]. Таким образом, механизмы выживания бактерий при различных температурах тесно связаны не только с адаптацией/персистенцией в окружающей среде, но и с формированием их патогенетического потенциала.
Анализ отечественной и зарубежной литературы показал ограниченное количество публикаций, посвященных роли изменений композиций ЖК в процессе адаптации/персистенции холерных вибрионов. Единичные исследования посвящены в основном характеристике жирнокислотного состава штаммов с позиций поиска хемотаксономических маркеров для дифференциации представителей рода Vibrio [Кузьменко, Головня, Вронова, 1980; Lambert et al., 1983; Urdaci, Marchand, Grimont, 1990]. Тогда как качественное и количественное определение спектров ЖК у штаммов возбудителя холеры (разных серо-групп), при стандартных и вариабельных условиях культивирования не проводилось.
Цель данной работы – изучение влияния температурного стресса на спектр штаммов V. cholerae O1, О139, non O1/non O139 серогрупп с различным набором детерминант патогенности, выделенных от больных и из проб воды поверхностных водоемов с использованием метода газовой хроматографии в сочетании с масс-спектрометрией (ГХ/МС).
Материалы и методы
В работе использовали штаммы V. cholerae с различным набором детерминант патогенности: 2 штамма V. сholerae O1 El Tor (18332 ctx+ tcp+; P-20000 Δctx Δtcp), выделенных от больных и из воды поверхностных водоемов; 2 штамма V. cholerae Сlassical (13603, 680 ctx+ tcp+); 4 штамма V. cholerae О139 серогруппы, из которых 2 (P-16064, Р-16131 ctx+ tcp+) были выделены от больных и 2 атоксиген-ных (17682, 17678 Δctx Δtcp) – из проб воды поверхностных водоемов; 2 штамма V. cholerae nonO1/nonO139 серогрупп (P-20453, 20283 Δctx Δtcp), выделенных от больного и из балластных вод. Штаммы получали из Музея живых культур с центром патогенных для человека вибрионов ФКУЗ Ро-стовского-на-Дону противочумного института Роспотребнадзора, где их хранили в лиофилизированном состоянии.
Температурную характеристику роста исследуемых культур проводили в диапазоне от 4 до 45°С. Для этого взвесь холерных вибрионов вносили в 3 мл 1%-ной пептонной воды (рН 7.8) до конечной концентрации 109 м.к./мл по отраслевому стандарту мутности (ОСО-42-25-59-86 П) ГИСК им. Л.А. Тарасевича (в настоящее время – ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России) и инкубировали в течение 24 ч. Работу проводили в соответствии с требованиями биологической безопасности1. Оптическую плотность обеззараженных культур определяли на спектрофотометре фирмы Beckman (США) при 600 нм. Жизнеспособность оценивали по наличию роста после контрольного высева на чашки с агаром Мартена (рН 7.6, 37°С, 24 ч.). Учет КОЕ проводили по стандартной методике.
Для анализа влияния температурного стресса на спектр жирных кислот штаммов холерных вибрионов методом ГХ/МС клетки после выращивания осаждали центрифугированием при 14 000 об/мин в течение 10 мин. на холоду. Надосадочную жидкость отбрасывали, а осадок отмывали дважды от компонентов среды физиологическим раствором, забуференным фосфатным буфером рН 7.2. Препараты жирных кислот из бактериальных клеток получали по стандартной методике [Sherlock. MIS., 2012], включающей следующие этапы: сапонификацию, кислый метанолиз, экстракцию метиловых эфиров жирных кислот гексаном. Известно, что ЖК состав микроорганизмов более специфичен, если он дополнен другими липидными компонентами, такими как, оксикислоты, спирты, альдегиды, углеводороды и стерины. Поэтому с целью расширения спектра анализируемых соединений пробоподготовка включала дополнительный этап – обработку гексановой фракции O-бис(триметилсилил)-трифлуороацетамидом (BSTF). Данный реагент высоко активен в отношении гидроксильных, карбоксильных, тиоловых и аминогрупп, которые плохо подвергаются метилированию [Осипов, 2010; Moldoveanu, David, 2019].
Метиловые и триметилсилильные эфиры ЖК анализировали методом ГХ-МС на приборе «Маэстро 27802» (ИнтерЛаб, Москва), при помощи программного обеспечения «MSD ChemStation» и библиотеки масс-спектров NIST17.
Хроматографическое разделение проб осуществляли на капиллярной колонке Rtx-5MS (5% diphenyl/95% dimethyl polysiloxane) длиной 30 м, внутренний диаметр 0.25 мм, толщина слоя неподвижной фазы 0.25 µm в режиме линейного программирования температуры от 80 до 320°С со скоростью 4.8°С/мин. Ввод пробы проводили с помощью автосамплера в режиме без деления потока. Объем вводимой пробы 5 мкл. Газ-носитель – водород. Время цикла 47.013 мин. Идентификацию индивидуальных жирных кислот выполняли сравнением времен удержания анализируемых веществ с коммерческими стандартами ЖК: каприновая (ICN Pharmaceuticals), додекановая (ICN Pharmaceuticals), тетрадекановая (ICN Pharmaceuticals), гексадекановая (ICN Pharmaceuticals), стеариновая (ICN Pharmaceuticals), эйкозановая Serva), доказановая (ICN Pharmaceuticals), 2-гидроксидоказановая (Serva); холестерол (концентрация 1 мг/мл).
Полученные хроматограммы обрабатывали автоматически, пользуясь соответствующей опцией штатной программы обработки данных. Частично данные автоматической обработки требовали ручной проверки измерения пиков. Это относится к неполностью разделенным на хроматограмме пикам или малым пикам, находящимся в соседстве с более интенсивными. Эти пики находят, руководствуясь закономерностями их появления на хроматограмме – т. е. временем удержания, подтверждением ионами.
Содержание индивидуальных ЖК оценивали в относительных величинах (в процентах от общей суммы площадей пиков всех индивидуальных ЖК) и представляли в виде средних арифметических значений, полученных в трех экспериментах. Результаты оформлены в виде диаграмм, дополненных полосами погрешностей для рядов данных. Среднее значение и стандартное отклонение рассчитывали с помощью программы Microsoft Office Excel 2010. Статистическую значимость различий сравниваемых средних значений оценивали с помощью критериев Фридмана и Кендалла c использованием пакета прикладных программ «Statistica v. 6.1 for Microsoft Windows». Критический уровень значимости принимался равным 0.05.
Результаты и их обсуждение
Для изучения феномена толерантности и механизма, лежащего в основе адаптации клеток штаммов холерного вибриона к температурному стрессу, штаммы холерного вибриона культивировали в диапазоне температур от 4 до 45°С.
В результате изучения температурных характеристик роста исследуемых культур было выявлено, что у всех штаммов холерного вибриона диапазон роста составлял от 23 до 45°С, с оптимумом в области 28– 37°С. При 4°С рост практически отсутствовал, при сохранении жизнеспособности культуры (рис. 1). Таким образом, были определены температурные условия дальнейших экспериментов: оптимальная температура 37°С (контрольный вариант), 4°С – для моделирования холодового шока и 45°С – для моделирования теплового шока. Также изучался спектр ЖК при 23°С – средней температуре речной воды в летний период.
С помощью высокочувствительного и селективного метода ГХ/МС был изучен спектр ЖК штаммов: V. cholerae O1 El Tor, V. cholerae Сlassical, V. cholerae О139, V. сholerae non O1/non воды поверхностных водоемов. Анализ с набором выделенных от больных и из проб держания липидных компонентов проводили через 2 и 24 ч. инкубации. O139 серогрупп с различным детерминант патогенности.
У контрольных образцов штаммов холерных вибрионов, взятых в исследование (37°С, 24 ч. инкубации), детектировались следующие насыщенные жирные кислоты (НЖК): тетрадекановая (С14:0), гексадекановая (С16:0), гептадекановая (С17:0), октадекановая (С18:0). ННЖК были представлены гексадеце-новой (С16:1) – С16:1Δ7, С16:1Δ9, С16:1Δ11; гептадеценовой – С17:1Δ9, С17:1Δ10; октадеценовой (С18:1) – С18:1Δ6, С18:1Δ9, С18:1Δ11. У всех штаммов детектировалась 3-гидроксимиристиновая кислота (3-ОН14:0).
Анализ спектров ЖК, выявленных у исследованных штаммов V. cholerae, показал преимущественное содержание гексадекановой и гексадеценовой жирных кислот. Суммарное количество этих кислот варьировало от 50.4 до 62.9%. Исключение составили штамм V. сholerae nonO1/nonO139 20453, в ЖК-составе которого доминировали С16:1 (31.6%) и С18:1 (22.92%) ННЖК, и штамм V. сholerae О139 17682 с преобладанием С16:0 (46.65%) и С18:0 (19.8%) НЖК. Ранее рядом отечественных и зарубежных авторов [Кузьменко, Головня, Вронова, 1980; Lambert et al., 1983; Urdaci, Marchand, Grimont, 1990] проводился анализ спектров ЖК у штаммов бактерий, принадлежащих к семейству Vibrionaceae. Авторами отмечена высокая степень гомологии ЖК состава у представителей семейства. Основное различие заключалось в содержании С12:0 (додекановой), С14:0, С15:0 (пентадекановой) НЖК и некоторых разветвленных ЖК. Профили доминантных ЖК были аналогичны полученным в настоящем исследовании. Отношение НЖК к ННЖК у контрольных образцов штаммов, взятых в исследование, в среднем составило (47.41:44.77), у штамма 20453 – (27.07:59.74).
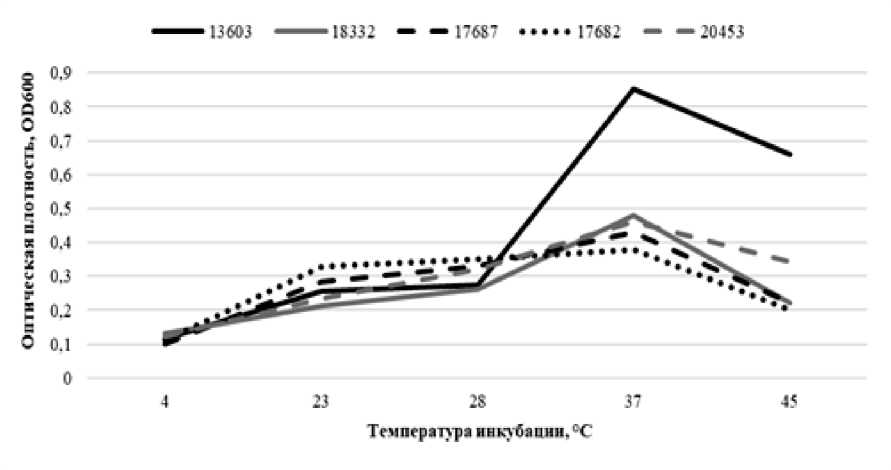
Рис. 1. Температурная характеристика роста штаммов V. cholerae [Temperature characteristics of the growth of V. cholerae strains]
Через 2 ч. инкубации в условиях холодового стресса значимых изменений в основных группах ЖК выявлено не было – С16:0 и С16:1 оставались доминатными ЖК. Тем не менее, в первые часы инкубации отмечено появление пиков соединений, необычных для возбудителя холеры – жасмоновой кислоты и фарнезола. Согласно литературным данным оксилипин – жасмоновая кислота, синтезируется и накапливается в клетках преимущественно при действии на организм повреждающего фактора и играет центральную роль в формировании адаптационного ответа на действие абиотических и биотических стрессов [Васюкова, Озерецковская, 2009]. Максимальный синтез жасмоновой кислоты отмечался у штаммов холерного вибриона классического биовара, достигая 5% от суммарной площади пиков соединений, детектируемых в клетке, что косвенно указывает на то, что данное соединение, возможно, играет роль в реакции холерных вибрионов на температурный (холодовой) стресс. В то же время у штаммов О139 се-рогруппы увеличение синтеза данного оксилипина наблюдали и при повышенной температуре культивирования – 45°С.
Для растений и некоторых микроорганизмов описана роль жасмоновой кислоты в качестве мобильной сигнальной молекулы, которая индуцирует экспрессию защитных генов, стимулирует накопление различных вторичных метаболитов, непосредственно участвующих в защитных реакциях [Wang, Wu, 2013].
Фарнезол, детектируемый в клетках штаммов холерных вибрионов классического биовара, является звеном в биосинтезе тритерпенов (через этап образования сквалена). Для ряда микроорганизмов показана его роль в качестве QS-молекулы в осуществлении внутри- и межвидовой хемокоммуникации [Сачивки-на, Подопригора, Марахова, 2020].
Через 24 ч. инкубации в условиях гипотермии у большинства штаммов содержание НЖК закономерно уменьшалось, а количество ННЖК увеличивалось. Отношение НЖК к ННЖК при 23°С составляло в среднем (40.61:51.85), а при 4°С – уже (26.24:63.46). Отмечены достоверные изменения в содержании С16:0, С15:0, С17:0, С16:1 и С18:1 по сравнению с контрольными образцами. Так, содержание пальмитиновой кислоты было снижено на 20–60%, а нечетные нормальные ЖК С15:0 и С17:0 полностью отсутствовали. В то же время содержание С16:1 увеличивалось на 25–40% (16:1), а С18:1 на 7–35%.
Помимо моноеновых ННЖК, у штаммов О1 серогруппы отмечалось появление полиеновых ЖК – С18:3, С20:5. Как известно из литературы, увеличение доли ННЖК является основным механизмом адаптации грамотрицательных бактерий к низким температурам. Накопление в мембранах моно- и полиеновых ЖК в cis-конфигурации способствует поддержанию ее активного – жидкокристаллического состояния, препятствуя переходу в фазу кристалл-гель за счет снижения температуры плавления. Так, температура плавления С16:0 (доминантной ЖК у холерных вибрионов при 37 и 45°С) составляет 62.5°С, а температура плавления С16:1 (доминантной ЖК при 4°С) – всего 1°С. Небезынтересно отметить, что при более длительной инкубации (7–10 дней) клеток в условиях холодового стресса наблюдался обратный процесс – значительное снижение содержания основных ННЖК – С16:1, С18:1 (в 2–8 раз) и увеличение НЖК. Рядом авторов высказано предположение, что подобная модификация липидного состава в сочетании с изменением мембранного потенциала и уровня гидрофобности приводит к снижению текучести мембраны, индуцируя переход в некультивируемое состояние (крайнюю форму адаптации) при длительной инкубации в условиях низких температур [Day, Oliver, 2004; Yoon, Lee, 2020].
У штаммов холерного вибриона О139 и nonO1/nonO139 серогрупп, выделенных из воды, наблюдали альтернативные реакции на холодовой шок. Так, у штамма V. сholerae nonO1/nonO139 20453 через сутки инкубации в условиях холодового стресса детектировали семикратное увеличение С16:0 – с 5.32% до 41%. У штамма V. сholerae О139 Р-17682 и Р-17687 на фоне снижения С16:0, отмечалось увеличение содержания более короткоцепочечной С14:0 в среднем до 30% (рис. 2).
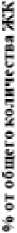
Вяе1с15оЖК ВС14:0 ВО5:0 006:0 BO6:1 0C17:O 807:1 108:0 008:1
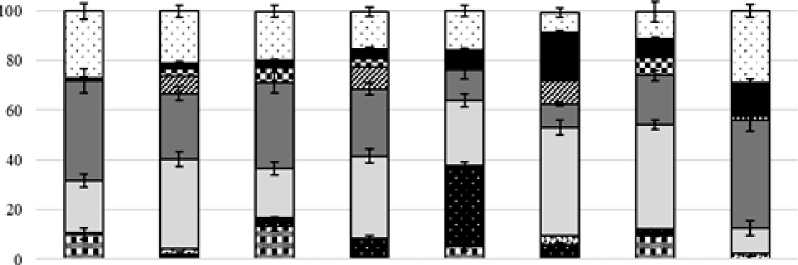
136034®€’ 13603 37®€ 183314®€ 18332 37®€ 17682 4®€ 17682 37®€ 20453 4®€ 20453 37®€ ШтяммыТ. сЬокгяе
Рис. 2. Спектр жирных кислот штаммов V. cholerae в условиях холодового стресса (4°С, 24 ч.) [Fatty acid spectrum of V. cholerae strains under cold stress conditions (4°С, 24 h)]
Помимо вариаций ЖК состава при пониженных температурах культивирования, у ряда штаммов V. choleraе регистрировали увеличение количества ненасыщенных жирных спиртов.
Необходимо отметить, что оптимальной для синтеза ЖК (температура, при которой площадь пиков и число отдельных представителей ЖК было максимальным) для большинства штаммов была температура 37°С. Исключение составляли штаммы V. choleraе О139 серогруппы, выделенные из воды. У водных штаммов Р-17682 и Р-17678 при температуре 23°С детектировались необычные для холерных вибрионов длинноцепочечные НЖК – бегеновая (С22:0), тетракозановая (С24:0), гексакозановая (С26:0), которые отсутствовали у контрольных образцов. Причем содержание С24:0 достигало 40%, конкурируя с С16:0, а количество С22:0 составляло 10–11%, конкурируя с С18:0 (рис. 3).
Воздействие теплового стресса приводило к значительным изменениям в ЖК составе V . choleraе . При сублетальных значениях температуры (45°С) детектировали появление trans -изомеров ННЖК, доля которых спустя 24 ч. достигала 26.14–77.3% от всего количества ННЖК. У штаммов О1 серогруппы по данному механизму изомеризовались как С16:1, так и С18:1 ННЖК, тогда как у штаммов V. choleraе О139 серогруппы (как водных, так и клинических), и у штаммов V. choleraе nonO1/nonO139 детектировались преимущественно trans-изомеры С18:1 ЖК. Необходимо отметить, что у некоторых штаммов детектировали наличие trans- изомеров и при пониженных температурах культивирования. Данный феномен может указывать на наличие альтернативных функций у trans -ННЖК при термическом стрессе, либо об индивидуальных особенностях штаммов.
Повышенная температура культивирования служила сигналом также для активации путей синтеза соединений класса фенилпропаноидов – гликолевой, салициловой, пиперониловой, фенил(бен-зен)пропановой, бензойной и толуиновой кислот, кумаринов, циннаматов – пики которых детектировали через 2 ч. инкубации клеток возбудителя холеры в условиях теплового стресса. У вибрионов О1 серо-группы они составляли 7–13% от всех детектируемых соединений.
■ С14;0 СС15Д OC16:0 0C16:1 HC17;0 0C17J «CIS:» DC18:1 ЯС22Л ЭС24Л DC26;0
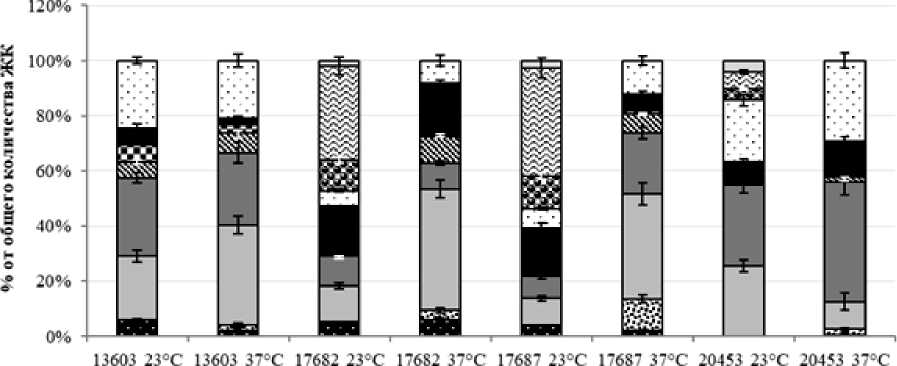
Штаммы Г. cholerae
Рис. 3. Спектр жирных кислот штаммов V. cholerae при пониженной температуре (23°С, 24 ч.) [The spectrum of fatty acids of V. cholerae strains at a reduced temperature (23°С, 24 h)]
Биосинтез ароматических соединений является важным метаболическим путем для жизнедеятельности микроорганизмов, растений и некоторых эукариотических организмов. Этот путь включает большое разнообразие соединений, участвующих в таких важных биологических процессах, как образование структурных блоков для синтеза белка, сидерофоров, вторичных метаболитов, таких как пигменты и антимикробные вещества. Некоторые продукты этого пути оказывают цитотоксический эффект в отношении эукариотических клеток [Díaz-Quiroz et al., 2014]. Промежуточные продукты синтеза коричной кислоты – салициловая и бензойная кислоты – в настоящее время рассматриваются как эндогенные поли-функциональные биорегуляторы фенольной природы, принимающие участие в клеточном сигналинге, ростовых процессах, формировании адаптивных реакций организмов [Колупаев, Ястреб, 2013]. Летучий метил салицилат играет также важную роль в аллелопатических взаимоотношениях в биоценозах наряду с летучими производными липоксигеназного метаболизма (метилжасмонат, ноненали и др.) [Васюкова, Озерецковская, 2007]. Пиперониловая кислота, синтезируемая штаммами классического биовара при повышенной температуре, является аналогом транс-метоксикоричной. Существуют данные, что молекулы пиперониловой кислоты участвуют в репарации клеточных повреждений, вызванных действием стрессирующих факторов [Shalk et al., 1998; Lee et al., 2018].
Азелаиновая кислота, накапливаемая в клетках V. cholerae при 45°С, участвует в межвидовом взаимодействии и в реакции на стрессовые условия [Javvadi et al., 2018; Palmieri et al., 2019].
Через 24 ч. инкубации в условиях гипертермии регистрировали резкое увеличение содержания НЖК, обусловленное в первую очередь синтезом пальмитиновой и стеариновой кислот, доля которых составляла 37–62% и 20–34%, соответственно. Отношение НЖК к ННЖК в среднем составляло (75.87:19.59) (рис. 4).
Начиная с 37°С, у возбудителя холеры детектировался синтез ω-циклических жирных кислот – циклопентанундекановой (cycl11:0) и циклопентантридекановой (cycl13:0), количество которых достигало 3–5% в условиях теплового стресса (45°С). Как следует из литературных данных, введение циклопентанового кольца в молекулу жирной кислоты способствует стабилизации мембраны, препятствуя ее избыточному разжижению, тем самым обеспечивая ее функционирование в стрессовых условиях уже через несколько часов после воздействия высоких температур [Li et al., 2002].
Помимо нормальных прямоцепочечных ЖК у холерных вибрионов детектировались также разветвленные ЖК – в iso - и anteiso -конфигурациях. При 4°С разветвленные ЖК были представлены в основном anteiso -изомерами, а при 37 и 45°С – iso -изомерами.
Аnteiso-разветвленные ЖК у холерных вибрионов были представлены 12-метил миристиновой (а15:0), 13-метил пентадекановой (а16:0), 14-метил пальмитиновой (а17:0), 15-метил гептадекановой ЖК(а18:0). Количество их колебалось от 0 до 36%. Iso-разветвленные ЖК были представлены – 12-метил тридекановой (i14:0), 13-метил миристиновой (i15:0), 14-метил пентадекановой (i16:0), 16-метил гептадекановой (i18:0). Содержание их варьировало от 0 до 12.2% в зависимости от штамма, времени и температуры инкубации. Известно, что разветвленные ЖК благодаря особенностям химического строения мо- гут выполнять адаптивную функцию, сохраняя оптимальную текучесть и пластичность мембраны при резких изменениях температуры окружающей среды [Siliakus, Oost, Kengen, 2017].
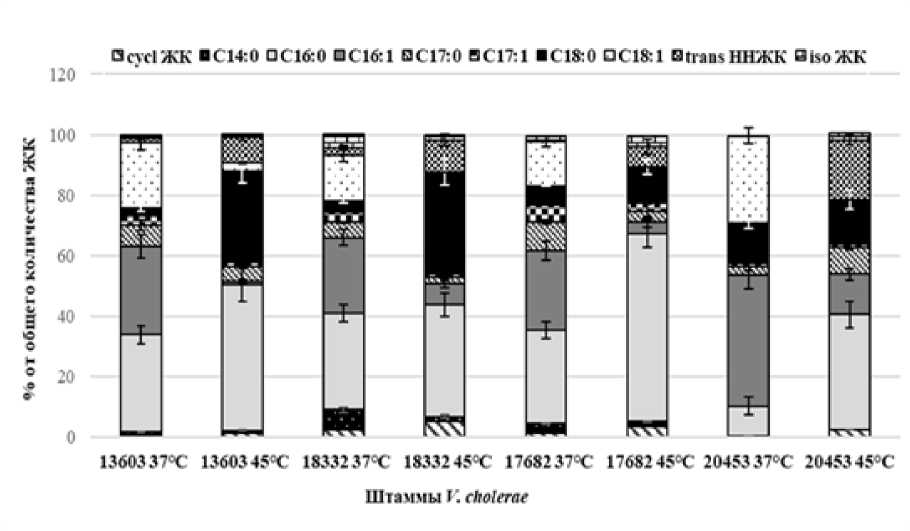
Рис. 4. Спектр жирных кислот штаммов V. cholerae в условиях теплового стресса (45°С, 24 ч.) [Fatty acid spectrum of V. cholerae strains under heat stress conditions (45°С, 24 h)]
Для оценки достоверности различий в содержании основных (мажорных) групп ЖК в клетках возбудителя холеры при изменении температуры культивирования были использованы непараметрические критерии Фридмана и Кендалла. Полученные результаты позволяют говорить о статистической значимости различий в содержании следующих доминантных ЖК в исследованных штаммах V. cholerae при пониженной (4°С), стандартной (37°С) и повышенной температурах культивирования (45°С): С16:0 (р = 0.0141), С16:1 (р = 0.012860), С17:0 (р = 0.0275), С18:0 (р = 0.00002), С18:1 (р = 0.00027).
Таким образом, температурный стресс влияет на спектр ЖК штаммов V. сholerae . Можно предположить, что изменения в ЖК составе являются одним из механизмов термической адаптации холерных вибрионов и маркерами температурного стресса.
Заключение
Методом ГХ/МС у штаммов V. cholerae O1, O139, nonO1/nonO139 серогрупп был изучен спектр ЖК в широком диапазоне температур: от 4 до 45°С. Детектированы качественные и количественные изменения в составе ЖК у штаммов холерных вибрионов под влиянием температурного стресса. Выявлены отличия в реакции на холодовой стресс у штаммов, выделенных от больных и из воды поверхностных водоемов. Реакция штаммов, выделенных от больных, на гипотермию заключалась в увеличении содержания ННЖК – С16:1, С18:1, синтезе аnteiso- разветвленных ЖК. Штаммы, выделенные из воды поверхностных водоемов, напротив, реагировали увеличением синтеза НЖК – С14:0, С16:0. Реакция на тепловой стресс у большинства изученных штаммов, независимо от набора детерминант патогенности и источника выделения, имела общую тенденцию: увеличение суммарного количества НЖК, синтез trans-изомеров ННЖК, появление ω-алициклических и iso-разветвленных ЖК. Помимо ремоделирования жирнокислотного состава мембраны, под действием температурного стресса отмечен синтез оксилипинов, фенилпропаноидов, терпеноидов.
Характер и динамика наблюдаемых изменений в спектрах жирных кислот под влиянием термического стресса свидетельствуют о наличии «запаса» экологической пластичности у холерного вибриона, способствующей сохранению возбудителя в разных биоценозах.
Список литературы Влияние температурного стресса на спектр жирных кислот штаммов Vibrio cholerae
- Бахолдина С.И., Соловьева Т.Ф. Экологические аспекты вирулентности бактерий псевдотуберкулеза // Вестник ДВО РАН. 2009. № 3. С. 85-89. URL: https: //cyberleninka.ru/artide/n/ecologicheskie-aspekty-virulentnosti-bacteriy-pseudotuberculeza (дата обращения: 11.09.2020).
- Васюкова Н.И., Озерецковская О.Л. Индуцированная устойчивость растений и салициловая кислота (обзор) // Прикладная биохимия и микробиология. 2007. Т. 43, № 4. С. 405-411. URL: https://elibrary.ru/download/elibrary_9534588_50848214.pdf.
- Васюкова Н.И., Озерецковская О.Л. Жасмонат-зависимая защитная сигнализация в тканях растений. // Физиология растений. 2009. Т. 56, № 5. С. 643-653. URL: http://elibrary.ru /item.asp?id =12900977.
- Колупаев Ю.Е., Ястреб Т.О. Стресс-протекторные эффекты салициловой кислоты и ее структурных аналогов // Физиология и биохимия культ. растений. 2013. Т. 45, № 2. С. 113-126. URL: http://dspace.nbuv.gov.ua/bitstream/handle/123456789/66470/ 03Kolupaev.pdf?sequence= 1.
- Кузьменко Т.Е., Головня Р.В., Вронова Е.А. Исследование состава высших жирных кислот свободных липидов V. cholerae // Биоорганическая химия. 1980. Т. 1, № 6. С. 90-98.
- Осипов Г.А. Хромато-масс-спектрометрический анализ микроорганизмов и их сообществ, в клинических пробах при инфекциях и дисбиозах // Химический анализ в медицинской диагностике. М.: Наука, 2010. С. 293-368.
- Сачивкина Н.П., Подопригора И.В., Марахова А.И. Фарнезол: свойства, роль и перспективы использования при регулировании пленкообразования у грибов рода Candida // Фармация. 2020. Т. 69, № 6. С. 8-12. https://doi.org/10.29296/25419218-2020-06-02.
- Day A.P., Oliver J.D. Changes in membrane fatty acid composition during entry of Vibrio vulnificus into the viable but nonculturable state // J. Microbiol. 2004. Vol. 42, № 2. P. 69-73. PMID: 15357297.
- Diaz-Quiroz D.C. et al. Current perspectives on applications of shikimic and aminoshikimic acids in pharmaceutical chemistry // Research and Reports in Medicinal Chemistry. 2014. № 4. Р. 35-46. DOI: http://doi.org /10.2147/RRMC.S46560
- Eberlein C. et al. Immediate response mechanisms of gram-negative solvent-tolerant bacteria to cope with environmental stress: cis-trans isomerization of unsaturated fatty acids and outer membrane vesicle secretion // Appl. Microbiol. Biotechnol. 2018. Vol. 102. P. 2583-2593. DOI: http: //doi.org/10.1007/ s00253-018-8832-9.
- Heipieper H.J., Hachicho N. Bacterial solvent responses and tolerance: ris-trans isomerization // Hydrocarbon and lipid. Microbiology Protocols. / eds McGenity T., Timmis K., Nogales B. Berlin; Heidelberg: Springer, 2014. DOI: http://doi.org/10.1007/8623_2014_16.
- Heipeiper H.J., Meinhard F., Segura A. The cis-trans isomerase of unsaturated fatty acids in Pseudomonas and Vibrio: biochemistry, molecular biology and physiological function of a unique stress adaptive mechanism // Fems Microbiol. Let. 2003. Vol. 229, № 1. P. 1-7. DOI: http://doi.org /10.1016 /S0378-1097(03) 00792-4.
- Janse J.D. Fatty acid analysis in the identification, taxonomy and ecology of (plant pathogenic) Bacteria // Diagnosis and Identification of Plant Pathogens. Developments in Plant Pathology / eds Dehne H.W., Adam G., Diekmann M., Frahm J., Mauler-Machnik A., van Halteren P. Dordrecht: Springer, 1997. № 11. DOI: https://doi.org/10.1007/978-94-009-0043-1_13.
- Javvadi S.G. et al. The spent culture supernatant of Pseudomonas syringae contains azelaic acid // BMC Microbiol. 2018. Vol. 18. P. 1-11. DOI: http://doi.org/10.1186/s12866-018-1352-z.
- Lambert M.A. et al. Differentiation of Vibrionaceae species by their cellular fatty acid composition // Int. J. Syst. Bacteriol. 1983. Vol. 33, № 4. P. 777-792. DOI: http://doi.org/10.1099/00207713-33-4-777.
- Lee D.et al. Piperonylic acid stimulates keratinocyte growth and survival by activating epidermal growth factor receptor (EGFR) // Sci. Rep. 2018. Vol. 9. P. 8. DOI: http://doi.org /10.1038/s41598-017-18361-3.
- Li J. et al. Temperature- and surfactant-induced membrane modifica tions that alter Listeria monocytogenes nisin sensitivity by different mechanisms // Appl. Environ. Microbiol. 2002. Vol. 68, № 12. P. 5904-5910. DOI: http://doi.org/10.1128/ aem.68.12 5904 -5910. 2002.
- Moldoveanu S.B., David V. Derivatization Methods in GC and GC/MS // Gas Chromatography / ed. Peter Kusch. 2019. 142 p. DOI: 10.5772/intechopen.81954.
- Moravec A.N. et al. Exogenous polyunsaturated fatty acids impact membrane remodeling and affect virulence phenotypes among pathogenic Vibrio species // Appl. Environ. Microbiol. 2017. Vol. 83, № 22. P. 1-16. doi: 10.1128/AEM.01415-17.
- Palmieri F. et al. Chapter two-oxalic acid, a molecule at the crossroads of bacterial-fungal interactions // Advan. Appl. Microbiol. 2019. Vol. 106. P. 49-77. DOI: http://doi.org/10.1016 /bs.aambs.2018.10.001.
- Poger D., Caron B., Mark A.E. Effect of methyl-branched fatty acids on the structure of lipid bilayers // J. Physical. Chem. 2014. Vol. 118, № 48. P. 13838-13848. DOI: http: //doi.org/10.1021 /jp503910r.
- Poger D., Caron B., Mark A.E. Ring to rule them all: the effect of cyclopropane fatty acids on the fluidity of lipid bilayers // J. Physical. Chem. B. 2015. Vol. 119, № 17. P. 5487-5495. DOI: http: //doi.org /10.1021/acs.jpcb.5в00958.
- Poger D., Mark A.E. Effect of ring size in ю-alicyclic fatty acids on the structural and dynamical properties associated with fluidity in lipid bilayers // Langmuir. 2015. Vol. 31, № 42. P. 11574-11582. DOI: http://doi.org/10.1021/acs.langmuir.5b02635.
- Rowe H.M., Hantley J.F. From the outside - in: The Francisella tularensis envelope and virulence // Front Cell Infect. Microbiol. 2015. № 5. P. 94. DOI: http://doi.org/10.3389/fcimb.2015.00094.
- Seydlova G. et al. The extent of the temperature-induced membrane remodeling in two closely related Bordetella species reflects their adaptation to diverse environmental niches // J. Biol. Chem. 2017. Vol. 292, № 19. P. 8048-8058. DOI: http://doi.org /10.1074/jbc.M117.781559.
- Shalk M. et al. Piperonylic acid, a selective, mechanism-based inactivator of the trans-cinnamate 4-hydroxylase: a new tool to control the flux of metabolites in the phenylpropanoid pathway // Plant Physiol. 1998. Vol. 118. P. 209-218. DOI: http://doi.org /10.1104/ pp.118.1.209.
- Sherlock. Microbial Identification System. V 6.2. MIS Operating Manual. Newark: Sandy Dr, 2012.
- Siliakus M.F., Oost J., Kengen S.W.M. Adaptations of archeal and bacterial membranes to variations in temperture, pH and pressure // Extremophiles. 2017. Vol. 21. P. 651-670. DOI: http://doi.org /10.1007/s00792-017-0939-x.
- Smith D.S. et al. Polyunsaturated fatty acids cause physiological and behavioral changes in Vibrio algino-lyticus and Vibrio fischeri // Microbiologyopen. 2021. Vol. 10, № 5. P. 1-16. doi: 10.1002/mbo3.1237.
- Urdaci M.C., Marchand M., Grimont P.A. Characterization of 22 Vibrio species by gas chromatography analysis of their cellular fatty acids // Res. Microbiol. 1990. Vol. 141, № 4. P. 437-452. DOI: http://doi.org/10.1016/0923-2508(90)90070-7
- Vigh L., Landry J., Nakamoto H. Membrane regulation of the stress response from prokaryotic models to mammalian cells // Ann. NY Acad. Sci. 2007. Vol. 1113, № 1. P. 40-51. DOI: http://doi.org /10.1196/annals.1391.027.
- Wang L., Wu J. The essential role of jasmonic acid in plant herbivore interactions using the wild tobacco Nicotiana attenuate as a model // J. Gen. Genomics. 2013. Vol. 40. P. 597-606. DOI: http://doi.org /10.1016 /j.jgg.2013.10.001.
- Watson H. Biological membranes // Essays Biochem. 2015. Vol. 59. P. 43-69. DOI: http://doi.org/10.1042/bse0590043.
- Yoon J-H, Lee S-Y. Characteristics of viable-but-nonculturable Vibrio parahaemolyticus induced by nutrient-deficiency at cold temperature // Crit. Rev. Food Sci. Nutr. 2020. Vol. 60, № 8. P. 1302-1320. DOI: 10.1080/ 10408398.2019.1570076.


