Влияние условий на процесс железовосстановления в техногенных водных объектах
Автор: Шерышева Н.Г., Плетнева С.Ю.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Водные экосистемы
Статья в выпуске: 5-1 т.13, 2011 года.
Бесплатный доступ
Представлены результаты исследований процесса биологического железовосстановления донного микробного сообщества в канале условно чистых промышленных стоков предприятий северного узла г. Тольятти. Биологическое восстановление происходило более интенсивно на биотопе «зона смешения» по сравнению с биотопом «сток», что связано со снижением концентрации загрязняющих веществ в результате их разбавления волжской водой на участке поступления стоков из канала в водохранилище. Активность железовосстанавливающих микроорганизмов в техногенных водных экосистемах выше по сравнению с природными. Предполагается, что в промышленных стоках в этот процесс включаются другие эколого-трофические группы, в частности углеводородокисляющие бактерии.
Анаэробное железовосстановление, донное микробное сообщество, техногенные водные экосистемы
Короткий адрес: https://sciup.org/148200325
IDR: 148200325 | УДК: 579:628.3
Influence conditions on the process of iron reduction in technogenic water objects
We present result of our study biological iron reduction by the benthic microbial community in an industrial waste channel near the city of Togliatti. The biological iron reduction was found to be more intensive in the mixing zone, where waste water flow mixes with unpolluted water from Kuybyshev Reservoir, compared to the undiluted waste flow. Intensity of the iron reduction depends on the pollutants concentrations in water. As the waste flow is diluted, concentrations of pollutants decrease, and intensity of the iron reduction increases. The overall activity of the iron reducing microorganisms in the industrial waste ecosystems is higher than the similar activity in natural ecosystems. We explain this increased activity with more diversified microbial community. Some other microbial trophic groups, including hydrocarbon-oxidizing bacteria, can take part in the process of the biological iron reduction.
Текст научной статьи Влияние условий на процесс железовосстановления в техногенных водных объектах
культур железовосстанавливающих бактерий: 10% отобранного материала вводили в герметичные бутылочки с предварительно подготовленной анаэробной питательной средой «А» (20 мл). Приготовленные таким способом образцы донных осадков доставляли в лабораторию и экспонировали в термостате при 30°С в течение двух месяцев. В среде измеряли концентрацию двухвалентного железа и численность бактерий через каждые 6 суток.
Среда «А» для культивирования железоредук-торов, приготовленная с применением техники анаэробного культивирования микроорганизмов, имела следующий состав (г/л дистиллированной воды): Fe 3 (PO 4 ) 2 x8H 2 O - 10 г; NaH 2 PO 4 - 0,6; NH 4 Cl - 1,5; MgSO 4 х 7H 2 O - 0,1; MgCl 2 х 6H 2 O - 0,1; KCl - 0,1; Na 2 MoO 4 x 2H 2 O - 0,001; раствор витаминов - 10 мл; микроэлементов - 3 мл; рН = 7,0-7,5 [7, 13].
Железовосстанавливающую активность бактерий оценивали по накоплению Fe(II) в среде. Концентрацию двухвалентного железа определяли феррозиновым методом спектрофотометрически (СФ-46) при 562 нм после экстракции проб 0,5 н соляной кислотой в течение 15 мин [14].
Химический анализ воды выполнен сотрудниками лаборатории прикладной экологии Института экологии Волжского бассейна РАН.
Численность клеток бактерий определена прямым подсчетом в камере Горяева [11].
Район исследования. Канал проходит по восточной части Центрального района г. Тольятти через промкомзону Автозаводского района и впадает в Куйбышевское водохранилище ниже села Под-степки. Промышленные стоки через трубы, выведенные из земляной дамбы, сбрасываются в устье канала, сообщающегося с приплотинным плесом водохранилища (рис. 1).
Длина от дамбы (места сброса химстоков из трубы) до выхода в прибрежную зону водоема составляет 270 м. Стенки и дно канала бетонированы, берега покрыты кустарником. Вдоль берега произ- растает высшая водная растительность: рогоз, лопух, череда. На поверхности воды развивается ряска. Дно канала заилено.
Исследования проводились на двух станциях (рис. 1): ст. 1 «сток» - место непосредственного поступления сточных вод из труб в устье канала и ст. 2 «зона смешения», расположенная на участке выхода сточных вод из канала в открытую часть, где они смешиваются с водами Куйбышевского водохранилища.
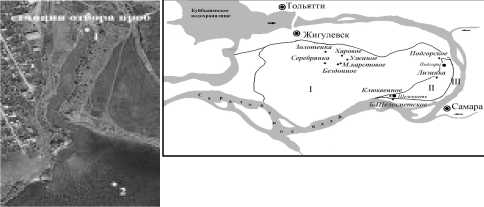
Рис. 1. Схема устья канала сточных вод северного промузла: ст. 1 «сток» - место непосредственного поступления сточных вод из труб, проходящих через дамбу; ст. 2 «зона смешения» - район выхода вод из канала в открытую часть водохранилища
Рис. 2. Схема расположения озер на территории Национального Парка «Самарская Лука»: I - возвышенность, II - надпойменная терраса, III - Шелехмет-ская пойма
Следует отметить разные источники формирования донных отложений. Осадки в районе выхода труб из дамбы образуются главным образом за счет склонового стока и абразии берегов . Донные отложения на ст. 2, находятся в прибрежной зоне ложа водохранилища и на их формирование, кроме отмеченных факторов, оказывают влияние и другие условия осадкообразования, характерные для водоема в целом: почвообразующие породы, эрозионные процессы, взвеси, осаждающейся детрит, абразивный материал [5].
В работе для сравнения приводятся результаты исследований, проведенных на природных водоемах Самарской Луки (рис. 2).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Характеристика донных отложений как биотопов . В канале стоков формируются техногенные донные осадки, представленные песком и глиной (табл. 1). Дно канала на участке «сток» покрыто серым песком , содержащим черные техногенные частицы и небольшой слой ила. Песок имеет нейтральную реакцию среды , интенсивный запах нефтепродуктов и сероводорода . В «зоне смешения» донные осадки представлены глиной оранжево-коричневого цвета с примесью песка и характеризуются слабокислой реакцией среды (рН), более низкими значениями температуры , менее интенсивным запахом нефтепродуктов и сероводорода.
Важным свойством донных отложений является физико-химическая поглотительная способность, благодаря которой они адсорбируют из воды значительное количество различных химических соединений [2]. Из результатов химического анализа воды (табл. 2) следует, что донные отложения на «стоке» аккумулируют химические вещества в значительно большей степени , по сравнению с «зоной смешения». Вода в месте поступления из труб содержит на 1-2 порядка больше азота (нитратов, нитритов, аммония), сульфатов, сероводорода, гидрокарбонатов, калия, натрия. Известно, что крайне высокие концентрации отмеченных биогенных элементов угнетают развитие микрофлоры.
Таблица 1. Физико-химические показатели донных осадков канала
|
Место отбора проб |
Глубина отбора, м |
Характер осадка |
Влажность, % |
С |
р Н |
H 2 S* |
|
Сток |
1,5 |
серый илистый песок |
84 |
26,0 |
7, 0 |
+ + |
|
Зона смешения |
2,0 |
оранжевокоричневая глина с песком |
82 |
3,5 |
6, 5 |
+ |
Примечание: * - присутствие сероводорода
В химическом составе стока отмечено высокое содержание алюминия и особо токсичных тяжелых металлов - меди, цинка, никеля. Сосредоточение в донных отложениях высоких концентраций этих веществ может представлять значительную опасность для гидробионтов [1]. На станции «зона смешения» происходит снижение концентраций загрязняющих веществ в результате разбавления сточных вод - процесса, протекающего вследствие перемешивания сточных вод с водной массой водохранилища.
Таким образом, в донных отложениях исследованных участков канала, при рассмотрении их в качестве биотопов, создаются неравнозначные условия обитания для микробного населения. Осадки различны по механической структуре, количественному содержанию компонентов химического состава. Сообщество донных микроорганизмов биотопа «сток» в большей степени подвержено техногенной нагрузке по сравнению с биотопом «зона смешения».
Биологическое восстановление Fe(III) при культивировании техногенных донных осадков на минеральной среде «А» проходило в три стадии и проявило направленность, установленную ранее авторами на накопительных бактериальных культурах, полученных из природных водных экосистем [10, 13], однако интенсивность и количественные характеристики были значительно выше.
Так, на первой стадии, характеризующейся наибольшей интенсивностью, резкое помутнение сре- ды произошло уже на следующие сутки в результате увеличения численности бактерий. При этом начальные серый и оранжево-коричневый цвета суспензии изменились до черного. Бактериальный рост сопровождался резким увеличением в среде растворенного двухвалентного Fe(II), образующе- гося в результате акцептирования Fe(III) электронов, высвобождающихся при окислении субстрата. Интенсивное восстановление Fe(III) происходило в течение шести суток. Причем, сообщества из исследуемых биотопов проявили разную железовосстанавливающую активность (рис. 2).
Таблица 2. Концентрации химических веществ в воде канала промышленных стоков и озер Самарской Луки
|
Показатель |
Станции канала сточных вод |
Водоемы Самарской Луки* |
|
|
Сток |
Зона смешения |
||
|
Температура, °С |
26,8 |
20 |
10,2 - 21,0 |
|
рН |
8,65 |
7,94 |
5,85 - 7,74 |
|
Растворенный кислород, мл О/м3 |
9,77 |
8,85 |
0 - 10,3 |
|
БПК полн., мг О/м3 |
14,89 |
9,54 |
- |
|
Бихроматная окисляемость, мг О/м3 |
50,5 |
13,1 |
- |
|
Кремний, мг/ м3 |
4,89 |
3,44 |
1,84 - 4,52 |
|
Фосфаты (по Р), мг/м3 |
0,605 |
0,029 |
0,05 - 0,86 |
|
Магний, мг/м3 |
16,4 |
7,77 |
0,9 - 24,4 |
|
Азот минеральный (по N) мг/м3 |
12,40 |
1,54 |
0,49 - 2,01 |
|
Сульфат-анион, мг/м3 |
172,2 |
56 |
3,2 - 59,2 |
|
Железо, мг/м3 |
0,085 |
0,05 |
0,41 - 4,17 |
|
Сероводород, мг/м3 |
0,013 |
не определяется |
0 - 0,026 |
|
Гидрокарбонаты, мг/м3 |
269,38 |
98,12 |
12,4-227,1 |
|
Жесткость, мг+ экв/м3 |
3,6 |
2,2 |
0,57 - 4,53 |
|
Калий, мг/м3 |
1,48 |
0,61 |
- |
|
Натрий, мг/м3 |
480 |
8,9 |
- |
|
Марганец, Mn2+ мг/м3 |
0,031 |
0,014 |
- |
|
Алюминий, мг/м3 |
0,244 |
не определятся |
- |
|
Медь, мг/м3 |
0,0094 |
0,0056 |
- |
|
Цинк, мг/м3 |
0,082 |
0,029 |
- |
|
Никель, мг/м3 |
0,0062 |
0,055 |
- |
Примечание: «-» - нет данных; * - по: [3]
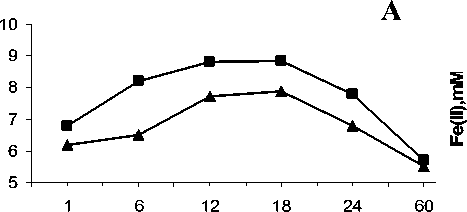
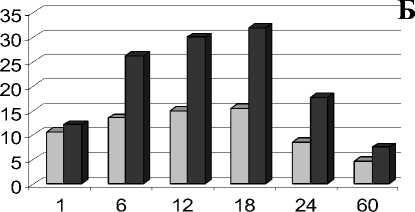
Наибольшая численность клеток (N = 6,6 × 108 кл/мл) и количество восстановленного железа (Fe(II) = 26,3 mM) регистрировались в суспензии, полученной из станции «зона смешения». В образце, полученном из станции «сток», отмеченные показатели имели значения 4 × 107 кл/мл и 13,5
Fe(II) mM, соответственно. На второй стадии (7-12-тые сутки) отмечалось замедление бактериального роста и продукции Fe(II), хотя и достигаются максимальные значения численностей бактерий (4,9 × 107 кл/мл и 7 × 108 кл/мл) и концентраций двухвалентного железа (15,5 mM и 32 mM).
сутки
сутки
сток -■— зона смешения
□ сток □ зона смешения
Рис. 2. Изменение численности бактерий ( А ) и концентрации двухвалентного железа ( Б ) в питательной среде при культивировании микроорганизмов, полученных из донных осадков канала
Третья стадия (8-60-тые сутки) отличается от двух предыдущих качественно: происходит резкое снижение титра клеток до ~5 х 105 кл/мл и концентраций двухвалентного железа до 4,6-7,5 mM. В варианте «зона смешения» отмечено осветление среды (рис. 3). Такие изменения вызваны качественным преобразованием формы железа в результате кристаллизации: из растворенного состояния двухвалентное железо переходит в нерастворимые минеральные частицы. В результате этого процесса образуется минеральный осадок, состоящий из нерастворимых соединений двухвалентного железа, который выпадает на дно. Снижение численности бактерий происходит в результате сорбции их на твердой фазе.
При микроскопическом исследовании полученного осадка были обнаружены минеральные час- тицы различных прямоугольных форм (рис. 4). При воздействии на осадок концентрированной соляной кислотой происходило интенсивное выделение сероводорода. Черный цвет осадка, форма кристаллов и результат качественного тестирования указывают на образование сульфидов железа, что наиболее вероятно в присутствии высоких концентраций сульфатов в среде (см. табл. 1).

Рис. 3. Изменение структуры питательной среды под действием Fe(III) восстанавливающих микроорганизмов, полученных из донных осадков : А - стока, Б – зоны смешения

Рис. 4. Образование минеральных частиц в процессе восстановления соединений Fe(III) микробным донным сообществом канала (увеличение х 1000)
Представляется очевидным, что более высокая железовосстанавливающая активность донного сообщества в «зоне смешения» обусловлена снижением негативного воздействия высоких концентраций загрязняющих и токсических веществ в виду их разбавления волжской водой. Важное значение, на наш взгляд, имеет и положение этого биотопа, находящегося в переходной зоне – между каналом и прибрежной зоной водохранилища. Обогащение органическим и биогенным веществом водохранилищных вод способствует проявлению «краевого эффекта», т.е. вовлечению в данном случае в процесс Fe(III) восстановления других популяций микробного населения.
Сопоставление полученных авторами данных с результатами исследований, выполненных ранее по природным водоемам теми же методами [810], показало разный уровень железовосстанавливающей активности донных сообществ. Количество двухвалентного железа в ряду озерных илов оставило 4,5-16 mМ (рис. 5). В образцах же, полученных из техногенных осадков канала железо восстанавливалось бактериями значительно интенсивнее – более чем в 2 раза (Fe(II) = 15-32 mМ) (рис. 5).
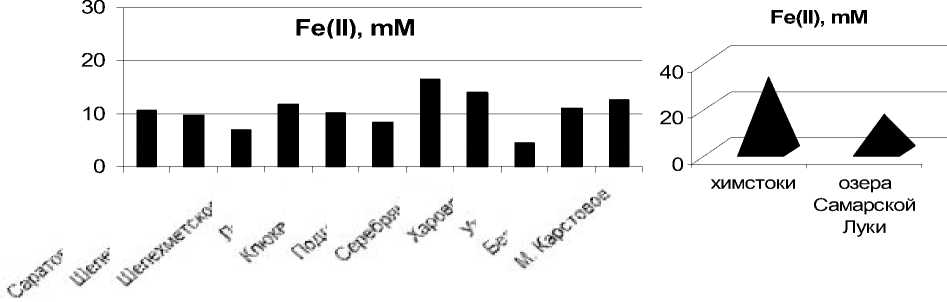
Рис. 5 . Концентрации двухвалентного железа в питательных средах при восстановлении пирофосфата Fe(III) микроорганизмами, полученными из донных отложений озер Самарской Луки, Саратовского водохранилища и техногенных стоков
Такие различия обусловлены рядом причин. Как известно, структура сообщества определяется физико-химическими условиями среды обитания. Озера, на которых проводились исследования, располагаются на территории Национального парка «Самарская Лука» (рис. 2) и поэтому не испытывают антропогенной нагрузки. К примеру, вода в них содержит меньше сульфатов, азота (табл. 1).
Одним из определяющих факторов функционирования донного микробного населения является количество, происхождение, состав и доступность органического вещества [4]. В озерных илах органическое вещество, представляющее питание для микроорганизмов, формируется из растительного и животного детрита. В канале донные осадки накапливают техногенное органическое вещество, включающее и производные нефтепродуктов. Наличие углеводородов способствует развитию углеводородокисляющей микрофлоры, активно участвующей в процессах цикла железа.
Было установлено, что диссимиляционная редукция Fe(III) является основополагающим процессом в анаэробном окислении органического вещества и в деструкции нефти и нефтепродуктов [10]. Также экспериментально показано, что угле-водородокисляющие бактерии снижают содержание общего железа в ливневых стоках [6]. Причем наиболее активно проявляет себя ассоциация уг-леводородокисляющих и Fe(III) восстанавливающих бактерий (рис. 6).
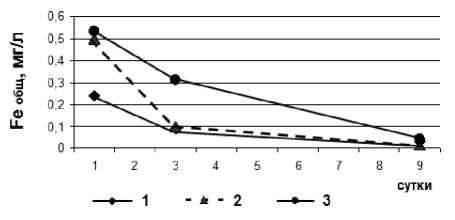
Рис. 6. Снижение концентрации общего железа в сточной воде при культивировании бактериальных ассоциаций: 1, 2 – углеводородокисляющих бактерии; 3- углеводородокисляющих и железовосстанавливающих бактерий
ЗАКЛЮЧЕНИЕ
В техногенных условиях процесс железовос-становления имеет общую направленность: интенсивное накопление ионов двухвалентного железа в среде – качественное изменение форм железа – образование минерального осадка. В целом процесс идет более интенсивно по сравнению с естественными водоемами, что, по-видимому, связано с вовлечением других групп микроорганизмов.
В техногенной экосистеме канала промышленных химических стоков наибольший уровень железовосстановления выявлен в «зоне смешения». Высокую активность сообщества на этом биотопе обуславливает сочетание факторов: генезис донных отложений; снижение токсичного влияния высоких концентраций химических веществ в результате перемешивания сточных и водохранилищных вод; наличие техногенного органического вещества, являющимся пищевым субстратом для определенных экологотрофических групп микроорганизмов; обогащение биогенными элементами, поступающими с водами водохранилища.
Авторы выражают искреннюю благодарность сотруднику Института экологии Волжского бассейна РАН к.г.н. Л.А. Выхристюк за критические и ценные замечания к работе.
Список литературы Влияние условий на процесс железовосстановления в техногенных водных объектах
- Бреховских В.Ф., Казмирук Т.Н., Казмирук В.Д. Донные отложения Иваньковского водохранилища: состояние, состав, свойства. Ин-т вод. проблем РАН. М.: Наука, 2006. 176 с.
- Выхристюк Л.А., Варламова О.Е. Донные отложения и их роль в экосистеме Куйбышевского водохранилища. Самара, 2003. 174 с.
- Жариков В.В., Горбунов М.Ю., Быкова С.В., Уманская М.В., Тарасова Н.Г., Буркова Т.Н., Шерышева Н.Г. Протисты и бактерии озер Самарской области//Под ред. д.б.н. В.В. Жарикова. Тольятти: Кассандра, 2009. 240 с.
- Дзюбан А.Н. Деструкция органического вещества и цикл метана в донных отложениях внутренних водоемов. Ярославль: Принтхаус, 2010. 192 с.
- Куйбышевское водохранилище (научно-информационный справочник)/Отв. ред. Г.С. Розенберг, Л.А. Выхристюк. Тольятти: ИЭВБ РАН, 2008. 123 с.
- Потехина Ж. С., Шерышева Н. Г., Ракитина Т.А., Поветкина Л.П., Литвиненко М.Н. Снижение содержания солей железа и нефтепродуктов в промышленных ливневых стоках с помощью микроорганизмов/Мат-лы III Всеросс. научно-практ. конф. «Экологические проблемы биодеградации промышленных, строительных материалов и отходов производств». Пенза, 2000. С. 114-116.
- Потехина Ж. С., Шерышева Н. Г., Бычек-Гущина И.А., Готтшалк Г. Анаэробный рост бактерий на метане с Fe(III)восстановлением, как электрон акцептирующим процессом//Известия СНЦ РАН, 2000. Т.2, № 2. С. 371-379.
- Потехина Ж.С., Шерышева Н.Г., Уманская М.В., Поспелова М.Д. Биологическое Fe(III) восстановление в водоемах Самарской Луки//Заповедное дело России: принципы, проблемы, приоритеты: Мат-лы междунар. науч. конф. -Бахилова Поляна, 2003. Т. 1. С. 40-43.
- Потехина Ж.С., Н.Г. Шерышева, Т.А. Ракитина Л.П. Поветкина, Литвиненко М.Н. Биологическое восстановление Fe(III) в разных горизонтах донных отложений озер Самарской Луки//Мат-лы Всеросс. науч. конф. «Современные аспекты экологии и экологического образования». Казань, 2005. С. 284-286.
- Потехина Ж.С. Метаболизм Fe(III) восстанавливающих бактерий. Тольятти: ИЭВБ РАН, 2006. 225 с.
- Практикум по микробиологии//Под ред. Н.С. Егорова. М.: Изд-во Моск. ун-та, 1976. 307 с.
- Шерышева Н. Г. Особенности процесса Fe(III) восстановления в донных отложениях озер Самарской Луки//Экологические проблемы бассейнов крупных рек -3: Тез. докл. Междунар. конф. Тольятти: ИЭВБ РАН, 2003. С.319.
- Daniel R., Warnecke F., Potekhina J.S., Gottschalk G. Identification of the syntrophic partners in a coculture coupling anaerobic methanol oxidation to Fe(III) reduction//FEMS Microbiol. Lett. 1999. V. 180. P. 197-203.
- Lovley, D.R., Phillips, E.J.P. Organic matter mineralization with reduction of ferric iron in anaerobic sediments//Appl. Env. Microbiol. 1986. V. 51. P. 683-689.
- Lovley D.R. Organic matter mineralization with the reduction of ferric iron//Geomicrob. J. 1987. V. 5, № 314. P. 375-399.


