Влияние условий синтеза порошка оксида иттрия, легированного ионами неодима, на морфологию
Автор: Борисов В.Н., Лысенко О.В., Колесова Т.В., Толмачва И.Г., Кононова Р.П., Сериков А.С.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 4 т.16, 2024 года.
Бесплатный доступ
Исследована зависимость формы и размера частиц оксида иттрия, легированного ионами неодима, от способа синтеза: гомогенное и гетерогенное соосаждение. Для гомогенного соосаждения показана зависимость формы и размера частиц оксида иттрия, легированного ионами неодима, от концентрации исходных солей в растворе, от соотношения концентраций ионов иттрия к осадителю в растворе, от времени старения осадка во время синтеза, от температуры синтеза. Установлено, что для гомогенного соосаждения форма частиц не изменяется при переходе от прекурсора до синтезированного оксида иттрия - образуются частицы сферической формы. Методами инфракрасной спектрометрии и рентгенофазового анализа установлена природа прекурсора - прекурсор рентгеноаморфный, имеющий гидрокарбонатную природу. Размер частиц при переходе от прекурсора до синтезированного оксида иттрия уменьшается на 10-20 %. Для гетерогенного соосаждения показана зависимость формы и размера частиц от природы осадителя (раствор аммиака и раствор аммония углекислого кислого). Также было изучено влияние концентрации исходных солей и температуры синтеза на форму и размер частиц. Установлено, что для гетерогенного соосаждения вне зависимости от осадителя форма частиц не изменяется при переходе от прекурсора до синтезированного оксида иттрия - при использовании в качестве осадителя аммиака получаются частицы игольчатой формы, собранные в агломераты, при использовании в качестве осадителя раствора аммония углекислого кислого получаются частицы пластинчатой формы. Методами инфракрасной спектрометрии и рентгенофазового анализа установлена природа прекурсора: при использовании в качестве осадителя раствора аммония углекислого кислого прекурсор рентгеноаморфный, имеющий гидрокарбонатную природу, а при использовании в качестве осадителя раствора аммиака - смесь гидратов оксогидроксонитратов иттрия. Размер частиц при переходе от прекурсора до синтезированного оксида иттрия практически не изменяется для частиц полученных соосаждением раствором аммиака и уменьшается в 2 раза для частиц полученных соосаждением раствором аммония углекислого кислого.
Оксид иттрия, гомогенное осаждение, гетерогенное осаждение, морфология частиц
Короткий адрес: https://sciup.org/147246070
IDR: 147246070 | УДК: 546.64+546.657 | DOI: 10.14529/chem240408
The effect of the synthesis conditions of yttrium oxide powder doped with neodymium on morphology
The dependence of shape and particle size of Nd-doped yttrium oxide powder on the synthesis method was investigated, covering homogeneous and heterogeneous co-precipitation. For the homogeneous co-precipitation method, the dependence of shape and particle size of Nd-doped yttrium oxide powder on the concentration of the initial salts in a solution, the ratio of concentrations of yttrium ions to the precipitator in the solution, the aging time of the precipitate during synthesis, and synthesis temperatures were investigated. It was found that for homogeneous co-precipitation the particle shape did not change during the transition from the precursor to synthesized yttrium oxide: spherical particles were formed. The nature of the precursor was established by infrared spectrometry and X-ray fluorescence analysis. The precursor was X-ray amorphous, of bicarbonate nature. The particle size decreased by 10-20% during the transition from the precursor to the synthesized yttrium oxide. For the heterogeneous co-precipitation method, the dependence of shape and particle size on precipitator nature (ammonia solution and ammonium bicarbonate solution) were investigated. Besides, the effect of the concentration of the initial salts and the synthesis temperature on the shape and particle size) was studied. It was found that for heterogeneous co-precipitation, regardless of the precipitator nature, the particle shape did not change after conversion from the precursor to the synthesized yttrium oxide. Needle-shaped particles collected in agglomerates were obtained with ammonia as the precipitator. Plate-shaped particles were obtained with a solution of ammonium bicarbonate as the precipitator. The precursor nature was established by infrared spectrometry and X-ray phase analysis. The precursor was X-ray amorphous, of bicarbonate nature, if a solution of ammonium bicarbonate was used as the precipitator. The precursor was a mixture of hydrates of yttrium oxohydroxonitrates, if ammonia was used as the precipitator. The particle size obtained by the co-precipitation method with ammonia as precipitator did not change during the conversion from the precursor to the synthesized yttrium oxide, while the particle size obtained by the co-precipitation method with ammonium bicarbonate as precipitator decreased by 2 times.
Текст научной статьи Влияние условий синтеза порошка оксида иттрия, легированного ионами неодима, на морфологию
В настоящее время все большее значение приобретает изготовление новых высокоплотных керамических материалов, созданных на основе чистых наноразмерных оксидов металлов, в том числе оксида иттрия. Высокий интерес к оксиду иттрия обусловлен тем, что он является исходным веществом для изготовления оптических материалов, обладающих высоким светопропуска-нием в видимой и ИК-области спектра, высокой термо- и химической стойкостью, и является перспективным материалом при изготовлении активных элементов твердотельных лазеров, люминофоров и сцинтилляторов. Однако существует ряд трудностей, возникающих при изготовлении монокристаллов оксида иттрия оптического качества, которые связаны, в первую очередь, с высокой температурой его плавления (2430–2450 °C) [1, 2].
Невысокая стоимость, потенциальная возможность изготовления кристаллов с хорошим оптическим качеством и большой апертуры, а также большие значения теплопроводности оксида иттрия (0,013 Вт/(м·К) для Y2O3 и 0,0014 Вт/(м·К) для иттрий-алюминиевого граната), позволяют керамику на его основе выдвинуть на одну из ведущих позиций в ряду известных лазерных кристаллических материалов для фемтосекундных лазеров [1, 2].
Для получения прозрачной керамики решающее значение имеет выбор сырья. Исходный порошок обязательно должен соответствовать строгим требованиям. Размер частиц, распределение их по размерам, морфология, фазовая и химическая чистота, степень агломерации порошка оказывают существенное влияние на спекание и микроструктуру керамики [3–5]. Форма и размер частиц оксида иттрия напрямую зависят от способа его получения: лазерная абляция [6, 7], золь-гель метод [8, 9], метод осаждения [10, 11], гидротермальный метод [12, 13] и т. д.
Наиболее простым и не требующим дорогостоящего оборудования методом синтеза мелкодисперсных порошков оксида иттрия является осаждение (или соосаждения в случае получения легированного оксида иттрия). Сущность метода заключается в получении нерастворимых соединений (прекурсоров) из растворов солей иттрия, последующем отделении осадка от маточного раствора и термической обработки прекурсора. В данном методе различают:
-
– гомогенное осаждение, при котором образование прекурсора происходит при медленном разложении осадителя в растворе [14–19];
-
– гетерогенное осаждение, при котором образование осадка происходит в момент добавления раствора осадителя к раствору солей (прямое осаждение), и наоборот – добавления раствора солей к раствору осадителя (обратное осаждение) [20–25].
Изменение условий осаждения приводит к изменению состава получаемого прекурсора и, как следствие, к изменению формы и размера частиц получаемого порошка оксида.
Целью данной работы являлось изучение влияния условий синтеза на форму и размер частиц оксида иттрия, легированного ионами неодима (Nd:Y 2 O 3 ).
Для достижения данной цели проводили исследования зависимости формы и размера частиц Nd:Y 2 O 3 :
-
– от способа осаждения: гомогенного и гетерогенного обратного;
-
– концентрации исходных солей;
-
– температуры термообработки.
Для метода гетерогенного обратного соосаждения также проводили исследования зависимости формы и размера частиц от природы осадителя (аммиак и гидрокарбонат аммония).
Для всех методов осаждения отслеживали связь между формой и размером частиц прекурсора и синтезированного оксида.
Экспериментальная часть
В качестве исходных материалов для получения оксида иттрия, допированного ионами неодима, использовали:
– нитрат иттрия 6-водный, «хч», ТУ 6-09-4676-83;
-
– нитрат неодима 6-водный (импортный) ABCR кат. № AB 202388.
В качестве осадителя использовали:
– карбамид «чда», ГОСТ 6691-77;
– аммоний углекислый кислый, «хч» ГОСТ 3762-78;
– аммиак водный, «осч 23-5» ГОСТ 24147-80.
Метод гомогенного соосаждения
Нитраты иттрия и неодима растворяли в дистиллированной воде при помощи магнитной мешалки для получения раствора с концентрацией ионов иттрия 0,099 моль/л и ионов неодима 0,001 моль/л.
Карбамид растворяли в дистиллированной воде при помощи магнитной мешалки для получения раствора с концентрацией в диапазоне от 1 до 2 моль/л.
Растворы карбамида и смеси нитратов иттрия и неодима смешивали при помощи магнитной мешалки, добавляли дистиллированной воды для получения раствора с суммарной концентрацией ионов металлов в диапазоне от 0,01 до 0,02 моль/л и с концентрацией карбамида в интервале от 0,5 до 1 моль/л. Соотношение концентрации ионов металлов к концентрации карбамида в растворе составляло от 1:50 до 1:100
Раствор, состоящий из смеси водных растворов нитратов иттрия и неодима и раствора карбамида, нагревали в стеклянном стакане до температуры ~ 90 °С при постоянном перемешивании и после начала выпадения осадка выдерживали в течение 1–3 часов.
Метод гетерогенного обратного соосаждения
Аммоний углекислый кислый растворяли в дистиллированной воде при помощи магнитной мешалки без нагрева, его концентрация составляла 1,5 моль/л. Водный раствор аммиака готовили разбавлением аммиака водного дистиллированной водой в соотношении 1:4.
Нитраты иттрия и неодима растворяли в дистиллированной воде при помощи магнитной мешалки для получения раствора с концентрацией ионов иттрия в диапазоне от 0,0099 до 0,099 моль/л и ионов неодима в диапазоне от 0,0001 до 0,001 моль/л. Соотношение концентрации ионов иттрия к концентрации ионов неодима в растворе составляло 99:1
Синтез порошка Nd:Y 2 O 3 проводили методом гетерогенного обратного соосаждения из растворов нитратов раствором аммония углекислого кислого (далее по тексту – гетерогенное сооса-ждение бикарбонатом аммония) и водным раствором аммиака (далее по тексту – гетерогенным соосаждение аммиаком) при поддержании рН раствора 7,0 ± 0,1. Скорость капельного приливания раствора нитратов ~ 10 см3/мин. Старение осадка проводили в течение 2 часов при перемешивании на магнитной мешалке.
Полученные осадки фильтровали при помощи вакуум-фильтра. Осадок на фильтре промывали дистиллированной водой и этиловым спиртом, затем сушили на воздухе в течение не менее 6 часов. Полученные порошки прекурсора прокаливали при температурах 700 °С, 1000 °С и 1250 °С в течение 2 часов.
Методы исследования
Для определения свойств и структуры прекурсора использовали следующие методы:
-
– совмещенный термический анализ (СТА), включающий термогравиметрический анализ (ТГА) и метод дифференциальной сканирующей калориметрии (ДСК);
-
– ИК-спектрометрия;
-
– рентгенофазовый анализ (РФА);
-
– сканирующая электронная микроскопия.
Фазовый состав, форму и размер частиц порошка Nd:Y 2 O 3 определяли с помощью:
-
– РФА;
-
– сканирующей электронной микроскопии.
РФА выполнен на рентгеновском дифрактометре на излучении CuKα в диапазоне углов 2ϴ с 16 до 95 градусов, с шагом – 0,02 градуса, время накопления импульсов – 3 секунды. Режим съемки: U = 40 кВ, I = 40 мA.
Исследование процесса термического разложения образцов проводили в инертной среде (азот) в интервале температур от 25 °С до 1000 °С со скоростью нагрева 10 °С/мин на термоанализаторе (пределы допускаемой относительной погрешности измерений температуры ±1,5 %, массы ±1 %). В ходе исследования получали кривые зависимости изменения массы от време-ни/температуры (ТГ-кривые), а также ДТГ-кривые – производные от ТГ-кривых, позволяющие установить момент времени или температуру, при которой изменение массы происходит с максимальной скоростью.
Результаты и обсуждение
Исследование прекурсора оксида иттрия
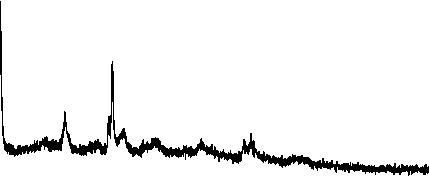
Дифрактограммы порошков прекурсоров, полученных методами гомогенного соосаждения и гетерогенного соосаждения бикарбонатом аммония и аммиаком, представлены на рис. 1.
Как видно из рис. 1, прекурсоры Nd:Y2O3, полученные методом гомогенного соосаждения и гетерогенного соосаждения бикарбонатом аммония аморфным, а также прекурсор, полученный гетерогенным соосаждением аммиаком имеют кристаллическую структуру. Установлено, что прекурсор, полученный гетерогенным соосаждением аммиаком представляет собой смесь гидратов оксогидроксонитратов иттрия.
По результатам ТГА (рис. 2–4) термическое разложение исследованных порошков прекурсоров происходит в несколько стадий.
б)
70 80
20 , град.
о
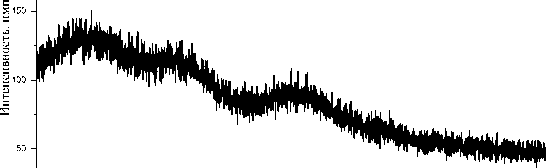
10 20 30 40 50 60 70 80
20 град
в)
Рис. 1. Дифрактограмма порошка прекурсора Nd:Y 2 O 3 , полученного методом: а – гомогенного соосаждения; б – методом гетерогенного соосаждения аммиаком; в – гетерогенного соосаждения бикарбонатом аммония
На начальных участках ДТГ-кривых всех исследованных образцов наблюдается эндотермический эффект, соответствующий удалению химически связанной воды. Затем начинается процесс деструкции прекурсоров.
Для образца, полученного методом гомогенного соосаждения (см. рис. 2), этот процесс идёт практически с постоянной скоростью до температуры « 600 ° С. Далее отмечается резкое возрастание скорости процесса: как видно по ДТГ-кривым, максимальная скорость наблюдается при температуре 633 ° С, завершающая температура ступени разложения - 660 ° С. Общая потеря массы указанного порошка при температуре 750 ° С достигает 43 % и, далее, до 1000 ° С изменения массы практически не происходит.
Окончание процесса разложения прекурсора, полученного гетерогенным соосаждением бикарбонатом аммония (см. рис. 4), происходит при температуре 713 ° С. Для образца, полученного гетерогенным соосаждением аммиаком (см. рис. 3), процесс заканчивается значительно раньше – при температуре 518 ° С.
Также на ДТГ-кривых образцов, полученных гетерогенным соосаждением аммиаком и бикарбонатом аммония, в интервале температур от 300 ° С до завершающих температур процесса разложения наблюдается эндотермический эффект (температура пика 280 ° С и 380 ° С соответственно), обусловленный разложением прекурсора.
В результате проведенного термического анализа определена температура синтеза Nd:Y 2 O 3 из прекурсоров – 700 °C.
По данным ИК-спектрометрии (рис. 5) спектр образцов прекурсоров, полученных гомогенным соосаждением и гетерогенным соосаждением бикарбонатом аммония, имеет набор полос поглощения, характерных для колебаний связей «C-O» в группе HCO 3 -, «N-O» и «N-H», что может свидетельствовать о гидрокарбонатной природе прекурсоров. Спектр образца прекурсора, полученного гетерогенным соосаждением аммиаком, имеет набор полос поглощения, характерных для колебаний связей «O-H» в группе OH-, «N-H» «N-O», что согласуется с данными РФА – смесь гидратов оксогидроксонитратов иттрия.
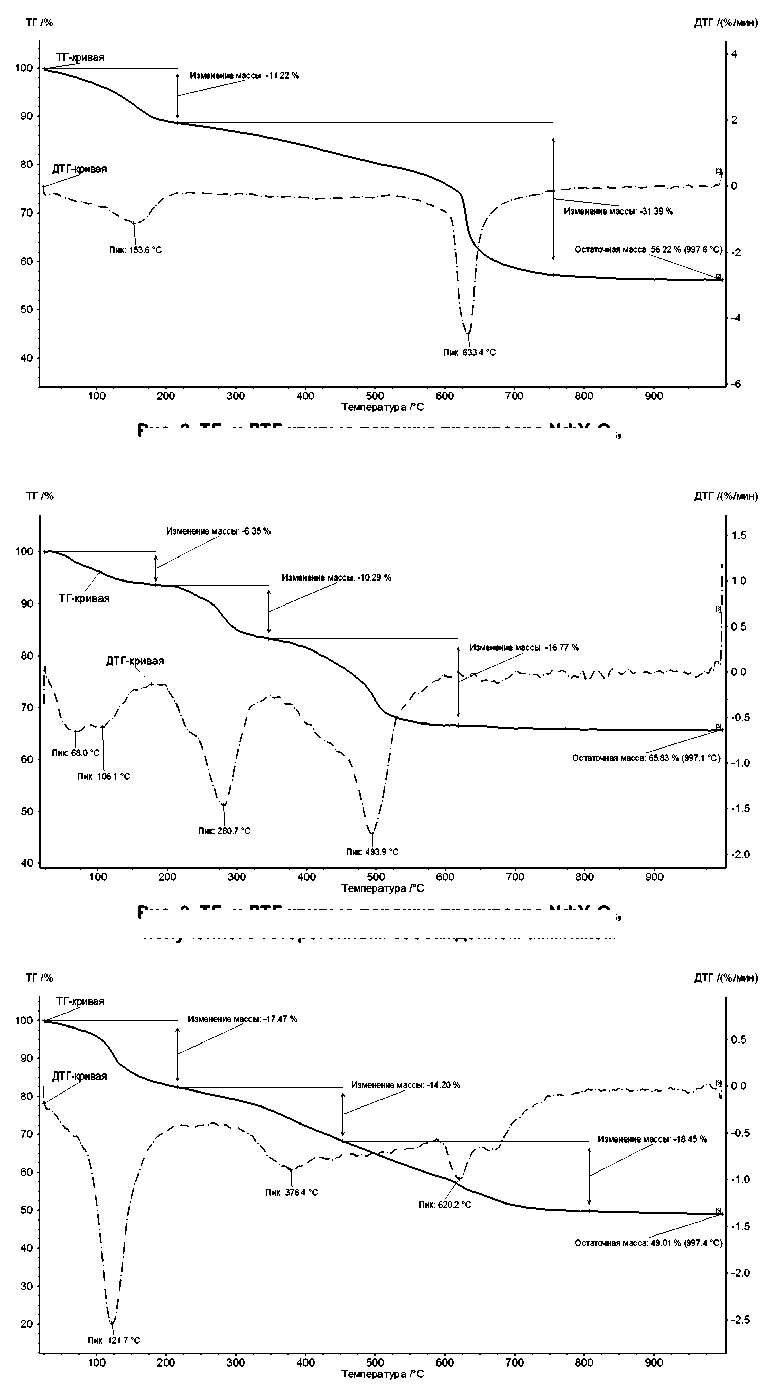
Рис. 4. ТГ- и ДТГ-кривые порошка прекурсора Nd:Y 2 O 3 , полученного гетерогенным соосаждением бикарбонатом аммония
Рис. 2. ТГ- и ДТГ-кривые порошка прекурсора Nd:Y 2 O 3 , полученного методом гомогенного соосаждения
Рис. 3. ТГ- и ДТГ-кривые порошка прекурсора Nd:Y 2 O 3 , полученного гетерогенным соосаждением аммиаком
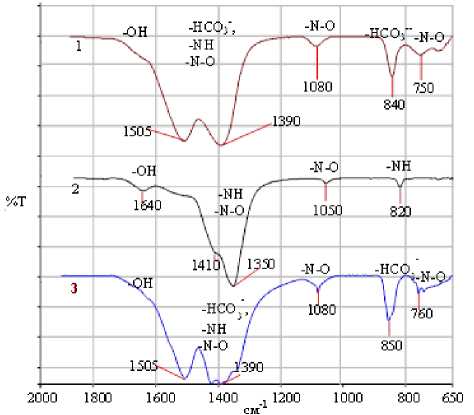
Рис. 5. Спектры НПВО прекурсоров:
1 – гомогенное соосаждение, 2 – гетерогенное соосаждение аммиаком; 3 – гетерогенное соосаждение бикарбонатом аммония
На рис. 6 представлены снимки с электронного микроскопа частиц прекурсоров, полученных методами гомогенного соосаждения и гетерогенного соосаждения бикарбонатом аммония и аммиаком, которые имеют разную морфологию.

а)

б)
Рис. 6. Электронные снимки частиц порошка прекурсора Nd:Y 2 O 3 : а – гомогенное соосаждение; б – гетерогенное соосаждение аммиаком; в – гетерогенное соосаждение бикарбонатом аммония

495 nm
>2 * 485 nm
448 nm
456 nm
355 nm
IMm
в)
Исследование синтезированного порошка оксида иттрия, легированного ионами неодима
Дифрактограмма порошка оксида иттрия, полученного методом гомогенного соосаждения, представлена на рис. 7.
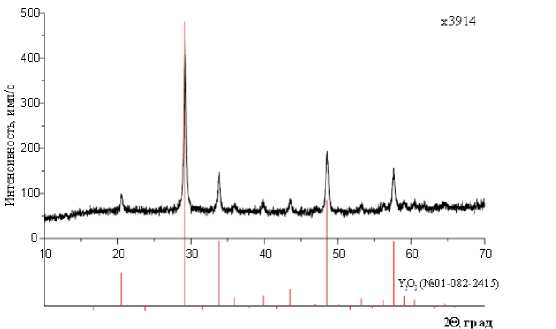
Рис. 7. Дифрактограмма порошка Nd:Y 2 O 3
Как видно из рис. 7, дифрактограмма представлена только линиями, принадлежащими соединению Y 2 O 3 , карточка № 01-082-2415, с кубической решеткой.
Дифрактограммы образцов, полученных из прекурсоров гетерогенного соосаждения бикарбонатом аммония и аммиаком, идентичны представленной.
Гомогенное соосаждение
Исследование зависимости формы и размера частиц оксида иттрия от концентрации ионов иттрия в исходном растворе и от времени старения
На рис. 8 представлены снимки с электронного микроскопа частиц оксида иттрия, полученных гомогенным соосаждением при различных концентрациях иттрия в растворе. Соотношение концентраций [Y3+]/[(NH 2 ) 2 CO] составляло 1:50.
При анализе данных видно, что с увеличением концентрации суммарной концентрации ионов иттрия и неодима частицы оксида иттрия становятся менее сферическими, более крупными и сильнее срастаются в агломераты.

а)

б)

в)
Рис. 8. Электронные снимки частиц порошков Nd:Y 2 O 3 :
а – С(Y 3+ + Nd 3+ ) = 0,01 моль/л; б – С(Y 3+ + Nd 3+ ) = 0,015 моль/л; в – С(Y 3+ + Nd 3+ ) = 0,02 моль/л
Как видно из рис. 6 и 8, как для прекурсора, так и для синтезированного оксида прослеживается сферическая форма частиц. Стоит отметить, что размер сферических частиц оксида иттрия уменьшается на 10–20 % в сравнении с размером частиц прекурсора, что делает возможным проведение оценки формы и размера частиц на стадии прекурсора.
Увеличение времени выдержки осадка от 1 до 3 часов и увеличение температуры изотермической выдержки с 90 до 100 °С не оказывают влияние на форму и размер частиц.
Зависимость формы и размера частиц от температуры синтеза
Форма частиц Nd:Y 2 O 3 при температурах 700 °C и 1000 °C не меняется, при увеличении температуры до 1200 °C происходит увеличение размеров и слипание частиц (рис. 9).

а) б)
Рис. 9. Электронные снимки частиц порошка Nd:Y 2 O 3 : а – синтез при 700 °C в течение 2 часов; б – синтез при 1250 °C в течение 2 часов
Гетерогенное обратное соосаждение
Зависимость формы и размера частиц от природы осадителя и условий осаждения
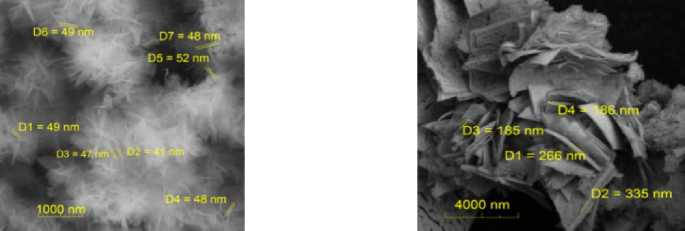
На рис. 10 представлены снимки со сканирующего электронного микроскопа частиц оксида иттрия, полученных гетерогенным соосаждением бикарбонатом аммония (б) и аммиаком (а).
Как видно из рис. 10, частицы порошка Nd:Y2O3, полученные гетерогенным соосаждением раствором аммония углекислого кислого, представлены в виде пластинок толщиной (110–
250) нм. Частицы порошка Nd:Y 2 O 3 , полученные гетерогенным соосаждением раствором аммиака, представлены иголками толщиной 20–40 нм, собранными в агломераты. При этом частицы прекурсора (см. рис. 6) и синтезированного оксида иттрия имеют одинаковое строение. Размер частиц игольчатой формы прекурсора и Nd:Y2O3 практически не изменяется, в то время как размер частиц пластинчатой формы уменьшается практически в 2 раза.
а) б)
Рис. 10. Электронные снимки частиц порошка Nd:Y 2 O 3 а – соосаждение аммиаком; б – соосаждение бикарбонатом аммония
Изменение суммарной концентрации ионов иттрия и неодима в растворе в диапазоне от 0,01 моль/л до 0,1 моль/л не приводит к изменению размера и формы частиц.
Зависимость формы и размера частиц от температуры синтеза
На рис. 11–12 представлены снимки частиц Nd:Y 2 O 3 , полученных гетерогенным соосаждени-ем бикарбонатом аммония и аммиаком при различных температурах синтеза: 700 °C, 1000 °C и 1250 °C. При увеличении температуры синтеза от 700 до 1000 °C частицы, полученные гетерогенным соосаждением бикарбонатом аммония, сохраняют свою форму. При увеличении температуры до 1250 °C в пластинках наблюдается образование сферических частиц и пустот. Для частиц, полученных гетерогенным соосаждением аммиаком при температурах синтеза 700 °C и 1000 °C, форма частиц не изменяется, а размер частиц увеличивается примерно в 2 раза. При увеличении температуры синтеза до 1250 °C форма и размер частиц меняется: образуются частицы овальной формы с размером от 240 до 280 нм, жестко связанные в агломераты.

а)

б)

в)
Рис. 11. Электронные снимки частиц порошка Nd:Y 2 O 3 , полученного соосаждением бикарбонатом аммония: а – 700 °C; б – 1000 °C; в – 1250 °C

а)

б)

в)
Рис. 12. Электронные снимки частиц порошка Nd:Y 2 O 3 , полученного соосаждением аммиаком: а – 700 °C; б – 1000 °C; в – 1250 °C
Заключение
Таким образом, методами РФА, ИК-спектрометрии, электронной микроскопии и ТГ- и ДСК-анализом исследованы зависимости формы и размера частиц оксида иттрия, легированного ионами неодима, от вида осадителя, концентрации исходных компонентов и температуры синтеза. Показано, что при изменении осадителя изменяется форма и размер частиц синтезируемого оксида: сферическая форма при использовании карбамида в качестве осадителя, пластинчатая форма при использовании раствора бикарбоната аммония в качестве осадителя и игольчатая форма при использовании раствора аммиака в качестве осадителя. Установлено, что форма частиц прекурсора и синтезированного оксида иттрия не изменяется в процессе термической обработки. Также установлено, что увеличение концентрации ионов иттрия в исходном растворе до 0,015 моль/л в случае гомогенного соосаждения приводит к началу образования жестких агломератов. Для гетерогенного обратного осаждения изменение концентрации ионов иттрия в растворе до 0,1 моль/л не приводит к существенным изменениям формы и размера частиц.
Список литературы Влияние условий синтеза порошка оксида иттрия, легированного ионами неодима, на морфологию
- Коновалов А.А. Оптически прозрачная керамика на основе Yb(Nd):Y2O3, полученная из синтезированных карбонатов дис. канд. хим. наук. М.: Учреждение Российской академии наук Институт металлургии и материаловедения им. А.А. Байкова РАН, 2010. 148 с.
- Huang XY, Zhang X, Hu ZW, et al. // Opt Mater. 2019. V. 92. P. 359. D01: 10.1016/j.optmat.2019.04.047
- Garanin, S.G., Dmitriuk, A.V., Zhlin, A.A., et al // J. Opt. Technol. 2010. V. 77, No. 6. P. 52. D01: 10.1364/J0T.77.000565
- Yavetskiy R.P., Kosyanov D.Yu, Baumer V.N. et al. // J. Rare Earths. 2014. V. 32, No. 4. P. 320. DOI: 10.1016/S1002-0721 (14)60074-0
- Zhang, J., Zhang, Z., Tang, Z., et al. // J. Mater. Process. Technol. 2002. V. 121, No. 2-3. P. 265. DOI: 10.1016/S0924-0136(01)01263-8
- Kaygorodov A.S., Ivanov V.V., Khrustov V.R. et al. // J. Eur. Ceram. Soc. 2007. V. 27. P. 1165. D01: 10.1016/j.jeurceramsoc.2006.05.027
- Zheng C., Yang G., Zhang K. et al. //J. Alloys Compd.. 2015. V. 648. P. 838. DOI: 10.1016/j.jallcom.2015.06.258
- Wang N., He J. //J. Lumin. 2023. V. 257. P. 119718. DOI: 10.1016/j.jlumin.2023.119718
- Boukerika A., Guerbous L. // J. Lumin. 2014 V. 145. P. 148. DOI: 10.1016/j.jlumin.2013.07.037
- Liu Y, Qin X, Xin H, et al. // J. Eur. Ceram. Soc. 2013. V. 33. P. 2625. DOI: 10.1016/j.jeurceramsoc.2013.04.029
- Li J., Liu W., Jiang B. et. Al. // J. Alloys. Compd. 2012. V. 515. P. 49. DOI: 10.1016/j.jallcom.2011.10.083
- Tomaszewski H., Weglarz H., De Gryse R. // J. Eur. Ceramic. Soc. V. 17, Iss. 2. P.403. DOI: 10.1016/s0955-2219(96)00192-6
- Devaraju M. K., Yin S., Sato T. // Nanotechnology. 2009. V. 20 (305302). P. 1. DOI: 10.1088/0957-4484/20/30/305302
- Иванов М.Г., Копылов Ю.Л., Кравченко В.Б и др. //Неорган. материалы. 2014. Т. 50, № 9. С. 1028. DOI: 10.7868/S0002337X14090048
- Багаев С.Н., Каминский А.А., Копылов Ю.Л. и др. // Квантовая электроника. 2013. Т. 43, № 3. С. 271. DOI: 10.1070/QE2013v043n03ABEH015138
- Liu W. // Mater. Lett. 2013. V. 96. P. 42. DOI: 10.1016/j.matlet.2012.12.104
- Huang Y., Jiang D., Zhang J., et al. // Ceram. Int.. 2011. V. 37. P. 3523. DOI: 1016/j.ceramint.2011.06.008
- Sordelet D., Akinc M. // J. Colloid. Interface. Sci. 1988. V. 122, Iss. l. P. 47. DOI: 1016/0021 -9797(88)90286-X
- Sohn S., Kwon Y., Kim Y. et al. // Powder. Technol. 2004. V. 142, Iss. 2-3. P. l36. D0I: 10.1016/j.powtec.2004.03.013
- Kabir M., Ghahari M., Afarani M.S. //Ceram. Int. 2014. V. 40. P. 10877. DOI: 10.1016/j. cera-mint.2014.03.081
- Kumar D., Sharma M„ Pandey O.P // Opt. Mater. 2014. V. 36 P. 1131. DOI: 10.1016/j.optmat.2014.02.014
- Mouzon J., Nordell P., Thomas A. et al. // J. Eur. Ceram. Soc. 2007. V. 27. P. 1991. DOI: 10.1016/j.jeurceramsoc.2006.05.103
- Jadhav A., Pawar A.C., Kim W. et al. // J. Phys. Chern. A. 2009. V. 113. P. 16652. DOI: 10.1021/jp903067j
- Gowd G. S, Patra M. K., Songara S. et al. // J. Lumin. 2012. V. 132. P. 2023. DOI: 10.1016/j.jlumin.2O12.03.004
- Wang N., Zhang X., Bai Z. et al. // Ceram. Int. 2014. V. 40. P. 10877. DOI: 10.1016/ j.powtec.2010.06.006


