Влияние васкулярного эндотелиального фактора роста на сперматогенез после облучения электронами дозой 2 гр
Автор: Демяшкин Григорий Александрович, Бондурко Любовь Николаевна, Фомина Наталья Константиновна, Севанькаева Лариса Евгеньевна, Михина Людмила Николаевна, Глушак Валентина Вадимовна, Щекин Владимир Иванович
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 1, 2022 года.
Бесплатный доступ
Плазма, обогащенная тромбоцитами (PRP), потенциально влияет на восстановление тканей за счет стимуляции пролиферации и дифференцировки клеток-предшественников. Цель исследования - оценка влияния васкулярного эндотелиального фактора роста (VEGF) на сперматогенез после облучения электронами дозой 2 Гр. Материалы и методы. Семенники экспериментальных животных 5 групп (I - контроль (n=10), II - 2IR (n=35; доза - 2 Гр), III - 2IR+LP-PRP+IGF-1 (n=30), IV - 2IR+LP-PRP (n=30), V - LP-PRP (n=30)) были изучены методом световой микроскопии и с помощью иммуногистохимических реакций с антителами к VEGF. Результаты. После облучения обнаружили уменьшение количества VEGF-позитивных клеток, которое восстанавливалось на фоне введения PRP. Выводы. Облучение электронами дозой 2 Гр в семенниках приводит к уменьшению VEGF-позитивных клеток, а введение PRP, содержащей в т.ч. васкулярный эндотелиальный фактор роста, усиливает репаративные процессы, восстанавливая сперматогенез.
Сперматогенез, апоптоз, бесплодие, семенные канальцы, бета-излучение
Короткий адрес: https://sciup.org/14123513
IDR: 14123513 | УДК: 591.463.12
Effect of vascular endothelial growth factor on spermatogenesis after 2 gy electron irradiation
Platelet-rich plasma (PRP) influences tissue repair, stimulating the proliferation and differentiation of progenitor cells. The aim of the study was to evaluate the effect of vascular endothelial growth factor (VEGF) on spermatogenesis after 2 Gy electron irradiation. Materials and Methods. Light microscopy and immunohistochemical reactions with antibodies to VEGF were used to examine testes of 5 groups of experimental animals (Group 1 - control (n=10), Group 2 - 2IR (n=35), Group 3 - 2IR+LP-PRP+IGF-1 (n=30), Group 4 - 2IR+LP-PRP (n=30), Group 5 - LP-PRP (n=30)). Results. After irradiation, a decrease in the number of VEGF-positive cells was observed, which was restored under PRP administration. Conclusion. 2 Gy electron irradiation of the testes leads to a decrease in VEGF-positive cells. PRP administration, containing vascular endothelial growth factor, enhances reparative processes and restores spermatogenesis.
Текст научной статьи Влияние васкулярного эндотелиального фактора роста на сперматогенез после облучения электронами дозой 2 гр
Введение. Одной из наиболее частых причин снижения фертильности у мужчин, затрагивающего около 7 % населения, является ионизирующее излучение, используемое для лечения злокачественных опухолей яичек [1]. Некоторые авторы сообщают о том, что под действием облучения наблюдается снижение количества сперматозоидов, изменение их морфологии и подвижности, что связано с нарушением репликации ДНК и транскрипции РНК [2].
Регуляция сперматогенеза на всех стадиях осуществляется одним из паракринных факторов местного действия – васкулярным эндотелиальным фактором роста (VEGF), который продуцируется в т.ч. тромбоцитами [3]. VEGF способствует пролиферации и дифференцировке сперматогоний, влияет на микросреду яичка и, следовательно, на формирование сперматозоидов [4].
В последнее время васкулярный эндотелиальный фактор роста используют в различ-
ных областях медицины, в т.ч. и для коррекции сниженной фертильности у мужчин, но его влияние на сперматогенез остается малоизученным.
Цель исследования. Оценка влияния васкулярного эндотелиального фактора роста на сперматогенез после облучения электронами дозой 2 Гр.
Материалы и методы. Исследование проводили на базах Медицинского радиологического научного центра им. А.Ф. Цыба и Сеченовского Университета. Использовали самцов половозрелых крыс линии Wistar. Все манипуляции выполняли согласно Международным рекомендациям по проведению медикобиологических исследований с использованием животных (ЕЭС, Страсбург, 1985) и Хельсинкской декларации Всемирной медицинской ассоциации.
Экспериментальные животные (n=135) были поделены на 5 групп: I – контрольные крысы (n=10), которым внутрибрюшинно вво-
дили физиологический раствор (0,9 % раствор NaCl, 33,6 мл/кг); II (n=35), III (n=30), IV (n=30) группы – однократное локальное облучение семенников электронами (доза 2 Гр, мощность дозы 1 Гр/мин, энергия 10 МэВ, частота 9 Гц, диаметр поля 100 мм, использован линейный акселератор NOVAC-11). Кроме того, в III группе крысам вводили плазму, обогащенную тромбоцитами, с низким содержанием лейкоцитов (LP-PRP) и рекомбинантный инсулиноподобный фактор роста (IGF-1); в IV и V группах – LP-PRP. Длительность эксперимента – 84 сут – выбрана в соответствии с продолжительностью двух циклов сперматогенеза крыс. Животных всех групп выводили из эксперимента путем введения высоких доз анестетика. Извлеченные семенники взвешивали, фиксировали в растворе Буэна, заливали в парафиновые блоки, срезы толщиной 3–4 мкм окрашивали гематоксилином и эозином и готовили для иммуногистохимического исследования.
Микроскопический анализ выполняли с помощью системы видеомикроскопии (микроскоп Leica DM2000, Германия; камера Leica ICC50 HD; компьютер Platrun LG), морфометрические данные получали с использованием программного обеспечения для обработки и
анализа изображений Leica Application Suite, Version 4.9.0.
Для иммуногистохимического исследования в качестве первичных использовали кроличьи поликлональные антитела к VEGF-A (Millipore; клон ABS82; 1:50), вторичных – универсальные антитела (HiDef Detection™ HRP Polymer system, Cell Marque, США). Ядра клеток докрашивали гематоксилином Майера. Подсчет клеток (в %) проводили в 10 случайно отобранных полях зрения при увеличении ×400.
Полученные в результате подсчета данные обрабатывали с использованием компьютерной программы SPSS 12 for Windows statistical software package (IBM Analytics, США). Сравнение между группами проводили с использованием однофакторного дисперсионного анализа ANOVA со значимостью p<0,01.
Результаты и обсуждение. В семенниках контрольной группы отмечали умеренную положительную цитоплазматичекую ИГХ-реак-цию с антителами к VEGF во всех половых клетках на разных стадиях сперматогенеза (22,1 ± 3,4 %), особенно в сперматогониях, а также в клетках Сертоли и Лейдига (табл. 1, рис. 1).
Таблица 1
Table 1
Доля VEGF-позитивных клеток в семенниках групп животных, %
The proportion of VEGF-positive cells in testes of the experimental and control animals, %
|
Группа Group |
Половые клетки Germ cells |
Клетки Сертоли Sertoli cells |
Клетки Лейдига Leydig cells |
|
Контроль Control |
89,2 ± 1,1 |
84,1 ± 2,1 |
76,2 ± 2,4 |
|
2IR 84-е сут 2IR 84th day |
12,2 ± 1,1 |
83,2 ± 1,3 |
74,1 ± 1,5 |
|
2IR+LP-PRP+IGF-1 84-е сут 2IR+LP-PRP+IGF-1 84th day |
76,4 ± 2,3 |
84,1 ± 1,1 |
76,6 ± 2,1 |
|
2IR+LP-PRP 84-е сут 2IR+LP-PRP 84th day |
71,1 ± 1,3 |
83,3 ± 1,5 |
75,2 ± 1,3 |
|
LP-PRP 84-е сут LP-PRP 84th day |
88,2 ± 1,0 |
83,7 ± 0,7 |
75,7 ± 1,3 |
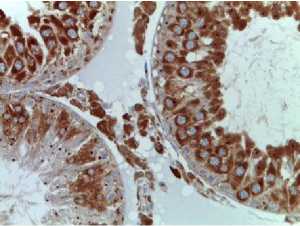
Контрольная группа Control group
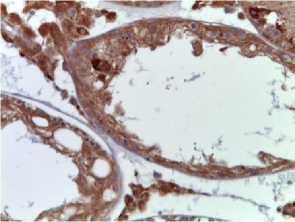
II группа Group II (2IR)
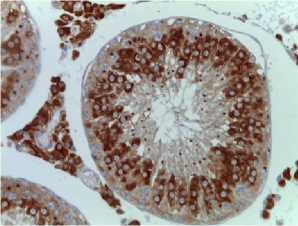
III группа Group III (2IR+LP-PRO+IGP-1)
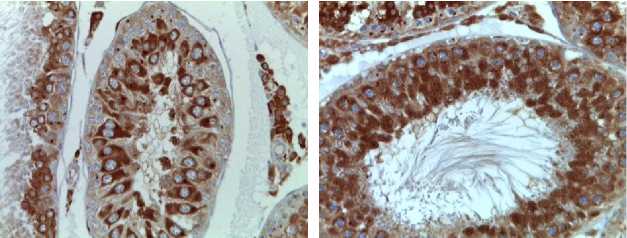
IV группа V группа
Group IV (2IR+LP-PRP)
V group (LP-PRP)
Рис. 1. Семенные канальцы крыс после локального облучения электронами дозой 2 Гр. Иммуногистохимические реакции с антителами к VEGF-A, докрашивание гематоксилином, ×400
Fig. 1. Seminiferous tubules of rats after local electron irradiation (2 Gy).
Immunohistochemical reactions with antibodies to VEGF-A, stained with hematoxylin, magnification ×400
Через 2 нед. после локального облучения у животных II, III, IV групп обнаружили нарушение гистоархитектоники семенников, проявляющееся гипосперматогенезом. Данные патоморфологические изменения сохранялись во II группе весь период эксперимента.
После облучения наблюдали снижение числа ИГХ-позитивных половых клеток в 2,0 раза (10,2 ± 1,2 %) по сравнению с группой контроля.
У животных III и IV групп на фоне введения LP-PRP, содержащей в т.ч. васкулярный эндотелиальный фактор роста, обнаружили постепенное увеличение VEGF-окрашенных половых клеток в 2,0 раза (18,2 ± 1,2 %) и 1,5 раза (16,1 ± 1,1 %) соответственно, в первую очередь пула сперматогенных стволовых клеток, сперматогоний, что, вероятно, связано с действием VEGF. При этом в III группе репаративные процессы произошли с опереже-
нием на 3–4 нед. за счет того, что животным дополнительно вводили рекомбинантный IGF-1.
В V группе, не подвергавшейся облучению, после введения LP-PRP значительных изменений по сравнению с контролем не выявлено.
Члены семейства VEGF (VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E) являются лигандами трансмембранных рецепторов VEGFR-1, VEGFR-2 и VEGFR-3 [5], которые экспрессируются в т.ч. в сперматогони-альных стволовых клетках. Реализация положительных эффектов происходит при связывании VEGF с его рецептором после аутофосфорилирования и последующей активации PI3K/AKT- и Ras/MAPK-путей [6, 7, 9, 10]. В результате активации данных путей наблюдаются неоваскулогенез и увеличение площади кровеносных сосудов в семенниках, что улучшает трофику и проницаемость гематоте-
стикулярного барьера для транспорта биологически активных веществ [8], тем самым стимулируя пролиферацию и дифференцировку половых клеток, способствуя восстановлению сперматогенеза и спермиогенеза, усиливая эффекты других факторов роста [9].
Заключение. Облучение электронами дозой 2 Гр в семенниках приводит к уменьшению VEGF-позитивных клеток, а введение PRP, содержащей в т.ч. васкулярный эндотелиальный фактор роста, усиливает репаративные процессы, восстанавливая сперматогенез.
Список литературы Влияние васкулярного эндотелиального фактора роста на сперматогенез после облучения электронами дозой 2 гр
- Serdarogullari M. Causes of Male Infertility. Experimed. 2020; 10 (3): 144-147.
- Kesari K.K, Agarwal A., Henkel R. Radiations and male fertility. Reproductive Biology and Endocrinology. 2018; 16 (1): 118.
- EDN: WXBBXX
- Kubatiev A.A., Borovaya T.G., Zhukhovitskii V.G., Shevlyagina N. V., Andreevskaya S.G. Platelets: a modern view on the structure and function. Patogenez (Pathogenesis). 2016; 14 (1): 4-13.
- EDN: XIPZEJ
- Ntemou E., Kadam P., Laere S. V., Saen D. V., Vicini E., Goossens E. Effect of recombinant human vascular endothelial growth factor on testis tissue xenotransplants from prepubertal boys: a three-case study. Reprod. Biomed. Online. 2019; 39 (1): 119-133.
- DOI: 10.1016/j.rbmo.2019.02.012
- Cross M., Dixelius J., Matsumoto T., Claesson-Welsh L. VEGF-receptor signal transduction. Trends in Biochemical Sciences. 2003; 28 (9): 488-494.
- DOI: 10.1016/S0968-0004(03)00193-2
- Pandey A., Singhi E., Arroyo J.P., Ikizler T.A., Gould E., Brown J., Beckman J., Harrison D., Moslehi J. Mechanisms of VEGF (Vascular Endothelial Growth Factor) Inhibitor-Associated Hypertension and Vascular Disease. Hypertension. 2018; 71 (2): e1-e8.
- DOI: 10.1161/HYPERTENSIONAHA.117.10271 EDN: GSHTVT
- Nakatsu M., Samson R., Perez-del-Pulgar S., Aoto J., Aitkenhead M., Taylor K., Carpenter P., Hughes C. VEGF121 and VEGF165 Regulate Blood Vessel Diameter Through Vascular Endothelial Growth Factor Receptor 2 in an in vitro Angiogenesis Model. Laboratory investigation. 2003; 83 (12): 1873-1885.
- DOI: 10.1097/01.lab.0000107160.81875.33
- Elmi A., Zannoni A., Govoni N., Bertocchi M., Forni M., Ventrella D., Bacci M.L. Uncovering the Physiological Mechanisms Underlying the Roe Deer (Capreolus capreolus) Testicular Cycle: Analyses of Gelatinases and VEGF Patterns and Correlation with Testes Weight and Testosterone. Animals. 2020; 10 (3): 444.
- DOI: 10.3390/ani10030444
- Santos T., Cavariani M.M., Pereira D.N., Schimming B.C., Chuffa L.G., Domeniconi R.F. Maternal Protein Restriction Modulates Angiogenesis and AQP9 Expression Leading to a Delay in Postnatal Epidid-ymal Development in Rat. Cells. 2019; 8 (9): 1094.
- DOI: 10.3390/cells8091094
- Leung D. W., Cachianes G., Kuang W.J., Goeddel D.V., Ferrara N. Vascular endothelial growth factor is a secreted angiogenic mitogen. Science. 1989; 246 (4935): 1306-1309.
- DOI: 10.1126/science.2479986 EDN: HIVMRP


